人教版九年级化学第六单元课题1《金刚石、石墨和C60》学案(含答案)
文档属性
| 名称 | 人教版九年级化学第六单元课题1《金刚石、石墨和C60》学案(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 103.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-10-30 00:00:00 | ||
图片预览

文档简介
《金刚石、石墨和C60》学案
【学习目标】:
1.了解金刚石和石墨的物理性质和主要用途。
2.知道碳单质的化学性质。
3.知道不同的元素可以组成不同的物质,同一种元素也可以组成不同的物质。
4.以人类对碳单质的认识为例,引导学生形成“科学是发展”的观点。
【课前预习】:
1.碳的单质有 、 和 等,其中 是天然存在的最硬的物质, 是最软的矿物之一,金刚石和石墨物理性质的差异是因为 。
2.一个C60分子是由 个碳原子构成的,它形似足球,它主要应用于 的研究。
3.木炭和活性炭都具有 性,是因为它们具有 的结构。
4.碳的单质在常温下化学性质 。
5.碳具有可燃性。① 碳在氧气中充分燃烧的反应方程式 ;② 碳在氧气中不充分燃烧的反应方程式 。
6.碳具有还原性。碳在高温条件下还原CuO的实验现象为 ,化学方程式为 。
【课堂练习】:
1.下列关于金刚石和石墨的说法正确的是( )
A.组成元素相同 B.原子的排列方式相同
C.都能导电 D.硬度都很大
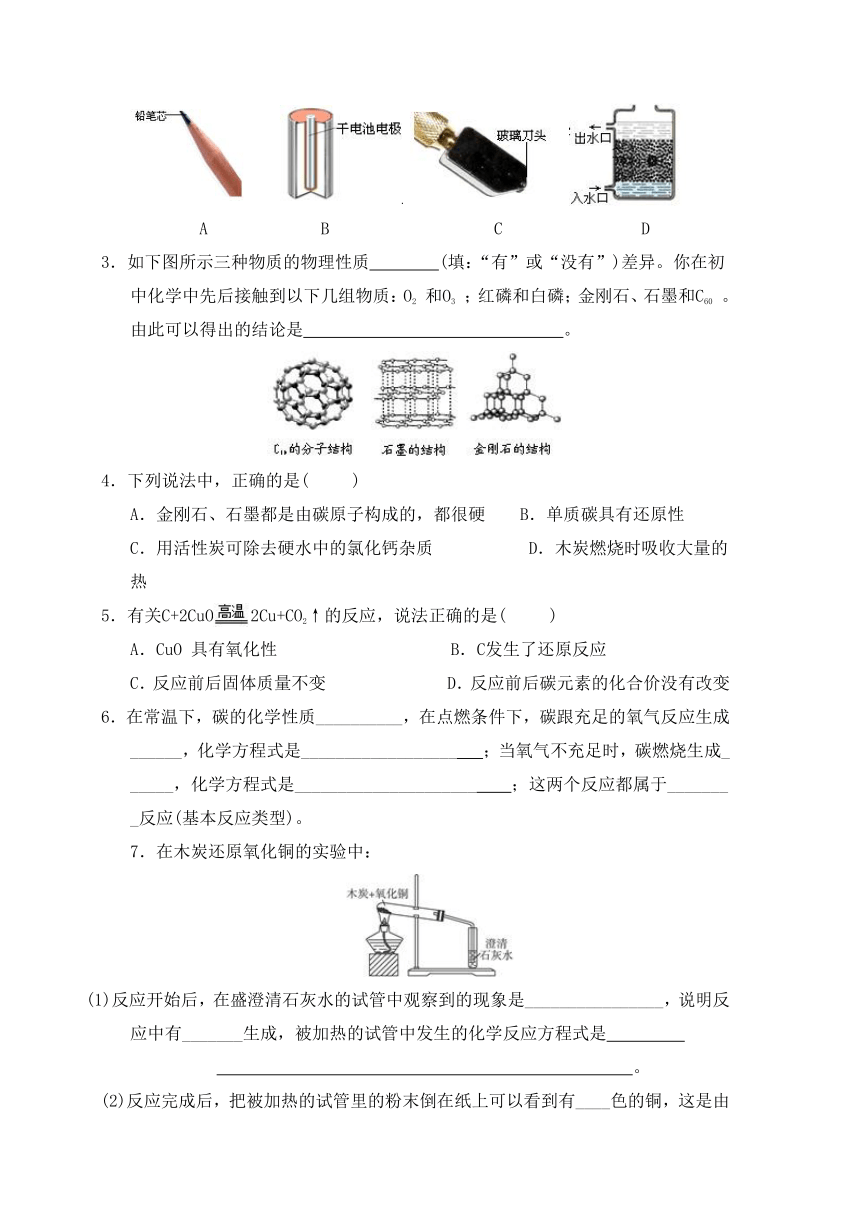
2.碳单质存在形式有多种,用途各不相同。下图中体现活性炭用途的是( )
A B C D
3.如下图所示三种物质的物理性质 (填:“有”或“没有”)差异。你在初中化学中先后接触到以下几组物质:O2 和O3 ;红磷和白磷;金刚石、石墨和C60 。由此可以得出的结论是 。
4.下列说法中,正确的是( )
A.金刚石、石墨都是由碳原子构成的,都很硬 B.单质碳具有还原性
C.用活性炭可除去硬水中的氯化钙杂质 D.木炭燃烧时吸收大量的热
5.有关C+2CuO2Cu+CO2↑的反应,说法正确的是( )
A.CuO 具有氧化性 B.C发生了还原反应
C.反应前后固体质量不变 D.反应前后碳元素的化合价没有改变
6.在常温下,碳的化学性质__________,在点燃条件下,碳跟充足的氧气反应生成______,化学方程式是__________________ ;当氧气不充足时,碳燃烧生成______,化学方程式是_____________________ ;这两个反应都属于________反应(基本反应类型)。
7.在木炭还原氧化铜的实验中:
(1)反应开始后,在盛澄清石灰水的试管中观察到的现象是________________,说明反应中有_______生成,被加热的试管中发生的化学反应方程式是
。
(2)反应完成后,把被加热的试管里的粉末倒在纸上可以看到有____色的铜,这是由于 。
(3)右图中酒精灯上加一金属网罩的作用__________________________。
(4)实验结束时,应先_____________,再撤掉____________。
【课后巩固】:
1.下列变化属于化学变化的是( )
A.金刚石制成钻石 B.石墨制成金刚石
C.木炭使NO2褪色 D.石墨导电
2.澳大利亚科学家发现了纯碳新材料 “碳纳米泡沫”,每个泡沫含有约4 000个碳原子,直径约6到9nm,在低于-183℃时,泡沫具有永久磁性。下列叙述正确的是( )
A.“碳纳米泡沫”和金刚石的性质相同
B.“碳纳米泡沫”在氧气中充分燃烧的产物只有二氧化碳
C.“碳纳米泡沫”是碳单质
D.“碳纳米泡沫”是一种新型的碳化合物
3.关于碳的化学性质,叙述不正确的是( )
A.温度越高,碳的活泼性越强
B.碳具有还原性,炽热的碳能使氧化铜还原成铜
C.碳在氧气中充分燃烧放出热量,而不充分燃烧吸收热量
D.碳在常温下能长时间保存不变质
4. 石墨烯是新发现的二维空间材料,它是由石墨制成的新型碳单质,金刚石、石墨、C60和石墨烯的结构示意图如下图所示,下列关于这四种物质的说法中正确的是( )
A.都是黑色固体 B.都质软可作润滑剂
C.碳原子排列方式都相同 D.在氧气中充分燃烧都生成二氧化碳
5.(1)纯净的金刚石是无色透明、 形状的固体。它是天然存在的最 的物质,可用来裁玻璃。
(2)电车与电缆接触的部分称作“电刷”,制作“电刷”的物质是一种碳的单质,这种碳单质是 (填名称)。该物质应该具备的性质是 (填序号)。①硬度大 ②导热性 ③导电性
(3)活性炭具有 的结构,具有 能力,制糖工业利用活性炭来脱色制白糖。
(4)古代一些书法家、画家用墨(用炭黑等制成)书写或绘制的字画能够保存很长时间不变色,这是由于 。
6.将黑色粉末A、B混合装入试管中加强热,生成红色固体C,同时放出无色气体D。加热A并通入D时只生成一种气体E。根据上述内容,回答下列问题:
(1)写出各物质的化学式:A ;B ;C ;D ;E .
(2)写出A和B、A和D反应的化学方程式: , .
7.小明同学在实验室用木炭和氧化铜的混合物17.2g,在老师的指导下,用酒精喷灯加热使之充分反应,冷却后称量固体的剩余物为12.8g,该同学所称的CuO质量为多少克?
课题1 金刚石、石墨和C60
课前预习:
1.金刚石,石墨,C60,金刚石,石墨,碳原子的排列方式不同
2.60,超导方面
3.吸附,疏松多孔
4.不活泼
5.① C+O2CO2;② 2C+O22CO。
6.黑色粉末逐渐变成红色, C+2CuO2Cu+CO2↑。
课堂练习:
1.A 2.D 3.有同种元素可形成不同的单质。 4.B 5.A
6.稳定 二氧化碳 C+O2CO2 一氧化碳 2C+O22CO 化合
7.(1)澄清石灰水变浑浊 二氧化碳 C+2CuO2Cu+CO2↑
(2)亮红 木炭有还原性,能与氧化铜反应,生成金属铜
(3)使酒精灯的火焰集中,使被加热部位的温度更高
(4)把导气管从澄清石灰水中移出 酒精灯
课后巩固:
1.B 2.A 3.C 4.D
5.(1)正八面体、硬 ;(2)石墨、③;(3)疏松多孔、吸附;(4)在常温下,碳的化学性质不活泼
6.(1)C;CuO;Cu;CO2;CO (2)C+2CuO2Cu+CO2↑;C+CO22CO
7.解:
【学习目标】:
1.了解金刚石和石墨的物理性质和主要用途。
2.知道碳单质的化学性质。
3.知道不同的元素可以组成不同的物质,同一种元素也可以组成不同的物质。
4.以人类对碳单质的认识为例,引导学生形成“科学是发展”的观点。
【课前预习】:
1.碳的单质有 、 和 等,其中 是天然存在的最硬的物质, 是最软的矿物之一,金刚石和石墨物理性质的差异是因为 。
2.一个C60分子是由 个碳原子构成的,它形似足球,它主要应用于 的研究。
3.木炭和活性炭都具有 性,是因为它们具有 的结构。
4.碳的单质在常温下化学性质 。
5.碳具有可燃性。① 碳在氧气中充分燃烧的反应方程式 ;② 碳在氧气中不充分燃烧的反应方程式 。
6.碳具有还原性。碳在高温条件下还原CuO的实验现象为 ,化学方程式为 。
【课堂练习】:
1.下列关于金刚石和石墨的说法正确的是( )
A.组成元素相同 B.原子的排列方式相同
C.都能导电 D.硬度都很大
2.碳单质存在形式有多种,用途各不相同。下图中体现活性炭用途的是( )
A B C D
3.如下图所示三种物质的物理性质 (填:“有”或“没有”)差异。你在初中化学中先后接触到以下几组物质:O2 和O3 ;红磷和白磷;金刚石、石墨和C60 。由此可以得出的结论是 。
4.下列说法中,正确的是( )
A.金刚石、石墨都是由碳原子构成的,都很硬 B.单质碳具有还原性
C.用活性炭可除去硬水中的氯化钙杂质 D.木炭燃烧时吸收大量的热
5.有关C+2CuO2Cu+CO2↑的反应,说法正确的是( )
A.CuO 具有氧化性 B.C发生了还原反应
C.反应前后固体质量不变 D.反应前后碳元素的化合价没有改变
6.在常温下,碳的化学性质__________,在点燃条件下,碳跟充足的氧气反应生成______,化学方程式是__________________ ;当氧气不充足时,碳燃烧生成______,化学方程式是_____________________ ;这两个反应都属于________反应(基本反应类型)。
7.在木炭还原氧化铜的实验中:
(1)反应开始后,在盛澄清石灰水的试管中观察到的现象是________________,说明反应中有_______生成,被加热的试管中发生的化学反应方程式是
。
(2)反应完成后,把被加热的试管里的粉末倒在纸上可以看到有____色的铜,这是由于 。
(3)右图中酒精灯上加一金属网罩的作用__________________________。
(4)实验结束时,应先_____________,再撤掉____________。
【课后巩固】:
1.下列变化属于化学变化的是( )
A.金刚石制成钻石 B.石墨制成金刚石
C.木炭使NO2褪色 D.石墨导电
2.澳大利亚科学家发现了纯碳新材料 “碳纳米泡沫”,每个泡沫含有约4 000个碳原子,直径约6到9nm,在低于-183℃时,泡沫具有永久磁性。下列叙述正确的是( )
A.“碳纳米泡沫”和金刚石的性质相同
B.“碳纳米泡沫”在氧气中充分燃烧的产物只有二氧化碳
C.“碳纳米泡沫”是碳单质
D.“碳纳米泡沫”是一种新型的碳化合物
3.关于碳的化学性质,叙述不正确的是( )
A.温度越高,碳的活泼性越强
B.碳具有还原性,炽热的碳能使氧化铜还原成铜
C.碳在氧气中充分燃烧放出热量,而不充分燃烧吸收热量
D.碳在常温下能长时间保存不变质
4. 石墨烯是新发现的二维空间材料,它是由石墨制成的新型碳单质,金刚石、石墨、C60和石墨烯的结构示意图如下图所示,下列关于这四种物质的说法中正确的是( )
A.都是黑色固体 B.都质软可作润滑剂
C.碳原子排列方式都相同 D.在氧气中充分燃烧都生成二氧化碳
5.(1)纯净的金刚石是无色透明、 形状的固体。它是天然存在的最 的物质,可用来裁玻璃。
(2)电车与电缆接触的部分称作“电刷”,制作“电刷”的物质是一种碳的单质,这种碳单质是 (填名称)。该物质应该具备的性质是 (填序号)。①硬度大 ②导热性 ③导电性
(3)活性炭具有 的结构,具有 能力,制糖工业利用活性炭来脱色制白糖。
(4)古代一些书法家、画家用墨(用炭黑等制成)书写或绘制的字画能够保存很长时间不变色,这是由于 。
6.将黑色粉末A、B混合装入试管中加强热,生成红色固体C,同时放出无色气体D。加热A并通入D时只生成一种气体E。根据上述内容,回答下列问题:
(1)写出各物质的化学式:A ;B ;C ;D ;E .
(2)写出A和B、A和D反应的化学方程式: , .
7.小明同学在实验室用木炭和氧化铜的混合物17.2g,在老师的指导下,用酒精喷灯加热使之充分反应,冷却后称量固体的剩余物为12.8g,该同学所称的CuO质量为多少克?
课题1 金刚石、石墨和C60
课前预习:
1.金刚石,石墨,C60,金刚石,石墨,碳原子的排列方式不同
2.60,超导方面
3.吸附,疏松多孔
4.不活泼
5.① C+O2CO2;② 2C+O22CO。
6.黑色粉末逐渐变成红色, C+2CuO2Cu+CO2↑。
课堂练习:
1.A 2.D 3.有同种元素可形成不同的单质。 4.B 5.A
6.稳定 二氧化碳 C+O2CO2 一氧化碳 2C+O22CO 化合
7.(1)澄清石灰水变浑浊 二氧化碳 C+2CuO2Cu+CO2↑
(2)亮红 木炭有还原性,能与氧化铜反应,生成金属铜
(3)使酒精灯的火焰集中,使被加热部位的温度更高
(4)把导气管从澄清石灰水中移出 酒精灯
课后巩固:
1.B 2.A 3.C 4.D
5.(1)正八面体、硬 ;(2)石墨、③;(3)疏松多孔、吸附;(4)在常温下,碳的化学性质不活泼
6.(1)C;CuO;Cu;CO2;CO (2)C+2CuO2Cu+CO2↑;C+CO22CO
7.解:
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
