人教版九年级化学课件:3.3元素 (共42张PPT)
文档属性
| 名称 | 人教版九年级化学课件:3.3元素 (共42张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-10-30 00:00:00 | ||
图片预览







文档简介
(共42张PPT)
课题3 元素
自主预习
阅读书本59-60页的有关内容,完成下列问题:
1.氧气是由 元素组成,水是由 、 元素组成,二氧化碳是由 、 元素 组成,氧气、水、二氧化碳分子中都含有氧原子,它们核内质子数都是8,化学上把这些氧原子统称为 。 元素就是 的总称。
2. _ ___?决定于元素的种类。
3.地壳里各种元素的含量从高到低的前四位是: _ _______;地壳中含量最多的非金属元素 __ _ ;地壳中含量最多的金属元素 _ ___。生物细胞中含量最多的元素是 。
一、元素
(1)什么是元素:
元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
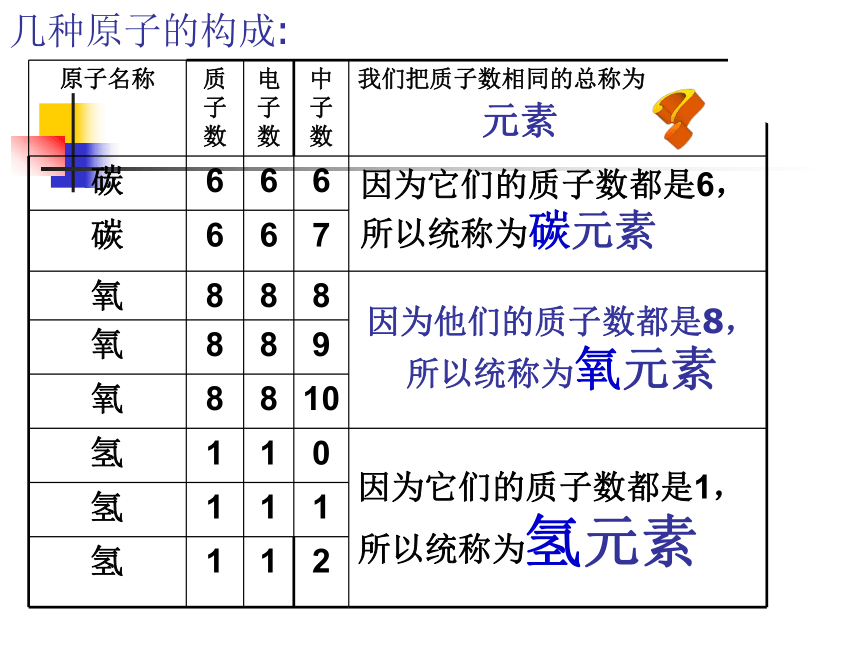
几种原子的构成:
元素
因为它们的质子数都是6,所以统称为碳元素
因为它们的质子数都是1,所以统称为氢元素
因为他们的质子数都是8,所以统称为氧元素
原子名称 质子数 电子数 中子数 我们把质子数相同的总称为
碳 6 6 6
碳 6 6 7
氧 8 8 8
氧 8 8 9
氧 8 8 10
氢 1 1 0
氢 1 1 1
氢 1 1 2
CO2
SO2
P2O5
H2O
MgO
CuO
Al2O3
Fe3O4
C O2
S O2
P2 O5
H2 O
Mg O
Cu O
Al2 O3
Fe3 O4
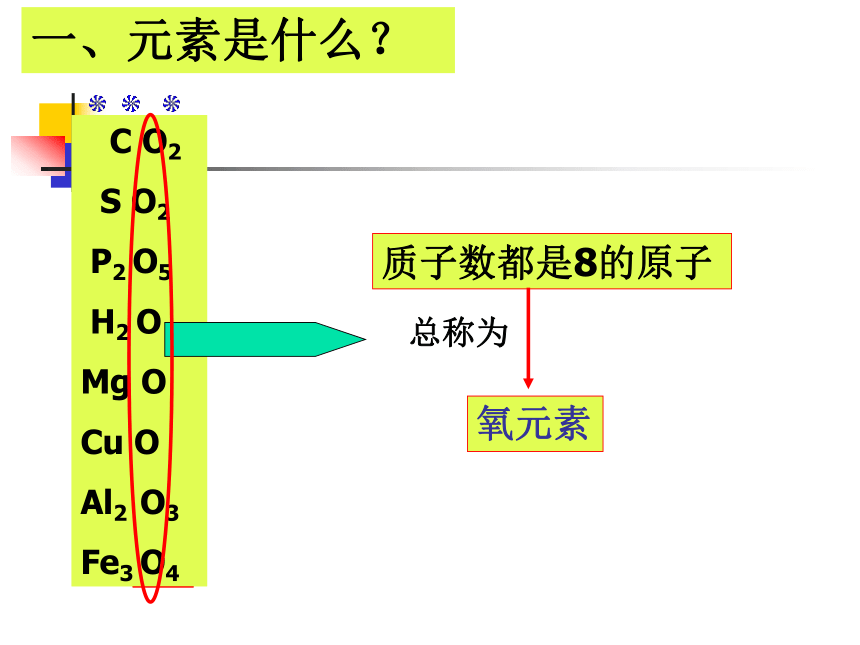
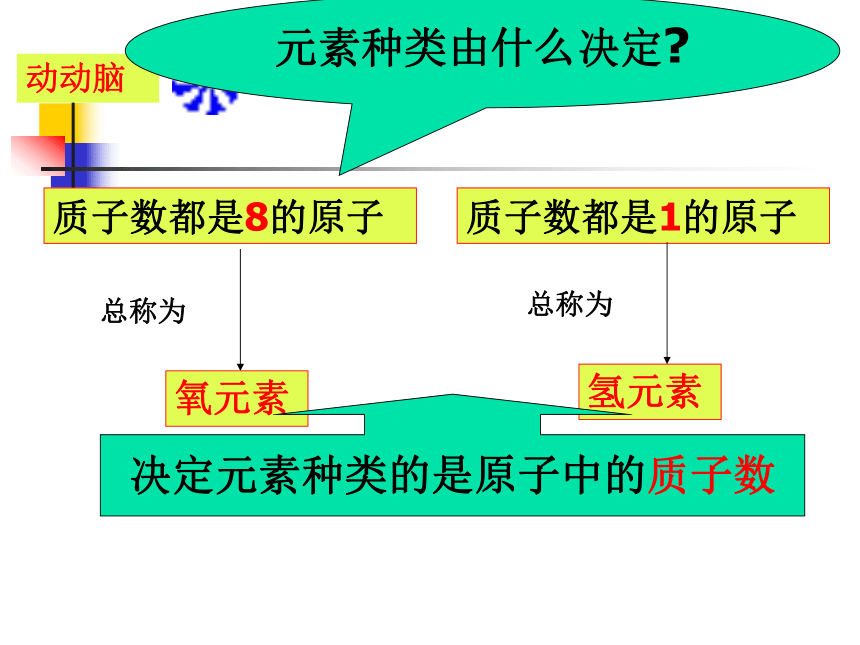
质子数都是8的原子
氧元素
一、元素是什么?
HCl
H2S
H2SO4
H2SO3
H2CO3
HNO3
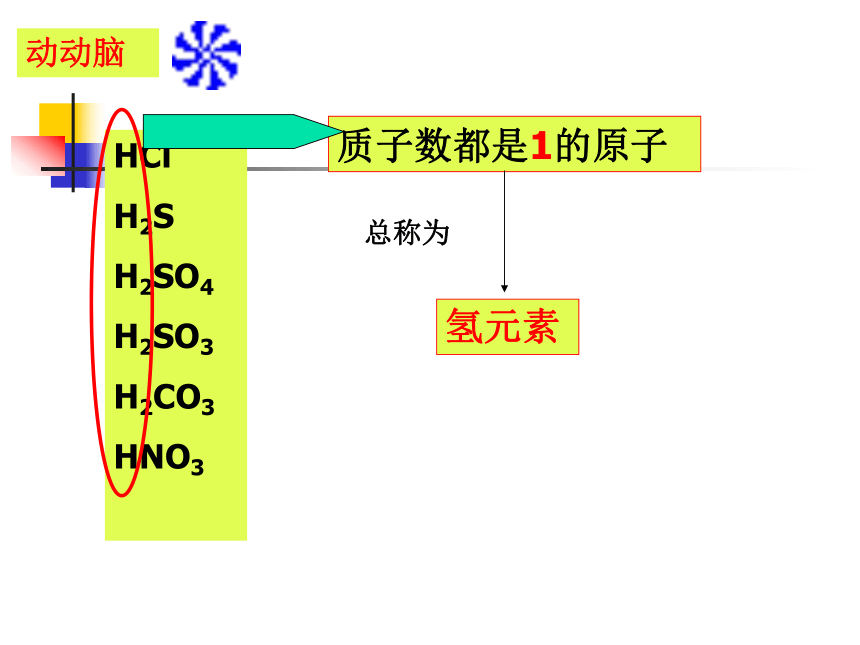
质子数都是1的原子
氢元素
动动脑
动动脑
决定元素种类的是原子中的质子数
元素种类由什么决定?
把核电荷数为8(即质子数为8)的所有的氧原子
氧气、水、二氧化碳、氧化汞中都有氧元素
核电荷数为1的所有氢原子统称为氢元素
核电荷数为6的所有的碳原子统称为碳元素
判断某两个原子是否为同种元素的依据是什么?
核电荷数即核内质子数相同,元素相同
核电荷数即核内质子数不同,元素不同
统称为氧元素
由核电荷数(即核内质子数)决定的。
元素的种类:
元素的化学性质主要由:
最外层电子数决定。
小组讨论:
元素与原子的对比
(2)元素与原子的比较:
具有相同核电荷数(即核内质子数)的一类原子的总称。
化学变化中的最小粒子
用于描述物质的宏观组成;只讲种类,不表示个数
用于描述微观构成;既表示种类,又讲个数
水是由氢元素和氧元素组成的
一个水分子是由2个氢原子和1个氧原子构成的。
元素是一类原子的总称,原子和元素是个体和总体的关系。化学反应中元素种类不变,原子种类和个数也不变。
元素 原子
概念
区别
举例
联系
水由什么组成?
水由什么构成?
而水分子由什么构成?
水分子由氧原子和氢原子构成;
想一想:
水由氢元素和氧元素组成;
物质由元素来组成;
分子由原子来构成
组
成
构
成
一个水分子由一个氧原子和二个氢原子构成;
构
成
水由水分子构成
物质由微粒来构成;
物质的种类非常多,已知的就有3 000多万种。但是组成这些物质的元素并不多。到目前为止,已经发现的元素只有一百余种。
物质是由元素组成的
都含有钙元素
(3)元素的存在---生活中
都含有锌元素
(3)元素的存在---生活中
铁强化酱油
(3)元素的存在---生活中
都含有铁元素
N元素
氮肥
生活中的元素
新稀宝(锌硒宝片)
(3)元素的存在:
配料表:含锌硒碘蛋白质粉,明胶等。
功效成分:锌 40-80mg/kg
硒 1.0-2.0mg/kg
碘 20-30mg/kg
以上都是指元素的含量
按质量计,各种元素在地壳里的含量差别很大,如图所示。地壳里氧、硅、铝、铁的含量相对较多。
(4)地壳中元素的含量由多到少依次是:氧、硅、铝、铁。
1.地壳中含量前四位的元素:
氧、硅、铝、铁
4.空气中含量最多的元素:
氮
5.海水中含量最多的金属元素:
钠
6.生物细胞中含量前三位的元素:
氧、碳、氢
2.地壳中含量最多的金属元素:
铝
3.地壳中含量最多的非金属元素:
氧
7.人体中含量最多的金属元素:
钙
(5)元素的分类
元素
金属元素:
非金属元素:
铁元素、铜元素、铝元素、金元素、汞元素
“钅”旁及汞
“石“旁
“气”旁
“氵”旁
固态非金属元素:
碳、硫、磷
液态非属元素:
溴
气态非金属元素:
氧、氟、氯
稀有气体元素:
氦、氖、氩、氪
科学是没有国界的,科学又是为大众的。为了书写和学术交流的方便,采用国际统一的符号来表示各种元素。
二、元素符号
自主预习
阅读书本第61页的有关内容,完成下列问题:
1书写元素符号时要注意:由一个字母表示的元素符号要 ;由两个字母表示的元素符号,第一个字母 写,第二个字母 写。
2用3分钟集体诵读教材62页中表3-4中的元素符号和名称。老师出示元素名称学生写符号,看谁写的又快又准。
3元素符号表示的意义:表示一种 ,还表示一个 。
4元素分为: 元素、 元素、 气体。
每种元素都用一个国际上通用的符号来表示,这种符号叫元素符号。
(1)元素符号的定义:
???
???
(2)元素符号的书写:“一大二小”原则
①.由一个字母表示的元素符号要大写;
②.由两个字母表示的元素符号,第一个字母
大写,第二个字母小写。
如:H、O、N等
如: Cu 、Ca 、Ne、Na、Mg、 Mn等
注意:
1、Co和CO
2、Ca和Cu
3、 Ag和Hg
(3)元素符号的含义
O
小组讨论 :
(3)元素符号表示的意义:
思考:
元素符号O表示的意义?
元素符号表示① 一种元素(宏观含义),
还表示②这种元素的一个原子(微观含义)。
元素符号O:
表示氧元素;
表示一个氧原子
③有些元素符号还表示一种单质:
金属:Fe、Cu、Ag
固态非金属:C、S、P
稀有气体:He、Ne
通常有两种含义
某元素
某元素的一个原子
想一想:
(1)元素符号N、Cu、Ne、C表示的意义?
Cu
N
表示氮元素
一个氮原子
表示铜元素
一个铜原子
Ne
表示氖元素
表示一个氖原子
C
表示碳元素
表示一个碳原子
铜单质
氖气
碳单质
(2)符号H、2H表示的意义?
注意:元素符号前有数字只表示微观的意义(几个某原子),不表示宏观意义(某元素)。
H:
表示氢元素;
表示一个氢原子
2H:
表示2个氢原子
1、说说下列符号的意义
2、用符号和数字表达含义
5个氧原子: 2个铜原子:
氮元素 : 3个磷原子:
5O
2Cu
N
3P
Cl :
2N:
2Mg:
nS:
练习:
氯元素、一个氯原子
2个氮原子
2个镁原子
n个硫原子
超级市场里有成百上千种商品,为了便于顾客选购,必须分门别类、有序地摆放。
自主预习
1.元素周期表共7个横行,18个纵行。每一个横行叫做一个 ,共有 周期。每一个纵行叫做一个 (8、9、10三个纵行共同组成一个族),共有 族。
2.元素周期表按元素原子 核电荷 递增的顺序给元素编了号,叫做 。原子序数= = = 。
3.观察书本最后一页元素周期表:金属用 色表示;非金属用 ,表示。第一周期除外,每周期开头的是 元素,靠近尾部的是 元素;结尾的是 元素。
4根据元素周期表能得到的信息:左上角的数字表示 ,字母表示 ,汉字表示 ,下方的数字表示 。
三、元素周期表简介
O
氧
8
16.00
原子序数
元素符号
元素名称
相对原子质量
核电荷数
质子数
小组讨论 :
教师点拨 :
1、元素周期表上分两大区域
2、横行——叫周期:
7个横行就是7个周期。
3、纵行——族:
18个纵行16个族
小结:
周期数=电子层数
原子序数=质子数=核电荷数=电子数
规律:同一横行(周期)从左至右,质子数逐渐递增;
同一横行(周期)从左至右,最外层电子数逐渐递增。
元素
物质
原子
分子
宏观组成:
构成
构成
构成
具有相同核电荷数的同类原子
?组成
物质、 元素、分子、原子间的术语关系如何表达呢?
只讲种类
不讲个数
微观构成:
既讲种类
又讲个数
本课题小结
1、元素的概念
元素就是具有相同核电荷数(即相同质子数)的同一类原子的总称。
2、元素符号的书写
3、元素符号表示的意义
4、元素周期表
再见
课题3 元素
自主预习
阅读书本59-60页的有关内容,完成下列问题:
1.氧气是由 元素组成,水是由 、 元素组成,二氧化碳是由 、 元素 组成,氧气、水、二氧化碳分子中都含有氧原子,它们核内质子数都是8,化学上把这些氧原子统称为 。 元素就是 的总称。
2. _ ___?决定于元素的种类。
3.地壳里各种元素的含量从高到低的前四位是: _ _______;地壳中含量最多的非金属元素 __ _ ;地壳中含量最多的金属元素 _ ___。生物细胞中含量最多的元素是 。
一、元素
(1)什么是元素:
元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
几种原子的构成:
元素
因为它们的质子数都是6,所以统称为碳元素
因为它们的质子数都是1,所以统称为氢元素
因为他们的质子数都是8,所以统称为氧元素
原子名称 质子数 电子数 中子数 我们把质子数相同的总称为
碳 6 6 6
碳 6 6 7
氧 8 8 8
氧 8 8 9
氧 8 8 10
氢 1 1 0
氢 1 1 1
氢 1 1 2
CO2
SO2
P2O5
H2O
MgO
CuO
Al2O3
Fe3O4
C O2
S O2
P2 O5
H2 O
Mg O
Cu O
Al2 O3
Fe3 O4
质子数都是8的原子
氧元素
一、元素是什么?
HCl
H2S
H2SO4
H2SO3
H2CO3
HNO3
质子数都是1的原子
氢元素
动动脑
动动脑
决定元素种类的是原子中的质子数
元素种类由什么决定?
把核电荷数为8(即质子数为8)的所有的氧原子
氧气、水、二氧化碳、氧化汞中都有氧元素
核电荷数为1的所有氢原子统称为氢元素
核电荷数为6的所有的碳原子统称为碳元素
判断某两个原子是否为同种元素的依据是什么?
核电荷数即核内质子数相同,元素相同
核电荷数即核内质子数不同,元素不同
统称为氧元素
由核电荷数(即核内质子数)决定的。
元素的种类:
元素的化学性质主要由:
最外层电子数决定。
小组讨论:
元素与原子的对比
(2)元素与原子的比较:
具有相同核电荷数(即核内质子数)的一类原子的总称。
化学变化中的最小粒子
用于描述物质的宏观组成;只讲种类,不表示个数
用于描述微观构成;既表示种类,又讲个数
水是由氢元素和氧元素组成的
一个水分子是由2个氢原子和1个氧原子构成的。
元素是一类原子的总称,原子和元素是个体和总体的关系。化学反应中元素种类不变,原子种类和个数也不变。
元素 原子
概念
区别
举例
联系
水由什么组成?
水由什么构成?
而水分子由什么构成?
水分子由氧原子和氢原子构成;
想一想:
水由氢元素和氧元素组成;
物质由元素来组成;
分子由原子来构成
组
成
构
成
一个水分子由一个氧原子和二个氢原子构成;
构
成
水由水分子构成
物质由微粒来构成;
物质的种类非常多,已知的就有3 000多万种。但是组成这些物质的元素并不多。到目前为止,已经发现的元素只有一百余种。
物质是由元素组成的
都含有钙元素
(3)元素的存在---生活中
都含有锌元素
(3)元素的存在---生活中
铁强化酱油
(3)元素的存在---生活中
都含有铁元素
N元素
氮肥
生活中的元素
新稀宝(锌硒宝片)
(3)元素的存在:
配料表:含锌硒碘蛋白质粉,明胶等。
功效成分:锌 40-80mg/kg
硒 1.0-2.0mg/kg
碘 20-30mg/kg
以上都是指元素的含量
按质量计,各种元素在地壳里的含量差别很大,如图所示。地壳里氧、硅、铝、铁的含量相对较多。
(4)地壳中元素的含量由多到少依次是:氧、硅、铝、铁。
1.地壳中含量前四位的元素:
氧、硅、铝、铁
4.空气中含量最多的元素:
氮
5.海水中含量最多的金属元素:
钠
6.生物细胞中含量前三位的元素:
氧、碳、氢
2.地壳中含量最多的金属元素:
铝
3.地壳中含量最多的非金属元素:
氧
7.人体中含量最多的金属元素:
钙
(5)元素的分类
元素
金属元素:
非金属元素:
铁元素、铜元素、铝元素、金元素、汞元素
“钅”旁及汞
“石“旁
“气”旁
“氵”旁
固态非金属元素:
碳、硫、磷
液态非属元素:
溴
气态非金属元素:
氧、氟、氯
稀有气体元素:
氦、氖、氩、氪
科学是没有国界的,科学又是为大众的。为了书写和学术交流的方便,采用国际统一的符号来表示各种元素。
二、元素符号
自主预习
阅读书本第61页的有关内容,完成下列问题:
1书写元素符号时要注意:由一个字母表示的元素符号要 ;由两个字母表示的元素符号,第一个字母 写,第二个字母 写。
2用3分钟集体诵读教材62页中表3-4中的元素符号和名称。老师出示元素名称学生写符号,看谁写的又快又准。
3元素符号表示的意义:表示一种 ,还表示一个 。
4元素分为: 元素、 元素、 气体。
每种元素都用一个国际上通用的符号来表示,这种符号叫元素符号。
(1)元素符号的定义:
???
???
(2)元素符号的书写:“一大二小”原则
①.由一个字母表示的元素符号要大写;
②.由两个字母表示的元素符号,第一个字母
大写,第二个字母小写。
如:H、O、N等
如: Cu 、Ca 、Ne、Na、Mg、 Mn等
注意:
1、Co和CO
2、Ca和Cu
3、 Ag和Hg
(3)元素符号的含义
O
小组讨论 :
(3)元素符号表示的意义:
思考:
元素符号O表示的意义?
元素符号表示① 一种元素(宏观含义),
还表示②这种元素的一个原子(微观含义)。
元素符号O:
表示氧元素;
表示一个氧原子
③有些元素符号还表示一种单质:
金属:Fe、Cu、Ag
固态非金属:C、S、P
稀有气体:He、Ne
通常有两种含义
某元素
某元素的一个原子
想一想:
(1)元素符号N、Cu、Ne、C表示的意义?
Cu
N
表示氮元素
一个氮原子
表示铜元素
一个铜原子
Ne
表示氖元素
表示一个氖原子
C
表示碳元素
表示一个碳原子
铜单质
氖气
碳单质
(2)符号H、2H表示的意义?
注意:元素符号前有数字只表示微观的意义(几个某原子),不表示宏观意义(某元素)。
H:
表示氢元素;
表示一个氢原子
2H:
表示2个氢原子
1、说说下列符号的意义
2、用符号和数字表达含义
5个氧原子: 2个铜原子:
氮元素 : 3个磷原子:
5O
2Cu
N
3P
Cl :
2N:
2Mg:
nS:
练习:
氯元素、一个氯原子
2个氮原子
2个镁原子
n个硫原子
超级市场里有成百上千种商品,为了便于顾客选购,必须分门别类、有序地摆放。
自主预习
1.元素周期表共7个横行,18个纵行。每一个横行叫做一个 ,共有 周期。每一个纵行叫做一个 (8、9、10三个纵行共同组成一个族),共有 族。
2.元素周期表按元素原子 核电荷 递增的顺序给元素编了号,叫做 。原子序数= = = 。
3.观察书本最后一页元素周期表:金属用 色表示;非金属用 ,表示。第一周期除外,每周期开头的是 元素,靠近尾部的是 元素;结尾的是 元素。
4根据元素周期表能得到的信息:左上角的数字表示 ,字母表示 ,汉字表示 ,下方的数字表示 。
三、元素周期表简介
O
氧
8
16.00
原子序数
元素符号
元素名称
相对原子质量
核电荷数
质子数
小组讨论 :
教师点拨 :
1、元素周期表上分两大区域
2、横行——叫周期:
7个横行就是7个周期。
3、纵行——族:
18个纵行16个族
小结:
周期数=电子层数
原子序数=质子数=核电荷数=电子数
规律:同一横行(周期)从左至右,质子数逐渐递增;
同一横行(周期)从左至右,最外层电子数逐渐递增。
元素
物质
原子
分子
宏观组成:
构成
构成
构成
具有相同核电荷数的同类原子
?组成
物质、 元素、分子、原子间的术语关系如何表达呢?
只讲种类
不讲个数
微观构成:
既讲种类
又讲个数
本课题小结
1、元素的概念
元素就是具有相同核电荷数(即相同质子数)的同一类原子的总称。
2、元素符号的书写
3、元素符号表示的意义
4、元素周期表
再见
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
