仁爱版化学九年级上册 2.1 多组分的空气 课件(27张PPT)
文档属性
| 名称 | 仁爱版化学九年级上册 2.1 多组分的空气 课件(27张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 623.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-11-07 00:00:00 | ||
图片预览








文档简介
课件27张PPT。科普版九年级化学专题二
单元一 多组分的空气一、空气是由什么组成的 为了搞清楚空气的成分,很多科学家致力于这方面的研究,如瑞典化学家舍勒和英国化学家普里斯特里.其中最有名的就是法国化学家拉瓦锡做的实验.
拉瓦锡
(1743—1794)法国化学家,他建立燃料燃烧理论,创立了化学物质分类新体系,开创了化学发展新纪元。实验方法:曲颈甑(盛空气)中加热汞。
实验原理:汞+氧气→氧化汞
氧化汞→汞+氧气
实验现象: ①银白色的液态汞变成红色粉末(氧化汞)。
②容器内里空气体积减少约1/5(氧气);剩余气体约4/5(氮气)。
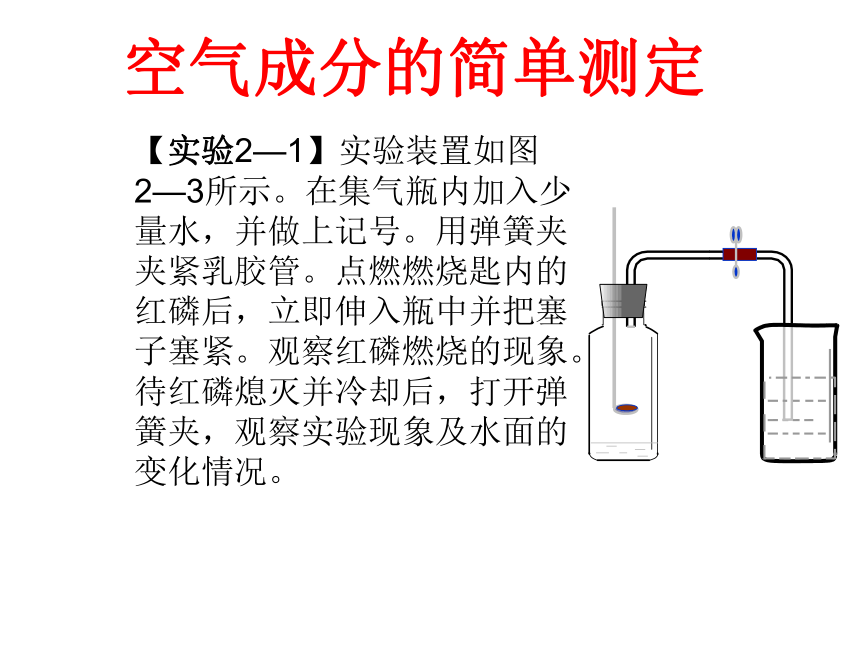
实验结论:空气由氧气和氮气组成,其中氧气约占空气总体积的1/5。拉瓦锡研究空气成分所用的装置空气成分的简单测定【实验2—1】实验装置如图2—3所示。在集气瓶内加入少量水,并做上记号。用弹簧夹夹紧乳胶管。点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧。观察红磷燃烧的现象。待红磷熄灭并冷却后,打开弹簧夹,观察实验现象及水面的变化情况。1、空气中氧气含量的测定
实验原理:根据某物质只与空气中氧气反应且生成固体,从而使密闭容器内的气体体积减小,压强变小,在外界大气压的作用下使密闭容器内的水面上升来测量的。
现象:有大量白烟产生,广口瓶内液面上升约1/5体积
结论:O2约占空气总体积1/5;
注意: ①可燃物要求:该物质要足量且在空气中就能燃烧;燃烧后产物是固体。 ②装置要求:气密性良好
磷+氧气 点燃 五氧化二磷
P O2 P2O5想一想
1.根据实验现象,分析广口瓶内剩余气体具有怎样的性质? 答:可得出剩余4/5 气体为N2的性质,①不支持燃烧,也不能燃烧,②难溶于水2、试验中红磷为何要过量?答:耗尽瓶内氧气充分3、为什么试验中要冷却至室温才打开止水夹?
因为高温气体体积大,若不冷却至室温瓶内的水不会上升1/5. 4、为什么点燃的红磷要立即伸入集 气瓶中?防止白烟污染空气。1)红磷量不足
2)装置气密性不好
3)瓶内温度没有冷却到室温讨 论P27拉瓦锡通过实验得出的结论是氧气占空气总体积的1/5 ,而在我们的实验中,为什么气体减少的体积小于1/5 ?2、空气的组成空气氧气二氧化碳水蒸气稀有气体氮气及其他气体杂质78%21%0.03%0.03%0.94%( N2 )( O2 )( CO2 )( H2 O )(体积分数)纯净物:由一种物质组成如:N2、O2、CO2、P、P2O5、H2O混合物:由多种物质组成如:空气 、海水 、河水 、矿泉水等 注意:(1)纯净物可以用专门的化学符号来表示。如氮气、氧气、二氧化碳可分别表示为N2、 O2、CO2等。
(2)混合物中各物质各自保持着各自的性质。例如:空气中的氮气、氧气、二氧化碳等都保持着各自的性质。3、物质的分类纯净物和混合物的比较练习:判断下列物质是混合物还是纯净物? 海水、自来水、蒸馏水、空气、氧气、河水、矿泉水、糖水、雪碧饮料、五氧化二磷、冰水混合物练习:判断下列物质是混合物还是纯净物? 海水、自来水、蒸馏水、空气、氧气、河水、矿泉水、糖水、雪碧饮料、五氧化二磷、冰水混合物1、氧气的用途:(1)供给呼吸(2)支持燃烧曾经叫“养气”二、空气是一种宝贵的资源:2、氮气的性质和用途无色、无味的气体。难溶于水熔沸点低。密度:1.251g/L不能燃烧不能支持燃烧用途:(不活泼)化工原料食品充气包装冷冻剂超导试验车保护气制氮肥3、稀有气体的性质和用途(2)稀有气体无色、无味,化学性质很不活泼。(3)用途:保护气、电光源激光技术、低温麻醉(1)稀有气体是氦氖氩氪氙等气体的总称三、保护空气温室效应酸雨对建筑物的腐蚀酸雨对森林的破坏臭氧空洞空气的污染及其防止1.空气中有害物质有害气体:二氧化硫(SO2)、一氧化碳(CO)、
二氧化氮(N02)烟尘(可吸入颗粒物)2、空气污染的危害:
3、防治措施:
严重损害人体健康,影响作物生长,破坏生态平衡.全球气候变暖,臭氧层破坏和酸雨等加强大气质量监测,改善环境状况,使用清洁能源,工厂的废气经处理过后才能排放,积极植树、造林、种草等课堂练习1、夏天从冰箱里拿出一瓶饮料,
放在空气中,饮料外壁会潮湿,
说明空气中含有( )
A.氮气 B.氧气
C.水蒸气 D.二氧化碳
2、要在一充满空气的瓶子中,将其中的氧气除去,又不增加其他气体的成分。下列物质在瓶中燃烧可达到目的的是( )
A.木碳 B.硫磺 C.铁丝 D.红磷
CCD
单元一 多组分的空气一、空气是由什么组成的 为了搞清楚空气的成分,很多科学家致力于这方面的研究,如瑞典化学家舍勒和英国化学家普里斯特里.其中最有名的就是法国化学家拉瓦锡做的实验.
拉瓦锡
(1743—1794)法国化学家,他建立燃料燃烧理论,创立了化学物质分类新体系,开创了化学发展新纪元。实验方法:曲颈甑(盛空气)中加热汞。
实验原理:汞+氧气→氧化汞
氧化汞→汞+氧气
实验现象: ①银白色的液态汞变成红色粉末(氧化汞)。
②容器内里空气体积减少约1/5(氧气);剩余气体约4/5(氮气)。
实验结论:空气由氧气和氮气组成,其中氧气约占空气总体积的1/5。拉瓦锡研究空气成分所用的装置空气成分的简单测定【实验2—1】实验装置如图2—3所示。在集气瓶内加入少量水,并做上记号。用弹簧夹夹紧乳胶管。点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧。观察红磷燃烧的现象。待红磷熄灭并冷却后,打开弹簧夹,观察实验现象及水面的变化情况。1、空气中氧气含量的测定
实验原理:根据某物质只与空气中氧气反应且生成固体,从而使密闭容器内的气体体积减小,压强变小,在外界大气压的作用下使密闭容器内的水面上升来测量的。
现象:有大量白烟产生,广口瓶内液面上升约1/5体积
结论:O2约占空气总体积1/5;
注意: ①可燃物要求:该物质要足量且在空气中就能燃烧;燃烧后产物是固体。 ②装置要求:气密性良好
磷+氧气 点燃 五氧化二磷
P O2 P2O5想一想
1.根据实验现象,分析广口瓶内剩余气体具有怎样的性质? 答:可得出剩余4/5 气体为N2的性质,①不支持燃烧,也不能燃烧,②难溶于水2、试验中红磷为何要过量?答:耗尽瓶内氧气充分3、为什么试验中要冷却至室温才打开止水夹?
因为高温气体体积大,若不冷却至室温瓶内的水不会上升1/5. 4、为什么点燃的红磷要立即伸入集 气瓶中?防止白烟污染空气。1)红磷量不足
2)装置气密性不好
3)瓶内温度没有冷却到室温讨 论P27拉瓦锡通过实验得出的结论是氧气占空气总体积的1/5 ,而在我们的实验中,为什么气体减少的体积小于1/5 ?2、空气的组成空气氧气二氧化碳水蒸气稀有气体氮气及其他气体杂质78%21%0.03%0.03%0.94%( N2 )( O2 )( CO2 )( H2 O )(体积分数)纯净物:由一种物质组成如:N2、O2、CO2、P、P2O5、H2O混合物:由多种物质组成如:空气 、海水 、河水 、矿泉水等 注意:(1)纯净物可以用专门的化学符号来表示。如氮气、氧气、二氧化碳可分别表示为N2、 O2、CO2等。
(2)混合物中各物质各自保持着各自的性质。例如:空气中的氮气、氧气、二氧化碳等都保持着各自的性质。3、物质的分类纯净物和混合物的比较练习:判断下列物质是混合物还是纯净物? 海水、自来水、蒸馏水、空气、氧气、河水、矿泉水、糖水、雪碧饮料、五氧化二磷、冰水混合物练习:判断下列物质是混合物还是纯净物? 海水、自来水、蒸馏水、空气、氧气、河水、矿泉水、糖水、雪碧饮料、五氧化二磷、冰水混合物1、氧气的用途:(1)供给呼吸(2)支持燃烧曾经叫“养气”二、空气是一种宝贵的资源:2、氮气的性质和用途无色、无味的气体。难溶于水熔沸点低。密度:1.251g/L不能燃烧不能支持燃烧用途:(不活泼)化工原料食品充气包装冷冻剂超导试验车保护气制氮肥3、稀有气体的性质和用途(2)稀有气体无色、无味,化学性质很不活泼。(3)用途:保护气、电光源激光技术、低温麻醉(1)稀有气体是氦氖氩氪氙等气体的总称三、保护空气温室效应酸雨对建筑物的腐蚀酸雨对森林的破坏臭氧空洞空气的污染及其防止1.空气中有害物质有害气体:二氧化硫(SO2)、一氧化碳(CO)、
二氧化氮(N02)烟尘(可吸入颗粒物)2、空气污染的危害:
3、防治措施:
严重损害人体健康,影响作物生长,破坏生态平衡.全球气候变暖,臭氧层破坏和酸雨等加强大气质量监测,改善环境状况,使用清洁能源,工厂的废气经处理过后才能排放,积极植树、造林、种草等课堂练习1、夏天从冰箱里拿出一瓶饮料,
放在空气中,饮料外壁会潮湿,
说明空气中含有( )
A.氮气 B.氧气
C.水蒸气 D.二氧化碳
2、要在一充满空气的瓶子中,将其中的氧气除去,又不增加其他气体的成分。下列物质在瓶中燃烧可达到目的的是( )
A.木碳 B.硫磺 C.铁丝 D.红磷
CCD
同课章节目录
- 专题一 走进化学殿堂
- 单元1 化学使生活更美好
- 单元2 如何学习化学
- 专题二 空气和水
- 单元1 多组分的空气
- 单元2 氧气
- 单元3 自然界的水
- 专题三 物质的构成
- 单元1 构成物质的微粒
- 单元2 组成物质的元素
- 单元3 纯净物组成的表示方法
- 专题四 燃料与燃烧
- 单元1 燃烧与灭火
- 单元2 碳及其化合物
- 单元3 化石燃料的利用
- 专题五 化学变化及其表示
- 单元1 化学变化是有条件的
- 单元2 质量守恒定律
- 单元3 化学方程式
- 专题六 物质的溶解
- 单元1 物质的溶解过程
- 单元2 物质的溶解性
- 单元3 物质的溶解性的改变
- 学生实验
- 实验1 实验基本操作
- 实验2 氧气的实验室制取与性质
- 实验3 燃烧的条件
- 实验4 二氧化碳的实验室制取与性质
- 实验5 一定浓度溶液的配置
