鲁科版化学 必修一 4.1 硅 无机非金属材料(共20张ppt)
文档属性
| 名称 | 鲁科版化学 必修一 4.1 硅 无机非金属材料(共20张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 431.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-11-13 00:00:00 | ||
图片预览







文档简介
课件20张PPT。化学1(必修)第四章第1节 硅 无机非金属材料
(第1课时)学习目标1.了解硅在自然界中的存在形式
2.掌握硅的性质、用途和工业制法
3.掌握二氧化硅的性质和用途预习检测1、硅在地壳中的含量?
在地壳中的含量仅次于氧,居第二位。
2、硅在自然界中的存在形态?
没有游离态的硅,只有以化合态存在的硅。
3、单质硅有几种同素异形体?
硅有晶体硅和无定形硅两种。
4、单质硅的物理性质?1)晶体硅是灰黑色,有金属光泽,
硬而脆的固体
2)熔、沸点高、硬度大
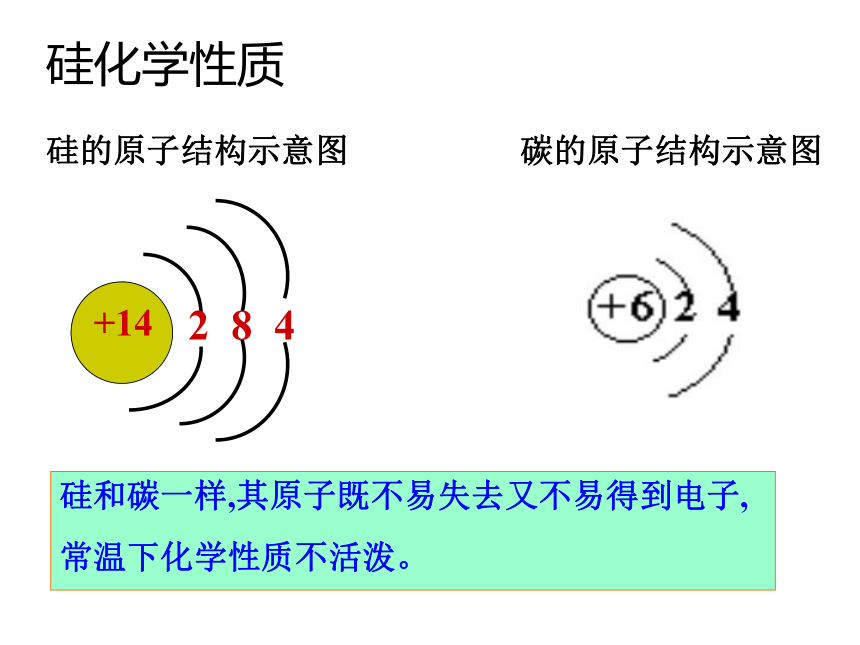
3)晶体硅是良好的半导体4.硅的物理性质晶体硅单晶硅单质硅硅的原子结构示意图硅和碳一样,其原子既不易失去又不易得到电子,
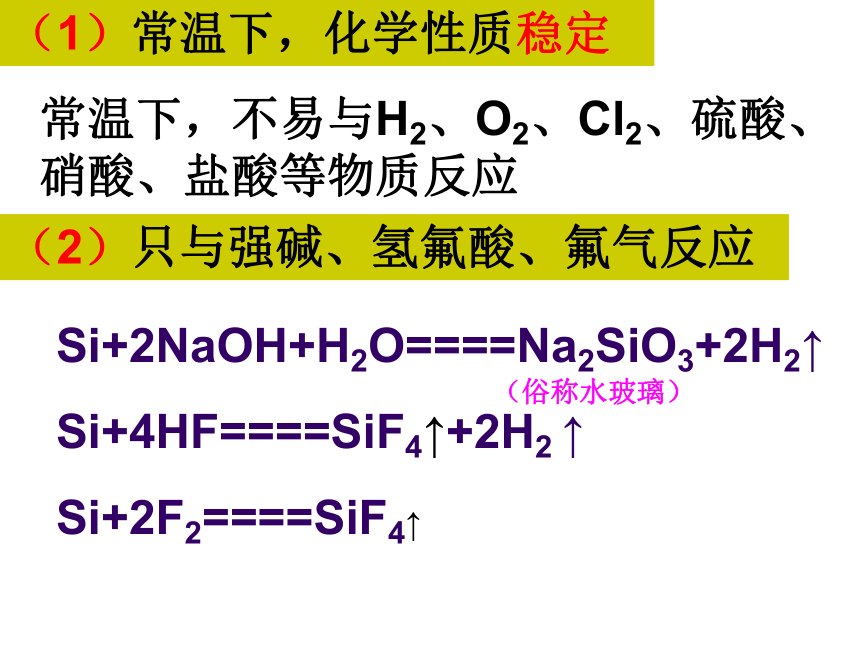
碳的原子结构示意图硅化学性质常温下化学性质不活泼。(1)常温下,化学性质稳定常温下,不易与H2、O2、Cl2、硫酸、
硝酸、盐酸等物质反应(2)只与强碱、氢氟酸、氟气反应(燃烧,放出大量的热)(3)加热,Si能与某些非金属单质反应工业上单质硅的制取原料:焦碳(C)和二氧化硅(SiO2)设备:电炉原理:②指出上反应中的氧化剂和还原剂。①上述反应属于哪种基本反应类型? 粗硅: 高纯硅:将粗硅与Cl2在高温下反应,然后把产物蒸馏
出后用氢气在高温下还原,可得到高纯硅。高纯硅:
集成电路、 晶体管、硅整流器
等半导体材料,还可以制太阳
能电池。
变压器铁芯(含硅4%的钢有导磁性)
耐酸设备(含硅15%左右的钢有耐酸性)
制合金:硅的用途二、二氧化硅 1.存在: 3.二氧化硅的物理性质晶体硬度 ,熔点 , 溶于水大高难2.SiO2的结构4.二氧化硅的化学性质(1)酸性氧化物的通性SiO2+2NaOH===Na2SiO3+H2O?你学过哪些酸性氧化物?能发生哪
些反应?③与某些盐反应②与碱性氧化物反应SiO2+4HF=SiF4↑+ 2H2O(2)特性
二氧化硅可以和氢氟酸反应4、二氧化硅和二氧化碳性质比较物 质物理
性质化 学 性 质状 态熔沸点与水反应与NaOH溶液与碱性氧
化物反应CO2SiO2与酸反应 1.利用二氧化硅怎样制取硅酸?2.氢氧化钠溶液是用什么装置保存,为什么?
3.氢氟酸能保存在玻璃瓶中吗?为什么?合作探究1.利用二氧化硅怎样制取硅酸?2.氢氧化钠溶液是用什么装置保存,为什么?
不能用玻璃塞,可用橡胶塞的玻璃试剂瓶。
3.氢氟酸能保存在玻璃瓶中吗?为什么?合作探究SiO2+2NaOH===Na2SiO3+H2ONa2SiO3+2HCl=2NaCl+H2SiO3↓不能,玻璃中二氧化硅可以和氢氟酸反应4、二氧化硅和二氧化碳性质比较物 质物理
性质化 学 性 质状 态熔沸点与水反应与NaOH溶
液反应与碱性氧
化物反应CO2气态低CO2+H2O=H2CO3CO2+2NaOH=Na2CO3+2H2OCO2+CaO CaCO3SiO2固态高不反应SiO2+2NaOH=Na2SiO3+2H2OSiO2+CaO CaSiO3与酸反应不与酸反应4HF+SiO2==SiF4↑+2H2O 5.二氧化硅的用途 水晶制光学仪器和工艺品 玛瑙制精密轴承和装饰品 石英表、石英钟 石英玻璃制化学仪器 制光导纤维 制普通玻璃 作建筑材料本节内容小结:1.硅①硅的存在②硅的化学性质③硅的用途跟踪练习1、在室温下,下列物质不能晶体硅反应的是( )
A、F2 B、KOH溶液
C、HF D、Cl2
2、(1)浓硝酸 (2)水 (3)氢氟酸 (4)烧碱溶液中,能与二氧化硅起化学反应的是( )
A、(1)(2) B、(3)(4)
C、(1)(4) D、 (2) (3)
3、能储存在带有玻璃塞的磨口试剂瓶的试剂是( )
A、液溴 B、氢氧化钾
C、氢氟酸 D、石灰水
D B A
(第1课时)学习目标1.了解硅在自然界中的存在形式
2.掌握硅的性质、用途和工业制法
3.掌握二氧化硅的性质和用途预习检测1、硅在地壳中的含量?
在地壳中的含量仅次于氧,居第二位。
2、硅在自然界中的存在形态?
没有游离态的硅,只有以化合态存在的硅。
3、单质硅有几种同素异形体?
硅有晶体硅和无定形硅两种。
4、单质硅的物理性质?1)晶体硅是灰黑色,有金属光泽,
硬而脆的固体
2)熔、沸点高、硬度大
3)晶体硅是良好的半导体4.硅的物理性质晶体硅单晶硅单质硅硅的原子结构示意图硅和碳一样,其原子既不易失去又不易得到电子,
碳的原子结构示意图硅化学性质常温下化学性质不活泼。(1)常温下,化学性质稳定常温下,不易与H2、O2、Cl2、硫酸、
硝酸、盐酸等物质反应(2)只与强碱、氢氟酸、氟气反应(燃烧,放出大量的热)(3)加热,Si能与某些非金属单质反应工业上单质硅的制取原料:焦碳(C)和二氧化硅(SiO2)设备:电炉原理:②指出上反应中的氧化剂和还原剂。①上述反应属于哪种基本反应类型? 粗硅: 高纯硅:将粗硅与Cl2在高温下反应,然后把产物蒸馏
出后用氢气在高温下还原,可得到高纯硅。高纯硅:
集成电路、 晶体管、硅整流器
等半导体材料,还可以制太阳
能电池。
变压器铁芯(含硅4%的钢有导磁性)
耐酸设备(含硅15%左右的钢有耐酸性)
制合金:硅的用途二、二氧化硅 1.存在: 3.二氧化硅的物理性质晶体硬度 ,熔点 , 溶于水大高难2.SiO2的结构4.二氧化硅的化学性质(1)酸性氧化物的通性SiO2+2NaOH===Na2SiO3+H2O?你学过哪些酸性氧化物?能发生哪
些反应?③与某些盐反应②与碱性氧化物反应SiO2+4HF=SiF4↑+ 2H2O(2)特性
二氧化硅可以和氢氟酸反应4、二氧化硅和二氧化碳性质比较物 质物理
性质化 学 性 质状 态熔沸点与水反应与NaOH溶液与碱性氧
化物反应CO2SiO2与酸反应 1.利用二氧化硅怎样制取硅酸?2.氢氧化钠溶液是用什么装置保存,为什么?
3.氢氟酸能保存在玻璃瓶中吗?为什么?合作探究1.利用二氧化硅怎样制取硅酸?2.氢氧化钠溶液是用什么装置保存,为什么?
不能用玻璃塞,可用橡胶塞的玻璃试剂瓶。
3.氢氟酸能保存在玻璃瓶中吗?为什么?合作探究SiO2+2NaOH===Na2SiO3+H2ONa2SiO3+2HCl=2NaCl+H2SiO3↓不能,玻璃中二氧化硅可以和氢氟酸反应4、二氧化硅和二氧化碳性质比较物 质物理
性质化 学 性 质状 态熔沸点与水反应与NaOH溶
液反应与碱性氧
化物反应CO2气态低CO2+H2O=H2CO3CO2+2NaOH=Na2CO3+2H2OCO2+CaO CaCO3SiO2固态高不反应SiO2+2NaOH=Na2SiO3+2H2OSiO2+CaO CaSiO3与酸反应不与酸反应4HF+SiO2==SiF4↑+2H2O 5.二氧化硅的用途 水晶制光学仪器和工艺品 玛瑙制精密轴承和装饰品 石英表、石英钟 石英玻璃制化学仪器 制光导纤维 制普通玻璃 作建筑材料本节内容小结:1.硅①硅的存在②硅的化学性质③硅的用途跟踪练习1、在室温下,下列物质不能晶体硅反应的是( )
A、F2 B、KOH溶液
C、HF D、Cl2
2、(1)浓硝酸 (2)水 (3)氢氟酸 (4)烧碱溶液中,能与二氧化硅起化学反应的是( )
A、(1)(2) B、(3)(4)
C、(1)(4) D、 (2) (3)
3、能储存在带有玻璃塞的磨口试剂瓶的试剂是( )
A、液溴 B、氢氧化钾
C、氢氟酸 D、石灰水
D B A
