人教版(五四制)八年级全册化学 3.2.1 原子的构成 课件(24张PPT)
文档属性
| 名称 | 人教版(五四制)八年级全册化学 3.2.1 原子的构成 课件(24张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-11-30 00:00:00 | ||
图片预览







文档简介
课件24张PPT。课题 2 原子的结构 复习2、 在电解水的实验中,水的 分解为氧
和氢 ,每 个氧原子重新组合一个氧 ,每 个氢原子重新组合一个氢 。
3、由此可知:分子是由 构成的,分子在化学反应中可以再分成 ,而原子在化学变化中却 ,即原子是 。分子 原子 两两分子 分子 原子 化学变化中的最小的粒子原子 不可再分原子 1、1个水分子是由 和 构成的。 两个氢原子一个氧原子原子真是最小的粒子吗?
在任何情况下原子都不能再分吗?
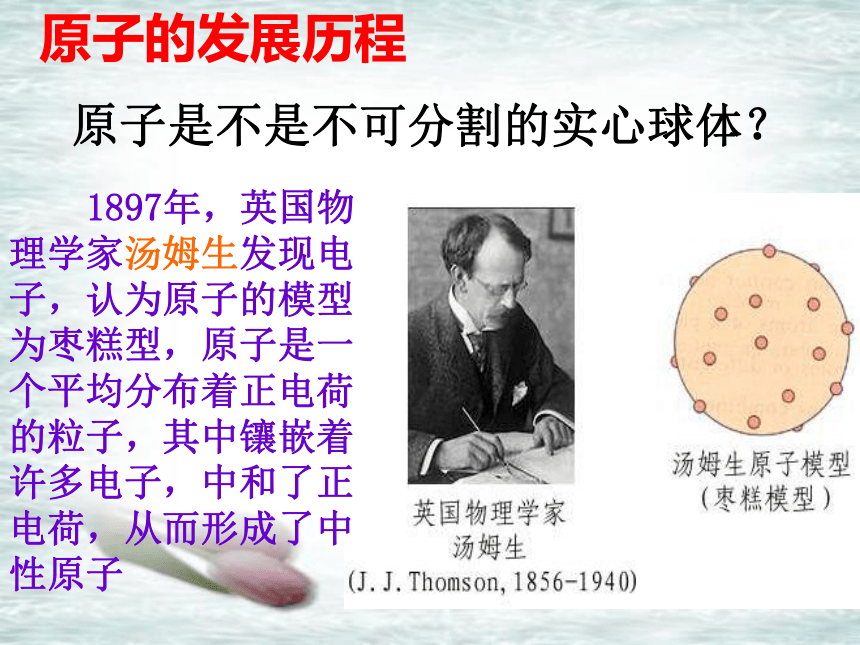
课题 2 原子的结构第三单元 物质构成的奥秘第1课时道尔顿于1803年提出科学假说:物质由原子组成,原子是不可分割的实心球体,同种原子的性质和质量相同.原子的发现历程改写这一论断的是科学家汤姆生。原子的发展历程 1897年,英国物理学家汤姆生发现电子,认为原子的模型为枣糕型,原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子原子是不是不可分割的实心球体? 1909年至1911年,英国物理学家卢瑟福和他的合作者通过α粒子的散射实验,提出了原子结构的核式结构学说。 即:在原子的中心有一个带正电荷的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星环绕太阳运转一样。iiiiiiiiiiiiiiii金箔a粒子讨论:为什么有的a粒子可以穿透金箔,有的不行?你能解释其中的道理吗?金原子不为实心球体,中间有个核。原子 原子核蚂蚁 5 mm200 m原子可分怎么分的呢?一、原子的构成原 子(带正电)(带正电)(带负电)(不带电)思考1:请结合表3-1,以氧原子为例说明原子是怎样构成的。表3-1表3-2(不带电)思考2:原子是由带电的粒子构成的,
但是原子不显电性?为什么? 每个质子带一个
单位正电荷每个电子带一个
单位负电荷小结【思考2小结】:
1、原子是由居于原子中心、带_____的原子核和核外带___ ___ 的电子构成,原子核是由_______和______构成。由于它们所带的电荷数_______ ,电性 ,所以整个原子______(填显或不显)电性。
2、 = = 。正电负电质子中子相等相反不显核电荷数质子数核外电子数观察表格(表3-1) ,你能获得哪些信息?1、构成原子的粒子一般是质子、中子、电子2.在原子中,质子数=电子数3.质子数和中子数不一定相等4.不同种类的原子, 质子数不相同,核外电子数也不相同=核电荷数不是所有的原子都有中子,氢原子的中子数为0 。一个氧原子是由8个质子、8个中子和 8个电子构成的。1、质子带正电,中子不带电,电子带负电。3、质子和中子的质量很小,但比电子大很多,2、中子不带电,所以原子核的电性由质子决定,因此原子核带正电。原子的质量主要集中在 。原子核表3-2 构成原子的粒子的电性和质量课堂练习
1、据报道,1994年12月科学家发现了
一种新元素,它的原子核内有质子111个,
中子161个,则该元素核外电子____。111 3、在原子里质子数等于( )
(A)中子数 (B)电子数
(C)中子数和电子数之和 (D)原子量
B2、不显电性的一组粒子是( )
A、质子、中子、电子 B、原子核、原子、分子
C、中子、电子、原子 D、中子、原子、分子D4、下列关于原子核的说法中正确的是(? ? ) A、原子的质量主要集中在原子核中? ? ? ? ? B、任何原子核都是由质子和中子构成 C、有的原子的核电荷数不等于核内质子数 D、原子核的体积占原子的大部分A5、下列叙述中错误的是(? )
①原子是化学变化中的最小粒子
②原子是不能再分的粒子
③一切物质都是由原子直接构成的
④一切原子核都是由质子和中子构成的
⑤原子不显电性
⑥原子之间有间隔
A.①和②? ? ? ? B.②③和④? ? ?
C.③和⑤? ? ? ?D.③和⑥B6、在分子、原子、原子核、质子、中子、电子这些粒子中:
1) 能直接构成物质的粒子有___________
能保持物质化学性质的粒子有___________
2)? 显示电中性的粒子有______________
质量最小的粒子有___________________
3)? 带正电的粒子有___________________
带负电的粒子有___________________
4)? 在同一原子中数目一定相等的_____________分子、原子分子分子、原子、中子电子质子、原子核电子质子和电子我来小结:展示自己
让我们共同分享你的喜悦(带正电) 化学就象你头顶上的果实,
只要肯稍作努力,成功的
甜蜜就属于你!
祝你成功!谢谢指导 再见
和氢 ,每 个氧原子重新组合一个氧 ,每 个氢原子重新组合一个氢 。
3、由此可知:分子是由 构成的,分子在化学反应中可以再分成 ,而原子在化学变化中却 ,即原子是 。分子 原子 两两分子 分子 原子 化学变化中的最小的粒子原子 不可再分原子 1、1个水分子是由 和 构成的。 两个氢原子一个氧原子原子真是最小的粒子吗?
在任何情况下原子都不能再分吗?
课题 2 原子的结构第三单元 物质构成的奥秘第1课时道尔顿于1803年提出科学假说:物质由原子组成,原子是不可分割的实心球体,同种原子的性质和质量相同.原子的发现历程改写这一论断的是科学家汤姆生。原子的发展历程 1897年,英国物理学家汤姆生发现电子,认为原子的模型为枣糕型,原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子原子是不是不可分割的实心球体? 1909年至1911年,英国物理学家卢瑟福和他的合作者通过α粒子的散射实验,提出了原子结构的核式结构学说。 即:在原子的中心有一个带正电荷的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星环绕太阳运转一样。iiiiiiiiiiiiiiii金箔a粒子讨论:为什么有的a粒子可以穿透金箔,有的不行?你能解释其中的道理吗?金原子不为实心球体,中间有个核。原子 原子核蚂蚁 5 mm200 m原子可分怎么分的呢?一、原子的构成原 子(带正电)(带正电)(带负电)(不带电)思考1:请结合表3-1,以氧原子为例说明原子是怎样构成的。表3-1表3-2(不带电)思考2:原子是由带电的粒子构成的,
但是原子不显电性?为什么? 每个质子带一个
单位正电荷每个电子带一个
单位负电荷小结【思考2小结】:
1、原子是由居于原子中心、带_____的原子核和核外带___ ___ 的电子构成,原子核是由_______和______构成。由于它们所带的电荷数_______ ,电性 ,所以整个原子______(填显或不显)电性。
2、 = = 。正电负电质子中子相等相反不显核电荷数质子数核外电子数观察表格(表3-1) ,你能获得哪些信息?1、构成原子的粒子一般是质子、中子、电子2.在原子中,质子数=电子数3.质子数和中子数不一定相等4.不同种类的原子, 质子数不相同,核外电子数也不相同=核电荷数不是所有的原子都有中子,氢原子的中子数为0 。一个氧原子是由8个质子、8个中子和 8个电子构成的。1、质子带正电,中子不带电,电子带负电。3、质子和中子的质量很小,但比电子大很多,2、中子不带电,所以原子核的电性由质子决定,因此原子核带正电。原子的质量主要集中在 。原子核表3-2 构成原子的粒子的电性和质量课堂练习
1、据报道,1994年12月科学家发现了
一种新元素,它的原子核内有质子111个,
中子161个,则该元素核外电子____。111 3、在原子里质子数等于( )
(A)中子数 (B)电子数
(C)中子数和电子数之和 (D)原子量
B2、不显电性的一组粒子是( )
A、质子、中子、电子 B、原子核、原子、分子
C、中子、电子、原子 D、中子、原子、分子D4、下列关于原子核的说法中正确的是(? ? ) A、原子的质量主要集中在原子核中? ? ? ? ? B、任何原子核都是由质子和中子构成 C、有的原子的核电荷数不等于核内质子数 D、原子核的体积占原子的大部分A5、下列叙述中错误的是(? )
①原子是化学变化中的最小粒子
②原子是不能再分的粒子
③一切物质都是由原子直接构成的
④一切原子核都是由质子和中子构成的
⑤原子不显电性
⑥原子之间有间隔
A.①和②? ? ? ? B.②③和④? ? ?
C.③和⑤? ? ? ?D.③和⑥B6、在分子、原子、原子核、质子、中子、电子这些粒子中:
1) 能直接构成物质的粒子有___________
能保持物质化学性质的粒子有___________
2)? 显示电中性的粒子有______________
质量最小的粒子有___________________
3)? 带正电的粒子有___________________
带负电的粒子有___________________
4)? 在同一原子中数目一定相等的_____________分子、原子分子分子、原子、中子电子质子、原子核电子质子和电子我来小结:展示自己
让我们共同分享你的喜悦(带正电) 化学就象你头顶上的果实,
只要肯稍作努力,成功的
甜蜜就属于你!
祝你成功!谢谢指导 再见
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
