人教版化学九年级上册第六单元 碳和碳的氧化物课题2 二氧化碳制取的研究 教案
文档属性
| 名称 | 人教版化学九年级上册第六单元 碳和碳的氧化物课题2 二氧化碳制取的研究 教案 |

|
|
| 格式 | zip | ||
| 文件大小 | 45.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-07 00:00:00 | ||
图片预览


文档简介
《二氧化碳制取的研究》教案
【学习目标】?
1、在教师的指导下,通过阅读与分析能准确的用化学方程式表达实验室制取二氧化碳的反应原理。
2、通过阅读、讨论和分析气体发生装置和收集装置应考虑的因素,自己设计制取二氧化碳的装置,然后利用设计的装置制取二氧化碳,
3、在新情境下通过观察和分析二氧化碳的性质,准确的找出验满二氧化碳的方法以及检验二氧化碳的方法。
4、在新情境下通过同伴讨论,在教师的提示下总结出实验室制取气体的思路和方法。
【重难点?】
1、指导学生掌握制取气体时实验仪器和收集方法的选择。
2、从实验室制取气体的设计思路和方法出发,学习二氧化碳的实验室制法。
教具准备?:试管、铁架台、锥形瓶、长颈漏斗、导管、橡胶塞、雪碧、澄清石灰水、药匙、镊子、大理石、碳酸钠、稀盐酸、稀硫酸
【导入新课】
首先请看“雪碧”产生的气体通入到澄清石灰水中发生的现象。请问这是什么气体
学生:二氧化碳。
教师:我们到底如何来制取较纯净二氧化碳呢?
【提问:】实验室制取气体,应考虑哪些因素?提示请以实验室制取氧气为例。
学生:药品选择、反应原理、装置选择、收集方法、检验方法、验满方法、操作步骤及注意事项
【多媒体展示】含碳酸根离子的化合物?[例:碳酸钠Na2CO3、大理石或石灰石主要成分是CaCO3]能与稀盐酸(HCl)或稀硫酸(H2SO4)反应生成二氧化碳。
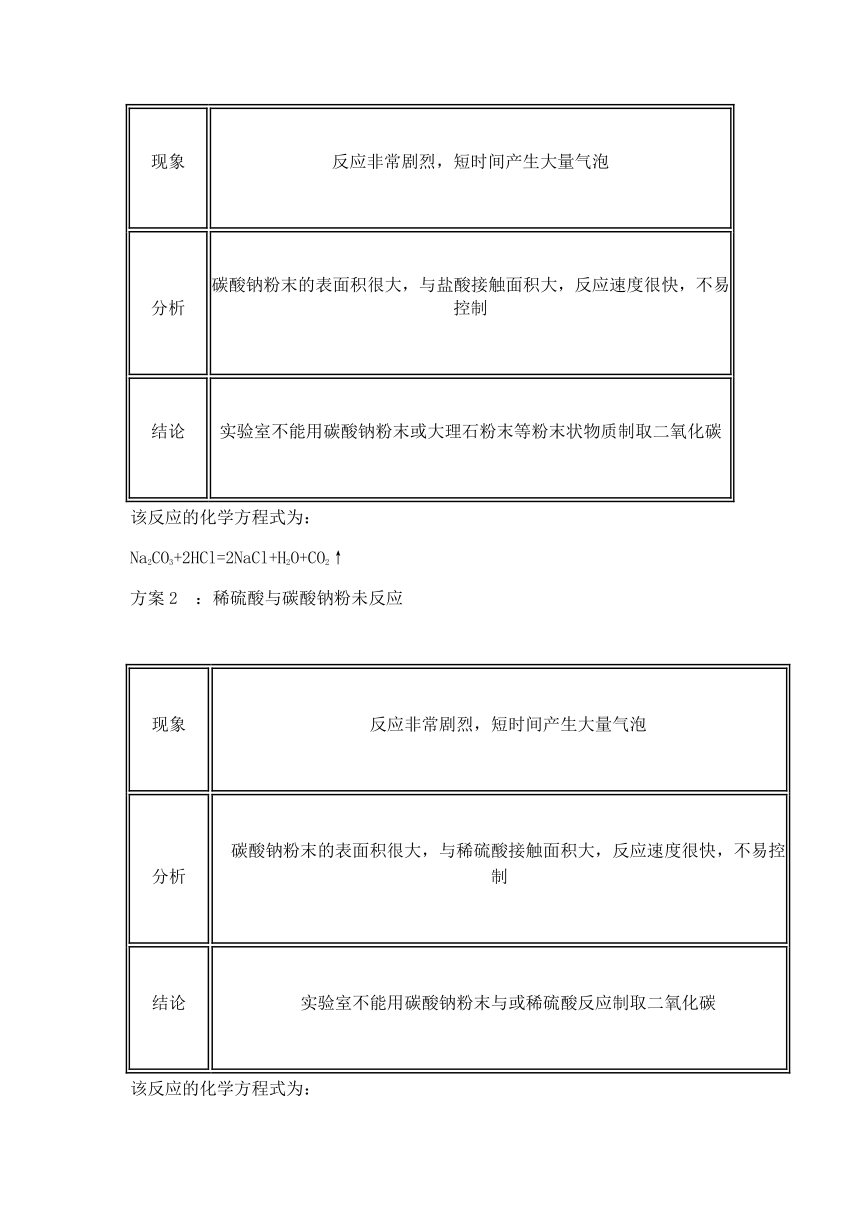
【复习展示】方案1?:稀盐酸与碳酸钠粉末反应
???????????
?现象? ?反应非常剧烈,短时间产生大量气泡?
?分析? ?碳酸钠粉末的表面积很大,与盐酸接触面积大,反应速度很快,不易控制?
?结论? ?实验室不能用碳酸钠粉末或大理石粉末等粉末状物质制取二氧化碳?
该反应的化学方程式为:
Na2CO3+2HCl=2NaCl+H2O+CO2↑
方案2?:稀硫酸与碳酸钠粉未反应
???????????
?现象? ??反应非常剧烈,短时间产生大量气泡?
?分析? ??碳酸钠粉末的表面积很大,与稀硫酸接触面积大,反应速度很快,不易控制?
?结论? ??实验室不能用碳酸钠粉末与或稀硫酸反应制取二氧化碳?
该反应的化学方程式为:
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
方案3:稀硫酸与大理石(或石灰石)反应
???????????
?现象? ?刚开始有大量气泡产生,一段时间后,气泡逐渐减少 ,反应逐渐停止。?
?分析? ?虽然该反应能生成二氧化碳:CaCO3+H2SO4=CaSO4+H2O+CO2↑?但生成的CaSO4微溶于水,覆盖在大理石表面,形成一层薄膜,使大理石与酸不能接触,反应难以进行。?
?结论? ?实验室制取二氧化碳不能用稀硫酸代替稀盐酸?
方案4:稀盐酸与大理石(或石灰石)反应
???????????
?现象? ??有大量气泡产生,固体物质逐渐减少,反应速率适中。?
?分析? ??该反应能均匀产生气体,速率适中,便于收集,适用于实验室制取二氧化碳,该反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑?
?结论? ??实验室常用稀盐酸与大理石(或石灰石)反应来制取二氧化碳?
(板书:一、实验室制取二氧化碳原理的探究1?、药品:大理石或石灰石和稀盐酸2、反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑)
【设问】在有药品和知道反应原理的前提下我们要如何选择制取二氧化碳气体的装置呢?
【多媒体展示】怎样设计实验室制取气体的装置(见课本P110)
【问题与讨论】1、填表比较二氧化碳和氧气的性质;想一想实验室制取二氧化碳的装置是否与制取氧气的装置相同?为什么?
2、在设计二氧化碳制取装置时可以选用哪些仪器,所选用的部分仪器可用生活中的哪些物品来代替?
【参考装置】
1、气体发生装置(教师展示给学生)
2、气体收集装置
【讨论】
二氧化碳气体能不能用排水法收集,为什么??
【多媒体展示】实验室里可用下列装置来制取二氧化碳
(板书:二、实验室制取二氧化碳的装置:1、发生装置:固液常温型2、收集装置:向上排空气法)
【讨论】
1、怎样检验生成的气体是二氧化碳?
2、怎样检验二氧化碳是否收集满?
3、讨论并归纳实验室制取二氧化碳的操作步骤
仪器连接→检查气密性→加大理石→加稀盐酸→收集气体
【学生实验探究】
通过讨论,各小组组装一套制取二氧化碳的实验装置,并制取一瓶二氧化碳气体
【课堂练习1】
1、实验室中检验二氧化碳用____________;
2、实验室中检验氧气用________________;
3?、实验室中验满二氧化碳用____________ _____________________;
4、实验室中验满氧气(向上排空气法)用____________________________;实验室中用排水法收集氧气时看到________________现象时说明氧气已经满了。
【课堂练习2】5.下图为实验室制取二氧化碳的装置图,有哪些错误?请改正。
6.某同学利用下图做制取二氧化碳的装置图,回答下列问题:
(1)当左边气体发生装置连接好了之后,接着应进行的步骤是________________。
(2)实验时,加入试剂的顺序_________。
(3)收集时,导管接近集气瓶底部的原因是______________________________________。
(4)长颈漏斗下端插入液面以下的原因是_____________________________________。
【拓展练习】
通常状况下,氢气(H2)是一种无色无味的气体,密度比空气小,难溶于水;实验室用锌粒(Zn)和稀硫酸(H2SO4)反应在常温下制取它,请你根据已学知识设计一套实验室制取氢气的装置。
【拓展升华】
实验室制取气体的思路和方法
(1)选择适当的反应,包括反应物和反应条件
(2)选择合适的实验发生装置
(3)选择合适的实验收集装置
【课堂小结】本节课我们主要学习了实验室制取二氧化碳的反应原理和反应装置,并了解实验室制取气体的一般思路和方法,今后我们还要学习更多气体的制取方法和装置,应及时归纳总结。
【课外作业】
1. 自已利用生活生活中的一些生活用品组装一套制取二氧化碳的装置
2. 【板书设计】
一、实验室制取二氧化碳原理的探究
1?、药品:大理石或石灰石和稀盐酸
2、反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
二、实验室制取二氧化碳的装置:
1、发生装置:固液常温型
2、收集装置:向上排空气
3、验满:用燃着的木条放在集气瓶口,熄灭则满
4、检验:倒入澄清的石灰水,振荡变浑浊则是二氧化碳
?
?
【课后反思】
本节课是初中化学重要的实验探究课,知识性与实验性都很强。学生通过学习应能够根据反应原理选择合理的制取气体的仪器,但是还要给学生一定的自我探究空间才可以使学生掌握的更好,学生分组实验时,教师应及时指出学生做错的步骤,以提高学生的实验技能。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
