人教版化学九年级下册第九单元 溶液单元复习与测试
文档属性
| 名称 | 人教版化学九年级下册第九单元 溶液单元复习与测试 |  | |
| 格式 | zip | ||
| 文件大小 | 233.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-07 17:55:04 | ||
图片预览




文档简介
第九单元《溶液》测试题
一、单选题(每小题只有一个正确答案)
1.物质的性质决定其用途,下列说法不正确的是( )
A.甲烷作燃料,是因为甲烷具有可燃性
B.铜作导线,是因为铜具有良好的导电性
C.洗洁精洗涤油污,是因为洗洁精能溶解油污
D.活性炭除冰箱异味,是因为活性炭具有吸附性
2.下列去污原理属于乳化作用的是( )
A.汽油除油污 B.洗发精洗发
C.酒精擦拭摄像机磁头 D.干洗店干洗衣物
3.将下列物质分别放入水中,能形成乳浊液的是( )
A.白醋 B.食用油 C.食盐 D.酒精
4.现有溶质质量分数为8%的食盐水40g,要使溶质质量分数达到20%,以下说法正确的是( )
A.加入食盐4g B.蒸发水分20g
C.蒸发水分24g D.加入质量分数为8%的食盐水40g
5.如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
A.t2℃时,三种物质的溶解度是a>b>c
B.t2℃时,将a物质50g(不含结晶水)放入100g水中充分溶解得到a的饱和溶液
C.将t2℃时,三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a=c
D.升温可将c的不饱和溶液变为饱和溶液
6.科学的学习要注意对概念的理解。下列有关“一定”的叙述正确的是( )
A.溶液中一定含有水
B.溶液一定由两种或两种以上物质组成
C.无色透明的液体一定是溶液
D.饱和溶液的溶质质量分数一定比不饱和溶液的大
7.实验室用氯化钠配制 50.0g 溶质的质量分数为 10%的氯化钠溶液,下列说法错误的是( )
A.用天平称取 5.0g 氯化钠
B.用量程为 10ml 的量筒量取所需的水
C.溶解氯化钠时,使用的玻璃仪器有烧杯、玻璃棒
D.将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签
8.对图所示溶液的认识中,不正确的是( )
A.是稳定均一的混合物 B.溶质为NaCl
C.溶质和溶剂的质量比为1:10 D.溶质质量分数为10%
9.下列实验不能达到目的的是( )
A.探究铁、铝、铜的活动性强弱 B.探究CO2是否与水发生了反应 C.探究影响反应速率的因素 D.探究温度对物质溶解速率的影响
A.A B.B C.C D.D
10.推理是学习化学的一种重要方法,下列推理正确的是( )
A.氧化物中含有氧元素,所以含有氧元素的化合物都是氧化物
B.溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小
C.碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
11.如图为甲、乙两种固体物质的溶解度曲线,下列有关说法中错误的是( )
A.40℃时,两种物质的饱和溶液的溶质质量分数相等
B.60℃时,将甲、乙的饱和溶液都蒸发掉10g水,析出甲的晶体质量比析出乙的晶体质量大
C.20℃时,甲物质的溶解度比乙物质的溶解度大
D.60℃时,将30g甲物质放入50g水中,所得溶液中溶质质量与溶剂质量之比是3:5
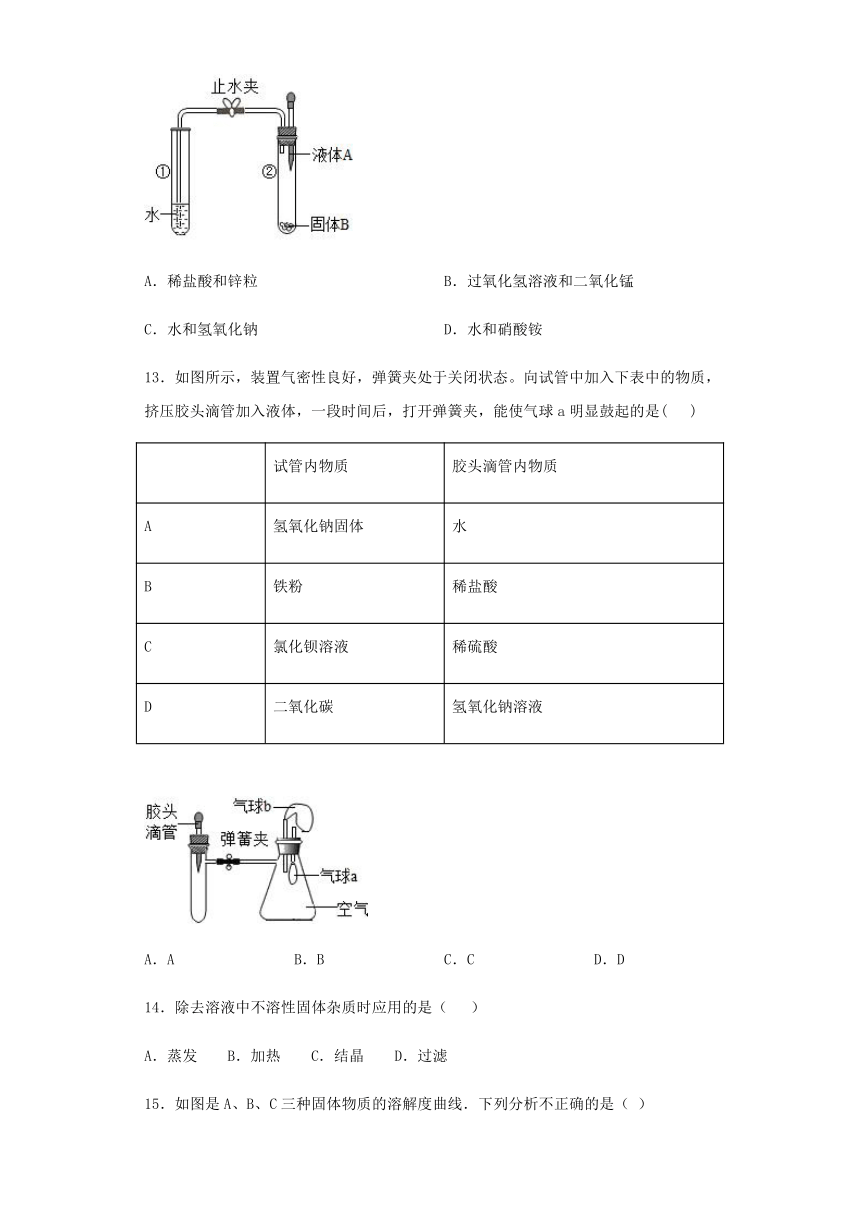
12.如图所示,将液体A滴入试管②中与固体B接触,一段时间后打开止水夹,若试管①中的导管口有气泡产生,则液体A和固体B的组合不可能是( )
A.稀盐酸和锌粒 B.过氧化氢溶液和二氧化锰
C.水和氢氧化钠 D.水和硝酸铵
13.如图所示,装置气密性良好,弹簧夹处于关闭状态。向试管中加入下表中的物质,挤压胶头滴管加入液体,一段时间后,打开弹簧夹,能使气球a明显鼓起的是( )
试管内物质 胶头滴管内物质
A 氢氧化钠固体 水
B 铁粉 稀盐酸
C 氯化钡溶液 稀硫酸
D 二氧化碳 氢氧化钠溶液
A.A B.B C.C D.D
14.除去溶液中不溶性固体杂质时应用的是( )
A.蒸发 B.加热 C.结晶 D.过滤
15.如图是A、B、C三种固体物质的溶解度曲线.下列分析不正确的是( )
A.50℃时,三种物质的溶解度由大到小的顺序是A>B>C
B.50℃时,把50gA放入50g水中能形成75gA的饱和溶液
C.将C的饱和溶液变为不饱和溶液,可采用降温的方法
D.分别将三种物质的饱和溶液从50℃将至20℃时,所得溶液溶质质量分数大小关系是B>C=A
二、填空题
16.用固体配制:
(1)步骤:________、________、________、________。
(2)仪器:________、________、________、________、________、________。
17.某兴趣小组的同学探究分子的运动,实验如下图所示。图中试管A和装置D的试管中装有体积和浓度相同的浓氨水,试管B和C中装有体积和浓度相同的酚酞溶液。
(1)实验①和实验②都会出现的现象是______,但出现此现象的快慢不同。
(2)请从微观的角度解释产生上述现象快慢不同的原因是______。
18.如图所示是A、B两种固体物质的溶解度曲线,根据曲线回答下列问题:
①在 ℃时,A、B两物质的溶解度相等.
②在t2℃时,将30g固体A加入50g水中,充分溶解后所得溶液的质量 g.
③在t2℃时,要使A得不饱和溶液变为饱和溶液,可采取得方法 (填一种).
④在t2℃时,等质量的A、B两种固体物质分别加入水中,都完全溶解得到的饱和溶液质量A B.(填 “>”,“=”,“<”)
19.20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到四个各盛有50g水的烧杯中,充分溶解,其溶解情况如下表:
物质 甲 乙 丙 丁
未溶解固体的质量/g 4.2 2 0 9.2
(1)所得四杯溶液 ______ 一定是饱和溶液.
(2)如何判断丙溶液是否为饱和溶液 ______ .
(3)向乙溶液中继续加入3g乙物质,此时乙溶液质量为 ______
(4)四杯溶液中溶剂的质量大小为 ______ .
20.如图为甲、乙、丙三种物质的溶解度曲线。
(1)从甲的饱和溶液中得到甲,可采用的方法是_____;
(2)将t3℃时甲、乙、丙的饱和溶液降温到t1℃,三种溶液溶质的质量分数由大到小的关系是_____;
(3)将t2℃时80g甲的饱和溶液和70g水混合,所得溶液溶质的质量分数为_____。
三、推断题
21.某化学第二课堂小组利用已学过的知识,准备利用含FeSO4和CuSO4的废水(无其他难溶杂质),从中获得硫酸亚铁晶体,其流程如下图所示:
(1)整个流程中,进行了两次操作1,操作1是_____________(填操作名称)。
(2)金属X 是______(填化学符号),其加入废水后发生反应的化学方程式为:____________;固体A中含有__________(填化学符号)。写出固体A与稀硫酸反应的化学方程式为:____________________。
(3)通过冷却结晶法得到硫酸亚铁晶体前需要进行操作2,请问操作2是________。
22.A、B、C、D、E、F均是初中化学中的常见物质,其中A、D为单质,其余均为化合物,B、C由两种相同元素组成。
(1)A在D中完全燃烧和不完全燃烧时,生成不同的气体。B溶液在一定条件下可反应生成C和无色气体D,C和D都与生命活动息息相关。B溶液中的溶质是 (用化学式表示)
(2)如图所示将固体E放入大烧杯中的水里,小烧杯中F的饱和溶液变浑浊。
则E的化学式可能为 ,产生此现象的原因是 。
四、实验题
23.实验室中,利用下列装置可以制取某些气体,请回答下列问题。
⑴写出带标号的仪器的名称:① ;② 。
⑵向气体发生装置内加入药品前,应该进行的操作是 。
⑶实验室若用高锰酸钾制取氧气,选择的发生装置是 ;用双氧水制氧气的化学方程式为 ;
⑷能用C装置收集的气体,必须具备的性质是 ;
⑸乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔。你认为制取乙炔应选择的发生装置是 ;收集装置是 (此空2分,回答不全将酌情扣分)。
24.在进行“一定溶质质量分数的氯化钠溶液的配制”实验活动中出现以下错误操作:
A氯化钠放在右盘 B氯化钠洒出 C俯视读数 D配好的溶液装瓶时洒出
(1)其中不影响所配溶液浓度的操作是_________(填序号)。
(2)造成所配溶液浓度偏大的操作为______(填序号),其原因是_____________。
五、计算题
25.如图是浓盐酸试剂瓶上标签的部分内容.请回答:
(1)该浓盐酸的溶质是________(填名称);
(2)现要配制的稀盐酸120g,需要这种浓盐酸________g.(写出计算过程)
26.为测定某大理石样品(含少量氯化钙和的不溶性杂质,杂质不参加化学反应)中碳酸钙的含量,取样品放入烧杯中,再向烧杯中加入稀盐酸,恰好完全反应。经测定烧杯内物质的总质量为(产生的气体全部逸出)计算
(1)生成二氧化碳的质量
(2)样品中碳酸钙的质量分数
(3)反应后所得溶液中溶质的质量分数(保留到)
参考答案
1.C 2.B 3.B 4.C 5.C 6.B 7.B 8.C 9.C 10.C 11.C 12.D 13.D 14.D 15.D 16.计算 称量 溶解 装瓶保存 托盘天平 药匙 量筒 胶头滴管 烧杯 玻璃棒
17.酚酞溶液变红色其他条件相同时,温度不同,分子运动速率不同(温度高时,分子运动速率加快)
18.①t1;②60;③加入A物质(或蒸发溶剂、降低温度);④<.
19. 甲、乙、丁 取样,向丙溶液中加入少量的丙物质,看是否继续溶解 68g 甲=乙=丙=丁
20.降温结晶 乙>甲>丙 20%
21. 过滤 Fe Fe + CuSO4=Cu + FeSO4 Cu、Fe Fe + H2SO4 =FeSO4 + H2↑ 蒸发(或者蒸发浓缩)
22.H2O2、NaOH或CaO,
23.(1)①铁架台 ②集气瓶 (2)检查装置的气密性
(3)A; 2H2O22H2O+O2↑
(4)密度比空气小且不与空气中的物质反应
(5)B; E
24.D C 量取水时,俯视刻度会造成所量取的水少于所需要的水
25.氯化氢0.5解:设需要这种浓盐酸的质量为x,根据溶液稀释前后溶质的质量不变,则:120g×3%=x×36%,x=10g。
26.(1)17.6g;(2)80%;(3)14.7%
同课章节目录
