2019——2020学年选修4人教版 第四章 第二节 化学电源(强化训练)
文档属性
| 名称 | 2019——2020学年选修4人教版 第四章 第二节 化学电源(强化训练) |

|
|
| 格式 | zip | ||
| 文件大小 | 404.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-10 00:00:00 | ||
图片预览



文档简介
第二节 化学电源
一、选择题
1.下列电池工作时,O2在正极放电的是( )
A.锌锰电池 B.氢燃料电池 C.铅蓄电池 D.镍镉电池
答案 B
2.铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的电池反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O,下列结论正确的是( )
A.Pb为正极,被氧化
B.溶液的pH不断减小
C.SO只向PbO2处移动
D.电解质溶液pH不断增大
答案 D
3.电子表和电子计算器的电源通常用微型银—锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应式为Ag2O+H2O+Zn===Zn(OH)2+2Ag。下列说法正确的是( )
A.Ag2O是正极,Zn是负极
B.Zn是正极,Ag2O是负极
C.工作时,电池负极区溶液pH增大
D.工作时,电子由Ag2O极经外电路流向Zn极
答案 A
4.一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通入乙烷和氧气,其电极反应式为C2H6+18OH--14e-===2CO+12H2O、7H2O+7/2O2+14e-===14OH-,有关此电池的推断正确的是( )
A.通氧气的电极为负极
B.参加反应的氧气与C2H6的物质的量之比为7∶2
C.放电一段时间后,KOH的物质的量浓度不变
D.电解质溶液中,CO向正极移动
答案 B
5.以氨气代替氢气来研发氨燃料电池是当前科研的一个热点,氨燃料电池使用的电解质溶液是KOH溶液,电池反应为4NH3+3O22N2+6H2O。下列有关说法错误的是( )
A.氨燃料电池在充电时,在阴极N2得电子被氧化
B.氨燃料电池在放电时,负极反应为2NH3-6e-+6OH-===N2+6H2O
C.以氨气代替氢气的主要原因是氨气易液化、易储存
D.燃料电池的能量转化率一般比普通的电池高
答案 A
6.甲醇燃料电池(DMFC)可用于笔记本电脑、汽车、遥感通讯设备等,它的一极通入甲醇,一极通入氧气;电解质是质子交换膜,它能传导氢离子(H+)。电池工作时,甲醇被氧化为二氧化碳和水,氧气在电极上的反应是O2+4H++4e-===2H2O。下列叙述中不正确的是( )
A.负极的反应式为CH3OH+H2O-6e-===CO2↑+6H+
B.电池的总反应式是2CH3OH+3O2===2CO2+4H2O
C.电池工作时,H+由正极移向负极
D.电池工作时,电子从通入甲醇的一极流出,经外电路流入通氧气的一极
答案 C
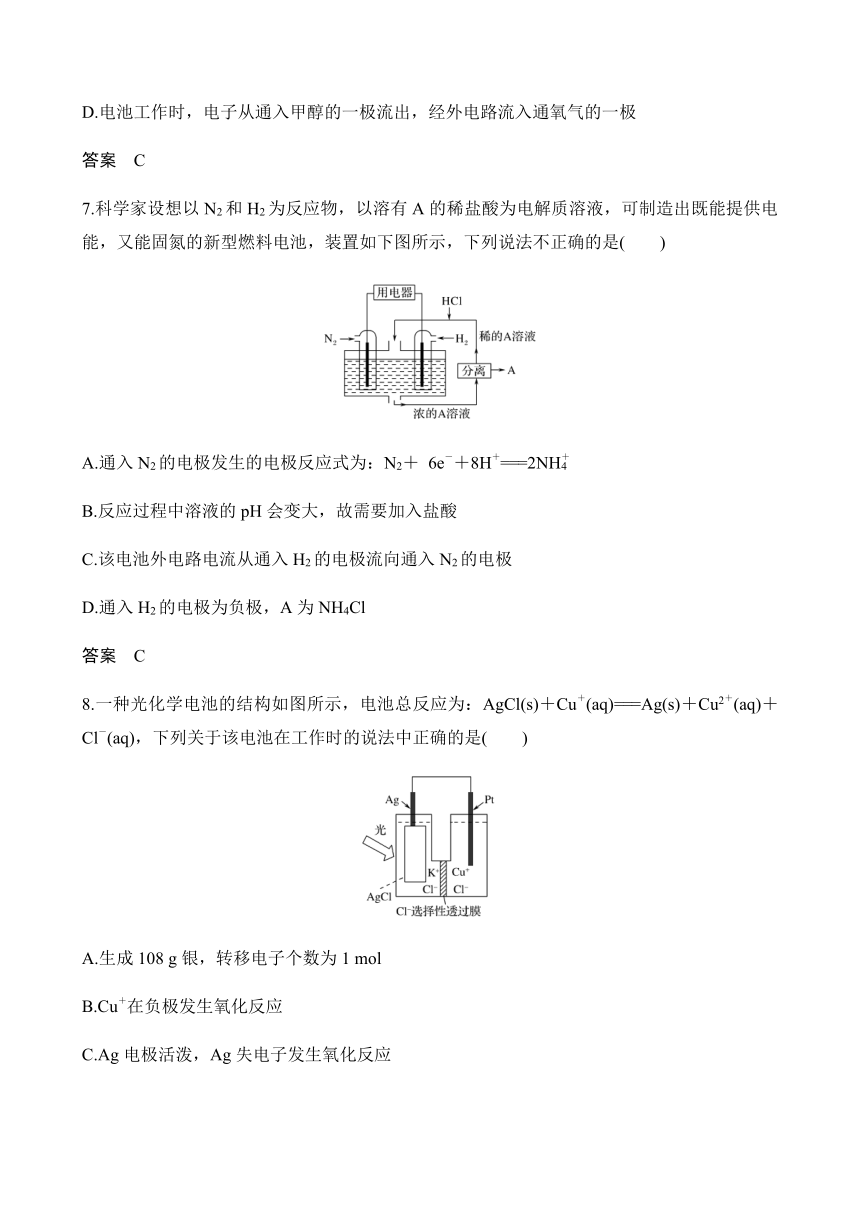
7.科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,下列说法不正确的是( )
A.通入N2的电极发生的电极反应式为:N2+ 6e-+8H+===2NH
B.反应过程中溶液的pH会变大,故需要加入盐酸
C.该电池外电路电流从通入H2的电极流向通入N2的电极
D.通入H2的电极为负极,A为NH4Cl
答案 C
8.一种光化学电池的结构如图所示,电池总反应为:AgCl(s)+Cu+(aq)===Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法中正确的是( )
A.生成108 g银,转移电子个数为1 mol
B.Cu+在负极发生氧化反应
C.Ag电极活泼,Ag失电子发生氧化反应
D.Cl-由负极迁移到正极
答案 B
9.科学家成功开发出便携式固体氧化物燃料电池,它以丙烷气体为燃料。电池中的一极通入空气,另一极通入丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-。下列对该燃料电池的说法不正确的是( )
A.在熔融电解质中,O2-由负极移向正极
B.该电池的总反应是C3H8+5O2===3CO2+4H2O
C.电路中每通过5 mol电子,约有5.6 L标准状况下的丙烷被完全氧化
D.通入丙烷的电极为电池负极,发生的电极反应为
C3H8-20e-+10O2-===3CO2+4H2O
答案 A
10.MFC(Microbial Fuel Cell)是一种利用微生物将有机物中的化学能直接转化成电能的装置,其在废水处理和新能源开发领域具有广阔的应用前景。如图为污水(主要溶质为葡萄糖)处理的实验装置,下列有关该装置的说法正确的是( )
A.为加快处理速度,装置需在高温环境中工作
B.负极的电极反应式为C6H12O6+6H2O-24e-===6CO2+24H+
C.放电过程中,H+由正极向负极移动
D.装置工作过程中,溶液的酸性逐渐增强
答案 B
11.如图是一种航天器能量储存系统原理示意图。下列说法正确的是( )
A.该系统中只存在3种形式的能量转化
B.装置Y中负极的电极反应式为O2+2H2O+4e-===4OH-
C.装置X能实现燃料电池的燃料和氧化剂再生
D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化
答案 C
二、非选择
12.设计出燃料电池使汽油氧化直接产生电流是本世纪最富有挑战性的课题之一。最近有人制造了一种燃料电池,一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-。回答如下问题:
(1)以丁烷代表汽油,写出这个电池放电时发生的化学反应的化学方程式:____________________________________________________________。
(2)写出这个电池的正极发生的反应:_______________________
____________________________________________________________。
负极发生的反应:_____________________________________________。
固体电解质里的O2-的移动方向是________________________________。
向外电路释放电子的电极是_____________________________________。
解析 由原电池原理知:负极失去的电子经导线转移到正极,根据电中性关系,内电路中,O2-向负极移动。
答案 (1)2C4H10+13O2===8CO2+10H2O
(2)O2+4e-===2O2- C4H10+13O2--26e-===4CO2+5H2O 向负极移动 负极
13.氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉。铂吸附气体的能力强,性质稳定。请回答:
(1)氢氧燃料电池能量转化的主要形式是__________________,在导线中电子流动方向为______(用a、b表示)。
(2)负极反应式为________。
(3)电极表面镀铂粉的原因是_____________________________________
____________________________________________________________。
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H22LiH
Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是______,反应Ⅱ中的氧化剂是______。
②已知LiH固体密度为0.82 g·cm-3,用锂吸收224 L(标准状况)H2,生成的LiH体积与被吸收的H2体积比值为____________。
③由②生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为________mol。
解析 (1)原电池的实质为化学能转化成电能,总反应为2H2+O2===2H2O,其中H2在负极失电子,即电子从a流向b。(2)负极为H2失电子生成H+,但溶液为KOH溶液,故负极反应为H2-2e-+2OH-===2H2O。(3)铂粉的接触面积大,可以增大电极单位面积吸附H2、O2分子数,可以加快反应速率。(4)①反应Ⅰ中Li从0价升至+1价,为还原剂,反应Ⅱ中H2O中的H从+1价降至0价,为氧化剂。②在反应Ⅰ中当吸收10 mol H2时,生成20 mol LiH,V==×10-3 L=195.12×10-3 L,则==8.71×10-4。③反应Ⅱ中20 mol LiH可生成20 mol H2,实际参加反应的H2为20 mol×80%=16 mol,每1 mol H2生成H2O时,转移2 mol电子,故导线中通过电子的物质的量为16 mol×2=32 mol。
答案 (1)化学能转变为电能 a流向b
(2)H2-2e-+2OH-===2H2O
(3)增大电极单位面积吸附H2、O2的分子数,加快反应速率
(4)①Li H2O ②8.71×10-4(或) ③32
14.酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物。该电池放电过程产生MnOOH。回收处理该废电池可得到多种化工原料。有关数据如下表所示:
溶解度/(g/100 g水)
温度/℃化合物 0 20 40 60 80 100
NH4Cl 29.3 37.2 45.8 55.3 65.6 77.3
ZnCl2 343 395 452 488 541 614
化合物 Zn(OH)2 Fe(OH)2 Fe(OH)3
Ksp近似值 10-17 10-17 10-39
回答下列问题:
(1)该电池的正极反应式为________________________________________,
电池反应的离子方程式为______________________________________。
(2)维持电流强度为0.5 A,电池工作5分钟,理论上消耗锌________g。(已知F=96 500 C·mol-1)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过________分离回收;滤渣的主要成分是MnO2、________和________,欲从中得到较纯的MnO2,最简便的方法为________,其原理是____________________________________________________________。
答案 (1)MnO2+H++e-===MnOOH 2MnO2+Zn+2H+===2MnOOH+Zn2+
[注:式中Zn2+可写为Zn(NH3),Zn(NH3)2Cl2等,H+可写为NH]
(2)0.05
(3)加热浓缩、冷却结晶 碳粉 MnOOH 在空气中加热 碳粉转变为CO2,MnOOH氧化为MnO2
