苏教版高中化学必修一专题3 第一单元 从铝土矿到铝合金 课件(共23张PPT)
文档属性
| 名称 | 苏教版高中化学必修一专题3 第一单元 从铝土矿到铝合金 课件(共23张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-12 00:00:00 | ||
图片预览








文档简介
(共23张PPT)
你在日常生活中见到过哪些铝制品?你能分析归纳出铝单质的物理性质和用途吗?
复习回忆
一、铝的物理性质与用途
银白色金属,密度小、有良好的导电导热性和延展性。可以用铝来制造电线和电缆,可作汽车、飞机、火箭材料,也能做各种铝质器皿
二、铝的原子结构
铝的原子结构示意图为
K Ca Na Mg Zn Fe Sn Pb H Cu Hg …
Al
Al的化学性质活泼,具有较强还原性
推进新课:
性质是由结构决定的,下面我们来复习铝的的原子结构
三、铝的化学性质
1 与非金属课件\铝与氧气反应.wmv(O2、Cl2 、S等)的反应
现象:
铝在氧气中剧烈燃烧,发出耀眼的白光。
反应方程式:
2.能写出Al和Cl2 、S反应的化学方程式吗?
2Al+3Cl2=2AlCl3
2Al+3S=Al2S3
△
△
结构决定性质,下面我们来学习铝的化学性质
过度:
问题探究
铝锅为什么可以用来煮饭?
铝具有良好的导热性能、常温下铝的表面被氧化,生成一层致密氧化物薄膜。
【观察与思考】:
取一块铝片,观察其表面的颜色.将铝片部分浸入4mol.L-1氢氧化钠溶液中,静置一段时间后取出,观察颜色变化.上述实验现象说明了什么?
现象:
浸入氢氧化钠溶液中的铝片表面变白
结论:
说明铝表面有氧化膜
阅读课本P64最上面一段了解铝制品的表面氧化着色
思考:
1 铝制餐具能否用清洁球擦洗?
2 加热铝片,有什么现象?说明什么?
2Al+6HCl= 2AlCl3+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
铝条未发生明显变化
铝条未发生明显变化
铝条上产生大量无色的气泡
铝条上产生大量无色的气泡
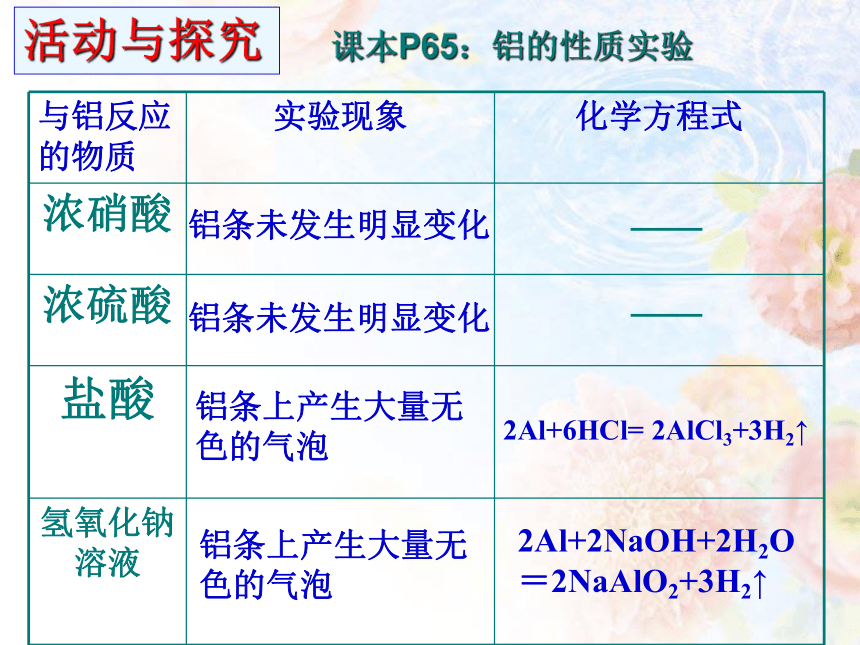
活动与探究
课本P65:铝的性质实验
与铝反应的物质 实验现象 化学方程式
浓硝酸
浓硫酸
盐酸
氢氧化钠溶液
交流与讨论
(2) 常温下,铝能与稀盐酸、氢氧化钠溶液反应放出气体,经检验为氢气。
< 1> 铝放入浓硫酸、浓硝酸中均未发生明显变化。
常温下,铝遇浓硫酸、浓硝酸时在表面生成致密的氧化膜而发生钝化
2Al+6HCl= 2AlCl3+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
原因?
练习:铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH物质的量之比为( )
A 1:1 B 2:1 C 3:1 D 1:3
C
2 与酸反应
A.与非氧化性酸反应<如盐酸﹑稀硫酸.>
B.与强氧化性酸反应 反应较复杂,但不生成氢气.
由上述探究和讨论可知铝的第二个化学性质为:
【推进新课】:
3 与强碱溶液反应
反应的机理:
铝与氢氧化钠反应是多步反应的结果:
2Al+6H2O==2Al(OH)3+3H2↑
+
﹙Al(OH)3+NaOH==NaAlO2+2H2O ﹚×2
2Al+6H2O+2NaOH==2NaAlO2+3H2↑+4H2O
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
标出铝与氢氧化钠反应的电子转移情况,并写出该反应的离子方程式。
③ 2Al+2H2O+2OH-==2AlO2- +3H2↑
① 2Al+6H2O+2NaOH==2NaAlO2+3H2↑+4H2O
失2×3 e-
得6×e-
试试看:
4 铝和盐溶液反应
根据金属活动性顺序的应用,铝能把排在它后面的金属从它们的盐溶液中置换出来,如:
2Al+3CuSO4 =3Cu+Al2(SO4)3
2Al+3Cu2+=3Cu+2Al3+
5 铝与某些氧化物反应RM\铝热反应.RM铝热反应.RM
现象:
化学方程式:
—铝热反应
发出耀眼的光芒、有熔融物生成。
2Al + Fe2O3 == 2Fe + Al2O3
高温
铝热剂
该反应的用途:
焊接铁轨、冶炼金属
实质:
Al与Fe2O3发生氧化还原反应
铝热反应用于焊接钢轨
焊接铁轨
铝热反应用于“定向爆破” ,主要是利用铝热反应熔断钢筋 使楼房定向倒塌
练习:
写出Al分别与Cr2O3 、 MnO2 、V2O5 的反应
铝化学性质活泼,反应中均作还原剂。
1、与非金属(O2、S、Cl2等)的反应
2、常温下,铝能与稀盐酸、氢氧化钠溶液反应放出氢气。
2Al+6HCl = 2AlCl3+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
总结与交流:
今天你学到了什么?
铝的物理性质与用途
4、铝与某些氧化物反应—铝热反应
3、铝和盐溶液反应
2Al+3CuSO4 =3Cu+Al2(SO4)3
5 铝跟水的反应
铝跟冷水几乎不反应,跟沸水能发生缓慢的反应
2Al+6H2O==2Al(OH)3+3H2↑
△
为什么铝制的炊具不能长时间盛放酸性、碱性或者含有食盐的食品?
阅读课本P66拓展视野后回答:
学生阅读P66拓展视野上面一段了解铝合金的性质及应用
1 除去镁粉中混有的少量铝粉,可选用下列溶液中的( )
A 盐酸 B 稀硫酸 C 氨水 D 浓氢氧化钾溶液
D
练习:
2、 取两份铝粉,一份投入足量浓氢氧化钠溶液中,一份投入足量盐酸中,充分反应,产生等量氢气。则两份铝粉的质量之比为:< >
A 1: 2 B 1: 3 C 3 : 2 D 1 : 1
D
4、 甲、乙两烧杯中各盛有100mL3 mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙= 1:2,则加入铝粉的质量为,< >
A.5.4g B.3.6g C.2.7g D.1.8g
A
C
3、 将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是( )
A.稀硝酸 B.稀盐酸 C.硝酸铜 D.氢氧化钠
你在日常生活中见到过哪些铝制品?你能分析归纳出铝单质的物理性质和用途吗?
复习回忆
一、铝的物理性质与用途
银白色金属,密度小、有良好的导电导热性和延展性。可以用铝来制造电线和电缆,可作汽车、飞机、火箭材料,也能做各种铝质器皿
二、铝的原子结构
铝的原子结构示意图为
K Ca Na Mg Zn Fe Sn Pb H Cu Hg …
Al
Al的化学性质活泼,具有较强还原性
推进新课:
性质是由结构决定的,下面我们来复习铝的的原子结构
三、铝的化学性质
1 与非金属课件\铝与氧气反应.wmv(O2、Cl2 、S等)的反应
现象:
铝在氧气中剧烈燃烧,发出耀眼的白光。
反应方程式:
2.能写出Al和Cl2 、S反应的化学方程式吗?
2Al+3Cl2=2AlCl3
2Al+3S=Al2S3
△
△
结构决定性质,下面我们来学习铝的化学性质
过度:
问题探究
铝锅为什么可以用来煮饭?
铝具有良好的导热性能、常温下铝的表面被氧化,生成一层致密氧化物薄膜。
【观察与思考】:
取一块铝片,观察其表面的颜色.将铝片部分浸入4mol.L-1氢氧化钠溶液中,静置一段时间后取出,观察颜色变化.上述实验现象说明了什么?
现象:
浸入氢氧化钠溶液中的铝片表面变白
结论:
说明铝表面有氧化膜
阅读课本P64最上面一段了解铝制品的表面氧化着色
思考:
1 铝制餐具能否用清洁球擦洗?
2 加热铝片,有什么现象?说明什么?
2Al+6HCl= 2AlCl3+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
铝条未发生明显变化
铝条未发生明显变化
铝条上产生大量无色的气泡
铝条上产生大量无色的气泡
活动与探究
课本P65:铝的性质实验
与铝反应的物质 实验现象 化学方程式
浓硝酸
浓硫酸
盐酸
氢氧化钠溶液
交流与讨论
(2) 常温下,铝能与稀盐酸、氢氧化钠溶液反应放出气体,经检验为氢气。
< 1> 铝放入浓硫酸、浓硝酸中均未发生明显变化。
常温下,铝遇浓硫酸、浓硝酸时在表面生成致密的氧化膜而发生钝化
2Al+6HCl= 2AlCl3+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
原因?
练习:铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH物质的量之比为( )
A 1:1 B 2:1 C 3:1 D 1:3
C
2 与酸反应
A.与非氧化性酸反应<如盐酸﹑稀硫酸.>
B.与强氧化性酸反应 反应较复杂,但不生成氢气.
由上述探究和讨论可知铝的第二个化学性质为:
【推进新课】:
3 与强碱溶液反应
反应的机理:
铝与氢氧化钠反应是多步反应的结果:
2Al+6H2O==2Al(OH)3+3H2↑
+
﹙Al(OH)3+NaOH==NaAlO2+2H2O ﹚×2
2Al+6H2O+2NaOH==2NaAlO2+3H2↑+4H2O
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
标出铝与氢氧化钠反应的电子转移情况,并写出该反应的离子方程式。
③ 2Al+2H2O+2OH-==2AlO2- +3H2↑
① 2Al+6H2O+2NaOH==2NaAlO2+3H2↑+4H2O
失2×3 e-
得6×e-
试试看:
4 铝和盐溶液反应
根据金属活动性顺序的应用,铝能把排在它后面的金属从它们的盐溶液中置换出来,如:
2Al+3CuSO4 =3Cu+Al2(SO4)3
2Al+3Cu2+=3Cu+2Al3+
5 铝与某些氧化物反应RM\铝热反应.RM铝热反应.RM
现象:
化学方程式:
—铝热反应
发出耀眼的光芒、有熔融物生成。
2Al + Fe2O3 == 2Fe + Al2O3
高温
铝热剂
该反应的用途:
焊接铁轨、冶炼金属
实质:
Al与Fe2O3发生氧化还原反应
铝热反应用于焊接钢轨
焊接铁轨
铝热反应用于“定向爆破” ,主要是利用铝热反应熔断钢筋 使楼房定向倒塌
练习:
写出Al分别与Cr2O3 、 MnO2 、V2O5 的反应
铝化学性质活泼,反应中均作还原剂。
1、与非金属(O2、S、Cl2等)的反应
2、常温下,铝能与稀盐酸、氢氧化钠溶液反应放出氢气。
2Al+6HCl = 2AlCl3+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
总结与交流:
今天你学到了什么?
铝的物理性质与用途
4、铝与某些氧化物反应—铝热反应
3、铝和盐溶液反应
2Al+3CuSO4 =3Cu+Al2(SO4)3
5 铝跟水的反应
铝跟冷水几乎不反应,跟沸水能发生缓慢的反应
2Al+6H2O==2Al(OH)3+3H2↑
△
为什么铝制的炊具不能长时间盛放酸性、碱性或者含有食盐的食品?
阅读课本P66拓展视野后回答:
学生阅读P66拓展视野上面一段了解铝合金的性质及应用
1 除去镁粉中混有的少量铝粉,可选用下列溶液中的( )
A 盐酸 B 稀硫酸 C 氨水 D 浓氢氧化钾溶液
D
练习:
2、 取两份铝粉,一份投入足量浓氢氧化钠溶液中,一份投入足量盐酸中,充分反应,产生等量氢气。则两份铝粉的质量之比为:< >
A 1: 2 B 1: 3 C 3 : 2 D 1 : 1
D
4、 甲、乙两烧杯中各盛有100mL3 mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙= 1:2,则加入铝粉的质量为,< >
A.5.4g B.3.6g C.2.7g D.1.8g
A
C
3、 将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是( )
A.稀硝酸 B.稀盐酸 C.硝酸铜 D.氢氧化钠
