人教版 九年级上册 化学 第六单元 课题2 二氧化碳制取的研究 教案
文档属性
| 名称 | 人教版 九年级上册 化学 第六单元 课题2 二氧化碳制取的研究 教案 |

|
|
| 格式 | zip | ||
| 文件大小 | 741.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-14 00:00:00 | ||
图片预览




文档简介
《二氧化碳制取的研究》教学设计
[教学目标]
1、 知识与技能:
(1)通过探究比较,了解实验室制取二氧化碳的理想原料。
(2)通过探究实验室制取二氧化碳的装置,培养学生的创新能力。并利用设计的装置制取二氧化碳。
(3)通过比较,归纳实验室取气体的思路和方法。。
2、 过程与方法:
(1)探究实验室制取二氧化碳的装置,并利用设计的装置制取二氧化碳。
(2)通过对二氧化碳制取的探究,提高和锻炼我们收集、加工简单信息的能力。
3、 情感、态度与价值观:
认识积极开展科学探究是学好化学的重要途径,在探究中培养集体协作精神。
[教学重点难点]
重点:实验室制取二氧化碳的化学反应原理、实验装置和制取方法。
难点:从实验室制取气体的设计思路出发,研讨实验室制取二氧化碳气体的方法。
[教学设想]
实验探究式
[课时安排]
1课时
[教学过程]
一、情景导入(时间 分钟)
观察家庭小实验(鸡蛋壳和醋酸反应)的现象,从中可以得出结论联系以前的内容和小实验,这些反应能否用于在实验室中制取二氧化碳?简要说明理由。
学生分析得出:不理想。(取材不便,条件限制,气体不纯)
二、提出问题(时间 分钟)
CO2与日常生活关系非常密切,空气中有CO2,人和动植物的呼吸、煤等燃料的燃烧都产生CO2,那么在实验室里怎样制取CO2?能不能用制氧气的实验装置来制取二氧化碳?
三、猜想与假设(时间 分钟)
甲:能 乙:不能。
四、收集、整理资料(时间 分钟)
1、二氧化碳的密度比空气大,能溶于水。
2、二氧化碳常用稀盐酸(液体)跟大理石[或石灰石](固体)反应来制取。
五、实验探究(时间 分钟)
1、对实验室制取CO2反应原理及所用药品的探究
(学生提供最熟悉方案)
①C + O2 CO2
②C+ 2CuO 2Cu + CO2↑
③2C+ Fe3O4 3Fe + 2CO2↑
教师引导学生:在实验室中制取气体要考虑产物纯度、条件是否容易达到等因素
(学生小组讨论,评价方案)
代表发言:①碳和氧气反应的结果比较复杂。如果氧气充足,那么最后制得的气体中混有杂质氧气;如果氧气不足,那么最后制得的气体中混有一氧化碳。
②③条件在实验室中不容易达到。
教师投影三个实验方案,学生分组探究:选择理想的药品。
实验1 碳酸钠和稀盐酸的反应
实验2 石灰石和稀硫酸的反应
实验3 石灰石和稀盐酸的反应
请小组代表说明发现了什么?获得结论并分析原因。
(1)使用的大理石或石灰石均为块状,反应速率适中。
(2)不能使用浓盐酸或稀硫酸来代替稀盐酸,因为浓盐酸具有挥发性,使制得的CO2气体中混有较多的氯化氢气体;稀硫酸与大理石反应生成微溶物覆盖在反应物表面,阻止反应进行。
(3)碳酸钠跟稀盐酸反应十分剧烈,迅速产生大量气体,反应太快,生成的二氧化碳不容易收集。
教师点拨:实验室通常用稀盐酸和石灰石(或大理石)反应来制取CO2。
引导学生书写反应的化学方程式。
CaCO3+2HCl=CaCl2+H2CO3
碳酸不稳定,易分解生成二氧化碳和水
H2CO3=H2O+CO2↑
总的反应式是CaCO3+2HCl=CaCl2+H2O+CO2↑
2、对实验室制取和收集CO2的装置进行探究
教师引导:气体的发生装置决定于反应物的状态和反应条件,气体收集装置取决于气体的密度和溶解性。
小组讨论完成下表:
投影:CO2和O2制取实验及相关性质比较(参考答案已给出)
反应物状态 反应条件 气体密度比空气大或小 是否与水反应
二氧化碳 固体+液体 常温(不加热) 大 是
氧气 固体或固体+液体 加热 略大 否
引导学生设计制取二氧化碳的装置。(学生在教师的帮助下完成)
考虑因素 设计装置的要求
反应物状态是固体和液体 容器口应竖直向上
反应条件为不需加热(常温) 不需酒精灯
二氧化碳能溶于水,密度比空气大 用向上排空气法收集
固体与液体接触立即反应 用长颈漏斗加液体,反应前将两种药品分别加入
装置的确定:
投影:不同的装置(给出尽可能多的装置组合,让学生选择)。
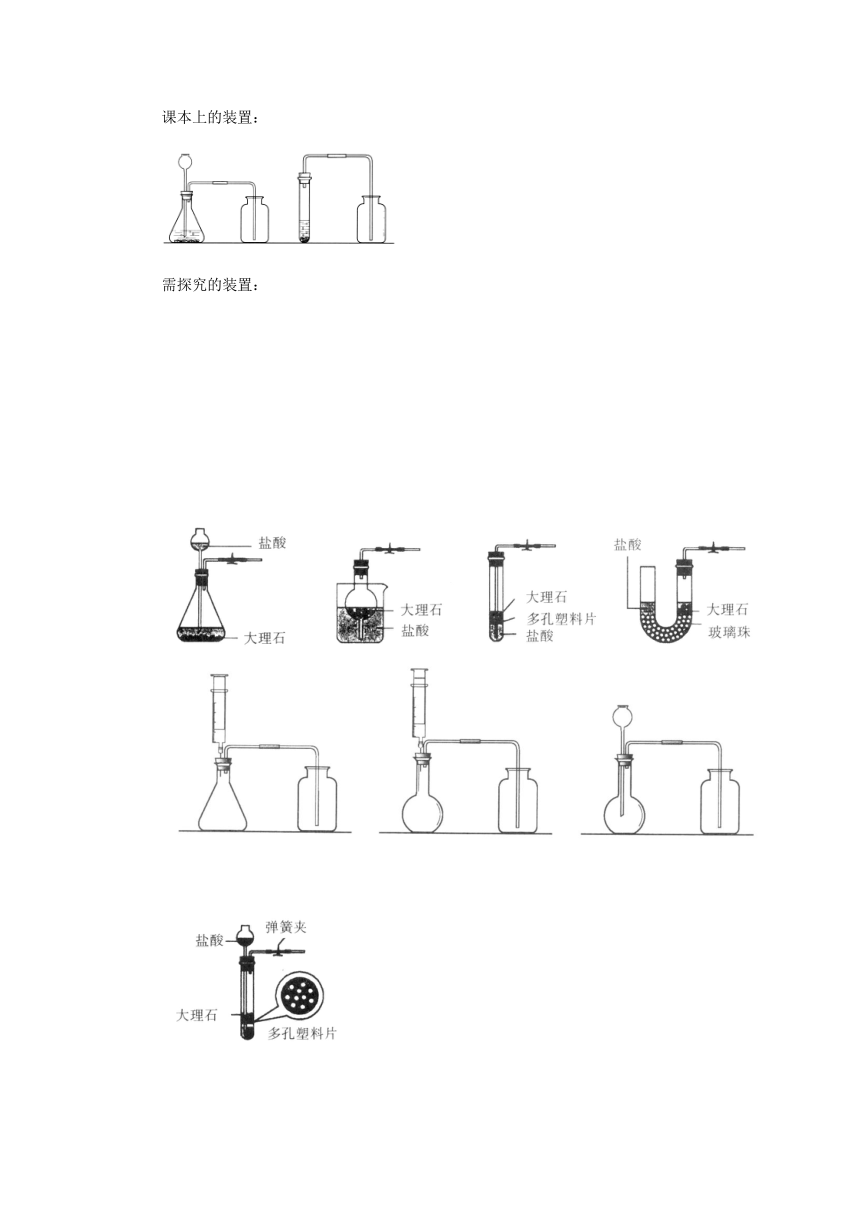
课本上的装置:
需探究的装置:
学生在选择的同时评价装置的易用性方面的优缺点。
选择一种装置制取一瓶二氧化碳。(小组合作,注意操作步骤及注意事项)
探究实验室制取二氧化碳的步骤:
①检查装置的气密性②加入石灰石或大理石③加入稀盐酸④收集O2
3、二氧化碳的检验和验满(学生独立操作完成)
①检验:利用澄清石灰水来检验CO2
化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O
具体方法是:将气体通入澄清石灰水中,如果石灰水变浑浊则通入的气体为CO2;如果未变浑浊,则不是CO2。
②验满:用燃着的木条放在集气瓶口,观察燃着木条的燃烧情况(是否熄灭)
六、获知概念(时间 分钟)
1、气体的实验室制取的方法和思路为:
①研究选择合适的反应物和反应条件(如加热、常温、加催化剂等);
②选择合适的实验装置;
③验证所制得的气体。
2、实验室制取CO2的操作步骤:
连 → 检 → 装 → 注 → 收 → 验
3、操作中的注意事项:
①取用大理石时,先将锥形瓶横放,把大理石放入瓶口使其缓慢滑到瓶底;
②长颈漏斗下端应浸没在液面以下,以防二氧化碳从漏斗口逸出;
③导管不能伸入瓶内太长,以刚漏出胶塞为宜;
④收集二氧化碳导管口应接近集气瓶底部以利于排净空气。
七、交流感想(时间 分钟)
(教师引导)通过本课题的学习,你们有哪些收获?还有哪些困惑?
(学生完成)
【板书设计】
第六单元 碳和碳的氧化物
课题2 二氧化碳制取的研究
【拓展探究】
提出问题:
右图是改进了的实验室制二氧化碳的装置,增添了带孔的塑料片和橡皮管夹。实验时现将块状的大理石(或石灰石)放在塑料片上,然后从长颈漏斗中加稀盐酸。当酸液与大理石接触时,反应即开始。此时只需用橡皮管夹就可控制反应的停止与发生。请你认真思索其中的道理,说明理由。
探究结果:
当橡皮导管被夹住时,产生的气体出不来,聚集在试管中产生压力,将酸液压回到长颈漏斗中,导致试管中液面降低到塑料片以下,与大理石脱离,反应即自动停止;当打开橡皮管夹时,气体从导管口排出,试管内压强减小,酸液回升到塑料片以上,与大理石接触,反应又开始。
【巧设练习】
随堂练习:
1、实验室制取纯净的二氧化碳气体,最适宜的反应物是( )。
A.碳酸钙和硫酸 B.石灰石和稀盐酸
C.石灰石和浓盐酸 D.氯化钙和稀盐酸
2、在实验室里制取氧气、二氧化碳时,它们的收集方法相同的是( )。
A.排水集气法 B.向下排空气法
C.排食盐水集气法 D.向上排空气法
3、能用来鉴定二氧化碳的试剂是( )。
A.水 B.澄清石灰水
C.燃着的木条 D.盐酸
4、实验室制取二氧化碳一般有五个步骤:①检查装置气密性②收集气体③向容器中加入小块大理石④按要求装配好仪器⑤向漏斗中注入盐酸.正确的顺序应该是( )。
A.④①③⑤② B.②⑤③①④
C.④③①⑤② D.④①⑤③②
5、实验室中长期存放石灰水的试剂瓶瓶壁会变白,这层物质主要是碳酸钙,欲洗净试剂瓶可用少量________。
6、某初三同学用浓盐酸和大理石反应制取CO2气体,并把制得的气体通入澄清石灰水中,石灰水却没有预期的那样变浑浊,试分析缘故________。
自主探究:
1、在500mL的烧杯里盛300mL溶质质量分数为20%的盐酸,然后往烧杯里放入一个生鸡蛋,并用硬纸片盖上烧杯,此时鸡蛋慢慢沉入烧杯底。一会儿,蛋壳周围便粘附着许多细小的气泡,随着气泡的增多,鸡蛋逐渐往上浮,直至鸡蛋与空气接触后又慢慢往下沉,如此反复浮沉,直到没有气泡产生,鸡蛋才不会上浮,此时鸡蛋已变成一个软壳蛋,试解释这个实验所发生的现象。
2、右图是实验室制取二氧化碳的实验图。该装置的特点是:打开弹簧夹,大理石和盐酸接触,发生反应;关闭弹簧夹后,盐酸被反应产生的CO2气体压回长颈漏斗,与大理石分离,停止反应。用该装置制备CO2可起到节约药品和取用方便的效果。下图装置中哪些可以起到与右图装置相同的效果?
【教后反思】
1、本课题的重点是指导学生掌握制取气体时实验仪器和收集方法的选择。鉴于学生在第二单元已经学过氧气的制法,具备一些制取气体的简单知识,教师可以选择在实际操作中让学生理解实验装置的选取,使学生尽快地从简单模仿到有目的地选择。
2、建议教学中教师先引导学生复习实验室制取氧气的实验装置,分析制取二氧化碳与制取氧气所用反应物的状态、反应条件以及生成物的性质,让学生在小组内或小组之间进行交流(要求能说出理由),并从中选出正确的和最佳的设计装置,使学生通过比较加深对实验的认识和理解。
3、建议教师在最后再次引导学生总结并比较实验室制取氧气、二氧化碳气体的异同点,使学生能逐渐把握住实验室制取气体的设计思路。
【课后拾贝】
碳酸钙与《石灰吟》
千锤万凿出深山,烈火焚烧若等闲;粉身碎骨浑不怕,要留清白在人间。
这是一首诗,也可以说是一个谜语,相传是明朝于谦在12岁时所作。它的谜底也就是诗的题目——《石灰吟》。这首七言绝句使用简练概括的语言,形象地描述了石灰石的一系列变化。石灰石的主要成分是碳酸钙,它常常聚集成一大片地层,构成整座的山峰。“千锤万凿出深山”就是说石灰石是从山中开采出来的。当把石灰石和焦炭放在窑中煅烧时,碳酸钙受热分解产生生石灰(CaO)和二氧化碳气体,这就是“烈火焚烧若等闲”。“粉身碎骨浑不怕”指的是生石灰与水发生的剧烈的放热的化学反应:CaO+H2O=Ca(OH)2,反应后,块状的生石灰就变成了粉末状的氢氧化钙,又叫熟石灰。氢氧化钙微溶于水,将氢氧化钙的悬浊液即石灰浆刷在墙上,氢氧化钙又和二氧化碳结成伙伴,重新变成碳酸钙,墙壁就显得非常洁白和坚硬,真是“要留清白在人间”的绝好写照。
? 课件说明
[整体说明]
课件的制作平台为PowerPoint,播放时单击鼠标就可以自动翻页。课件共分为六大部分,即引入、反应原理、制取和收集、检验和验满、小结、随堂练习等,涵盖整个教学过程。
[引入]
播放课件第2页
从生活中的小实验引入。
[反应原理]
播放课件第3~6页
首先提示实验室制取气体的一般要求,然后对已经学过的和与制取CO2有关的反应进行讨论,并分组进行实验探究,选择最佳方案。
[制取和收集]
播放课件第7~14页
本课题的核心部分。在提示实验装置的确定方法的基础上,引导学生分别对实验室制取CO2气体的发生装置和收集装置进行探究。然后给学生提供尽可能多的实验器材,让学生分组,自己组装一套装置只取一瓶CO2气体。在教学中应指导学生对不同组的实验装置进行比较,给予正确评价。接着给学生提供几种组装一起的方式,让学生深层探究,并分析实验装置优缺点,最后,让学生观看制取CO2的整个过程(动画直接按提示操作即可),从而引出检验和验满的方法。
[检验和验满]
播放课件第15页
学生已经学习过O2的检验和验满方法,引导学生联系气体的性质考虑问题。
[小结]
播放课件第16~17页
引导学生总结本课题的收获。
[随堂练习]
播放课件第18~20页
巩固本节课所学知识,重点放在对5、6题的分析。
设计
装置
验证
实验
原
理
气体发生装置比较
气体收集装置比较
气体性质比较
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
