人教版九年级化学下册第八单元课题2 金属的化学性质课件 (共20张PPT)
文档属性
| 名称 | 人教版九年级化学下册第八单元课题2 金属的化学性质课件 (共20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-15 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
人教版九年级化学第八单元
黄铜(铜、锌合金)外观和黄金极为相似,黄金饰品中的假货常常鱼目混珠,有些不法分子常以黄铜冒充黄金进行诈骗。
我们可用什么办法来鉴别它们呢?
?
慧眼识“金”
(1)在空气燃烧发出耀眼的白光,
生成白色固体
(2)在氧气中剧烈燃烧,火星四射,
生成黑色固体
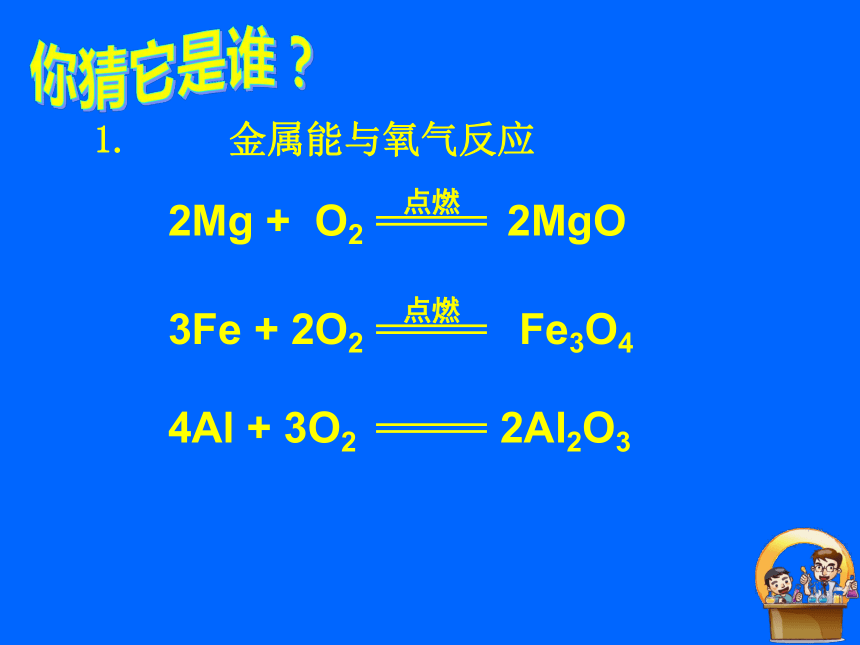
1. 金属能与氧气反应
1、所有的金属都能与氧气反应吗?
2、你知道它们和氧气反应的条件吗?
金属与氧气的反应
实 验
现 象
化学方程式
铜在酒精灯上加热
由红色变为黑色
△
2Cu+O2 = 2CuO
2.依次向四只试管中加入约2ml盐酸。
1.在试管中分别放入铜片、铁丝、锌粒、镁条。
2.金属与酸的反应
【实验方案】
仔细观察现象,并记录。试着写出化学方程式
无现象
反应较剧烈,产生较多气泡
Mg+2HCl==MgCl2+H2 ↑
Zn+2HCl==ZnCl2+H2 ↑
实验现象
反应很慢,产生少量的气泡,溶液变为浅绿色
剧烈反应,产生大量的气泡
无现象
Fe+2HCl==FeCl2+H2 ↑
【金属与盐酸反应现象记录】
【实验结论】:
镁、锌、铁比铜
活泼
金属 化学方程式
镁
锌
铁
铜
分别向装有硝酸银溶液与硫酸铝溶液的试管中插入铜丝
【实验方案】
仔细观察现象,并记录。试着写出化学方程式
3. 金属与金属化合物的反应
铝片表面覆盖一层红色的物质,溶液由蓝色变成无色(变浅)
2Al + 3 CuSO4= Al2( SO4)3+ 3Cu
铜丝表面覆盖一层银白色的物质,溶液由无色逐渐变成蓝色
Cu + 2AgNO3= Cu(NO3)2 +2Ag
无
【实验结论】:
比 活泼
Al
Cu
比 活泼
Cu
Ag
实验 现 象 化学方程式
铝片在硫酸铜溶液中
铜丝在硝酸银溶液中
铜丝在硫酸铝溶液中
金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强到弱
金属的位置越靠前,它的活动性就越强。
Mg
Fe
Cu
Zn
位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
Ag
位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
判断下列物质能否发生反应?若能,
写出相关化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(5)银与氯化铜溶液 (6)镁与硫酸亚铁溶液
解答:可发生反应的:(2)(4)(6)
化学方程式:
(2)Zn + CuSO4 = Cu + ZnSO4
(4)Al +3AgNO3 = Al(NO3)3 + 3Ag
(6)Mg + FeSO4 = MgSO4 +Fe
练 习 巩 固
分别在装有镁、铝、铁、铜的试管中加入稀盐酸,不能产生氢气的是( )
A.镁 B.铝 C.铁 D. 铜
练 习 巩 固
D
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
下列日常生活中常见的金属中,金属活动性最强的是( )
A. Fe B. Cu
C. Al D. Zn
C
练 习 巩 固
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
实验室制取氢气,可以选择的试剂是( )
A、锌和稀硫酸 B、银和稀盐酸
C、镁和硫酸铜 D、铜和稀盐酸
A
练 习 巩 固
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
下列物质中能与CuSO4溶液发生置换反应的是 ( )
A Ag B Fe
C NaOH溶液 D 稀盐酸
B
练 习 巩 固
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
答:方案一:把该金属放入稀盐酸溶液中,若有气泡产生,则是假黄金;若没有气泡产生,则证明该金属是真黄金。
方案二:把该金属上火上烧中,若变黑,则是假黄金;若不变色,则证明该金属是真黄金。
方案三:把该金属放入硝酸银溶液中,若金属表面有固体析出,则是假黄金;若没有现象,则证明该金属是真黄金。
方案四:咬一下该金属,若没有牙印的,则是假黄金;若有牙印的,则证明该金属是真黄金。
区别黄铜(铜锌合金)与黄金的方法
人教版九年级化学第八单元
黄铜(铜、锌合金)外观和黄金极为相似,黄金饰品中的假货常常鱼目混珠,有些不法分子常以黄铜冒充黄金进行诈骗。
我们可用什么办法来鉴别它们呢?
?
慧眼识“金”
(1)在空气燃烧发出耀眼的白光,
生成白色固体
(2)在氧气中剧烈燃烧,火星四射,
生成黑色固体
1. 金属能与氧气反应
1、所有的金属都能与氧气反应吗?
2、你知道它们和氧气反应的条件吗?
金属与氧气的反应
实 验
现 象
化学方程式
铜在酒精灯上加热
由红色变为黑色
△
2Cu+O2 = 2CuO
2.依次向四只试管中加入约2ml盐酸。
1.在试管中分别放入铜片、铁丝、锌粒、镁条。
2.金属与酸的反应
【实验方案】
仔细观察现象,并记录。试着写出化学方程式
无现象
反应较剧烈,产生较多气泡
Mg+2HCl==MgCl2+H2 ↑
Zn+2HCl==ZnCl2+H2 ↑
实验现象
反应很慢,产生少量的气泡,溶液变为浅绿色
剧烈反应,产生大量的气泡
无现象
Fe+2HCl==FeCl2+H2 ↑
【金属与盐酸反应现象记录】
【实验结论】:
镁、锌、铁比铜
活泼
金属 化学方程式
镁
锌
铁
铜
分别向装有硝酸银溶液与硫酸铝溶液的试管中插入铜丝
【实验方案】
仔细观察现象,并记录。试着写出化学方程式
3. 金属与金属化合物的反应
铝片表面覆盖一层红色的物质,溶液由蓝色变成无色(变浅)
2Al + 3 CuSO4= Al2( SO4)3+ 3Cu
铜丝表面覆盖一层银白色的物质,溶液由无色逐渐变成蓝色
Cu + 2AgNO3= Cu(NO3)2 +2Ag
无
【实验结论】:
比 活泼
Al
Cu
比 活泼
Cu
Ag
实验 现 象 化学方程式
铝片在硫酸铜溶液中
铜丝在硝酸银溶液中
铜丝在硫酸铝溶液中
金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强到弱
金属的位置越靠前,它的活动性就越强。
Mg
Fe
Cu
Zn
位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
Ag
位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
判断下列物质能否发生反应?若能,
写出相关化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(5)银与氯化铜溶液 (6)镁与硫酸亚铁溶液
解答:可发生反应的:(2)(4)(6)
化学方程式:
(2)Zn + CuSO4 = Cu + ZnSO4
(4)Al +3AgNO3 = Al(NO3)3 + 3Ag
(6)Mg + FeSO4 = MgSO4 +Fe
练 习 巩 固
分别在装有镁、铝、铁、铜的试管中加入稀盐酸,不能产生氢气的是( )
A.镁 B.铝 C.铁 D. 铜
练 习 巩 固
D
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
下列日常生活中常见的金属中,金属活动性最强的是( )
A. Fe B. Cu
C. Al D. Zn
C
练 习 巩 固
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
实验室制取氢气,可以选择的试剂是( )
A、锌和稀硫酸 B、银和稀盐酸
C、镁和硫酸铜 D、铜和稀盐酸
A
练 习 巩 固
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
下列物质中能与CuSO4溶液发生置换反应的是 ( )
A Ag B Fe
C NaOH溶液 D 稀盐酸
B
练 习 巩 固
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
答:方案一:把该金属放入稀盐酸溶液中,若有气泡产生,则是假黄金;若没有气泡产生,则证明该金属是真黄金。
方案二:把该金属上火上烧中,若变黑,则是假黄金;若不变色,则证明该金属是真黄金。
方案三:把该金属放入硝酸银溶液中,若金属表面有固体析出,则是假黄金;若没有现象,则证明该金属是真黄金。
方案四:咬一下该金属,若没有牙印的,则是假黄金;若有牙印的,则证明该金属是真黄金。
区别黄铜(铜锌合金)与黄金的方法
同课章节目录
