沪教版化学九年级上册 5.2 金属矿物 铁的冶炼 课件 (共20张PPT)
文档属性
| 名称 | 沪教版化学九年级上册 5.2 金属矿物 铁的冶炼 课件 (共20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-16 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
5.2 金属矿物
铁的冶炼
1.了解常见的金属矿物。
2.知道从铁矿石中将铁冶炼出来的方法。
3.了解冶炼金属的其他方法。
自主先学
赤铁矿Fe2O3
褐铁矿Fe2O3·XH2O
黄铁矿FeS2()
磁铁矿Fe3O4
孔雀石Cu2(OH)2CO3
赤铜矿Cu2O
一、常见的金属矿物
钢铁工业是衡量一个国家综合经济实力的标志性工业。你知道钢铁是怎么样炼成的吗?
我国几个大型的铁矿
辽宁鞍山
湖北大冶
四川攀枝花
金属的冶炼:
金属化合物
金属单质
转变成
铁的冶炼:
铁的化合物
转变成
铁单质
二.铁的冶炼
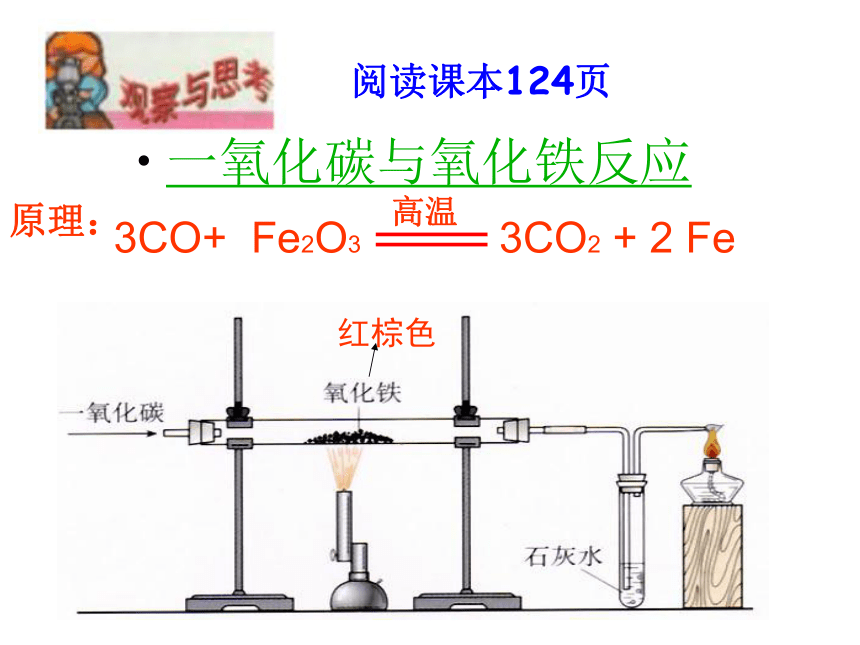
一氧化碳与氧化铁反应
红棕色
阅读课本124页
3CO+ Fe2O3 3CO2 + 2 Fe
高温
原理:
(1)向玻璃管内通入一氧化碳气体;(通入co)
(2)给氧化铁加热; (点燃酒精灯)
(3)停止加热; (熄灭酒精灯)
(4)待试管内的物质冷却后停止
通一氧化碳。 (停止通co)
实验步骤
(CO:
早出晚归
酒精灯:
迟到早退)
一氧化碳与氧化铁反应
实验前观察
颜色:__
状态:___
能否被磁铁吸起?_
红棕色
固体粉末
否
Fe2O3
实验后观察
颜色:__
状态:_______
能否被磁铁吸起?_
澄清石灰水__________
产物
黑色
固体粉末
能
结论:
产物中有铁和二氧化碳生成
变浑浊
1.红棕色的固体逐渐黑色
2. 澄清的石灰水变浑浊
归纳实验现象
写出有关化学反应方程式
CO+ Fe2O3 Fe+ CO2
高温
3
2
3
CO2+Ca(OH)2===CaCO3 +H2O
1、澄清石灰水的作
用是什么?
2、为什么要进行尾气处理?尾气如何处理?
3、实验中为什么要先通一段时间CO,再加热Fe2O3?
4、实验结束后,为什么要先停止加热继续通CO直至试管内物质冷却?
5、如何验证实验中产生了铁?
点燃或收集
检验生成的二氧化碳
因为CO有毒会污染环境
排出装置中的空气,防止加热时发生爆炸
防止热的铁再次被氧化以及防止石灰水倒吸
用磁铁吸引或加入稀酸
产生蓝色火焰
小组合作讨论完成
《合作助学》
三、工业炼铁
主要反应
原料
工业炼铁的主要设备是高炉
石灰石的作用是使有矿石中的杂质(如二氧化硅)转变成炉渣而除去
高炉中的主要反应
3CO+Fe2O3===2Fe+3CO2
C+CO2===2CO
C+O2===CO2
高温
高温
点燃
工业上炼得的不是纯铁
(生铁)——混合物
下图是实验室用一氧化碳还原氧化铁的实验装置图,试回答。
(1)仪器③的名称是___________________________。
(2)用CO与赤铁矿石炼铁的实验步骤:
①加热 ②通CO ③熄灭酒精灯 ④停止通CO
酒精灯
② ① ③ ④
(2)实验过程中仪器①中的现象是
仪器②中发生反应的化学方程式是__________________。
(3)尾气要处理的原因: 。
(4)如果将CO改为H2还要进行尾气处理吗?
CO有剧毒会污染空气
不需要,因为H2无毒
固体由红色变黑色
Ca(OH)2+C02====CaCO3↓+H20
2.炼铁的原料是( )
A、铁矿石、一氧化碳、空气
B、铁矿石、烟煤、生石灰
C、铁矿石、焦炭、空气
D、铁矿石、焦炭、石灰石、空气
D
3.下列变化过程不属于金属冶炼的是( )
A.电解氧化铝 B.铁在氧气中燃烧
C.金属氧化物与焦炭在高温下反应
D.高温下CO还原CuO
B
5.2 金属矿物
铁的冶炼
1.了解常见的金属矿物。
2.知道从铁矿石中将铁冶炼出来的方法。
3.了解冶炼金属的其他方法。
自主先学
赤铁矿Fe2O3
褐铁矿Fe2O3·XH2O
黄铁矿FeS2()
磁铁矿Fe3O4
孔雀石Cu2(OH)2CO3
赤铜矿Cu2O
一、常见的金属矿物
钢铁工业是衡量一个国家综合经济实力的标志性工业。你知道钢铁是怎么样炼成的吗?
我国几个大型的铁矿
辽宁鞍山
湖北大冶
四川攀枝花
金属的冶炼:
金属化合物
金属单质
转变成
铁的冶炼:
铁的化合物
转变成
铁单质
二.铁的冶炼
一氧化碳与氧化铁反应
红棕色
阅读课本124页
3CO+ Fe2O3 3CO2 + 2 Fe
高温
原理:
(1)向玻璃管内通入一氧化碳气体;(通入co)
(2)给氧化铁加热; (点燃酒精灯)
(3)停止加热; (熄灭酒精灯)
(4)待试管内的物质冷却后停止
通一氧化碳。 (停止通co)
实验步骤
(CO:
早出晚归
酒精灯:
迟到早退)
一氧化碳与氧化铁反应
实验前观察
颜色:__
状态:___
能否被磁铁吸起?_
红棕色
固体粉末
否
Fe2O3
实验后观察
颜色:__
状态:_______
能否被磁铁吸起?_
澄清石灰水__________
产物
黑色
固体粉末
能
结论:
产物中有铁和二氧化碳生成
变浑浊
1.红棕色的固体逐渐黑色
2. 澄清的石灰水变浑浊
归纳实验现象
写出有关化学反应方程式
CO+ Fe2O3 Fe+ CO2
高温
3
2
3
CO2+Ca(OH)2===CaCO3 +H2O
1、澄清石灰水的作
用是什么?
2、为什么要进行尾气处理?尾气如何处理?
3、实验中为什么要先通一段时间CO,再加热Fe2O3?
4、实验结束后,为什么要先停止加热继续通CO直至试管内物质冷却?
5、如何验证实验中产生了铁?
点燃或收集
检验生成的二氧化碳
因为CO有毒会污染环境
排出装置中的空气,防止加热时发生爆炸
防止热的铁再次被氧化以及防止石灰水倒吸
用磁铁吸引或加入稀酸
产生蓝色火焰
小组合作讨论完成
《合作助学》
三、工业炼铁
主要反应
原料
工业炼铁的主要设备是高炉
石灰石的作用是使有矿石中的杂质(如二氧化硅)转变成炉渣而除去
高炉中的主要反应
3CO+Fe2O3===2Fe+3CO2
C+CO2===2CO
C+O2===CO2
高温
高温
点燃
工业上炼得的不是纯铁
(生铁)——混合物
下图是实验室用一氧化碳还原氧化铁的实验装置图,试回答。
(1)仪器③的名称是___________________________。
(2)用CO与赤铁矿石炼铁的实验步骤:
①加热 ②通CO ③熄灭酒精灯 ④停止通CO
酒精灯
② ① ③ ④
(2)实验过程中仪器①中的现象是
仪器②中发生反应的化学方程式是__________________。
(3)尾气要处理的原因: 。
(4)如果将CO改为H2还要进行尾气处理吗?
CO有剧毒会污染空气
不需要,因为H2无毒
固体由红色变黑色
Ca(OH)2+C02====CaCO3↓+H20
2.炼铁的原料是( )
A、铁矿石、一氧化碳、空气
B、铁矿石、烟煤、生石灰
C、铁矿石、焦炭、空气
D、铁矿石、焦炭、石灰石、空气
D
3.下列变化过程不属于金属冶炼的是( )
A.电解氧化铝 B.铁在氧气中燃烧
C.金属氧化物与焦炭在高温下反应
D.高温下CO还原CuO
B
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
