人教版九年级化学下册第八单元课题2、金属的化学性质课件 (共20张PPT)
文档属性
| 名称 | 人教版九年级化学下册第八单元课题2、金属的化学性质课件 (共20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-17 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
1:铝片在常温下就能和氧气发生反应。
金属与氧气的反应
4Al+3O2 = 2Al2O3
银白色
白色
铝表面易失去光泽,铝有很好抗腐蚀能力
2:镁条在常温下就能和空气中的氧气发生氧化反应
2Mg + O2 = 2MgO
银白色
白色
燃烧的条件点燃
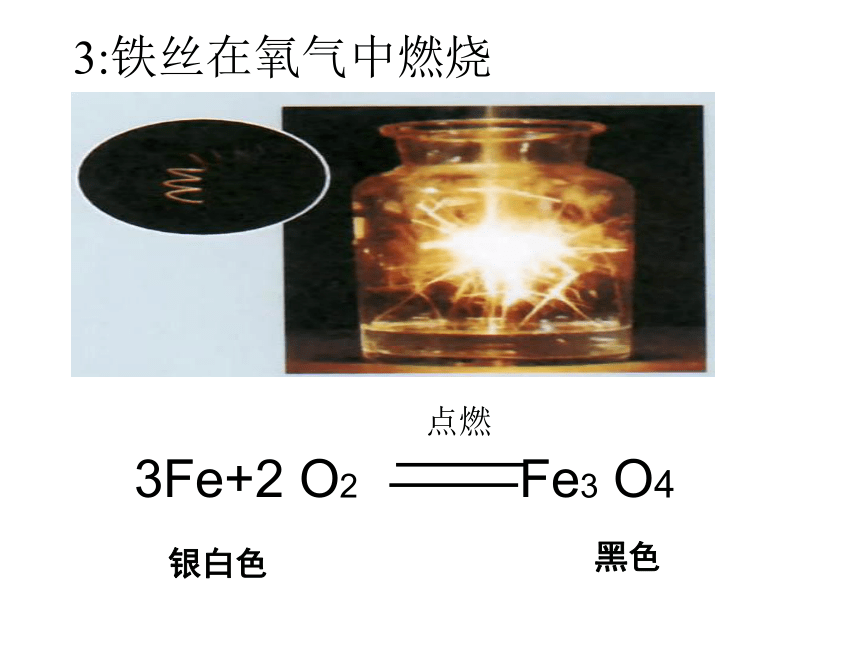
3Fe+2 O2 Fe3 O4
3:铁丝在氧气中燃烧
点燃
银白色
黑色
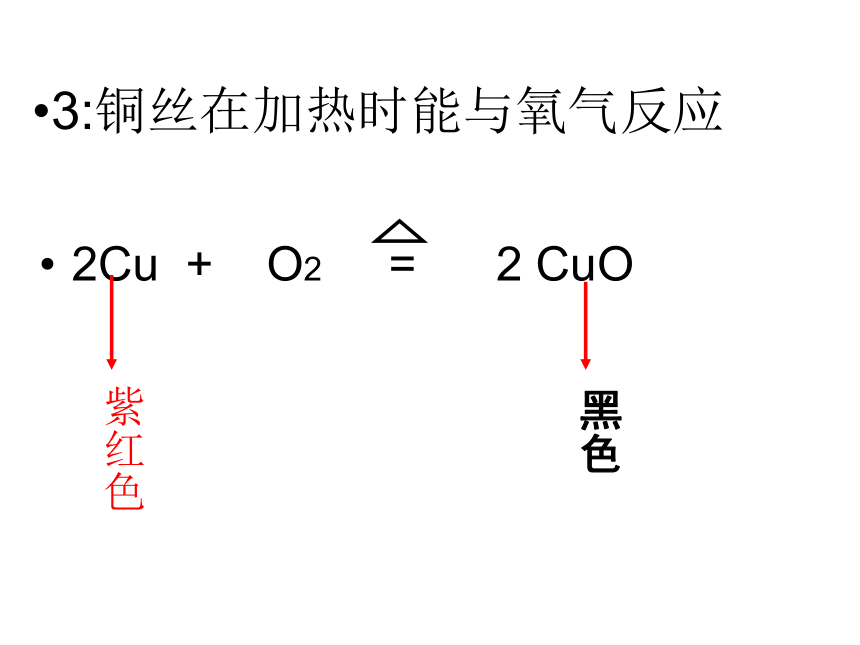
2Cu + O2 = 2 CuO
3:铜丝在加热时能与氧气反应
紫红色
黑色
你学过哪些金属与O2的反应?
Mg>Fe
Mg>Cu
实 验 现 象 化学方程式 活泼性
比较
铁丝在氧气中燃烧 ?火星四射,放出大量的热,黑色固体 ? 点燃
3Fe+2O2==Fe3O4 ?
镁在空气中燃烧 ?发出白光,放热,生成白色固体 ?? 点燃
2Mg+O2==2MgO
铜在酒精灯上加热 由红色变为黑色 △
2Cu+O2==2CuO
真金不怕烈火
金不能和氧气反应
zxxk
讨论1:从以上方程式你能得到哪些信息?
1.大多数金属都能与_______反应,
反应剧烈程度 ________ (相同,不相同)
2.金属的活动性:说明 _______ 较活泼,
________次之, ______很不活泼
Au
氧气
不相同
Al、Mg
Fe、Cu
所以我们可以通过金属与氧气反应
的难易程度来判断金属的活泼性
(2)为何不宜用钢刷来擦洗铝制餐具呢?
若用钢刷擦洗铝制品,
容易把氧化薄膜除掉,
从而起不到保护作用。
思考:P13 1T
讨论
铁钉和稀盐酸
镁和稀盐酸
锌和稀盐酸
铜和稀盐酸
铁、镁、锌能和稀盐酸或稀硫酸反应,反应剧烈
程度:镁﹥锌﹥铁,反应后生成了氢气,铜不能
和稀盐酸或稀硫酸反应
zxxk
金属与酸反应
1:镁与盐酸、硫酸反应的现象
固体溶解、大量气泡;
2:镁与盐酸反应的化学方程式
Mg +2HCl = MgCl2 + H2
3:镁与硫酸反应的化学方程式
Mg +H2SO4 = MgSO4 + H2
金属与酸反应
1:锌与盐酸、硫酸反应的现象
固体减少(溶解)、大量气泡;
2:锌与盐酸反应的化学方程式
Zn +2HCl = ZnCl2 + H2
3:锌硫酸反应的化学方程式
Zn +H2SO4 = ZnSO4 + H2
金属与酸反应
1:铁与盐酸、硫酸反应的现象
缓慢反应、少量气泡;溶液逐渐变浅绿色
2:铁与盐酸反应的化学方程式
Fe +2HCl = FeCl2 + H2
3:铁硫酸反应的化学方程式
Fe +H2SO4 = FeSO4 + H2
铁与盐酸、硫酸反应生成亚铁的化合物
金属与酸反应
1:铜与盐酸、硫酸反应的现象
无现象
倒入稀硫酸
Mg
Zn
Fe
Cu
Ag
现象:
1、锌、镁、铁放入稀硫酸中有气泡产生。
2、铜、银放入稀硫酸中无气泡产生。
3、镁与稀硫酸反应最快,其次为锌,铁反应较慢。
(3)由此推出 ,金属活动性顺序
__________________
根据反应可将金属分为两类:
活泼金属和不活泼金属
Mg、 Zn、Fe、Cu
活泼金属
不活泼金属
比较反应类型
Mg +2HCl = MgCl2 + H2
Fe +H2SO4 = FeSO4 + H2
Zn +H2SO4 = ZnSO4 + H2
单质
化合物
化合物
单质
比较三种基本反应类型
? 定义 举例
分解反应 AB →A + B + … (以一变多)? ?
化合反应 A + B + … → AB…(以多变一) ? ?
置换反应 A + BC → B + AC (以一换一 )? ?
置换反应
一种单质和一种化合物反应生成另一种单质和另一种化合物的反应叫置换反应
作业安排
1:写出镁、铝、铁与氧气反应的化学方程式
2:写出镁、铝、铁与盐酸反应的化学方程式
3:写出镁、铝、铁与硫酸反应的化学方程式
学科网
1:铝片在常温下就能和氧气发生反应。
金属与氧气的反应
4Al+3O2 = 2Al2O3
银白色
白色
铝表面易失去光泽,铝有很好抗腐蚀能力
2:镁条在常温下就能和空气中的氧气发生氧化反应
2Mg + O2 = 2MgO
银白色
白色
燃烧的条件点燃
3Fe+2 O2 Fe3 O4
3:铁丝在氧气中燃烧
点燃
银白色
黑色
2Cu + O2 = 2 CuO
3:铜丝在加热时能与氧气反应
紫红色
黑色
你学过哪些金属与O2的反应?
Mg>Fe
Mg>Cu
实 验 现 象 化学方程式 活泼性
比较
铁丝在氧气中燃烧 ?火星四射,放出大量的热,黑色固体 ? 点燃
3Fe+2O2==Fe3O4 ?
镁在空气中燃烧 ?发出白光,放热,生成白色固体 ?? 点燃
2Mg+O2==2MgO
铜在酒精灯上加热 由红色变为黑色 △
2Cu+O2==2CuO
真金不怕烈火
金不能和氧气反应
zxxk
讨论1:从以上方程式你能得到哪些信息?
1.大多数金属都能与_______反应,
反应剧烈程度 ________ (相同,不相同)
2.金属的活动性:说明 _______ 较活泼,
________次之, ______很不活泼
Au
氧气
不相同
Al、Mg
Fe、Cu
所以我们可以通过金属与氧气反应
的难易程度来判断金属的活泼性
(2)为何不宜用钢刷来擦洗铝制餐具呢?
若用钢刷擦洗铝制品,
容易把氧化薄膜除掉,
从而起不到保护作用。
思考:P13 1T
讨论
铁钉和稀盐酸
镁和稀盐酸
锌和稀盐酸
铜和稀盐酸
铁、镁、锌能和稀盐酸或稀硫酸反应,反应剧烈
程度:镁﹥锌﹥铁,反应后生成了氢气,铜不能
和稀盐酸或稀硫酸反应
zxxk
金属与酸反应
1:镁与盐酸、硫酸反应的现象
固体溶解、大量气泡;
2:镁与盐酸反应的化学方程式
Mg +2HCl = MgCl2 + H2
3:镁与硫酸反应的化学方程式
Mg +H2SO4 = MgSO4 + H2
金属与酸反应
1:锌与盐酸、硫酸反应的现象
固体减少(溶解)、大量气泡;
2:锌与盐酸反应的化学方程式
Zn +2HCl = ZnCl2 + H2
3:锌硫酸反应的化学方程式
Zn +H2SO4 = ZnSO4 + H2
金属与酸反应
1:铁与盐酸、硫酸反应的现象
缓慢反应、少量气泡;溶液逐渐变浅绿色
2:铁与盐酸反应的化学方程式
Fe +2HCl = FeCl2 + H2
3:铁硫酸反应的化学方程式
Fe +H2SO4 = FeSO4 + H2
铁与盐酸、硫酸反应生成亚铁的化合物
金属与酸反应
1:铜与盐酸、硫酸反应的现象
无现象
倒入稀硫酸
Mg
Zn
Fe
Cu
Ag
现象:
1、锌、镁、铁放入稀硫酸中有气泡产生。
2、铜、银放入稀硫酸中无气泡产生。
3、镁与稀硫酸反应最快,其次为锌,铁反应较慢。
(3)由此推出 ,金属活动性顺序
__________________
根据反应可将金属分为两类:
活泼金属和不活泼金属
Mg、 Zn、Fe、Cu
活泼金属
不活泼金属
比较反应类型
Mg +2HCl = MgCl2 + H2
Fe +H2SO4 = FeSO4 + H2
Zn +H2SO4 = ZnSO4 + H2
单质
化合物
化合物
单质
比较三种基本反应类型
? 定义 举例
分解反应 AB →A + B + … (以一变多)? ?
化合反应 A + B + … → AB…(以多变一) ? ?
置换反应 A + BC → B + AC (以一换一 )? ?
置换反应
一种单质和一种化合物反应生成另一种单质和另一种化合物的反应叫置换反应
作业安排
1:写出镁、铝、铁与氧气反应的化学方程式
2:写出镁、铝、铁与盐酸反应的化学方程式
3:写出镁、铝、铁与硫酸反应的化学方程式
学科网
同课章节目录
