沪教版九上化学 2.1性质活泼的氧气 学案
文档属性
| 名称 | 沪教版九上化学 2.1性质活泼的氧气 学案 |
|
|
| 格式 | zip | ||
| 文件大小 | 70.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-17 00:00:00 | ||
图片预览

文档简介
第一节 性质活泼的氧气
【学习目标】 1、认识实验室里用过氧化氢制取氧气原理及操作。2、了解催化剂的作用
【活动方案】
活动一、参与用过氧化氢溶液制取氧气的演示实验2(P36)
1、观察与思考:
(1) 分液漏斗上的分液漏斗可以用长颈漏斗代替,但其下端应该深入液面 (填上或下),防止生成的气体 ;但分液漏斗比长颈漏洞的优点是能控制反应速率得到 (填平稳、不平稳)的气流。
(2). 气密性检查:用止水夹关闭,打开分液漏斗活塞,向漏斗中加入水,水面不能持续流下,最终形成一段水柱 ,就说明气密性良好。 装药品时,先 后
(填固体药品、液体药品)
2. 过氧化氢制取氧气实验原理(反应的文字和符号式): 。
?
反应物状态
反应条件
仪器、装置选择
高锰酸钾
盛少量固体及加热的仪器——
(试管、酒精灯等)
双氧水和二氧化锰
+
无须加热,接触既迅速反应
固体与液体接触就反应需进行固液分离,以控制反应的进程,则选用分液漏斗、锥形瓶等
3、[师生讨论] 在讨论的基础上进行归纳并完成下列表格:
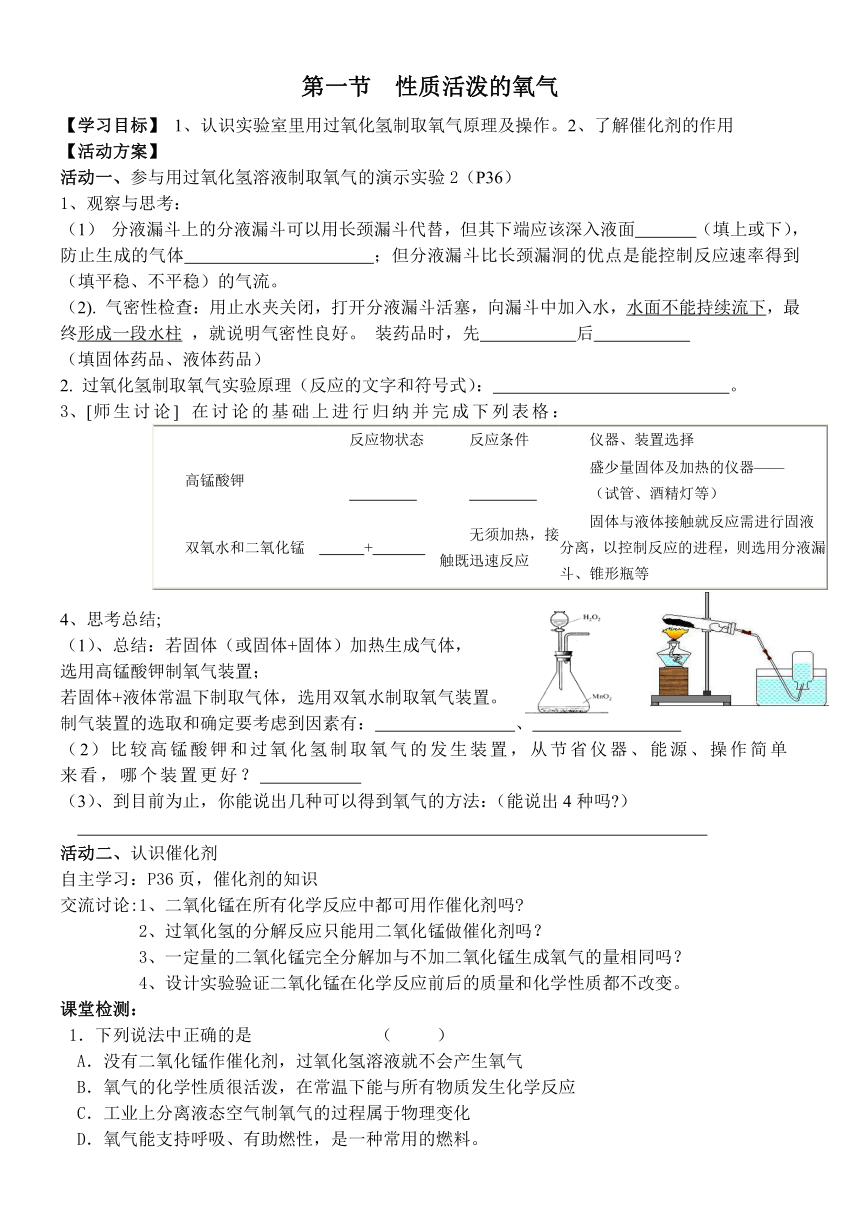
4、思考总结;
(1)、总结:若固体(或固体+固体)加热生成气体,
选用高锰酸钾制氧气装置;
若固体+液体常温下制取气体,选用双氧水制取氧气装置。
制气装置的选取和确定要考虑到因素有: 、
比较高锰酸钾和过氧化氢制取氧气的发生装置,从节省仪器、能源、操作简单来看,哪个装置更好?
(3)、到目前为止,你能说出几种可以得到氧气的方法:(能说出4种吗?)
活动二、认识催化剂
自主学习:P36页,催化剂的知识
交流讨论:1、二氧化锰在所有化学反应中都可用作催化剂吗?
2、过氧化氢的分解反应只能用二氧化锰做催化剂吗?
3、一定量的二氧化锰完全分解加与不加二氧化锰生成氧气的量相同吗?
4、设计实验验证二氧化锰在化学反应前后的质量和化学性质都不改变。
课堂检测:
1.下列说法中正确的是 ( )
A.没有二氧化锰作催化剂,过氧化氢溶液就不会产生氧气
B.氧气的化学性质很活泼,在常温下能与所有物质发生化学反应
C.工业上分离液态空气制氧气的过程属于物理变化
D.氧气能支持呼吸、有助燃性,是一种常用的燃料。
2.结合下列图示装置,回答有关问题:?
(1)写出图中标有字母的仪器名称:a b ?
(2)上述装置可用于实验室制取和收集某些气体:
①如果用高锰酸钾制氧气,应选用的发生装置是 (填序号),反应的文字及符合表达
式 ,所选发生装置中还缺少 。?
如果用过氧化氢和二氧化锰混合制氧气,应选用的发生装置是 (填序号),反应的文字及符合表达式 ,可以选用的收集装置是 (填序号),
3 以下仪器,请回答下列问题:
(1)仪器⑤的名称是 ;取用粉末状固体用到的仪器是 (填序号)。
(2)如果用加热KmnO4的方法制取氧气,制气装置应选仪器 (填序号)。其符号表达式为: ;
(3)如果用H2O2分解来制取氧气,制气装置最好选用仪器 (填序号),其反应的文字表达式为 收集方法为
(4)比较(2)和(3)两种制取氧气的方法,最好选用方法(3)的原因是
(5)把上面分解KmnO4制取氧气的仪器装配好后,检验该装置气密性的操作方法为: 。
4. 你已经掌握了实验室制取气体的有关规律,以下是老师提供的一些实验装置。请结合下图回答问题:
(2)写出实验室用B装置制取氧气的符号表达式 。
(3)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;②氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。小芳同学用加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的反应的发生装置是 ,收集装置是 。(填字母编号)
(4)小芳将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是 , 。
(5)请写出氨气和氧化铜反应的符号表达式 。
【学习目标】 1、认识实验室里用过氧化氢制取氧气原理及操作。2、了解催化剂的作用
【活动方案】
活动一、参与用过氧化氢溶液制取氧气的演示实验2(P36)
1、观察与思考:
(1) 分液漏斗上的分液漏斗可以用长颈漏斗代替,但其下端应该深入液面 (填上或下),防止生成的气体 ;但分液漏斗比长颈漏洞的优点是能控制反应速率得到 (填平稳、不平稳)的气流。
(2). 气密性检查:用止水夹关闭,打开分液漏斗活塞,向漏斗中加入水,水面不能持续流下,最终形成一段水柱 ,就说明气密性良好。 装药品时,先 后
(填固体药品、液体药品)
2. 过氧化氢制取氧气实验原理(反应的文字和符号式): 。
?
反应物状态
反应条件
仪器、装置选择
高锰酸钾
盛少量固体及加热的仪器——
(试管、酒精灯等)
双氧水和二氧化锰
+
无须加热,接触既迅速反应
固体与液体接触就反应需进行固液分离,以控制反应的进程,则选用分液漏斗、锥形瓶等
3、[师生讨论] 在讨论的基础上进行归纳并完成下列表格:
4、思考总结;
(1)、总结:若固体(或固体+固体)加热生成气体,
选用高锰酸钾制氧气装置;
若固体+液体常温下制取气体,选用双氧水制取氧气装置。
制气装置的选取和确定要考虑到因素有: 、
比较高锰酸钾和过氧化氢制取氧气的发生装置,从节省仪器、能源、操作简单来看,哪个装置更好?
(3)、到目前为止,你能说出几种可以得到氧气的方法:(能说出4种吗?)
活动二、认识催化剂
自主学习:P36页,催化剂的知识
交流讨论:1、二氧化锰在所有化学反应中都可用作催化剂吗?
2、过氧化氢的分解反应只能用二氧化锰做催化剂吗?
3、一定量的二氧化锰完全分解加与不加二氧化锰生成氧气的量相同吗?
4、设计实验验证二氧化锰在化学反应前后的质量和化学性质都不改变。
课堂检测:
1.下列说法中正确的是 ( )
A.没有二氧化锰作催化剂,过氧化氢溶液就不会产生氧气
B.氧气的化学性质很活泼,在常温下能与所有物质发生化学反应
C.工业上分离液态空气制氧气的过程属于物理变化
D.氧气能支持呼吸、有助燃性,是一种常用的燃料。
2.结合下列图示装置,回答有关问题:?
(1)写出图中标有字母的仪器名称:a b ?
(2)上述装置可用于实验室制取和收集某些气体:
①如果用高锰酸钾制氧气,应选用的发生装置是 (填序号),反应的文字及符合表达
式 ,所选发生装置中还缺少 。?
如果用过氧化氢和二氧化锰混合制氧气,应选用的发生装置是 (填序号),反应的文字及符合表达式 ,可以选用的收集装置是 (填序号),
3 以下仪器,请回答下列问题:
(1)仪器⑤的名称是 ;取用粉末状固体用到的仪器是 (填序号)。
(2)如果用加热KmnO4的方法制取氧气,制气装置应选仪器 (填序号)。其符号表达式为: ;
(3)如果用H2O2分解来制取氧气,制气装置最好选用仪器 (填序号),其反应的文字表达式为 收集方法为
(4)比较(2)和(3)两种制取氧气的方法,最好选用方法(3)的原因是
(5)把上面分解KmnO4制取氧气的仪器装配好后,检验该装置气密性的操作方法为: 。
4. 你已经掌握了实验室制取气体的有关规律,以下是老师提供的一些实验装置。请结合下图回答问题:
(2)写出实验室用B装置制取氧气的符号表达式 。
(3)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;②氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。小芳同学用加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的反应的发生装置是 ,收集装置是 。(填字母编号)
(4)小芳将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是 , 。
(5)请写出氨气和氧化铜反应的符号表达式 。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
