人教版高中化学必修二教学资料,复习补习资料(巩固练习):37【提高】《化学与自然资源的开发利用》全章复习与巩固
文档属性
| 名称 | 人教版高中化学必修二教学资料,复习补习资料(巩固练习):37【提高】《化学与自然资源的开发利用》全章复习与巩固 |
|
|
| 格式 | zip | ||
| 文件大小 | 338.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-18 00:00:00 | ||
图片预览





文档简介
《化学与自然资源的开发利用》全章复习与巩固
【学习目标】
1、了解金属矿物、海水等自然资源的综合利用;
2、认识化石燃料综合利用的意义;
3、体会化学对环境保护的意义。
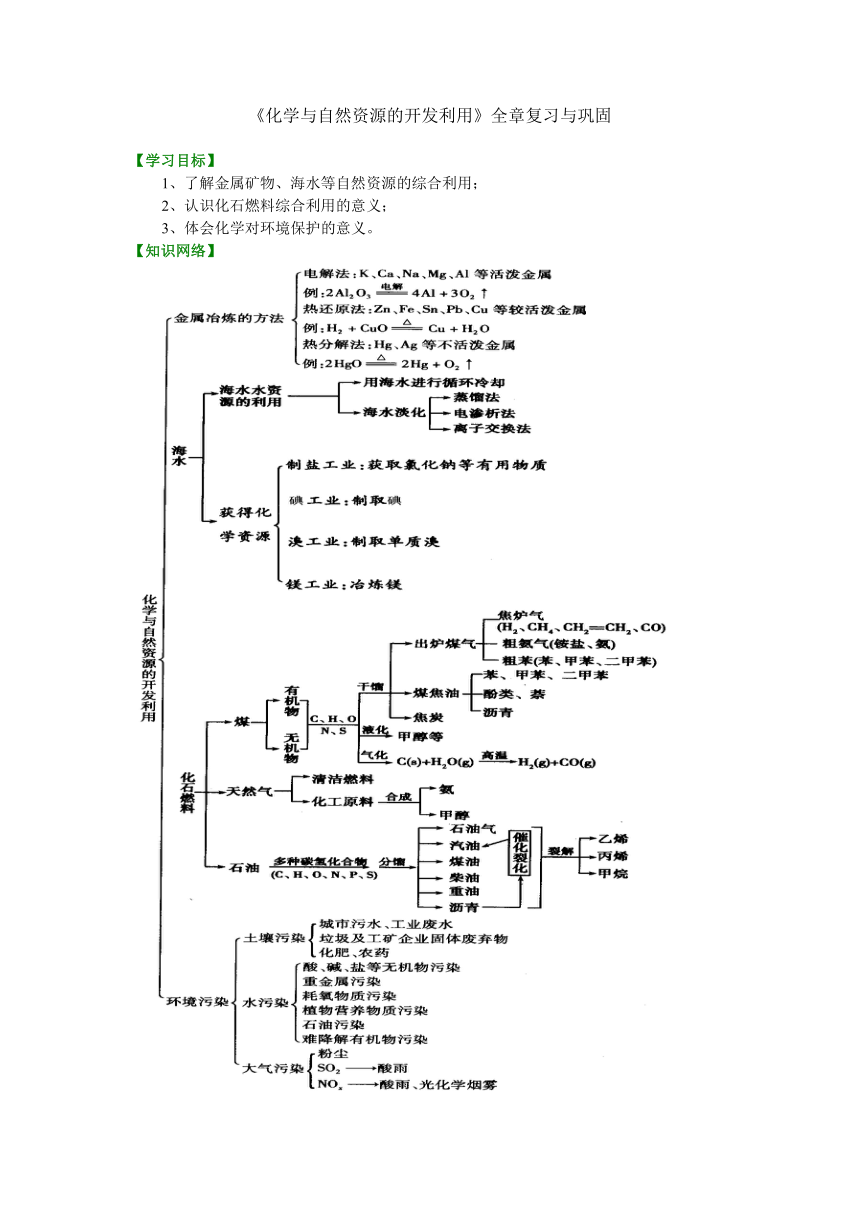
【知识网络】
【巩固练习】
一、选择题(每题有1-2个选项符合题意)
1.二战期间丹麦科学家玻尔被迫离开德军占领的祖国。为了表明一定要返回祖国的决心,他把心爱的金质诺贝尔奖章放在盛有王水(盐酸与硝酸的混合物)的玻璃容器中:
Au+HNO3+3HCl===AuCl3+NO↑+2H2O
战后玻尔返回祖国,从溶液中提取出金,又重新铸造成奖章,下列方法中,不能从溶有黄金的王水中提取出金的方法是( )。
A.萃取 B.蒸发灼烧
C.用Fe置换 D.电解
2.实验室将9 g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为18 g,则该氧化物粉末可能是( )。
A.Fe2O3和MnO2 B.MnO2和V2O5
C.Cr2O3和V2O5 D.Fe3O4和FeO
3.随着世界人口的急剧增长、工业的蓬勃发展,淡水供应危机日益成为世界关注的焦点,海水约占地球现有总水量的97%,海水淡化问题已成为科学家的主要研究方向,若实行海水淡化来供应饮用水,下列方法在原理上完全不可行的是( )。
A.加入明矾,使海水盐分沉淀而淡化
B.利用太阳能,将海水蒸馏淡化
C.将海水通过离子交换树脂,以除去所含的盐分
D.利用半透膜,采用反渗透法而使海水淡化
4.煤是重要的能源和化工原料,直接燃烧既浪费资源又污染环境。最近,某企业利用“煤粉加压气化制备合成气新技术”,让煤变成合成气(一氧化碳及氢气总含量≥90%),把煤“吃干榨尽”。下列有关说法正确的是( )。
①煤粉加压气化制备合成气过程涉及化学变化和物理变化 ②煤粉加压气化制备合成气过程涉及化学变化但没有物理变化 ③该技术实现了煤的清洁利用 ④该技术实现了煤的高效利用
A.①②③ B.①②④ C.①③④ D.②③④
5.(2019 浙江省东阳中学期中考)下列说法正确的是( )。
A.把煤加强热使之分解的过程叫煤的干馏
B.煤的气化属于化学变化
C.煤是工业上获得芳香烃的一种重要来源,主要存在于煤高温干馏所得的焦炉煤气中
D.煤中含有苯和甲苯,可用先干馏后分馏的方法把它们分离出来
6.煤的气化所得气体可用于城市家用燃气。下列选项中的气体均属于家用燃气有效成分的是( )。
A.CO、H2、N2 B.CO、CH4、H2
C.CO、CH4、CO2 D.CH4、H2、O2
7.第28届国际地质大会提供的资料显示,海底蕴藏着大量的天然气水合物,俗称可燃冰。其蕴藏量是地球上煤和石油的几百倍,因此是一种等待开发的巨大能源物质,对可燃冰的下列预测中错误的是( )。
A.高压、低温有助于可燃冰的形成
? ? ?B.可燃冰的主要可燃成分是甲烷
??? C.可燃冰是一种比较洁净的能源
???? D.可燃冰的微粒间存在着离子键
8.为了更好地解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻找新能源。以下做法中不能提高燃料的燃烧效率的是( )。
A.煤的气化与液化 B.液体燃料呈雾状喷出
C.通入过量的空气 D.将煤块粉碎
9.(2019 河北省沙河市期末考)某人坐在空调车内跟在一辆卡车后面,观察到这辆卡车在起动、刹车时排出黑烟,由此可推断这辆卡车所用的燃料是( )。
A.柴油 B.汽油 C.酒精汽油 D.液化石油气
10.(2019 河南濮阳期末考)近年来,我国许多城市禁止汽车使用含铅汽油,其主要原因是( )。
A.提高汽油燃烧效率 B.降低汽油成本 C.避免铅污染大气 D.铅资源短缺
11.某混合气体通过溴水(使其褪色),再通过灼热的氧化铜(使其由黑色变红色),再通过无水CuSO4白色粉末(使其变蓝色),再通过澄清石灰水(石灰水由澄清变浑浊,再变澄清),最后剩余气体在空气中点燃,火焰呈蓝色,这种混合气体是( )。
A.水煤气 B.焦炉煤气
C.石油液化气 D.高炉煤气
12.下列对于有机高分子化合物的认识不正确的是( )。
A.有机高分子化合物称为聚合物或高聚物,是因为它们大部分是由小分子通过聚合反应而制得的
B.有机高分子化合物的相对分子质量很大,但其结构是若干链节的重复
C.对于一种高分子材料,n是一个整数值,因而它的相对分子质量是确定的
D.高分子材料可分为天然高分子材料和合成高分子材料两大类
13.聚丙烯酸酯类涂料是目前市场上流行的墙面涂料之一,它具有弹性好、不易老化、耐擦洗、色泽亮丽等优点。其结构简式为,它属于( )。
①无机化合物 ②有机化合物 ③高分子化合物 ④离子化合物 ⑤共价化合物
A.①③④ B.①③⑤ C.②③⑤ D.②③④
14.下列广告宣传:
①某品牌八宝粥(含桂圆、红豆、糯米等)不含糖,适合糖尿病人食用 ②某品牌纯净水不含任何化学物质,可放心饮用 ③韭菜是天然的绿色食品 ④不要随意丢弃废纸,以免造成白色污染。其中错误的是( )。
A.仅② B.仅① C.仅②③④ D.①②③④
15.我国古代有“女娲补天”的传说,今天人类也面临“补天”的问题,下列采取的措施与今天所说的“补天”无关的是( )。
A.研究新型催化剂,消除汽车尾气的污染 B.禁止使用含氟电冰箱
C.倡导使用无磷洗衣粉 D.严格控制硝酸厂的尾气处理
16.人们把食品分为绿色食品、蓝色食品、白色食品等。绿色植物通过光合作用转化的食品叫绿色食品,海洋提供的食品叫蓝色食品,通过微生物发酵制得的食品叫白色食品。下面属于白色食品的是( )。
A.酱油 B.面粉 C.海带 D.菜油
17.下列有关环境问题的说法正确的是( )。
A.燃煤时加入适量石灰石,可减少废气中SO2的量
B.臭氧的体积分数超过10-4%的空气有利于人体健康
C.pH在5.6~7.0之间的降水通常称为酸雨
D.含磷合成洗涤剂易于被细菌分解,故不会导致水体污染
二、填空题
1.某河道两旁有甲、乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、 NO3-六种离子。甲厂排放的废水明显呈碱性,故甲厂废水中所含的三种离子是______、______、______;乙厂排放的废水中含有另外三种离子。如果加一定量的______(填“活性炭”、“硫酸亚铁”或“铁粉”),可以回收其中的金属______(填金属元素的符号)。另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的________(填写离子符号)转化为沉淀。经过滤后的废水主要含______(填化学式),可用来浇灌农田。
2.为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成气体(标准状况,下同)的体积为b L。反应的化学方程式是________;样品中铝的质量是________g。
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是________;氧化铁与铝的质量比是________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=__________。
3.判断下列反应能否发生,能发生的写出化学反应方程式,不能发生的说明理由。
(1)铝+氧化镁
________________________________________________________________________
________________________________________________________________________;
(2)铝+四氧化三铁
________________________________________________________________________
________________________________________________________________________;
(3)碳+氧化铝
________________________________________________________________________
________________________________________________________________________。
4.已知:A、B、F是家庭中常见的有机物,E是石油化工发展水平的标志。根据下图所示的转化关系回答问题。
(1)操作⑥的名称为__________。
(2)取代反应的范畴很广,①~⑤中属于取代反应的是__________。(填序号)
(3)请写出下列反应的化学方程式:
①_______________________________________________________________________;
③_______________________________________________________________________;
⑤_______________________________________________________________________。
(4)F是一种常见的高分子材料,它给我们带来了巨大的方便。然而,这种材料造成的当今的某一环境问题是__________。
【答案与解析】
一、选择题
1.A
【解析】Au是不活泼金属,用铁置换或电解的方法才能得到金,蒸发水分后可得到AuCl3固体,灼烧发生下列反应:2AuCl3=2Au+3Cl2↑。
2.AD
电子质量(转移1 mol e-生成金属的质量)为18 g/mol。
根据平均值规律,B项不可能生成金属单质18 g;同理,C项也不可能生成单质18 g;D项,Al完成反应时生成Fe的质量大于18 g,当氧化物粉末不足量时,生成的金属可能为18 g,D项正确。
3.A 【解析】海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等,利用排除法可以确定本题答案为A。 4.C
【解析】煤粉加压气化制备合成气过程中,既有物理变化,又有化学变化;气化后燃烧充分,且无污染。故选C项。
5.B
【解析】A项,将煤直接加强热会燃烧,故煤的干馏是将煤隔绝空气加强热使其分解的过程,故A错误;B项,煤的气化是煤和水在高温条件下反应生成CO和氢气的过程,有新物质生成,故为化学变化,故B正确;C项,焦炉煤气是多种气体的混合物,主要成分是甲烷、CO等,芳香烃存在于煤焦油中,故C错误;D项,煤中不含苯和甲苯,苯和甲苯是将煤干馏后生成的,故D错误。
6.B
【解析】家用燃气中不能含有N2、CO2和O2,利用排除法可确定本题答案是B。
7.D
【解析】可燃冰的主要成分是甲烷,是一种洁净的能源;高压、低温利于可燃冰的形成,离子键是带相反电荷的离子间的相互作用,故D错误。
8.C
【解析】将煤气化、液化,让液体燃料呈雾状喷出燃烧,将煤粉碎,都可以增大燃料与空气的接触面积,使燃料充分燃烧而提高其燃料效率;但通入过量的空气反而会带走燃料燃烧产生的部分热量,降低燃烧效率,故选C。
9.A
【解析】按一般常识,汽车所用的燃料为汽油,且酒精、液化石油气燃烧一般不会产生黑烟,所以答案应在B、C中选择。汽油的主要成分为C5—C11的烷烃,柴油的主要成分为C11—C16的烷烃,柴油分子中碳原子数目多于汽油中的碳原子数,而碳原子数越多的烷烃,其中碳的质量分数越大,燃烧时多发生不完全燃烧,生成碳等而产生黑烟,故排出黑烟者,其燃料为柴油。
10.C
【解析】铅是一种极毒的物质,是一种慢性中毒的元素,因为它能置换骨中的钙,储存在骨中而不显任何坏影响,人不会注意到它,一旦它开始溶在血液中,中毒已经很深了。铅中毒会导致死胎、流产、不育和弱智儿。现在的食品和日常生活用品对含铅量有明确的规定,尤其是儿童用品,如儿童玩具的表面油漆绝对不能用含铅量大的普通油漆,必须用特殊的无铅油漆。人们在生活中尽量少接触铅及含铅物品。汽油中的铅来自汽油添加剂——四乙基铅,它可以提高汽油的抗暴震性,提高汽油标号,但也污染了环境。所以,为了避免铅污染大扯,我国许多城市禁止汽车使用含铅汽油。
11.B
【解析】水煤气主要成分为CO、H2等,焦炉煤气主要成分为H2、CH4、C2H4、CO等,石油液化气主要成分为C3H4、C4H10,高炉煤气主要成分为CO2、CO、N2等。能符合题意的气体只有焦炉煤气。
12.C
【解析】有机高分子化合物分天然高分子化合物和合成高分子化合物两部分,合成高分子化合物主要由加聚、缩聚两类反应制备,加聚和缩聚是聚合反应的两个类型。对于高分子化合物来说,尽管相对分子质量很大,没有一个准确的相对分子质量,只有一个范围,但它们的结构均是由若干个链节组成的。
13.C
【解析】从组成来看,聚丙烯酸酯属于有机物中的高分子化合物;从价键结构来看,它属于共价化合物。
14.D
【解析】①中桂圆、红豆、糯米中本身就含有大量的淀粉,属糖类;②中H2O就是一种化学物质;③中天然的绿色食品是自然生长的,无污染,无人为因素的干预;④中白色污染指的是塑料,废纸不属于白色污染,全部错误。
15.C
【解析】今天所说的“补天”是指弥补臭氧层遭到破坏所造成的臭氧层变薄和臭氧空洞。氮氧化物、氟氯烃等都能破坏臭氧层,能杜绝或减少这些物质排放的措施都可以称为补天。
16.A
【解析】根据题中分类的标准,A是通过微生物发酵制得的食品。
17.A
【解析】A项中,CaCO3CaO+CO2↑,2CaO+2SO2+O22CaSO4;B项中,低空臭氧浓度过大对人体有害;C项中,酸雨的pH<5.6;D项中,水体含磷量高,会导致水体富营养化。
二、填空题
1.OH- Cl- K+ 铁粉 Ag Ag+、Cl-、Fe3+、OH- KNO3
【解析】甲厂排放的工业废水明显显碱性,一定含有OH-,与OH-可共存的离子有K+、Cl-、NO3-,考虑到Ag+与Cl-不能共存,所以甲厂废水中含OH-、K+、Cl-,乙厂废水中含Ag+、Fe3+和NO3-。在乙厂废水中加入一定量的铁粉可以回收银。若将两厂废水按适当比例混合,可将Ag+与Cl-、Fe3+与OH-分别转化为AgCl、Fe(OH)3沉淀。
2.
(2)2Al+Fe2O3Al2O3+2Fe 80∶27
(3)2∶3
【解析】(1)铝热剂中只有铝能与NaOH溶液反应,Fe2O3不能反应,铝与NaOH溶液反应的化学方程式为:
2Al+2NaOH+2H2O===2NaAlO2+3H2↑
2×27 3×22.4
x b L
(2)铝热剂点燃恰好完全反应,化学方程式为2Al+Fe2O3Al2O3+2Fe,由该方程式可推知:氧化铁与
3. (1)因为镁比铝活泼,所以铝不能夺取氧化镁中的镁
(2)8Al+3Fe3O44Al2O3+9Fe
(3)因为铝的还原性比碳强,所以碳不能夺取氧化铝里的铝
【解析】①高温下,铝只能把金属活动性顺序中排在其后面的金属及过渡金属从它们的氧化物中置换出来。②配平铝热反应方程式的方法是先配平氧原子,再配平其他原子。③C、H2和CO只能还原还原性比Al弱的金属,不能还原Al和比Al还原性强的金属。(1)金属活动性顺序中,Al排在Mg的后面,即Al不如Mg活泼,故Al不能置换出Mg。(2)类似Al与Fe2O3的反应 ,先写出反应物和生成物,再配平。配平时,先用最小公倍数法配平氧原子,再用观察法配平其他原子:
(3)Al的还原性比C、H2、CO都强,故高温下C与Al2O3不反应。
4.(1)分馏
(2)①②③
CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH
(4)白色污染
【解析】根据“E是石油化工发展水平的标志”可知E为乙烯。一方面,乙烯可以转化成F,另一方面,乙烯与水反应生成B。结合“B、F都是家庭中常见的物质”的信息,推断B是乙醇,F是聚乙烯。观察框图,C在酸性或碱性条件下都可以得到乙醇,说明C是某种酸与乙醇反应生成的酯。是什么酸呢?既然这种酸是家庭中常见的物质,则A是乙酸。其他答案可依次推出。
【学习目标】
1、了解金属矿物、海水等自然资源的综合利用;
2、认识化石燃料综合利用的意义;
3、体会化学对环境保护的意义。
【知识网络】
【巩固练习】
一、选择题(每题有1-2个选项符合题意)
1.二战期间丹麦科学家玻尔被迫离开德军占领的祖国。为了表明一定要返回祖国的决心,他把心爱的金质诺贝尔奖章放在盛有王水(盐酸与硝酸的混合物)的玻璃容器中:
Au+HNO3+3HCl===AuCl3+NO↑+2H2O
战后玻尔返回祖国,从溶液中提取出金,又重新铸造成奖章,下列方法中,不能从溶有黄金的王水中提取出金的方法是( )。
A.萃取 B.蒸发灼烧
C.用Fe置换 D.电解
2.实验室将9 g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为18 g,则该氧化物粉末可能是( )。
A.Fe2O3和MnO2 B.MnO2和V2O5
C.Cr2O3和V2O5 D.Fe3O4和FeO
3.随着世界人口的急剧增长、工业的蓬勃发展,淡水供应危机日益成为世界关注的焦点,海水约占地球现有总水量的97%,海水淡化问题已成为科学家的主要研究方向,若实行海水淡化来供应饮用水,下列方法在原理上完全不可行的是( )。
A.加入明矾,使海水盐分沉淀而淡化
B.利用太阳能,将海水蒸馏淡化
C.将海水通过离子交换树脂,以除去所含的盐分
D.利用半透膜,采用反渗透法而使海水淡化
4.煤是重要的能源和化工原料,直接燃烧既浪费资源又污染环境。最近,某企业利用“煤粉加压气化制备合成气新技术”,让煤变成合成气(一氧化碳及氢气总含量≥90%),把煤“吃干榨尽”。下列有关说法正确的是( )。
①煤粉加压气化制备合成气过程涉及化学变化和物理变化 ②煤粉加压气化制备合成气过程涉及化学变化但没有物理变化 ③该技术实现了煤的清洁利用 ④该技术实现了煤的高效利用
A.①②③ B.①②④ C.①③④ D.②③④
5.(2019 浙江省东阳中学期中考)下列说法正确的是( )。
A.把煤加强热使之分解的过程叫煤的干馏
B.煤的气化属于化学变化
C.煤是工业上获得芳香烃的一种重要来源,主要存在于煤高温干馏所得的焦炉煤气中
D.煤中含有苯和甲苯,可用先干馏后分馏的方法把它们分离出来
6.煤的气化所得气体可用于城市家用燃气。下列选项中的气体均属于家用燃气有效成分的是( )。
A.CO、H2、N2 B.CO、CH4、H2
C.CO、CH4、CO2 D.CH4、H2、O2
7.第28届国际地质大会提供的资料显示,海底蕴藏着大量的天然气水合物,俗称可燃冰。其蕴藏量是地球上煤和石油的几百倍,因此是一种等待开发的巨大能源物质,对可燃冰的下列预测中错误的是( )。
A.高压、低温有助于可燃冰的形成
? ? ?B.可燃冰的主要可燃成分是甲烷
??? C.可燃冰是一种比较洁净的能源
???? D.可燃冰的微粒间存在着离子键
8.为了更好地解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻找新能源。以下做法中不能提高燃料的燃烧效率的是( )。
A.煤的气化与液化 B.液体燃料呈雾状喷出
C.通入过量的空气 D.将煤块粉碎
9.(2019 河北省沙河市期末考)某人坐在空调车内跟在一辆卡车后面,观察到这辆卡车在起动、刹车时排出黑烟,由此可推断这辆卡车所用的燃料是( )。
A.柴油 B.汽油 C.酒精汽油 D.液化石油气
10.(2019 河南濮阳期末考)近年来,我国许多城市禁止汽车使用含铅汽油,其主要原因是( )。
A.提高汽油燃烧效率 B.降低汽油成本 C.避免铅污染大气 D.铅资源短缺
11.某混合气体通过溴水(使其褪色),再通过灼热的氧化铜(使其由黑色变红色),再通过无水CuSO4白色粉末(使其变蓝色),再通过澄清石灰水(石灰水由澄清变浑浊,再变澄清),最后剩余气体在空气中点燃,火焰呈蓝色,这种混合气体是( )。
A.水煤气 B.焦炉煤气
C.石油液化气 D.高炉煤气
12.下列对于有机高分子化合物的认识不正确的是( )。
A.有机高分子化合物称为聚合物或高聚物,是因为它们大部分是由小分子通过聚合反应而制得的
B.有机高分子化合物的相对分子质量很大,但其结构是若干链节的重复
C.对于一种高分子材料,n是一个整数值,因而它的相对分子质量是确定的
D.高分子材料可分为天然高分子材料和合成高分子材料两大类
13.聚丙烯酸酯类涂料是目前市场上流行的墙面涂料之一,它具有弹性好、不易老化、耐擦洗、色泽亮丽等优点。其结构简式为,它属于( )。
①无机化合物 ②有机化合物 ③高分子化合物 ④离子化合物 ⑤共价化合物
A.①③④ B.①③⑤ C.②③⑤ D.②③④
14.下列广告宣传:
①某品牌八宝粥(含桂圆、红豆、糯米等)不含糖,适合糖尿病人食用 ②某品牌纯净水不含任何化学物质,可放心饮用 ③韭菜是天然的绿色食品 ④不要随意丢弃废纸,以免造成白色污染。其中错误的是( )。
A.仅② B.仅① C.仅②③④ D.①②③④
15.我国古代有“女娲补天”的传说,今天人类也面临“补天”的问题,下列采取的措施与今天所说的“补天”无关的是( )。
A.研究新型催化剂,消除汽车尾气的污染 B.禁止使用含氟电冰箱
C.倡导使用无磷洗衣粉 D.严格控制硝酸厂的尾气处理
16.人们把食品分为绿色食品、蓝色食品、白色食品等。绿色植物通过光合作用转化的食品叫绿色食品,海洋提供的食品叫蓝色食品,通过微生物发酵制得的食品叫白色食品。下面属于白色食品的是( )。
A.酱油 B.面粉 C.海带 D.菜油
17.下列有关环境问题的说法正确的是( )。
A.燃煤时加入适量石灰石,可减少废气中SO2的量
B.臭氧的体积分数超过10-4%的空气有利于人体健康
C.pH在5.6~7.0之间的降水通常称为酸雨
D.含磷合成洗涤剂易于被细菌分解,故不会导致水体污染
二、填空题
1.某河道两旁有甲、乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、 NO3-六种离子。甲厂排放的废水明显呈碱性,故甲厂废水中所含的三种离子是______、______、______;乙厂排放的废水中含有另外三种离子。如果加一定量的______(填“活性炭”、“硫酸亚铁”或“铁粉”),可以回收其中的金属______(填金属元素的符号)。另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的________(填写离子符号)转化为沉淀。经过滤后的废水主要含______(填化学式),可用来浇灌农田。
2.为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成气体(标准状况,下同)的体积为b L。反应的化学方程式是________;样品中铝的质量是________g。
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是________;氧化铁与铝的质量比是________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=__________。
3.判断下列反应能否发生,能发生的写出化学反应方程式,不能发生的说明理由。
(1)铝+氧化镁
________________________________________________________________________
________________________________________________________________________;
(2)铝+四氧化三铁
________________________________________________________________________
________________________________________________________________________;
(3)碳+氧化铝
________________________________________________________________________
________________________________________________________________________。
4.已知:A、B、F是家庭中常见的有机物,E是石油化工发展水平的标志。根据下图所示的转化关系回答问题。
(1)操作⑥的名称为__________。
(2)取代反应的范畴很广,①~⑤中属于取代反应的是__________。(填序号)
(3)请写出下列反应的化学方程式:
①_______________________________________________________________________;
③_______________________________________________________________________;
⑤_______________________________________________________________________。
(4)F是一种常见的高分子材料,它给我们带来了巨大的方便。然而,这种材料造成的当今的某一环境问题是__________。
【答案与解析】
一、选择题
1.A
【解析】Au是不活泼金属,用铁置换或电解的方法才能得到金,蒸发水分后可得到AuCl3固体,灼烧发生下列反应:2AuCl3=2Au+3Cl2↑。
2.AD
电子质量(转移1 mol e-生成金属的质量)为18 g/mol。
根据平均值规律,B项不可能生成金属单质18 g;同理,C项也不可能生成单质18 g;D项,Al完成反应时生成Fe的质量大于18 g,当氧化物粉末不足量时,生成的金属可能为18 g,D项正确。
3.A 【解析】海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等,利用排除法可以确定本题答案为A。 4.C
【解析】煤粉加压气化制备合成气过程中,既有物理变化,又有化学变化;气化后燃烧充分,且无污染。故选C项。
5.B
【解析】A项,将煤直接加强热会燃烧,故煤的干馏是将煤隔绝空气加强热使其分解的过程,故A错误;B项,煤的气化是煤和水在高温条件下反应生成CO和氢气的过程,有新物质生成,故为化学变化,故B正确;C项,焦炉煤气是多种气体的混合物,主要成分是甲烷、CO等,芳香烃存在于煤焦油中,故C错误;D项,煤中不含苯和甲苯,苯和甲苯是将煤干馏后生成的,故D错误。
6.B
【解析】家用燃气中不能含有N2、CO2和O2,利用排除法可确定本题答案是B。
7.D
【解析】可燃冰的主要成分是甲烷,是一种洁净的能源;高压、低温利于可燃冰的形成,离子键是带相反电荷的离子间的相互作用,故D错误。
8.C
【解析】将煤气化、液化,让液体燃料呈雾状喷出燃烧,将煤粉碎,都可以增大燃料与空气的接触面积,使燃料充分燃烧而提高其燃料效率;但通入过量的空气反而会带走燃料燃烧产生的部分热量,降低燃烧效率,故选C。
9.A
【解析】按一般常识,汽车所用的燃料为汽油,且酒精、液化石油气燃烧一般不会产生黑烟,所以答案应在B、C中选择。汽油的主要成分为C5—C11的烷烃,柴油的主要成分为C11—C16的烷烃,柴油分子中碳原子数目多于汽油中的碳原子数,而碳原子数越多的烷烃,其中碳的质量分数越大,燃烧时多发生不完全燃烧,生成碳等而产生黑烟,故排出黑烟者,其燃料为柴油。
10.C
【解析】铅是一种极毒的物质,是一种慢性中毒的元素,因为它能置换骨中的钙,储存在骨中而不显任何坏影响,人不会注意到它,一旦它开始溶在血液中,中毒已经很深了。铅中毒会导致死胎、流产、不育和弱智儿。现在的食品和日常生活用品对含铅量有明确的规定,尤其是儿童用品,如儿童玩具的表面油漆绝对不能用含铅量大的普通油漆,必须用特殊的无铅油漆。人们在生活中尽量少接触铅及含铅物品。汽油中的铅来自汽油添加剂——四乙基铅,它可以提高汽油的抗暴震性,提高汽油标号,但也污染了环境。所以,为了避免铅污染大扯,我国许多城市禁止汽车使用含铅汽油。
11.B
【解析】水煤气主要成分为CO、H2等,焦炉煤气主要成分为H2、CH4、C2H4、CO等,石油液化气主要成分为C3H4、C4H10,高炉煤气主要成分为CO2、CO、N2等。能符合题意的气体只有焦炉煤气。
12.C
【解析】有机高分子化合物分天然高分子化合物和合成高分子化合物两部分,合成高分子化合物主要由加聚、缩聚两类反应制备,加聚和缩聚是聚合反应的两个类型。对于高分子化合物来说,尽管相对分子质量很大,没有一个准确的相对分子质量,只有一个范围,但它们的结构均是由若干个链节组成的。
13.C
【解析】从组成来看,聚丙烯酸酯属于有机物中的高分子化合物;从价键结构来看,它属于共价化合物。
14.D
【解析】①中桂圆、红豆、糯米中本身就含有大量的淀粉,属糖类;②中H2O就是一种化学物质;③中天然的绿色食品是自然生长的,无污染,无人为因素的干预;④中白色污染指的是塑料,废纸不属于白色污染,全部错误。
15.C
【解析】今天所说的“补天”是指弥补臭氧层遭到破坏所造成的臭氧层变薄和臭氧空洞。氮氧化物、氟氯烃等都能破坏臭氧层,能杜绝或减少这些物质排放的措施都可以称为补天。
16.A
【解析】根据题中分类的标准,A是通过微生物发酵制得的食品。
17.A
【解析】A项中,CaCO3CaO+CO2↑,2CaO+2SO2+O22CaSO4;B项中,低空臭氧浓度过大对人体有害;C项中,酸雨的pH<5.6;D项中,水体含磷量高,会导致水体富营养化。
二、填空题
1.OH- Cl- K+ 铁粉 Ag Ag+、Cl-、Fe3+、OH- KNO3
【解析】甲厂排放的工业废水明显显碱性,一定含有OH-,与OH-可共存的离子有K+、Cl-、NO3-,考虑到Ag+与Cl-不能共存,所以甲厂废水中含OH-、K+、Cl-,乙厂废水中含Ag+、Fe3+和NO3-。在乙厂废水中加入一定量的铁粉可以回收银。若将两厂废水按适当比例混合,可将Ag+与Cl-、Fe3+与OH-分别转化为AgCl、Fe(OH)3沉淀。
2.
(2)2Al+Fe2O3Al2O3+2Fe 80∶27
(3)2∶3
【解析】(1)铝热剂中只有铝能与NaOH溶液反应,Fe2O3不能反应,铝与NaOH溶液反应的化学方程式为:
2Al+2NaOH+2H2O===2NaAlO2+3H2↑
2×27 3×22.4
x b L
(2)铝热剂点燃恰好完全反应,化学方程式为2Al+Fe2O3Al2O3+2Fe,由该方程式可推知:氧化铁与
3. (1)因为镁比铝活泼,所以铝不能夺取氧化镁中的镁
(2)8Al+3Fe3O44Al2O3+9Fe
(3)因为铝的还原性比碳强,所以碳不能夺取氧化铝里的铝
【解析】①高温下,铝只能把金属活动性顺序中排在其后面的金属及过渡金属从它们的氧化物中置换出来。②配平铝热反应方程式的方法是先配平氧原子,再配平其他原子。③C、H2和CO只能还原还原性比Al弱的金属,不能还原Al和比Al还原性强的金属。(1)金属活动性顺序中,Al排在Mg的后面,即Al不如Mg活泼,故Al不能置换出Mg。(2)类似Al与Fe2O3的反应 ,先写出反应物和生成物,再配平。配平时,先用最小公倍数法配平氧原子,再用观察法配平其他原子:
(3)Al的还原性比C、H2、CO都强,故高温下C与Al2O3不反应。
4.(1)分馏
(2)①②③
CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH
(4)白色污染
【解析】根据“E是石油化工发展水平的标志”可知E为乙烯。一方面,乙烯可以转化成F,另一方面,乙烯与水反应生成B。结合“B、F都是家庭中常见的物质”的信息,推断B是乙醇,F是聚乙烯。观察框图,C在酸性或碱性条件下都可以得到乙醇,说明C是某种酸与乙醇反应生成的酯。是什么酸呢?既然这种酸是家庭中常见的物质,则A是乙酸。其他答案可依次推出。
