人教版高中化学选修4第四章第一节 原电池 课件(共31张PPT)
文档属性
| 名称 | 人教版高中化学选修4第四章第一节 原电池 课件(共31张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-18 00:00:00 | ||
图片预览







文档简介
(共31张PPT)
原电池
你能帮助格林太太吗?
你能帮助格林太太吗?
能源
一次能源:直接从自然界取得的
能源。
二次能源:一次能源经过加工、
转换得到的能源。
一次能源:
二次能源:
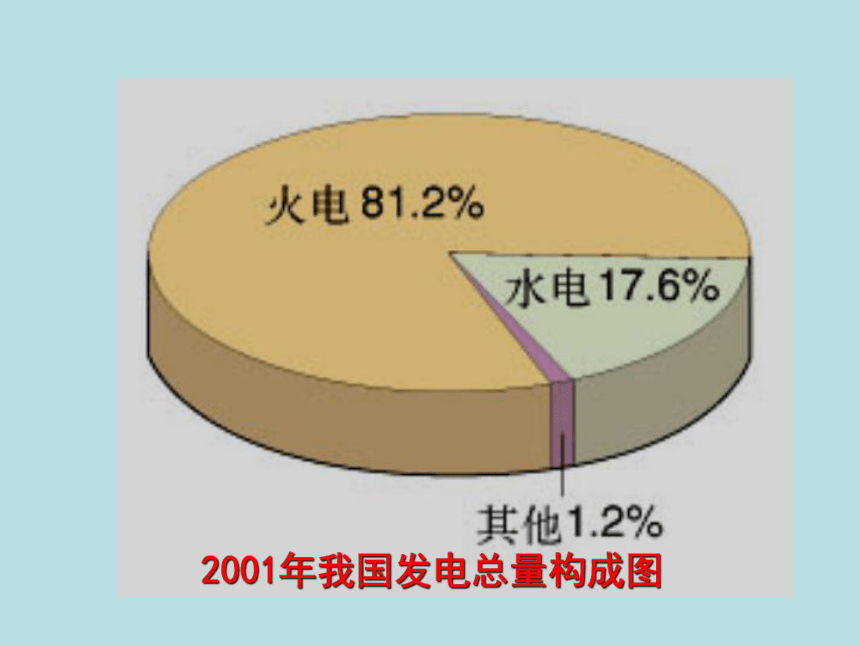
2001年我国发电总量构成图
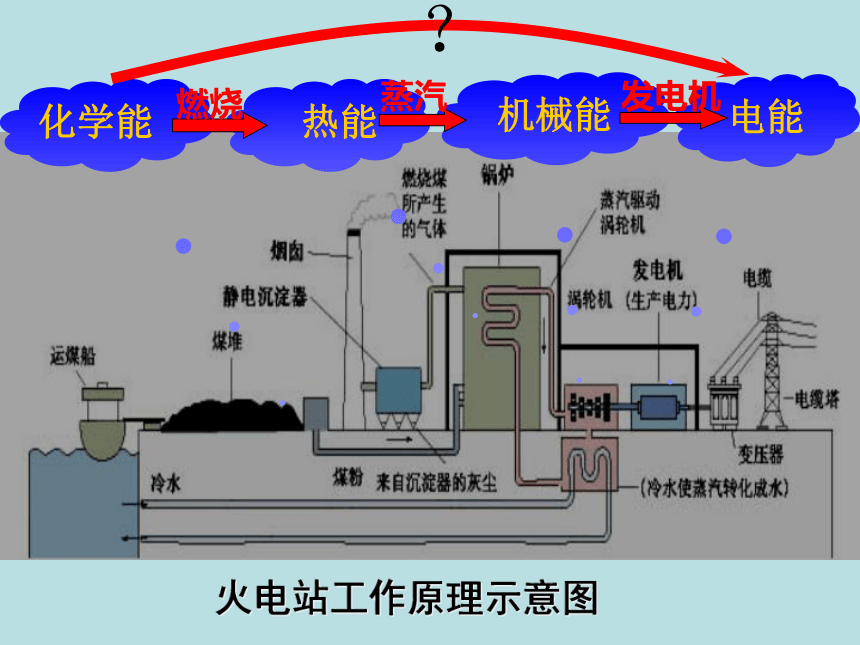
火电站工作原理示意图
化学能
电能
机械能
热能
?
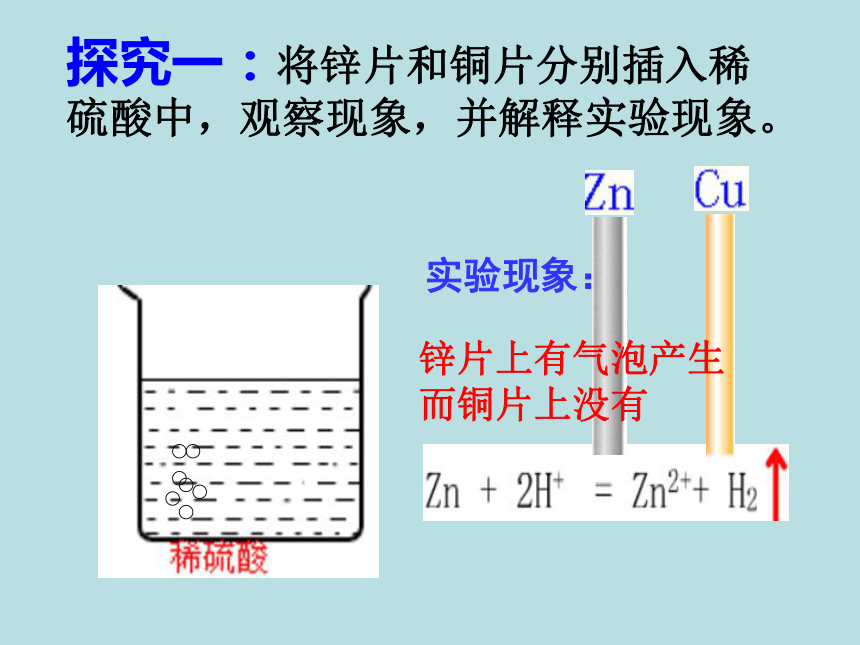
实验现象:
锌片上有气泡产生
而铜片上没有
探究一:将锌片和铜片分别插入稀硫酸中,观察现象,并解释实验现象。
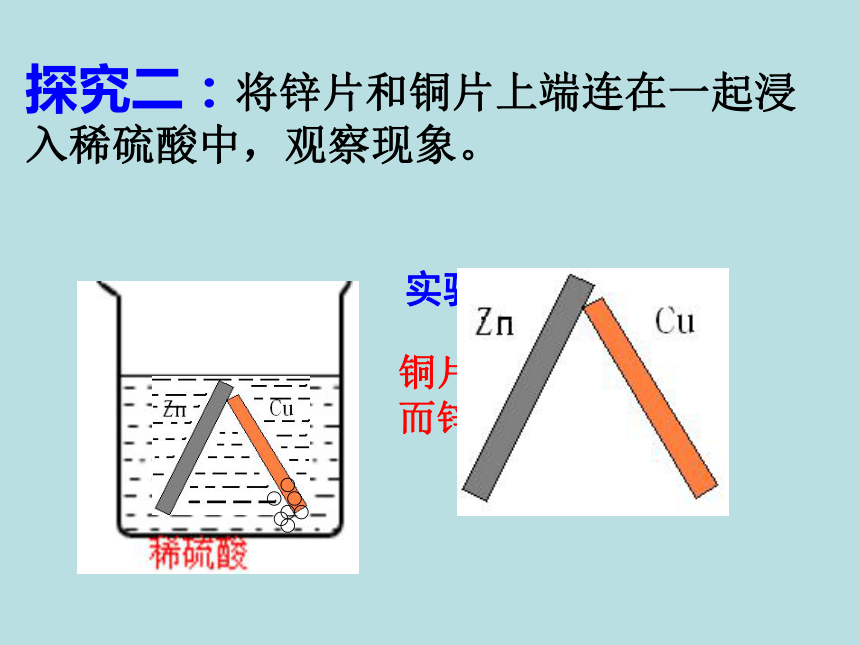
实验现象:
铜片上有气泡产生
而锌片上没有
探究二:将锌片和铜片上端连在一起浸入稀硫酸中,观察现象。
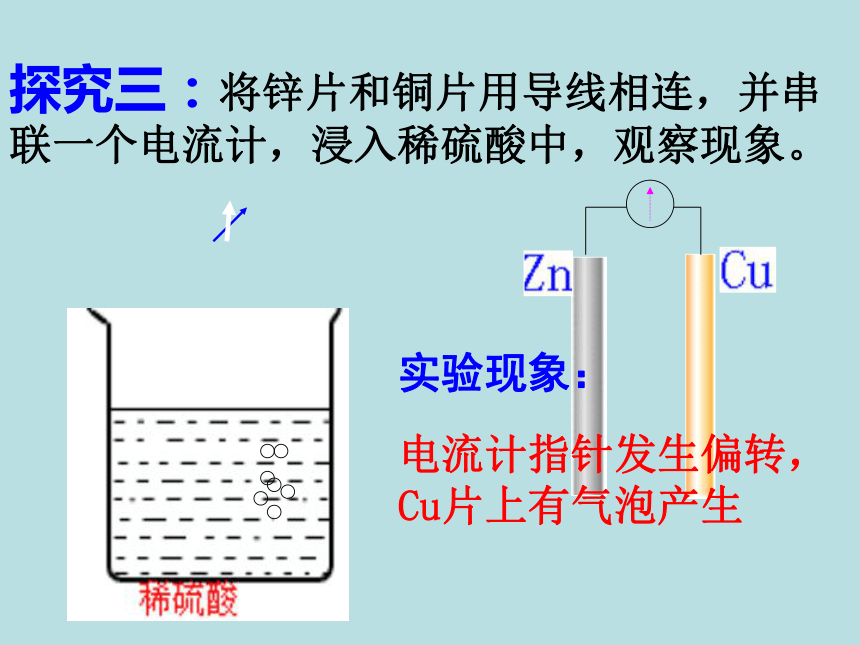
实验现象:
电流计指针发生偏转,
Cu片上有气泡产生
探究三:将锌片和铜片用导线相连,并串联一个电流计,浸入稀硫酸中,观察现象。
一·原电池
1·定义:
把化学能转化为电能的装置叫做原电池
2.原电池工作原理
负极:
锌片:Zn-2e-=Zn2+
铜片:2H++2e-=H2↑
总反应:
Zn+2H+=Zn2++H2↑
正极:
(失去电子,发生氧化反应)
(得到电子,发生还原反应)
原电池工作原理
较活泼的金属失去电子发生氧化反应,电子从较活泼金属(负极)通过外电路流向较不活泼的金属(正极)。
“电子从Zn极(负极)流出,流入Cu极(正极)”
失e-
氧化
反应
得e-
还原
反应
铜锌原电池微观模拟
工作原理小结:
1.外电路:电子由负极流向正极
2.内电路:阴离子移向负极
阳离子移向正极
3.电极反应:负极 Zn - 2e- =Zn2+
正极 2H++2e- =H2 ↑
3.原电池的形成条件
实验探究形成原电池的条件
(可以)
(可以)
(可以)
(不可以)
形成条件一:
活泼性不同的两个电极
负极:较活泼的金属
正极:较不活泼的金属、石墨等
第一组实验
Fe
Fe
(可以)
(不可以)
形成条件二:电极需插进电解质溶液中;
第二组实验
实验探究形成原电池的条件
第三组实验
形成条件三:必须形成闭合回路
(不可以)
实验探究形成原电池的条件
原电池形成条件:
1.活泼性不同的两个电极
2.电解质溶液
3.闭合电路
4.自发进行的氧化还原反应
判断下列哪些装置构成了原电池?若不是,请说明理由.
①
②
③
(×)
(×)
(∨)
④
(∨)
⑤
(∨)
练习1、
4.正负极判断方法
(1)活泼性 活泼的做负极
(2)电流流向 正极流向负极
(3)电子流向 负极流向正极
(4)电极现象 负极溶解变细,正极有气
泡或者变粗
(5)阴阳离子移动方向 阳离子移向正极
阴离子移向负极
(6)电极反应类型 负极失电子氧化反应
正极得电子还原反应
练习
⒈
请指出正负极名称,并写出电极反应式.
2H++2e-=H2↑
负极:
总反应:
正极:
Zn-2e-=Zn2+
Zn+2H+=Zn2++H2↑
负极:
正极:
总反应:
正极:
负极:
总反应:
Zn-2e- =Zn2+
2H++2e- =H2↑
Zn+2H+=Zn2++H2↑
Fe-2e - =Fe2+
Cu2++2e- =Cu
Fe+Cu2+=Fe2++Cu
正极(Al):
负极(Mg):
Mg-2e-= Mg2+
总反应式:
负极(Al)正极(Mg)
不活泼是相对的,活泼也是相对的
5.电极反应式书写
负极:电极材料本身失电子
正极:溶液中的阳离子得电子
两极得失电子数目相等
总反应:正负两极反应相加
有下列材料:Zn片(2片)、Cu片(2片)、
导线、水果 (西红柿、柑橘等)、电流计,
请设计一个装置使电流计指针发生偏转,
并画出设计草图。
Zn
把a、b、c、d四块金属片浸入稀硫酸中,用
导线两两相连组成原电池。若a、b相连时,a为
负极;c、d相连时,电流由d到c;a、c相连时,
c极上产生大量气泡,b、d相连时,b上有大量气
泡产生,则四种金属的活动性顺序由强到弱的为: ( )
A.a > b > c > d
B.a > c > d > b
C.c > a > b > d
D.b > d > c > a
B
如何设计一个原电池,其原电池
反应为:Cu+2FeCl3= 2FeCl2 +CuCl2
写出电极名称和电极反应式。
用铜作负极,碳棒作正极。
负极: Cu- 2e-=Cu2+
正极: 2Fe3+ + 2e- = 2Fe2+
思考题:
本节课小结:
一.原电池
1.定义:把化学能转化为电能的装置
2.工作原理:外电路电子由负极流向正极,
内电路阴阳离子定向移动
3.形成的条件: 活泼性不同的两个电极,电解质溶液,闭合电路,自发进行的
氧化还原反应
4.正负极判断方法:(1)活泼性 活泼的做负极
(2)电流流向 正极流向负极
(3)电子流向 负极流向正极
(4)电极现象 负极溶解变细,正极有气泡或者变粗
(5)阴阳离子移动方向 阳离子移向正极
阴离子移向负极
(6)电极反应类型 负极失电子氧化反应
正极得电子还原反应
5.电极反应式书写:
负极:电极材料本身失电子
正极:溶液中的阳离子得电子
两极得失电子数目相等
总反应:正负两极反应相加
原电池
你能帮助格林太太吗?
你能帮助格林太太吗?
能源
一次能源:直接从自然界取得的
能源。
二次能源:一次能源经过加工、
转换得到的能源。
一次能源:
二次能源:
2001年我国发电总量构成图
火电站工作原理示意图
化学能
电能
机械能
热能
?
实验现象:
锌片上有气泡产生
而铜片上没有
探究一:将锌片和铜片分别插入稀硫酸中,观察现象,并解释实验现象。
实验现象:
铜片上有气泡产生
而锌片上没有
探究二:将锌片和铜片上端连在一起浸入稀硫酸中,观察现象。
实验现象:
电流计指针发生偏转,
Cu片上有气泡产生
探究三:将锌片和铜片用导线相连,并串联一个电流计,浸入稀硫酸中,观察现象。
一·原电池
1·定义:
把化学能转化为电能的装置叫做原电池
2.原电池工作原理
负极:
锌片:Zn-2e-=Zn2+
铜片:2H++2e-=H2↑
总反应:
Zn+2H+=Zn2++H2↑
正极:
(失去电子,发生氧化反应)
(得到电子,发生还原反应)
原电池工作原理
较活泼的金属失去电子发生氧化反应,电子从较活泼金属(负极)通过外电路流向较不活泼的金属(正极)。
“电子从Zn极(负极)流出,流入Cu极(正极)”
失e-
氧化
反应
得e-
还原
反应
铜锌原电池微观模拟
工作原理小结:
1.外电路:电子由负极流向正极
2.内电路:阴离子移向负极
阳离子移向正极
3.电极反应:负极 Zn - 2e- =Zn2+
正极 2H++2e- =H2 ↑
3.原电池的形成条件
实验探究形成原电池的条件
(可以)
(可以)
(可以)
(不可以)
形成条件一:
活泼性不同的两个电极
负极:较活泼的金属
正极:较不活泼的金属、石墨等
第一组实验
Fe
Fe
(可以)
(不可以)
形成条件二:电极需插进电解质溶液中;
第二组实验
实验探究形成原电池的条件
第三组实验
形成条件三:必须形成闭合回路
(不可以)
实验探究形成原电池的条件
原电池形成条件:
1.活泼性不同的两个电极
2.电解质溶液
3.闭合电路
4.自发进行的氧化还原反应
判断下列哪些装置构成了原电池?若不是,请说明理由.
①
②
③
(×)
(×)
(∨)
④
(∨)
⑤
(∨)
练习1、
4.正负极判断方法
(1)活泼性 活泼的做负极
(2)电流流向 正极流向负极
(3)电子流向 负极流向正极
(4)电极现象 负极溶解变细,正极有气
泡或者变粗
(5)阴阳离子移动方向 阳离子移向正极
阴离子移向负极
(6)电极反应类型 负极失电子氧化反应
正极得电子还原反应
练习
⒈
请指出正负极名称,并写出电极反应式.
2H++2e-=H2↑
负极:
总反应:
正极:
Zn-2e-=Zn2+
Zn+2H+=Zn2++H2↑
负极:
正极:
总反应:
正极:
负极:
总反应:
Zn-2e- =Zn2+
2H++2e- =H2↑
Zn+2H+=Zn2++H2↑
Fe-2e - =Fe2+
Cu2++2e- =Cu
Fe+Cu2+=Fe2++Cu
正极(Al):
负极(Mg):
Mg-2e-= Mg2+
总反应式:
负极(Al)正极(Mg)
不活泼是相对的,活泼也是相对的
5.电极反应式书写
负极:电极材料本身失电子
正极:溶液中的阳离子得电子
两极得失电子数目相等
总反应:正负两极反应相加
有下列材料:Zn片(2片)、Cu片(2片)、
导线、水果 (西红柿、柑橘等)、电流计,
请设计一个装置使电流计指针发生偏转,
并画出设计草图。
Zn
把a、b、c、d四块金属片浸入稀硫酸中,用
导线两两相连组成原电池。若a、b相连时,a为
负极;c、d相连时,电流由d到c;a、c相连时,
c极上产生大量气泡,b、d相连时,b上有大量气
泡产生,则四种金属的活动性顺序由强到弱的为: ( )
A.a > b > c > d
B.a > c > d > b
C.c > a > b > d
D.b > d > c > a
B
如何设计一个原电池,其原电池
反应为:Cu+2FeCl3= 2FeCl2 +CuCl2
写出电极名称和电极反应式。
用铜作负极,碳棒作正极。
负极: Cu- 2e-=Cu2+
正极: 2Fe3+ + 2e- = 2Fe2+
思考题:
本节课小结:
一.原电池
1.定义:把化学能转化为电能的装置
2.工作原理:外电路电子由负极流向正极,
内电路阴阳离子定向移动
3.形成的条件: 活泼性不同的两个电极,电解质溶液,闭合电路,自发进行的
氧化还原反应
4.正负极判断方法:(1)活泼性 活泼的做负极
(2)电流流向 正极流向负极
(3)电子流向 负极流向正极
(4)电极现象 负极溶解变细,正极有气泡或者变粗
(5)阴阳离子移动方向 阳离子移向正极
阴离子移向负极
(6)电极反应类型 负极失电子氧化反应
正极得电子还原反应
5.电极反应式书写:
负极:电极材料本身失电子
正极:溶液中的阳离子得电子
两极得失电子数目相等
总反应:正负两极反应相加
