科粤版化学九年级下册 6.1 金属材料的物理特性 课件 (共21张PPT)
文档属性
| 名称 | 科粤版化学九年级下册 6.1 金属材料的物理特性 课件 (共21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 572.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-21 00:00:00 | ||
图片预览








文档简介
(共29张PPT)
九年级化学科粤版第六章 金属
6.1 奇妙的金属性质
这些金属制品有哪些相似的物理性质?
物理性质
常温下为固体(汞除外)
金属光泽
导电性
导热性
延展性
金属共同的物理性质
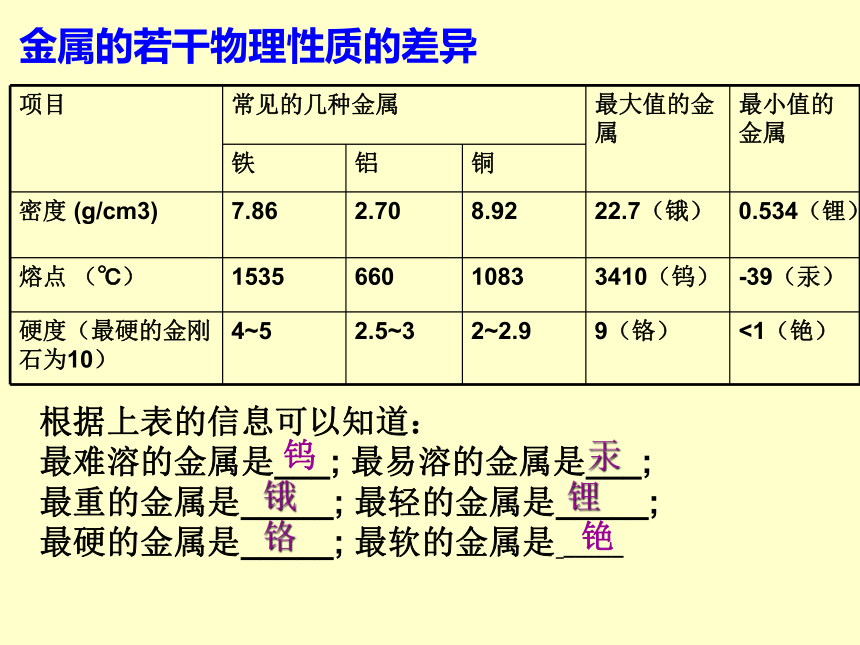
根据上表的信息可以知道:
最难溶的金属是___; 最易溶的金属是___;
最重的金属是_____; 最轻的金属是_____;
最硬的金属是_____; 最软的金属是 _____
金属的若干物理性质的差异
钨
汞
锂
锇
铬
铯
项目 常见的几种金属 最大值的金属 最小值的金属
铁 铝 铜
密度 (g/cm3) 7.86 2.70 8.92 22.7(锇) 0.534(锂)
熔点 (℃) 1535 660 1083 3410(钨) -39(汞)
硬度(最硬的金刚石为10) 4~5 2.5~3 2~2.9 9(铬) <1(铯)
金属的其他化学之最
人类最早发现和冶炼的金属──铜
目前世界年产量最高的金属──铁
地壳中含量最高的金属元素──铝
人体中含量最高的金属元素──钙
导电性、导热性最好的金属──银
延性最好的金属──铂
展性最好的金属──金
二、金属的化学性质
1.常温下铝跟空气中的氧气反应,生成致密的氧化膜
2.铝在纯氧中燃烧,发出耀眼白光,生成氧化铝
3.铁丝在纯氧中燃烧,火星四射,生成四氧化三铁
4.铜跟氧气在加热时反应,生成黑色的氧化铜
5.金不能与氧气反应(真金不怕火炼)
许多金属都能与氧气反应生成氧化物
(一)金属跟氧气反应:
讨论:从以下反应中你能得到哪些信息?
(1)4Al+3O2=2Al2O3 (常温)(2)2Cu+O2加热 2CuO
(3)2Mg+O2=2MgO (常温 )(4)Au + O2 →不反应
(5)3Fe+2 O2 点燃 Fe3 O4
综合上述信息可知:
1.大多数金属都能与_______反应,
反应剧烈程度 ________(相同,不相同)
2.金属的活动性:说明 _______ 较活泼,________次之, ______很不活泼
Au
氧气
不相同
Al、Mg
Fe、Cu
(1)铝在常温下能与氧气反应,那么我们用的铝制餐具是怎么回事呢?
金属铝在常温下发生缓慢氧化,形成一层致密的氧化物薄膜,从而阻止铝的进一步氧化,因而铝具有较好的抗腐蚀性。
(2)为何不宜用钢刷来擦洗铝制餐具呢?
若用钢刷擦洗铝制品,容易把氧化薄膜除掉,从而起不到保护作用。
思考:
镁与盐酸
锌与盐酸
铁与盐酸
铜放入盐酸中
反应非常激烈,放出大量无色气泡
反应较剧烈,放出大量无色气泡
反应较慢,有无色气泡放出由无色变为浅绿色
没有明显变化
Mg+2HCl=MgCl2+H2↑
Zn+2HCl =ZnCl2 +H2↑
Fe +2HCl =FeCl2 + H2↑
Mg+H2SO4=MgSO4+H2↑
Zn +H2SO4 =ZnSO4 +H2↑
Fe +H2SO4 =FeSO4 +H2↑
(二)金属与稀盐酸(或稀硫酸)反应
反应激烈,放出大量无色气泡
金 属 现象 反应的化学方程式
稀盐酸 稀硫酸 稀盐酸 稀硫酸
镁
铝
锌
铁
铜
金属活动性顺序:
k Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
?
?
金属活动性由强逐渐减弱
1.在金属活动性顺序中,金属的位置越靠前,它的活动性越强。
2.在金属活动性顺序中,位于氢前面的金属能置换出盐酸、稀硫酸中的氢
3.在金属活动性顺序中,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
这是重点吆!
(二)金属与稀盐酸(或稀硫酸)反应
Mg+2HCl=MgCl2+H2↑
Zn+2HCl =ZnCl2 +H2↑
Fe +2HCl =FeCl2 + H2↑
Mg+H2SO4=MgSO4+H2↑
Zn +H2SO4 =ZnSO4 +H2↑
Fe +H2SO4 =FeSO4 +H2↑
(三)金属与金属化合物溶液的反应
铝片表面有红色固体出现,溶液由蓝色变为无色
铁钉表面有红色固体出现,溶液由蓝色变为浅绿色
无明显变化
实 验 现 象 化学方程式
铝片浸入CuSO4溶液中 ? ?
铜片浸入Al2(SO4)3溶液中 ?
铁钉浸入CuSO4溶液中 ? ?
(三)金属与金属化合物溶液的反应
反应的化学方程式:
Mg + 2HCl == H2↑ + MgCl2
Zn + 2HCl == H2↑ + ZnCl2
Fe + 2HCl == H2↑ + FeCl2
Mg + H2SO4 ==
(氯化亚铁)
(硫酸亚铁)
Zn + H2SO4 == H2↑ + ZnSO4
Fe + H2SO4 == H2↑ + FeSO4
+ MgSO4
H2↑
反应的化学方程式:
Mg + 2HCl == H2↑ + MgCl2
Zn + 2HCl == H2↑ + ZnCl2
Fe + 2HCl == H2↑ + FeCl2
Mg + H2SO4 == H2↑ + MgSO4
Zn + H2SO4 == H2↑ + ZnSO4
Fe + H2SO4 == H2↑ + FeSO4
单质
化合物
化合物
单质
置换反应:
+
+
由一种单质与一种化合物反应,生成另一
种单质与另一种化合物的反应叫做置换反应。
物理性质
金属光泽、延展性、
导电性、导热性
化学性质
金属
性质
金属跟某些金属化合物溶液反应
金属的性质
大多数金属能与O2反应
许多金属能与稀盐酸(或稀硫酸)反应
课堂小结
练 习
2.人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。请回答:
(1)地壳中含量最多的金属元素是 。
(2)根据下图的应用实例,试说出金属具有的两点物理性质
3.下图是同学们经常使用的铅笔示意图。
(1)在组成铅笔的各种材料中,能导电的是 ,
燃烧时产物中有二氧化碳的是 。(每空只要求
填一 种,填序号)
(2)上图中④的主要成分是金属铝。将一小片该金属放入
稀盐酸中,观察到的现象是 ,反应
的化学方程式是 。
再 见!
九年级化学科粤版第六章 金属
6.1 奇妙的金属性质
这些金属制品有哪些相似的物理性质?
物理性质
常温下为固体(汞除外)
金属光泽
导电性
导热性
延展性
金属共同的物理性质
根据上表的信息可以知道:
最难溶的金属是___; 最易溶的金属是___;
最重的金属是_____; 最轻的金属是_____;
最硬的金属是_____; 最软的金属是 _____
金属的若干物理性质的差异
钨
汞
锂
锇
铬
铯
项目 常见的几种金属 最大值的金属 最小值的金属
铁 铝 铜
密度 (g/cm3) 7.86 2.70 8.92 22.7(锇) 0.534(锂)
熔点 (℃) 1535 660 1083 3410(钨) -39(汞)
硬度(最硬的金刚石为10) 4~5 2.5~3 2~2.9 9(铬) <1(铯)
金属的其他化学之最
人类最早发现和冶炼的金属──铜
目前世界年产量最高的金属──铁
地壳中含量最高的金属元素──铝
人体中含量最高的金属元素──钙
导电性、导热性最好的金属──银
延性最好的金属──铂
展性最好的金属──金
二、金属的化学性质
1.常温下铝跟空气中的氧气反应,生成致密的氧化膜
2.铝在纯氧中燃烧,发出耀眼白光,生成氧化铝
3.铁丝在纯氧中燃烧,火星四射,生成四氧化三铁
4.铜跟氧气在加热时反应,生成黑色的氧化铜
5.金不能与氧气反应(真金不怕火炼)
许多金属都能与氧气反应生成氧化物
(一)金属跟氧气反应:
讨论:从以下反应中你能得到哪些信息?
(1)4Al+3O2=2Al2O3 (常温)(2)2Cu+O2加热 2CuO
(3)2Mg+O2=2MgO (常温 )(4)Au + O2 →不反应
(5)3Fe+2 O2 点燃 Fe3 O4
综合上述信息可知:
1.大多数金属都能与_______反应,
反应剧烈程度 ________(相同,不相同)
2.金属的活动性:说明 _______ 较活泼,________次之, ______很不活泼
Au
氧气
不相同
Al、Mg
Fe、Cu
(1)铝在常温下能与氧气反应,那么我们用的铝制餐具是怎么回事呢?
金属铝在常温下发生缓慢氧化,形成一层致密的氧化物薄膜,从而阻止铝的进一步氧化,因而铝具有较好的抗腐蚀性。
(2)为何不宜用钢刷来擦洗铝制餐具呢?
若用钢刷擦洗铝制品,容易把氧化薄膜除掉,从而起不到保护作用。
思考:
镁与盐酸
锌与盐酸
铁与盐酸
铜放入盐酸中
反应非常激烈,放出大量无色气泡
反应较剧烈,放出大量无色气泡
反应较慢,有无色气泡放出由无色变为浅绿色
没有明显变化
Mg+2HCl=MgCl2+H2↑
Zn+2HCl =ZnCl2 +H2↑
Fe +2HCl =FeCl2 + H2↑
Mg+H2SO4=MgSO4+H2↑
Zn +H2SO4 =ZnSO4 +H2↑
Fe +H2SO4 =FeSO4 +H2↑
(二)金属与稀盐酸(或稀硫酸)反应
反应激烈,放出大量无色气泡
金 属 现象 反应的化学方程式
稀盐酸 稀硫酸 稀盐酸 稀硫酸
镁
铝
锌
铁
铜
金属活动性顺序:
k Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
?
?
金属活动性由强逐渐减弱
1.在金属活动性顺序中,金属的位置越靠前,它的活动性越强。
2.在金属活动性顺序中,位于氢前面的金属能置换出盐酸、稀硫酸中的氢
3.在金属活动性顺序中,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
这是重点吆!
(二)金属与稀盐酸(或稀硫酸)反应
Mg+2HCl=MgCl2+H2↑
Zn+2HCl =ZnCl2 +H2↑
Fe +2HCl =FeCl2 + H2↑
Mg+H2SO4=MgSO4+H2↑
Zn +H2SO4 =ZnSO4 +H2↑
Fe +H2SO4 =FeSO4 +H2↑
(三)金属与金属化合物溶液的反应
铝片表面有红色固体出现,溶液由蓝色变为无色
铁钉表面有红色固体出现,溶液由蓝色变为浅绿色
无明显变化
实 验 现 象 化学方程式
铝片浸入CuSO4溶液中 ? ?
铜片浸入Al2(SO4)3溶液中 ?
铁钉浸入CuSO4溶液中 ? ?
(三)金属与金属化合物溶液的反应
反应的化学方程式:
Mg + 2HCl == H2↑ + MgCl2
Zn + 2HCl == H2↑ + ZnCl2
Fe + 2HCl == H2↑ + FeCl2
Mg + H2SO4 ==
(氯化亚铁)
(硫酸亚铁)
Zn + H2SO4 == H2↑ + ZnSO4
Fe + H2SO4 == H2↑ + FeSO4
+ MgSO4
H2↑
反应的化学方程式:
Mg + 2HCl == H2↑ + MgCl2
Zn + 2HCl == H2↑ + ZnCl2
Fe + 2HCl == H2↑ + FeCl2
Mg + H2SO4 == H2↑ + MgSO4
Zn + H2SO4 == H2↑ + ZnSO4
Fe + H2SO4 == H2↑ + FeSO4
单质
化合物
化合物
单质
置换反应:
+
+
由一种单质与一种化合物反应,生成另一
种单质与另一种化合物的反应叫做置换反应。
物理性质
金属光泽、延展性、
导电性、导热性
化学性质
金属
性质
金属跟某些金属化合物溶液反应
金属的性质
大多数金属能与O2反应
许多金属能与稀盐酸(或稀硫酸)反应
课堂小结
练 习
2.人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。请回答:
(1)地壳中含量最多的金属元素是 。
(2)根据下图的应用实例,试说出金属具有的两点物理性质
3.下图是同学们经常使用的铅笔示意图。
(1)在组成铅笔的各种材料中,能导电的是 ,
燃烧时产物中有二氧化碳的是 。(每空只要求
填一 种,填序号)
(2)上图中④的主要成分是金属铝。将一小片该金属放入
稀盐酸中,观察到的现象是 ,反应
的化学方程式是 。
再 见!
