沪教版九上化学 3.1.4构成物质的基本微粒 离子 教案
文档属性
| 名称 | 沪教版九上化学 3.1.4构成物质的基本微粒 离子 教案 |

|
|
| 格式 | zip | ||
| 文件大小 | 47.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-22 00:00:00 | ||
图片预览

文档简介
第3章 第1节 构成物质的基本微粒---离子
沪教版 2013版
课标与《能力自测》评价指要的对照
课标
《能力自测》评价指要
1、知道离子是构成物质的一种微粒。
2、了解原子和离子可以相互转化。
3、初步认识核外电子在化学反应中的作用。
1、离子是构成物质的一种微粒。B级
2、形成物质是由微粒构成及其运动和变化的观点。B级
3、同一元素的原子和离子可以相互转化。B级
4、核外电子在化学反应中的作用。
B级。
教学背景分析
教材内容分析
主要内容为:离子是构成物质的一种微粒,化学变化中可能形成离子,原子和离子可以相互转化,初步认识核外电子在化学化学反应的的作用。
学情
分析
初二物理学中,学习了分子。学习了原子的构成、原子核的构成,知道分子、原子不显电性,但没有提及原子核内的质子数和核外电子数以及二者的数量关系。初三化学沪教版教材的第3章第一节的第一课时只简单提到构成物质的微粒有分子、原子、离子,学生对它们认识不多。
教学目标
1、知识与技能
①感受离子的存在,知道离子也是构成物质的一种粒子。
②了解离子的形成过程。
③了解分子、原子、离子之间的转化。
2、过程与方法
①通过观察实验,感受离子的存在。
②通过实验对比分析,知道化学变化中可以形成离子。
③观看多媒体动画演示,能体会到离子的形成过程。?
④学会用归纳总结的方法整理分子、原子、离子间的转化
3、情感态度与价值观
学生客观地认识物质,感受探索物质构成奥秘的乐趣。
重 难 点
分 析
重点:离子的存在和离子的形成过程。因为微粒肉眼看不见,化抽象为具体很重要,所以用高锰酸根定向移动体现离子的存在、用多媒体动画演示氯化钠形成过程来突破”离子形成过程”这一难点。
难点:离子的形成过程,分子、原子、离子之间的转化。由于有关分子、原子的内容学生知道不多,初二学习的内容不够具体。突破难点,我用水分子分解动画和氯化钠形成动画演示,从而让学生感悟分子、原子、离子之间的转化。
教学方法
实验教学法 多媒体教学法 对比分析法 归纳总结法
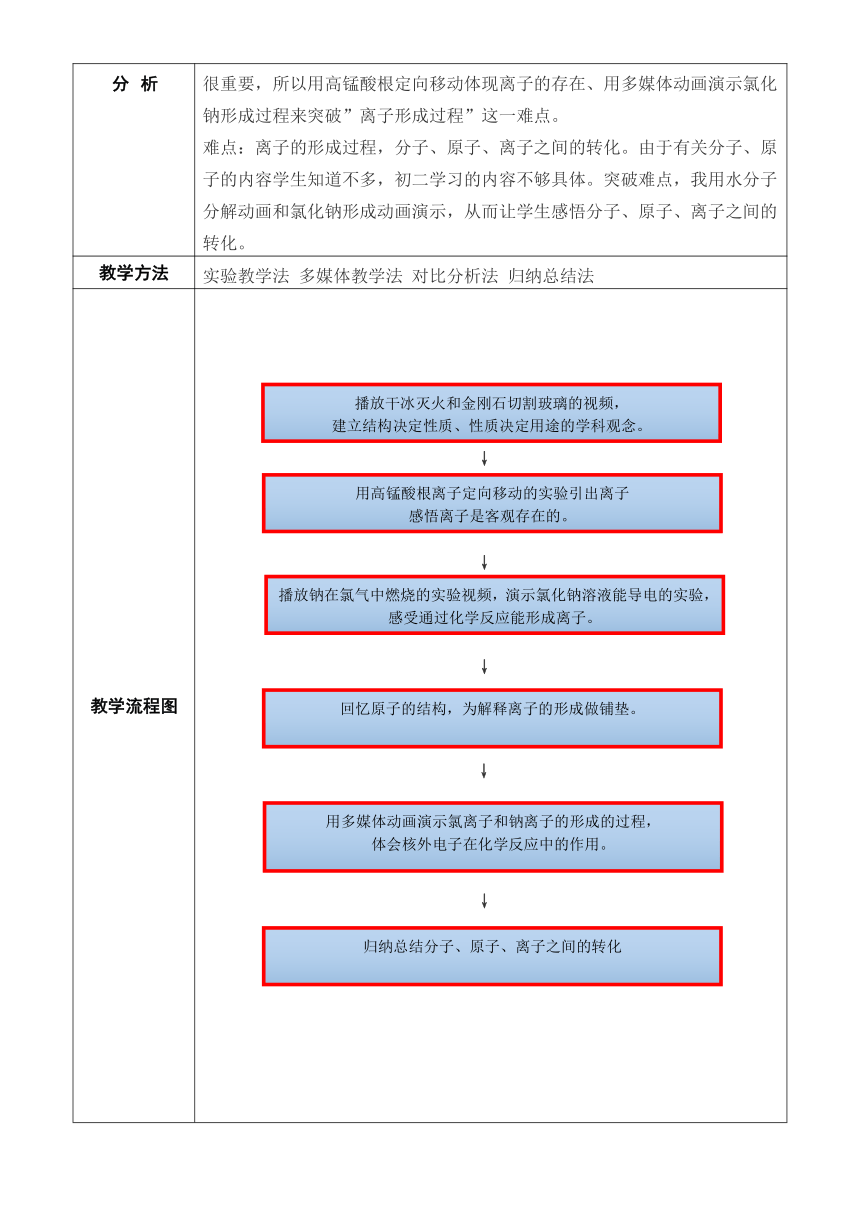
教学流程图
↓
↓
↓
↓
↓
教学过程
教 师 活 动
学 生 活 动
设计意图
导 入
播放:干冰灭和金刚石切割玻璃的视频。
讲述:结构决定性质、性质决定用途。
提问:干冰是由什么微粒构成的?
金刚石是由什么微粒构成的?
设问:展示高锰酸钾,高锰酸钾是由什么微粒构成的呢?。
学生认真观看视频并思考。
回答:二氧化碳分子;碳原子。
展示熟悉的宏观物质,引导学生走进微观世界。
导
学
导
学
导
学
一、离子是构成物质的一种微粒。
演示实验:将两层滤纸用硫酸钾溶液润湿,平铺在玻璃片上。滤纸中心轴处放一根蘸有紫红色高锰酸钾溶液的棉线。滤纸两侧加12伏直流电压。如图
请同学生表述实验现象
提问:紫色液体中有带电的微粒吗?
提问:离子的基本性质有哪些?
二、离子的形成和表示方法
1、离子的形成
播放:钠在氯气中燃烧的实验视频。
提问:这是物理变化还是化学变化?生成了什么?
演示:蔗糖溶液和氯化钠溶液的导电性对比实验。
提问:哪种溶液里有较多的自由移动的离子?
氯化钠是由什么微粒构成的?
教师过渡:氯离子和钠离子是怎样形成呢?我们还要从原子说起。
提问:原子的结构?
教师板书
原子核 质子(带正电荷)
原子 中子(不带电荷)
核外电子(带负电荷)
质子数=核外电子数
教师讲解:在不同的原子中,质子数不同、电子数也不同。在同一种原子中质子数等于电子数,每一个质子带一个单位的正电荷,每一个电子带一个单位的负电荷。质子数等于电子数所以原子不显电性。
多媒体动画演示:氯化钠的微观形成过程
重新演示动画:分析氯化钠形成过程 ,分析电子数与质子数的关系,提出阳离子、阴离子概念。
板书:
阳离子: 原子失去电子,带正电荷
质子数(+)>电子数(-)
阴离子: 原子得到电子,带负电荷
质子数(+)<电子数(-)
原子在形成离子过程中质子数变了吗?电子数变了吗?
总结:化学变化中电子起着重要作用。
教师讲解:离子的表示方法。
2、离子符号
钠离子 Na+ 钙离子 Ca2+
氯离子 Cl- 氧离子 O 2-
三、分子、原子、离子间的转化
分子和原子间的转化用动画演示。见课件
同学们仔细观察现象。
回答:紫色液体向阳极移动。
回答:有
回答:离子很小
离子是不断运动的
离子之间有空隙。离子显电性。
学生仔细观察
回答:化学变化
生成氯化钠
学生仔细观察,发现氯化钠溶液能导电,而蔗糖溶液不导电。
回答:氯化钠溶液中有较多的自由移动的离子。
回答:原子由原子核和核外电子构成。原子核由质子中子构成。质子带正电荷,电子带负电荷,中子不带电荷。原子不显电性。
学生仔细观察并与教师互动共同完成阳离子和阴离子的s相关内容。
回答:质子数没变
电子数改变。
学生练习书写:1、带一个单位正电荷的氢离子
2、带三个单位正电荷的铝离子
3、带两个单位正电荷的镁离子
4、带两个单位负电荷的硫离子
学生与老师互动,共同学习分子、原子、离子间的转化
用演示实验的方法让学生感悟离子的真实存在。
引出离子
用微粒的基本性质回答,培养学生迁移能力。
暗示钠原子、氯原子形成钠离子、氯离子是化学变化。
感悟:化学反应中能形成离子。
为解释离子形成做铺垫。
化微观为宏观,
有助于学生理解离子的形成,体会电子在化学变化中的作用
让学生练习使用化学用语。
构建知识体系
教学
反思
本课创新之处在于:通过实验,感受离子的客观存在,化微观为宏观、化抽象为具体,从而确立物质是由微粒构成的观念、确立微粒是运动和变化的观念。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
