河南省郑州市人教版九年级下册第九单元 9.3 溶液的浓度(共19张ppt)
文档属性
| 名称 | 河南省郑州市人教版九年级下册第九单元 9.3 溶液的浓度(共19张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-23 00:00:00 | ||
图片预览





文档简介
(共19张PPT)
溶液的浓度
师争杰
通过前面的学习,我们知道在同一温度、同一溶剂、同一物质的饱和溶液中溶质的质量大于非饱和溶液中溶质的质量,但我们如何比较不饱和溶液中溶质的多少呢?
写在前面的话:
世界上有个叫“死海”的地方,那么它的水与其他江河湖海中的水有什么区别呢?
死海水含盐量极高,且越到湖底越高,是普通海洋含盐份的10倍。最深处有湖水已经化石化(一般海水含盐量为3.5%,而死海的含盐量在23%~25%。表层水中的的盐分每公升达227至275克,深层水中达327克)。由于盐水浓度高,游泳者极易浮起。湖中除细菌外没有其他动植物。涨潮时从约旦河或其他小河中游来的鱼立即死亡。
查阅资料
什么是含盐量?
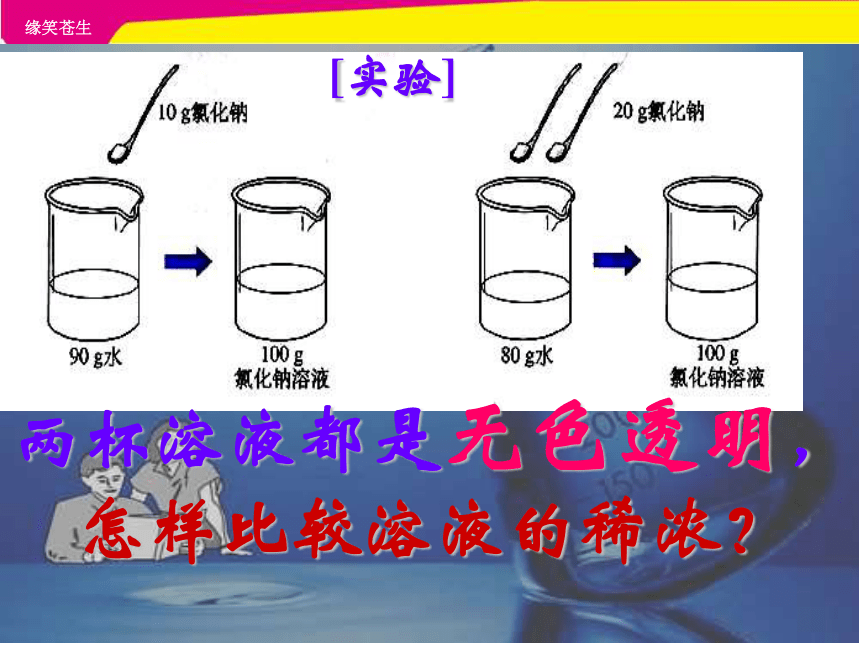
[实验]
两杯溶液都是无色透明,
怎样比较溶液的稀浓?
固体溶解
固体溶解
10%
20%
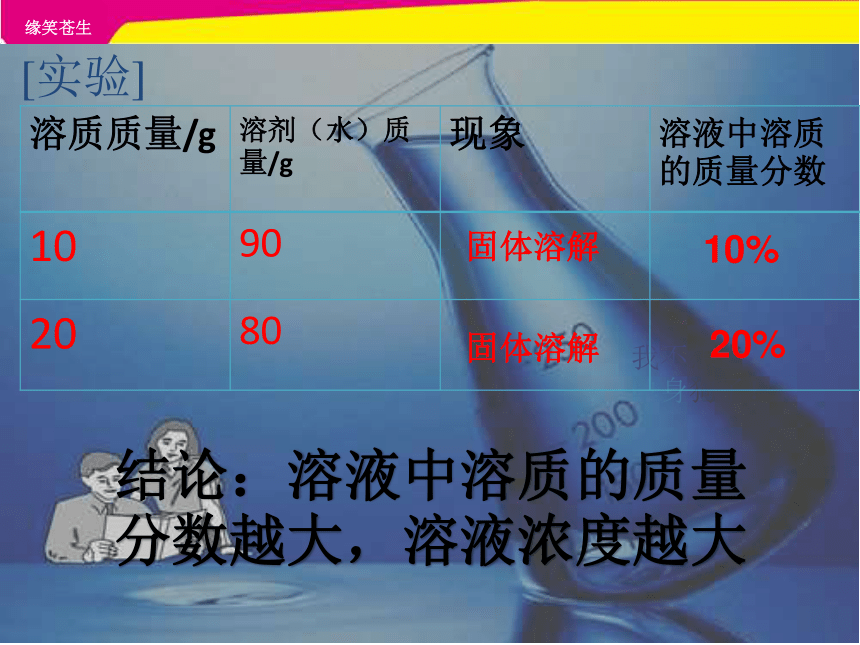
[实验]
溶质质量/g 溶剂(水)质量/g 现象 溶液中溶质的质量分数
10 90
20 80
[讨论]某氯化钠溶液中溶质的质量分数为10%,其含义是什么?
溶质质量:溶剂质量=
1:9
[题型一] :有关溶质、溶剂和溶液之间的换算
二、有关溶质质量分数的计算
?100%
计算的依据 :
溶质的质量分数
定义:溶质的质量与溶液的质量之比。(通常以百分数表示)
【例题1】在农业生产中,常需要用质量分数为16%的氯
化钠溶液来选种。现要配制150kg这种溶液,
需要氯化钠和水的质量各是多少?
【解】
答: 配制150kg质量分数为16%的氯化钠溶液
需24 kg氯化钠和126 kg水。
向20%的某浓溶液中加水后溶液、溶质和溶剂的质量如何变化? 如何解决有关溶液稀释的计算?
? [题型三] :有关溶液稀释或浓缩的计算
计算的依据 :
稀释前溶质质量 = 稀释后溶质质量
浓缩前溶质质量 = 浓缩后溶质质量
例题2:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液需要多少克水?课本44页
解:设稀释后溶液的质量为x
50g ?98% = X ?20%
答:需要水的质量195g
需要水的质量= 245 g– 50g = 195g
练习:配制10%硫酸98g,要98%硫酸(密度为1.84g/m L )多少mL ?
解:设需要98%硫酸的体积为V
V?1.84g/mL ?98% = 98g ?10%
V =
答:要98%硫酸5.4mL
1、20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液的溶质质量分数。
练习2、20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。
剩余溶液的溶质质量分数不变,仍是 10 %
解:
20g X10%
加水:
20g +2g
=9.1%
加盐:
20g X10%+2g
20g +2g
=18.2%
实验室用100g稀硫酸和多少g锌恰好完全反应可制得0.8g氢气。
H2SO4 + Zn = ZnSO4 + H2?
98 65
100g X
答:略
A解:设所需锌的质量为 X
X=66.3g
H2SO4 + Zn = ZnSO4 + H2?
65 2
X 0.8g
B解:设所需锌的质量为 X
X=26g
下面哪种解法正确?
饱和溶液的溶质质量分数=
溶解度
100g+溶解度
溶质的质量分数36% 是指:
溶质T0C时溶解度36g是指:
溶质质量分数与溶解度的比较
100g溶液中含有36g溶质。
在T0C 时,100g水最多溶解该溶质36g。
表示溶液中溶质
质量的多少
表示物质
溶解性的强弱
不一定
一 定
不一定
不一定
100克
单位为1,省略不写
必须饱和
质量单位(克)
溶质质量分数 溶解度
意 义
温 度
溶 剂 量
是否饱和
单 位
知识联系:
化学式中的元素质量分数与本节课中的溶液质量分数有什么相似之处?
质量分数的概念,你还在哪里听说过?
联系生活,辨析体积分数和质量分数:
我们生活中通常会听到白酒的度数,学完本课你能解释“白酒度数”的意义吗?
假如给以1千克的度数为90o的原酒,你能配置成各种度数的白酒吗?
回想起当年的“三鹿奶粉”事件,依旧让人心痛不已,想一想为什么“三聚氰胺”能提高牛奶或者奶粉中的氮含量?
三聚氰胺化学式:C3N3(NH2)3
我们学习知识为了造福的……
溶液的浓度
师争杰
通过前面的学习,我们知道在同一温度、同一溶剂、同一物质的饱和溶液中溶质的质量大于非饱和溶液中溶质的质量,但我们如何比较不饱和溶液中溶质的多少呢?
写在前面的话:
世界上有个叫“死海”的地方,那么它的水与其他江河湖海中的水有什么区别呢?
死海水含盐量极高,且越到湖底越高,是普通海洋含盐份的10倍。最深处有湖水已经化石化(一般海水含盐量为3.5%,而死海的含盐量在23%~25%。表层水中的的盐分每公升达227至275克,深层水中达327克)。由于盐水浓度高,游泳者极易浮起。湖中除细菌外没有其他动植物。涨潮时从约旦河或其他小河中游来的鱼立即死亡。
查阅资料
什么是含盐量?
[实验]
两杯溶液都是无色透明,
怎样比较溶液的稀浓?
固体溶解
固体溶解
10%
20%
[实验]
溶质质量/g 溶剂(水)质量/g 现象 溶液中溶质的质量分数
10 90
20 80
[讨论]某氯化钠溶液中溶质的质量分数为10%,其含义是什么?
溶质质量:溶剂质量=
1:9
[题型一] :有关溶质、溶剂和溶液之间的换算
二、有关溶质质量分数的计算
?100%
计算的依据 :
溶质的质量分数
定义:溶质的质量与溶液的质量之比。(通常以百分数表示)
【例题1】在农业生产中,常需要用质量分数为16%的氯
化钠溶液来选种。现要配制150kg这种溶液,
需要氯化钠和水的质量各是多少?
【解】
答: 配制150kg质量分数为16%的氯化钠溶液
需24 kg氯化钠和126 kg水。
向20%的某浓溶液中加水后溶液、溶质和溶剂的质量如何变化? 如何解决有关溶液稀释的计算?
? [题型三] :有关溶液稀释或浓缩的计算
计算的依据 :
稀释前溶质质量 = 稀释后溶质质量
浓缩前溶质质量 = 浓缩后溶质质量
例题2:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液需要多少克水?课本44页
解:设稀释后溶液的质量为x
50g ?98% = X ?20%
答:需要水的质量195g
需要水的质量= 245 g– 50g = 195g
练习:配制10%硫酸98g,要98%硫酸(密度为1.84g/m L )多少mL ?
解:设需要98%硫酸的体积为V
V?1.84g/mL ?98% = 98g ?10%
V =
答:要98%硫酸5.4mL
1、20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液的溶质质量分数。
练习2、20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。
剩余溶液的溶质质量分数不变,仍是 10 %
解:
20g X10%
加水:
20g +2g
=9.1%
加盐:
20g X10%+2g
20g +2g
=18.2%
实验室用100g稀硫酸和多少g锌恰好完全反应可制得0.8g氢气。
H2SO4 + Zn = ZnSO4 + H2?
98 65
100g X
答:略
A解:设所需锌的质量为 X
X=66.3g
H2SO4 + Zn = ZnSO4 + H2?
65 2
X 0.8g
B解:设所需锌的质量为 X
X=26g
下面哪种解法正确?
饱和溶液的溶质质量分数=
溶解度
100g+溶解度
溶质的质量分数36% 是指:
溶质T0C时溶解度36g是指:
溶质质量分数与溶解度的比较
100g溶液中含有36g溶质。
在T0C 时,100g水最多溶解该溶质36g。
表示溶液中溶质
质量的多少
表示物质
溶解性的强弱
不一定
一 定
不一定
不一定
100克
单位为1,省略不写
必须饱和
质量单位(克)
溶质质量分数 溶解度
意 义
温 度
溶 剂 量
是否饱和
单 位
知识联系:
化学式中的元素质量分数与本节课中的溶液质量分数有什么相似之处?
质量分数的概念,你还在哪里听说过?
联系生活,辨析体积分数和质量分数:
我们生活中通常会听到白酒的度数,学完本课你能解释“白酒度数”的意义吗?
假如给以1千克的度数为90o的原酒,你能配置成各种度数的白酒吗?
回想起当年的“三鹿奶粉”事件,依旧让人心痛不已,想一想为什么“三聚氰胺”能提高牛奶或者奶粉中的氮含量?
三聚氰胺化学式:C3N3(NH2)3
我们学习知识为了造福的……
同课章节目录
