人教版九年级上化学教学讲义,复习补习资料(含知识讲解,巩固练习):15元素
文档属性
| 名称 | 人教版九年级上化学教学讲义,复习补习资料(含知识讲解,巩固练习):15元素 |

|
|
| 格式 | zip | ||
| 文件大小 | 119.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-23 00:00:00 | ||
图片预览



文档简介
元素
【学习目标】
1.掌握元素的概念;知道元素的简单分类;初步认识元素周期表。
2.掌握元素符号的书写方法和所表示的意义;记住常见元素的名称和符号。
【要点梳理】
要点一、元素
1.概念:元素就是具有相同核电荷数(即核内质子数)的一类原子的总称。 例如:氕、氘、氚三种原子质子数都是1,中子数分别是0、1、2,这三种原子是质子数相同的一类原子,统称为氢元素。再如:质子数为6、中子数为6的碳原子和质子数为6、中子数为7的碳原子,由于两种原子质子数相同,所以都是碳元素。
2.元素的种类:共有100余种。按质量计,地壳中含量前四位元素是氧、硅、铝、铁(如下图所示)。 3.元素的分类:可分为金属元素和非金属元素两大类。碳、氢、氧等为非金属元素,铁、铜、铝为金属元素。
【要点诠释】
1.一种元素与另一种元素最本质的区别是:核电荷数(即质子数)不同。
2.元素中文名称的特点:金属元素除汞以外都是“金”旁,非金属元素按其单质在通常情况下的存在状态分别加“石”“气”等偏旁。因此,根据“偏旁”可以判断它们属于哪类元素。
3.元素和原子的比较:
元素
原子
概念
具有相同核电荷数的一类原子的总称
化学变化中的最小粒子
区分
只讲种类,不讲个数,没有数量多少的意义
既讲种类,又讲个数,有数量多少的含义
使用范围
用于描述物质的宏观组成
用于描述物质的微观构成
举例
水中含有氢元素和氧元素(或水是由氢元素和氧元素组成的)
一个水分子,是由两个氢原子和一个氧原子构成的
4.元素是宏观概念,只讲种类,不讲个数。元素与分子、原子、离子等微观概念的区别和联系(如下图所示):
(1)在讨论物质的组成时,一般用“某某物质由什么元素组成”来描述,其中只涉及类别,而没有数量多少的含义。如:水是由氢元素和氧元素组成的(或水是由氢、氧两种元素组成的);铁是由铁元素组成的。 (2)当讨论物质微观结构时,一般用“某某物质的分子是由多少原子构成的”。 如:每个水分子是由2个氢原子和1个氧原子构成的。 (3)由分子构成的物质,描述为“分子由原子构成”。 如:水分子是由氢原子和氧原子构成的。 (4)“水”、“铁”、“元素”、“组成”等都是宏观概念;“分子”、“原子”、“构成”等都是微观概念。在描述时,注意宏观概念对应宏观概念,微观概念对应微观概念。
要点二、元素符号
1.书写方法: (1)由一个字母表示的元素符号要大写; (2)由两个字母表示的元素符号,第一个字母要大写,第二个字母要小写。
例如:Cu表示铜元素,O表示氧元素,Ca表示钙元素。
2.元素符号的意义:
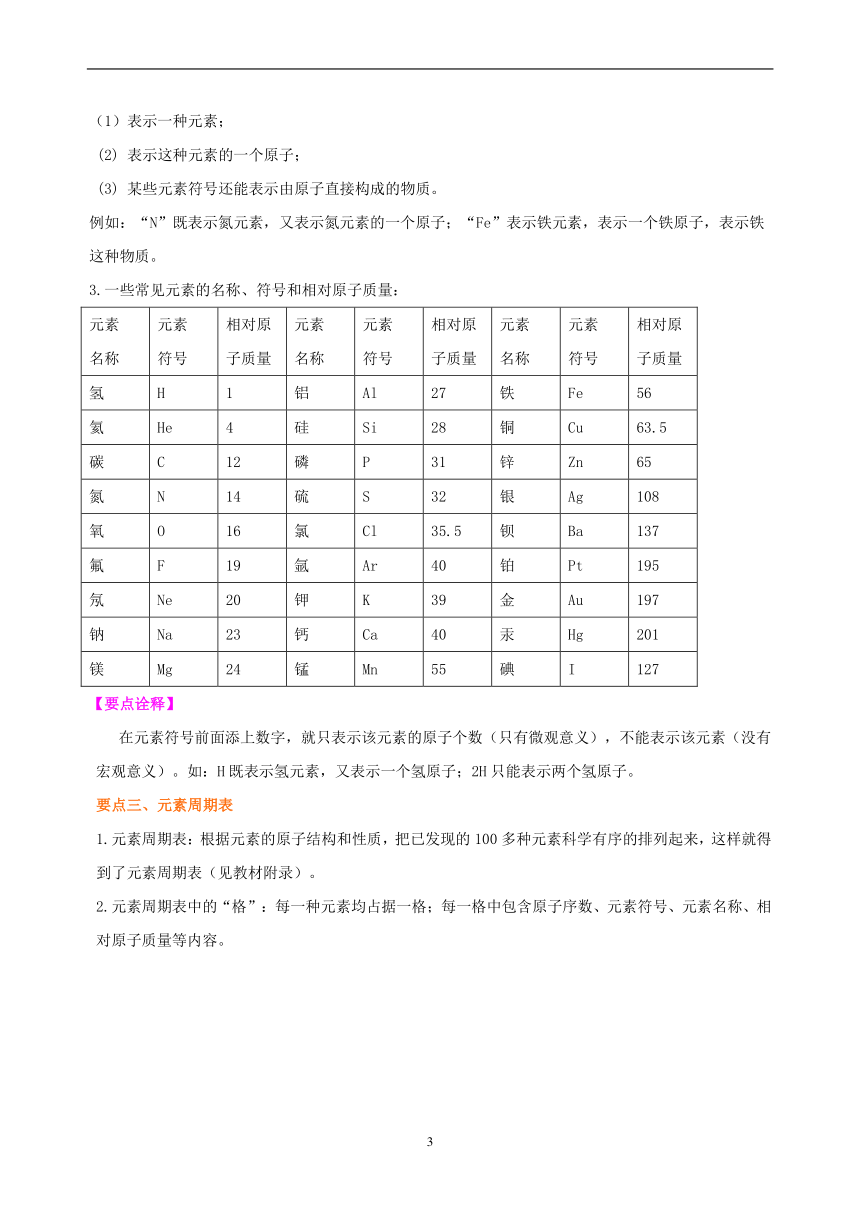
(1)表示一种元素;
(2) 表示这种元素的一个原子;
(3) 某些元素符号还能表示由原子直接构成的物质。 例如:“N”既表示氮元素,又表示氮元素的一个原子;“Fe”表示铁元素,表示一个铁原子,表示铁这种物质。
3.一些常见元素的名称、符号和相对原子质量:
元素
名称
元素
符号
相对原子质量
元素
名称
元素
符号
相对原子质量
元素
名称
元素
符号
相对原子质量
氢
H
1
铝
Al
27
铁
Fe
56
氦
He
4
硅
Si
28
铜
Cu
63.5
碳
C
12
磷
P
31
锌
Zn
65
氮
N
14
硫
S
32
银
Ag
108
氧
O
16
氯
Cl
35.5
钡
Ba
137
氟
F
19
氩
Ar
40
铂
Pt
195
氖
Ne
20
钾
K
39
金
Au
197
钠
Na
23
钙
Ca
40
汞
Hg
201
镁
Mg
24
锰
Mn
55
碘
I
127
【要点诠释】
在元素符号前面添上数字,就只表示该元素的原子个数(只有微观意义),不能表示该元素(没有宏观意义)。如:H既表示氢元素,又表示一个氢原子;2H只能表示两个氢原子。
要点三、元素周期表
1.元素周期表:根据元素的原子结构和性质,把已发现的100多种元素科学有序的排列起来,这样就得到了元素周期表(见教材附录)。
2.元素周期表中的“格”:每一种元素均占据一格;每一格中包含原子序数、元素符号、元素名称、相对原子质量等内容。
3.元素周期表中的“周期”和“族”:元素周期表共有7个周期(共7个横行)、16个族(共18个纵行,其中8、9、10三个纵行共同组成一个族)。
【要点诠释】
1.在周期表上用不同的颜色对金属元素、非金属元素做了分区。每周期(从左到右)开头是金属元素(第一周期除外),靠近尾部的是非金属元素,结尾的是稀有气体元素。
2.随着原子序数的递增,同一周期(从左到右)元素原子的最外层上的电子数由1个递增到8个,达到稀有气体元素原子的稳定结构,然后又重复出现原子最外层电子数从1个递增到8个的变化规律。这种规律性的变化是“元素周期表”名称的来源,它反映了元素之间的内在联系。
【典型例题】
类型一、考查元素概念
1.(2019?青岛中考)豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指( )
A.原子 B.分子 C.元素 D.单质
【思路点拨】豆类、动物肝脏中含有丰富的“铁和锌”不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述。
【答案】C 【解析】豆类、动物肝脏中含有丰富的“铁和锌”,主要是以无机盐的形式存在,不是以单质、分子、原子等形式存在,这里所指的“铁和锌”是强调存在的元素,与具体形态无关。
【总结升华】本题主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键。利用元素的知识可以解决生活中的很多问题,如食品标签上标明了一些元素的含量,在这里一般是指元素。 2.科学家发现了一种质子数与氢原子相同,但中子数比氢原子多一个的新原子,关于此原子的说法中,正确的是( ) A.属于一种新元素 B.跟氢原子相同的原子 C.是氢元素的另一种原子 D.与氢元素不同类的原子 【答案】C
【解析】某原子和氢原子质子数相同,则该原子和氢原子都属于氢元素。也可以说是氢元素的另一种原子。 【总结升华】元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
举一反三:
【变式1】某矿泉水标签上印有的主要矿物质成分及含量如下(单位为mg/L):Ca-20、K-3、Zn-0.06等。这里的Ca、K、Zn是指( ) A.原子 B.分子 C.单质 D.元素
【答案】D
【变式2】 A、B、C三种原子,质子数都是x个,但中子数都不相等,则A、B、C属于( )
A、同一种元素 B、同一种原子
C、不同种元素 D、不同种原子
【答案】A
类型二、考查元素符号的书写和意义
3.下列符号中,既表示一个原子,又表示一种元素,还表示一种物质的是( ) A.H B.O2 C.Hg D.N 【答案】C 【解析】Hg表示汞元素、一个汞原子、汞单质。
【总结升华】所有的元素符号都有两个意义:某元素、一个某原子。金属、稀有气体、部分固态非金属(如C、Si 等)还表示该物质。 举一反三:
【变式】下列符号只具有微观意义的是( ) A.H2O B.H C.2H D.He 【答案】C 【解析】A、D表示物质的化学式,都有宏观意义;B是氢的元素符号,表示一个氢原子和氢元素;化学符号的前边加上数字就只有微观意义,如“2H”表示2个氢原子,不能说成表示2个氢元素。
类型三、考查元素周期表 4.下图甲所示是元素周期表中硫元素的信息,对图中信息理解不正确的是( ) A.原子序数 B.元素名称 C.元素符号 D.中子数 【答案】D
【解析】图甲中32.06是硫元素的相对原子质量,不是中子数。
【总结升华】要记住元素周期表中每一格的意义。
举一反三:
【变式】(2019·兰州中考)铈(Ce)是一种常见的稀土元素,下列
有关说法中不正确的是( )
A.铈的相对原子质量是140.1 g
B.铈属于金属元素
C.铈的原子序数是58
D.铈原子核内有58个质子
【答案】A
元素
【巩固练习】
选择题 (每小题只有一个选项符合题意)
1.(2019·北京中考)决定元素种类的是( )
A.电子数 B.质子数 C.中子数 D.最外层电子数
2.碳元素与氧元素的本质区别是( )
A.质子数不同 B.电子数不同
C.中子数不同 D.最外层电子数不同
3.(2019·泰安中考)元素在自然界里分布不均匀,如智利富藏铜矿、澳大利亚多铁矿、我国山东富含黄金,但从整个地壳中元素的含量来看,最丰富的金属元素是( )
A.O B.Si C.Al D.Fe
4.地壳中含量最多的元素是 ( )
A.硅 B.铁 C.铝 D.氧
5.下列说法错误的是( ) A.元素可采用国际统一的符号来表示 B.元素周期表中原子序数与原子核电荷数在数值上相同 C.地壳中含量最多的金属元素是铁 D.化学变化中元素种类不会改变
6.日本福岛核泄漏事故发生之后,世界卫生组织提示谨慎服用碘片,这里的“碘”指的是( )
A.分子 B.原子 C.元素 D.单质
7.元素周期表是学习和研究化学的重要工具。从元素周期表中不能得到的信息是( )
A.元素符号 B.原子序数 C.相对原子质量 D.元素在自然界中的分布
8.美国铱星公司(已破产)原计划发射77颗卫星,以实现全球卫星通讯,其要发射卫星的数目恰好与铱元素(Ir)的原子核外电子数目相等。下列关于铱元素的各种说法中正确的是( )
A.铱原子的质子数为70
B.铱原子的相对原子量质量为77
C.铱原子的核电荷数为77
D.铱元素为非金属元素
9.据广州日报2011年5月17日的报道,广东紫金县违规排污事件造成的铅(Pb)污染已导致45人血铅超标。符号“Pb”不能表示(????)
A.铅元素 B.金属铅 C.一个铅原子 D.一个铅分子
10.表示4个氢原子的符号是(? )
A.4H2 B.4H C.2H2 D.H
11.下列元素分类错误的是( )
A.金属元素:金、银、铜、铂、钨
B.非金属元素:碳、氢、氮、磷、汞
C.稀有气体元素:氦、氖、氩、氪、氙
D.固体非金属元素:硫、硅、磷、碳
12.下列说法正确的是( )
A.具有相同核电荷数的一类原子总称为元素
B.原子是不能再分的最小粒子
C.分子是保持物质化学性质的唯一粒子
D.分子是构成物质的粒子,而原子不是
二、填空题
13.(2019·河南中考)元素周期表是学习化学的重要工具,图是表中的一格,
其中A表示________;B表示________。
14.下列关于“不一定”的说法中正确的是 。
①由分子构成的纯净物不一定只含一种分子;②质子数相等的粒子不一定是同种元素。
15.下列说法中,正确的是 。
①决定元素周期表中原子序数的是——核电荷数;②决定元素化学性质的是——原子的最外层电子数;③决定元素相对原子质量的是——质子数和中子数;④决定元素和原子种类的是——电子数。
【答案与解析】
1.【答案】B
【解析】元素是质子数(即核电荷数)相同的一类原子的总称,因此决定元素种类的是质子数(即核电荷数)。
2.【答案】A
【解析】元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
3.【答案】C
【解析】地壳中含量最丰富的金属元素是铝,元素符号为A1。
4.【答案】D 【解析】地壳中含量最多的元素是氧。地壳中含量前四位的元素是氧、硅、铝、铁。 5.【答案】C 【解析】元素周期表中原子序数与原子核电荷数在数值上相同;化学变化中元素种类不变;地壳中含量最多的金属元素是铝。 6.【答案】C
【解析】我们平时所说的含“锌”、“铁”、“碘”等指的是宏观意义上的元素,所以选C。
7.【答案】D
【解析】元素在自然界的分布,在元素周期表中是不能查出的,故D错误。
8.【答案】C
【解析】记住两个等量关系:在原子中,核电荷数=质子数=核外电子数;相对原子质量≈质子数+中子数。
9.【答案】D
【解析】Pb可以表示铅这种物质,也可以表示一个铅原子或铅元素;不能表示铅分子,因为铅是由原子构成的。
10.【答案】B
【解析】4H2表示4个氢分子。4H表示4个氢原子。2H2表示2个氢分子。H表示1个氢原子。?
11.【答案】B
【解析】B中汞是金属元素。
12.【答案】A
【解析】原子还能够被分为质子、中子、电子。分子是保持物质化学性质的一种粒子,原子也能够保持物质的化学性质。分子、原子、离子都是构成物质的粒子。
13.【答案】元素符号 相对原子质量
【解析】在元素周期表中,每格右上角的字母表示该元素的元素符号,下方的数字表示该元素的相对原子质量。
14.【答案】②
【解析】由分子构成的纯净物中一定只含一种分子,不然就是混合物,所以①中“不一定”是错的。质子数相等的粒子不一定都是原子,如一个氧分子中有两个氧原子,共有16个质子,一个硫原子也有16个质子,可是氧分子和硫原子不属同种元素,所以②的“不一定”正确。
15.【答案】①②③
【解析】决定元素和原子种类的是——核内质子数。
【学习目标】
1.掌握元素的概念;知道元素的简单分类;初步认识元素周期表。
2.掌握元素符号的书写方法和所表示的意义;记住常见元素的名称和符号。
【要点梳理】
要点一、元素
1.概念:元素就是具有相同核电荷数(即核内质子数)的一类原子的总称。 例如:氕、氘、氚三种原子质子数都是1,中子数分别是0、1、2,这三种原子是质子数相同的一类原子,统称为氢元素。再如:质子数为6、中子数为6的碳原子和质子数为6、中子数为7的碳原子,由于两种原子质子数相同,所以都是碳元素。
2.元素的种类:共有100余种。按质量计,地壳中含量前四位元素是氧、硅、铝、铁(如下图所示)。 3.元素的分类:可分为金属元素和非金属元素两大类。碳、氢、氧等为非金属元素,铁、铜、铝为金属元素。
【要点诠释】
1.一种元素与另一种元素最本质的区别是:核电荷数(即质子数)不同。
2.元素中文名称的特点:金属元素除汞以外都是“金”旁,非金属元素按其单质在通常情况下的存在状态分别加“石”“气”等偏旁。因此,根据“偏旁”可以判断它们属于哪类元素。
3.元素和原子的比较:
元素
原子
概念
具有相同核电荷数的一类原子的总称
化学变化中的最小粒子
区分
只讲种类,不讲个数,没有数量多少的意义
既讲种类,又讲个数,有数量多少的含义
使用范围
用于描述物质的宏观组成
用于描述物质的微观构成
举例
水中含有氢元素和氧元素(或水是由氢元素和氧元素组成的)
一个水分子,是由两个氢原子和一个氧原子构成的
4.元素是宏观概念,只讲种类,不讲个数。元素与分子、原子、离子等微观概念的区别和联系(如下图所示):
(1)在讨论物质的组成时,一般用“某某物质由什么元素组成”来描述,其中只涉及类别,而没有数量多少的含义。如:水是由氢元素和氧元素组成的(或水是由氢、氧两种元素组成的);铁是由铁元素组成的。 (2)当讨论物质微观结构时,一般用“某某物质的分子是由多少原子构成的”。 如:每个水分子是由2个氢原子和1个氧原子构成的。 (3)由分子构成的物质,描述为“分子由原子构成”。 如:水分子是由氢原子和氧原子构成的。 (4)“水”、“铁”、“元素”、“组成”等都是宏观概念;“分子”、“原子”、“构成”等都是微观概念。在描述时,注意宏观概念对应宏观概念,微观概念对应微观概念。
要点二、元素符号
1.书写方法: (1)由一个字母表示的元素符号要大写; (2)由两个字母表示的元素符号,第一个字母要大写,第二个字母要小写。
例如:Cu表示铜元素,O表示氧元素,Ca表示钙元素。
2.元素符号的意义:
(1)表示一种元素;
(2) 表示这种元素的一个原子;
(3) 某些元素符号还能表示由原子直接构成的物质。 例如:“N”既表示氮元素,又表示氮元素的一个原子;“Fe”表示铁元素,表示一个铁原子,表示铁这种物质。
3.一些常见元素的名称、符号和相对原子质量:
元素
名称
元素
符号
相对原子质量
元素
名称
元素
符号
相对原子质量
元素
名称
元素
符号
相对原子质量
氢
H
1
铝
Al
27
铁
Fe
56
氦
He
4
硅
Si
28
铜
Cu
63.5
碳
C
12
磷
P
31
锌
Zn
65
氮
N
14
硫
S
32
银
Ag
108
氧
O
16
氯
Cl
35.5
钡
Ba
137
氟
F
19
氩
Ar
40
铂
Pt
195
氖
Ne
20
钾
K
39
金
Au
197
钠
Na
23
钙
Ca
40
汞
Hg
201
镁
Mg
24
锰
Mn
55
碘
I
127
【要点诠释】
在元素符号前面添上数字,就只表示该元素的原子个数(只有微观意义),不能表示该元素(没有宏观意义)。如:H既表示氢元素,又表示一个氢原子;2H只能表示两个氢原子。
要点三、元素周期表
1.元素周期表:根据元素的原子结构和性质,把已发现的100多种元素科学有序的排列起来,这样就得到了元素周期表(见教材附录)。
2.元素周期表中的“格”:每一种元素均占据一格;每一格中包含原子序数、元素符号、元素名称、相对原子质量等内容。
3.元素周期表中的“周期”和“族”:元素周期表共有7个周期(共7个横行)、16个族(共18个纵行,其中8、9、10三个纵行共同组成一个族)。
【要点诠释】
1.在周期表上用不同的颜色对金属元素、非金属元素做了分区。每周期(从左到右)开头是金属元素(第一周期除外),靠近尾部的是非金属元素,结尾的是稀有气体元素。
2.随着原子序数的递增,同一周期(从左到右)元素原子的最外层上的电子数由1个递增到8个,达到稀有气体元素原子的稳定结构,然后又重复出现原子最外层电子数从1个递增到8个的变化规律。这种规律性的变化是“元素周期表”名称的来源,它反映了元素之间的内在联系。
【典型例题】
类型一、考查元素概念
1.(2019?青岛中考)豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指( )
A.原子 B.分子 C.元素 D.单质
【思路点拨】豆类、动物肝脏中含有丰富的“铁和锌”不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述。
【答案】C 【解析】豆类、动物肝脏中含有丰富的“铁和锌”,主要是以无机盐的形式存在,不是以单质、分子、原子等形式存在,这里所指的“铁和锌”是强调存在的元素,与具体形态无关。
【总结升华】本题主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键。利用元素的知识可以解决生活中的很多问题,如食品标签上标明了一些元素的含量,在这里一般是指元素。 2.科学家发现了一种质子数与氢原子相同,但中子数比氢原子多一个的新原子,关于此原子的说法中,正确的是( ) A.属于一种新元素 B.跟氢原子相同的原子 C.是氢元素的另一种原子 D.与氢元素不同类的原子 【答案】C
【解析】某原子和氢原子质子数相同,则该原子和氢原子都属于氢元素。也可以说是氢元素的另一种原子。 【总结升华】元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
举一反三:
【变式1】某矿泉水标签上印有的主要矿物质成分及含量如下(单位为mg/L):Ca-20、K-3、Zn-0.06等。这里的Ca、K、Zn是指( ) A.原子 B.分子 C.单质 D.元素
【答案】D
【变式2】 A、B、C三种原子,质子数都是x个,但中子数都不相等,则A、B、C属于( )
A、同一种元素 B、同一种原子
C、不同种元素 D、不同种原子
【答案】A
类型二、考查元素符号的书写和意义
3.下列符号中,既表示一个原子,又表示一种元素,还表示一种物质的是( ) A.H B.O2 C.Hg D.N 【答案】C 【解析】Hg表示汞元素、一个汞原子、汞单质。
【总结升华】所有的元素符号都有两个意义:某元素、一个某原子。金属、稀有气体、部分固态非金属(如C、Si 等)还表示该物质。 举一反三:
【变式】下列符号只具有微观意义的是( ) A.H2O B.H C.2H D.He 【答案】C 【解析】A、D表示物质的化学式,都有宏观意义;B是氢的元素符号,表示一个氢原子和氢元素;化学符号的前边加上数字就只有微观意义,如“2H”表示2个氢原子,不能说成表示2个氢元素。
类型三、考查元素周期表 4.下图甲所示是元素周期表中硫元素的信息,对图中信息理解不正确的是( ) A.原子序数 B.元素名称 C.元素符号 D.中子数 【答案】D
【解析】图甲中32.06是硫元素的相对原子质量,不是中子数。
【总结升华】要记住元素周期表中每一格的意义。
举一反三:
【变式】(2019·兰州中考)铈(Ce)是一种常见的稀土元素,下列
有关说法中不正确的是( )
A.铈的相对原子质量是140.1 g
B.铈属于金属元素
C.铈的原子序数是58
D.铈原子核内有58个质子
【答案】A
元素
【巩固练习】
选择题 (每小题只有一个选项符合题意)
1.(2019·北京中考)决定元素种类的是( )
A.电子数 B.质子数 C.中子数 D.最外层电子数
2.碳元素与氧元素的本质区别是( )
A.质子数不同 B.电子数不同
C.中子数不同 D.最外层电子数不同
3.(2019·泰安中考)元素在自然界里分布不均匀,如智利富藏铜矿、澳大利亚多铁矿、我国山东富含黄金,但从整个地壳中元素的含量来看,最丰富的金属元素是( )
A.O B.Si C.Al D.Fe
4.地壳中含量最多的元素是 ( )
A.硅 B.铁 C.铝 D.氧
5.下列说法错误的是( ) A.元素可采用国际统一的符号来表示 B.元素周期表中原子序数与原子核电荷数在数值上相同 C.地壳中含量最多的金属元素是铁 D.化学变化中元素种类不会改变
6.日本福岛核泄漏事故发生之后,世界卫生组织提示谨慎服用碘片,这里的“碘”指的是( )
A.分子 B.原子 C.元素 D.单质
7.元素周期表是学习和研究化学的重要工具。从元素周期表中不能得到的信息是( )
A.元素符号 B.原子序数 C.相对原子质量 D.元素在自然界中的分布
8.美国铱星公司(已破产)原计划发射77颗卫星,以实现全球卫星通讯,其要发射卫星的数目恰好与铱元素(Ir)的原子核外电子数目相等。下列关于铱元素的各种说法中正确的是( )
A.铱原子的质子数为70
B.铱原子的相对原子量质量为77
C.铱原子的核电荷数为77
D.铱元素为非金属元素
9.据广州日报2011年5月17日的报道,广东紫金县违规排污事件造成的铅(Pb)污染已导致45人血铅超标。符号“Pb”不能表示(????)
A.铅元素 B.金属铅 C.一个铅原子 D.一个铅分子
10.表示4个氢原子的符号是(? )
A.4H2 B.4H C.2H2 D.H
11.下列元素分类错误的是( )
A.金属元素:金、银、铜、铂、钨
B.非金属元素:碳、氢、氮、磷、汞
C.稀有气体元素:氦、氖、氩、氪、氙
D.固体非金属元素:硫、硅、磷、碳
12.下列说法正确的是( )
A.具有相同核电荷数的一类原子总称为元素
B.原子是不能再分的最小粒子
C.分子是保持物质化学性质的唯一粒子
D.分子是构成物质的粒子,而原子不是
二、填空题
13.(2019·河南中考)元素周期表是学习化学的重要工具,图是表中的一格,
其中A表示________;B表示________。
14.下列关于“不一定”的说法中正确的是 。
①由分子构成的纯净物不一定只含一种分子;②质子数相等的粒子不一定是同种元素。
15.下列说法中,正确的是 。
①决定元素周期表中原子序数的是——核电荷数;②决定元素化学性质的是——原子的最外层电子数;③决定元素相对原子质量的是——质子数和中子数;④决定元素和原子种类的是——电子数。
【答案与解析】
1.【答案】B
【解析】元素是质子数(即核电荷数)相同的一类原子的总称,因此决定元素种类的是质子数(即核电荷数)。
2.【答案】A
【解析】元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
3.【答案】C
【解析】地壳中含量最丰富的金属元素是铝,元素符号为A1。
4.【答案】D 【解析】地壳中含量最多的元素是氧。地壳中含量前四位的元素是氧、硅、铝、铁。 5.【答案】C 【解析】元素周期表中原子序数与原子核电荷数在数值上相同;化学变化中元素种类不变;地壳中含量最多的金属元素是铝。 6.【答案】C
【解析】我们平时所说的含“锌”、“铁”、“碘”等指的是宏观意义上的元素,所以选C。
7.【答案】D
【解析】元素在自然界的分布,在元素周期表中是不能查出的,故D错误。
8.【答案】C
【解析】记住两个等量关系:在原子中,核电荷数=质子数=核外电子数;相对原子质量≈质子数+中子数。
9.【答案】D
【解析】Pb可以表示铅这种物质,也可以表示一个铅原子或铅元素;不能表示铅分子,因为铅是由原子构成的。
10.【答案】B
【解析】4H2表示4个氢分子。4H表示4个氢原子。2H2表示2个氢分子。H表示1个氢原子。?
11.【答案】B
【解析】B中汞是金属元素。
12.【答案】A
【解析】原子还能够被分为质子、中子、电子。分子是保持物质化学性质的一种粒子,原子也能够保持物质的化学性质。分子、原子、离子都是构成物质的粒子。
13.【答案】元素符号 相对原子质量
【解析】在元素周期表中,每格右上角的字母表示该元素的元素符号,下方的数字表示该元素的相对原子质量。
14.【答案】②
【解析】由分子构成的纯净物中一定只含一种分子,不然就是混合物,所以①中“不一定”是错的。质子数相等的粒子不一定都是原子,如一个氧分子中有两个氧原子,共有16个质子,一个硫原子也有16个质子,可是氧分子和硫原子不属同种元素,所以②的“不一定”正确。
15.【答案】①②③
【解析】决定元素和原子种类的是——核内质子数。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
