科粤版化学九年级上册 4.2 水的组成 课件 (共21张PPT)
文档属性
| 名称 | 科粤版化学九年级上册 4.2 水的组成 课件 (共21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 828.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-27 00:00:00 | ||
图片预览








文档简介
(共21张PPT)
4.2 水的组成
复习 ● 导学
了解水的物理性质。
通过电解水实验,认识水的元素组成。
学习目标:
一、水的物理性质
纯水通常为 、 透明液体,一个标准大气压下,凝固点为 ,沸点为 , 时密度最大为 ;此时水分子间间隔最 。
无色
无味
0℃
100℃
4℃
1g/cm3
小
学习 ● 研讨
提出问题
水是由哪些元素组成的呢?
18世纪末以前
水被看作是由一种元素组成的
卡文迪发现发现水不是由一种元素组成的,是由氧元素和氢元素组成的
二、探究水的组成
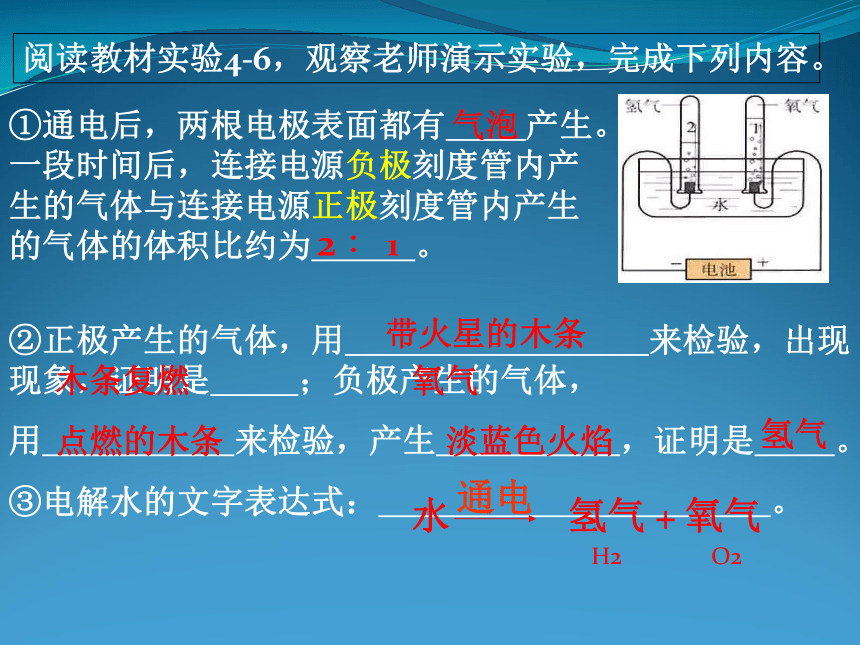
②正极产生的气体,用 来检验,出现 现象,证明是 ;负极产生的气体,
用 来检验,产生 ,证明是 。
阅读教材实验4-6,观察老师演示实验,完成下列内容。
①通电后,两根电极表面都有 产生。一段时间后,连接电源负极刻度管内产生的气体与连接电源正极刻度管内产生的气体的体积比约为 。
气泡
2 ∶ 1
③电解水的文字表达式: 。
点燃的木条
氢气
木条复燃
氧气
带火星的木条
淡蓝色火焰
结论2:水是由氢元素和氧元素组成的。
如何确定水分子中氢原子和氧原子的个数比呢?
思路:
已知:① V(H2):V(O2)=2:1
定律:同温同压下,不同气体的分子个数之比等于气体体积之比。
即:②N(H2):N(O2)=V(H2):V(O2)=2:1
又因为H2和O2都是双原子分子
所以:① N(H):N(O)= 2N(H2):2N(O2)=2:1
结论3:水的化学式为H2O。
思考:
在上述反应中,参加反应的分子、原子发生了怎样的变化?
结论4:在化学反应中分子可分,原子不可分,只是重新组合。
实验结论
①
②水由 组成的。
依据为反应前后元素的种类不变。
氢元素、氧元素
③水的化学式为H2O。
④在化学反应中分子可分,原子不可分,只是重新组合 。
宏观
微观
课堂练习
1.小红做电解水实验,在水中加入少量稀硫酸或氢氧化钠溶液,这是为了 ,若在连接电源的 极的玻璃管内得到10mL的氧气,同时可在连接电源的 极的玻璃管内得到 mL的 气;其文字表达式为 ,该反应属于 反应(填反应类型)。
2.保持水的化学性质的微粒是 ;保持氢气化学性质的微粒是 ;电解水没有发生变化的微粒是 ;电解水发生变化的微粒是 ;电解水生成的新微粒是 。
增强水的导电性
负
正
水分子
20
氢
分解
氢分子
分子
氢分子和氧分子
氢原子和氧原子
3.电解水实验说明了以下几个事实,其中错误的是( )。
A.水是一种氧化物
B.水在直流电的作用下能分解成氢气和氧气
C.水是由氢气和氧气组成的
D.在化学反应中,分子可分而原子不可分
4.某同学做电解水的实验时,发现负极与正极收集到的气体体积比大于2︰1,这与理论值不相符。接下来的做法不可取的是( )。
A.继续实验,查找原因
B.认为实验值与理论值相差不大,实验成功了
C.检查装置的气密性
D.推测原因之一可能是因为氧气与氢气在水中的溶解能力不同
5.通过本节课的学习,我们知道利用电解水可以证明水是由氢、氧元素组成的,你还有别的办法来证明水的组成吗?请简述实验的原理。
课堂小结
水是由 两种元素组成的 物;正极收集到 ;负极收集到 ,氢气和氧气的体积比为 ,质量比为 ,由实验得出水由氢氧元素组成的理论依据是 ,由此可指导我们在日后的学习中,可通过鉴定反应
的 来推断反应物的元素组成。
氢、氧
纯净
氧气
氢气
2:1
1:8
反应前后元素的种类不变
生成物
O
H
H
水分子
O
H
H
O
H
H
H
H
O
O
H
H
O
H
H
O
H
H
H
H
O
O
H
H
O
H
H
O
H
H
H
H
O
O
H
H
O
H
H
O
H
H
H
H
O
O
H
H
O
H
H
O
H
H
H
H
O
水是由 两种元素组成的 物;正极收集到 ;负极收集到 ,氢气和氧气的体积比为 ,质量比为 ,由实验得出水由氢氧元素组成的理论依据是 ,
由此可指导我们在日后的学习中,可通过鉴定反应的 来推断反应物的元素组成。
课堂小结
氢氧
氧化
氧气
氢气
2:1
1:8
反应前后元素种类不变
生成物
课堂练习
已知酒精在氧气中燃烧会生成二氧化碳(CO2)和水(H2O),则酒精中一定含有的元素素 ,可能含有的元素 。
碳元素、氢元素
氧元素
4.2 水的组成
复习 ● 导学
了解水的物理性质。
通过电解水实验,认识水的元素组成。
学习目标:
一、水的物理性质
纯水通常为 、 透明液体,一个标准大气压下,凝固点为 ,沸点为 , 时密度最大为 ;此时水分子间间隔最 。
无色
无味
0℃
100℃
4℃
1g/cm3
小
学习 ● 研讨
提出问题
水是由哪些元素组成的呢?
18世纪末以前
水被看作是由一种元素组成的
卡文迪发现发现水不是由一种元素组成的,是由氧元素和氢元素组成的
二、探究水的组成
②正极产生的气体,用 来检验,出现 现象,证明是 ;负极产生的气体,
用 来检验,产生 ,证明是 。
阅读教材实验4-6,观察老师演示实验,完成下列内容。
①通电后,两根电极表面都有 产生。一段时间后,连接电源负极刻度管内产生的气体与连接电源正极刻度管内产生的气体的体积比约为 。
气泡
2 ∶ 1
③电解水的文字表达式: 。
点燃的木条
氢气
木条复燃
氧气
带火星的木条
淡蓝色火焰
结论2:水是由氢元素和氧元素组成的。
如何确定水分子中氢原子和氧原子的个数比呢?
思路:
已知:① V(H2):V(O2)=2:1
定律:同温同压下,不同气体的分子个数之比等于气体体积之比。
即:②N(H2):N(O2)=V(H2):V(O2)=2:1
又因为H2和O2都是双原子分子
所以:① N(H):N(O)= 2N(H2):2N(O2)=2:1
结论3:水的化学式为H2O。
思考:
在上述反应中,参加反应的分子、原子发生了怎样的变化?
结论4:在化学反应中分子可分,原子不可分,只是重新组合。
实验结论
①
②水由 组成的。
依据为反应前后元素的种类不变。
氢元素、氧元素
③水的化学式为H2O。
④在化学反应中分子可分,原子不可分,只是重新组合 。
宏观
微观
课堂练习
1.小红做电解水实验,在水中加入少量稀硫酸或氢氧化钠溶液,这是为了 ,若在连接电源的 极的玻璃管内得到10mL的氧气,同时可在连接电源的 极的玻璃管内得到 mL的 气;其文字表达式为 ,该反应属于 反应(填反应类型)。
2.保持水的化学性质的微粒是 ;保持氢气化学性质的微粒是 ;电解水没有发生变化的微粒是 ;电解水发生变化的微粒是 ;电解水生成的新微粒是 。
增强水的导电性
负
正
水分子
20
氢
分解
氢分子
分子
氢分子和氧分子
氢原子和氧原子
3.电解水实验说明了以下几个事实,其中错误的是( )。
A.水是一种氧化物
B.水在直流电的作用下能分解成氢气和氧气
C.水是由氢气和氧气组成的
D.在化学反应中,分子可分而原子不可分
4.某同学做电解水的实验时,发现负极与正极收集到的气体体积比大于2︰1,这与理论值不相符。接下来的做法不可取的是( )。
A.继续实验,查找原因
B.认为实验值与理论值相差不大,实验成功了
C.检查装置的气密性
D.推测原因之一可能是因为氧气与氢气在水中的溶解能力不同
5.通过本节课的学习,我们知道利用电解水可以证明水是由氢、氧元素组成的,你还有别的办法来证明水的组成吗?请简述实验的原理。
课堂小结
水是由 两种元素组成的 物;正极收集到 ;负极收集到 ,氢气和氧气的体积比为 ,质量比为 ,由实验得出水由氢氧元素组成的理论依据是 ,由此可指导我们在日后的学习中,可通过鉴定反应
的 来推断反应物的元素组成。
氢、氧
纯净
氧气
氢气
2:1
1:8
反应前后元素的种类不变
生成物
O
H
H
水分子
O
H
H
O
H
H
H
H
O
O
H
H
O
H
H
O
H
H
H
H
O
O
H
H
O
H
H
O
H
H
H
H
O
O
H
H
O
H
H
O
H
H
H
H
O
O
H
H
O
H
H
O
H
H
H
H
O
水是由 两种元素组成的 物;正极收集到 ;负极收集到 ,氢气和氧气的体积比为 ,质量比为 ,由实验得出水由氢氧元素组成的理论依据是 ,
由此可指导我们在日后的学习中,可通过鉴定反应的 来推断反应物的元素组成。
课堂小结
氢氧
氧化
氧气
氢气
2:1
1:8
反应前后元素种类不变
生成物
课堂练习
已知酒精在氧气中燃烧会生成二氧化碳(CO2)和水(H2O),则酒精中一定含有的元素素 ,可能含有的元素 。
碳元素、氢元素
氧元素
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
