人教版化学选修四第四节金属的电化学腐蚀与防护课件(共22张PPT)
文档属性
| 名称 | 人教版化学选修四第四节金属的电化学腐蚀与防护课件(共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-29 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
第四节
金属的电化学腐蚀与防护
美国“尼米
兹”级核动
力航母造
价超过45
亿美元;
如果防腐
不到位,几年就会被腐蚀为变成一堆废铁。因此,美国海军每年用于航母维护费约为42亿美元。
一.金属腐蚀
金属与周围的气体或液体物质发生氧化还原反应而引起损耗的现象称为金属腐蚀。
定义:
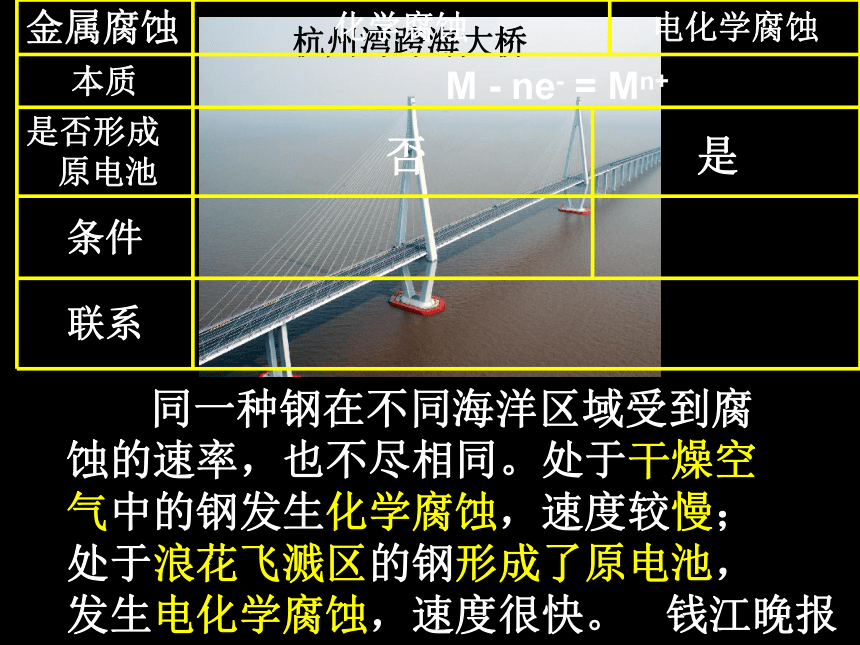
同一种钢在不同海洋区域受到腐蚀的速率,也不尽相同。处于干燥空气中的钢发生化学腐蚀,速度较慢;处于浪花飞溅区的钢形成了原电池,发生电化学腐蚀,速度很快。
钱江晚报
M - ne- = Mn+
是
否
金属腐蚀 化学腐蚀 电化学腐蚀
本质
是否形成原电池
条件
联系
1980年3月,在北海大埃科菲斯克油田作业的亚历山大·基定
德号钻井平台,在海浪的反复冲击下,5根巨大桩腿中的D号桩腿因6根撑管先后断裂,万余吨重的平台在25分钟内倾倒,123人遇难,造成近海石油钻探史上罕见的灾难。调查表明,此次事故是腐蚀疲劳所致。美国东部的一座铁桥,由于应力腐蚀开裂而塌落在俄亥俄河中,46人丧生……
这些屹立在蔚蓝大海中、甚至成为海上一景的庞然大物通常都拥有着一个共同的特点——由钢铁或钢筋混凝土打造的“钢躯铁干”。然而在海洋温和的表面下,却是一个十分苛刻的自然腐蚀环境,一道道美丽飞溅的浪花竟成为了“吃金属的老虎”。据了解,海洋工程结构设计寿命一般为几十年甚至上百年,但暴露于海洋环境中的工程结构极易受到腐蚀破坏,这些重大工程设施如果不能得到很好的腐蚀防护,将导致巨大的腐蚀破坏和经济损失。
海洋腐蚀就是金属等构件在海洋环境中发生的腐蚀,它造成的危害十分严重。“据有关统计,腐蚀损失占GDP的3%~5%,全世界每年因腐蚀而造成的直接经济损失约为7000亿美元。按最低比例3%计算,我国在2009年的GDP为33.5万亿元,腐蚀造成的直接经济损失达到1万亿元。”
海洋腐蚀造成巨大损失 一年"烂掉"万亿元
海水一年“腐蚀”掉1.2万亿
2010年,我国仅被海水腐蚀掉的钢,价值1.2万亿元,相当于每个中国人掏出1000元。
钱江晚报
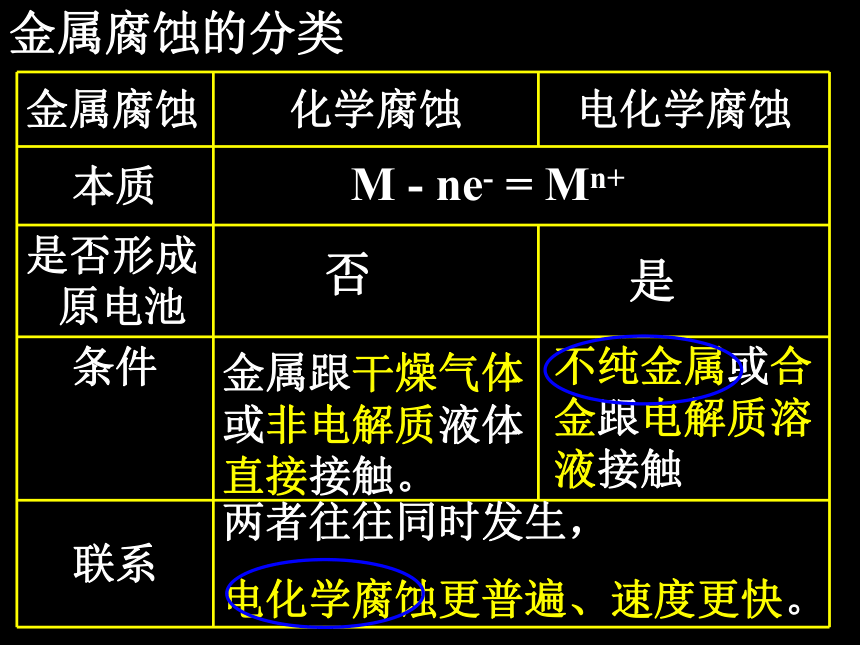
金属跟干燥气体或非电解质液体直接接触。
不纯金属或合金跟电解质溶液接触
是
否
两者往往同时发生,
电化学腐蚀更普遍、速度更快。
金属腐蚀的分类
M - ne- = Mn+
金属腐蚀 化学腐蚀 电化学腐蚀
本质
是否形成原电池
条件
联系
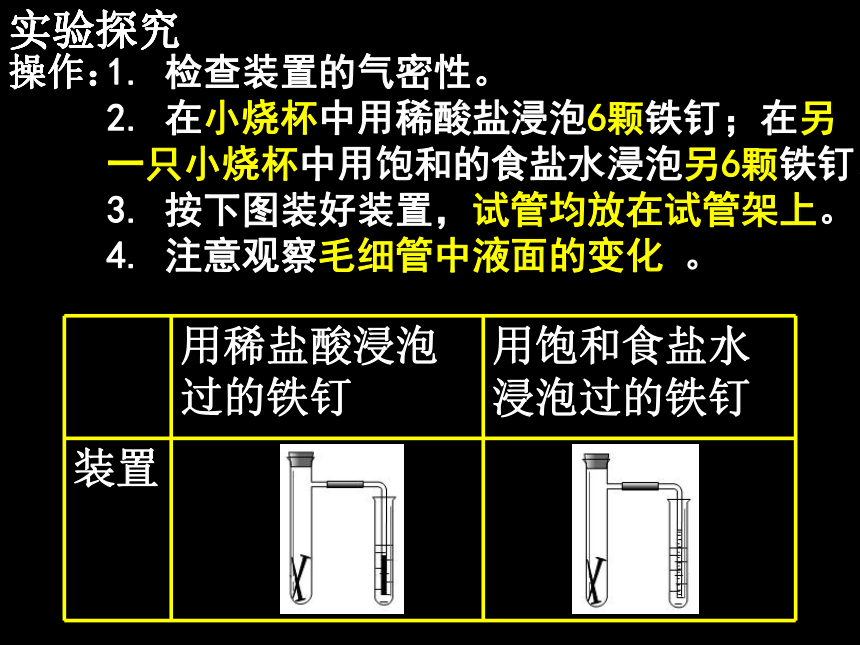
1. 检查装置的气密性。
2. 在小烧杯中用稀酸盐浸泡6颗铁钉;在另一只小烧杯中用饱和的食盐水浸泡另6颗铁钉。
3. 按下图装好装置,试管均放在试管架上。
4. 注意观察毛细管中液面的变化 。
操作:
实验探究
实验探究
实验探究
操作:
实验探究
操作:
用稀盐酸浸泡过的铁钉 用饱和食盐水浸泡过的铁钉
装置
毛细管中液面上升
毛细管中液面下降
吸氧腐蚀
析氢腐蚀
水膜呈中性或酸性很弱
水膜酸性较强
吸氧腐蚀
析氢腐蚀
反应中生成了气体
反应中消耗了气体
用稀盐酸浸泡过的铁钉 用饱和食盐水浸泡过的铁钉
实验现象
结论
负极反应
正极反应
总反应
类别
条 件
普遍性 比 更普遍
1. 大桥上处于浪花飞溅区的钢发生电化学腐蚀,且由于干湿交替,氧供应充分,盐分不断浓缩,腐蚀最严重。请写出该腐蚀过程中的正、负极反应。
2. 某段时间,空气污染严重,酸雨腐蚀了钢,该腐蚀属于 腐蚀。
学以致用
二、金属的防护
2.改善金属的内部组成结构。
思路:抑制金属失去电子。
传统方法
1.在金属表面覆盖保护层。
桥梁用传统方法来防腐,防护寿命一般仅在10年左右。
金属的电化学防护
思考:请应用你所学电化学知识设计方案保护钢铁,画出示意图,并标出电子流动的方向。
牺牲阳极的阴极保护法
外加电流的阴极保护法
正极,被保护
电解池原理
原电池原理
阴极
阳极(惰性电极)
负极,被腐蚀
原理
被保护金属作哪极
另一电极
金属电化学防护
开拓视野
常用外加电流的阴极保护法防护航母,应用 原理,钢作 极,用惰性电极作 极。
电解池
阴
阳
燃气工程中钢管的防腐方法
对于城市燃气系统,由于地下管网密集,阴极保护的外加电源对其它管道干扰大,会造成自身受益、他家受害的局面。采用比钢活泼的金属材料与钢管相连则不会出现此类情况,该方法的名称叫 。
应用 原理,钢作 极,比钢活泼的金属作 极。
牺牲阳极的阴极保护法
开拓视野
原电池
正
负
桥梁的防护
电弧喷铝 +复合漆
三重保护,耐腐蚀寿命30年以上。
开拓视野
下列各情况,其中Fe片腐蚀由快到慢的顺序: 。
电解池的阳极>原电池的负极>化学腐蚀
>原电池的正极>电解池的阴极
(5)>(2)>(1)>(3)>(4)
学以致用
(1)
(2)
下列情况下,铁被腐蚀还是被保护?写出电极反应。
学以致用
(09年广东高考)出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。下列说法正确的是(双选)
A. 锡青铜的熔点比纯铜高。
B.在自然环境中,锡青铜中的锡对铜起保护作用。
C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快。
D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程。
学以致用
B C
课堂小结
一、金属腐蚀
1.本质:金属单质失去电子变成阳离子。
金属腐蚀
2.分类
(形成原电池)
二、金属电化学的防护
思路:抑制金属单质失去电子。
1.牺牲阳极的阴极保护法。(原电池原理)
2.外加电流的阴极保护法。(电解池原理)
第四节
金属的电化学腐蚀与防护
美国“尼米
兹”级核动
力航母造
价超过45
亿美元;
如果防腐
不到位,几年就会被腐蚀为变成一堆废铁。因此,美国海军每年用于航母维护费约为42亿美元。
一.金属腐蚀
金属与周围的气体或液体物质发生氧化还原反应而引起损耗的现象称为金属腐蚀。
定义:
同一种钢在不同海洋区域受到腐蚀的速率,也不尽相同。处于干燥空气中的钢发生化学腐蚀,速度较慢;处于浪花飞溅区的钢形成了原电池,发生电化学腐蚀,速度很快。
钱江晚报
M - ne- = Mn+
是
否
金属腐蚀 化学腐蚀 电化学腐蚀
本质
是否形成原电池
条件
联系
1980年3月,在北海大埃科菲斯克油田作业的亚历山大·基定
德号钻井平台,在海浪的反复冲击下,5根巨大桩腿中的D号桩腿因6根撑管先后断裂,万余吨重的平台在25分钟内倾倒,123人遇难,造成近海石油钻探史上罕见的灾难。调查表明,此次事故是腐蚀疲劳所致。美国东部的一座铁桥,由于应力腐蚀开裂而塌落在俄亥俄河中,46人丧生……
这些屹立在蔚蓝大海中、甚至成为海上一景的庞然大物通常都拥有着一个共同的特点——由钢铁或钢筋混凝土打造的“钢躯铁干”。然而在海洋温和的表面下,却是一个十分苛刻的自然腐蚀环境,一道道美丽飞溅的浪花竟成为了“吃金属的老虎”。据了解,海洋工程结构设计寿命一般为几十年甚至上百年,但暴露于海洋环境中的工程结构极易受到腐蚀破坏,这些重大工程设施如果不能得到很好的腐蚀防护,将导致巨大的腐蚀破坏和经济损失。
海洋腐蚀就是金属等构件在海洋环境中发生的腐蚀,它造成的危害十分严重。“据有关统计,腐蚀损失占GDP的3%~5%,全世界每年因腐蚀而造成的直接经济损失约为7000亿美元。按最低比例3%计算,我国在2009年的GDP为33.5万亿元,腐蚀造成的直接经济损失达到1万亿元。”
海洋腐蚀造成巨大损失 一年"烂掉"万亿元
海水一年“腐蚀”掉1.2万亿
2010年,我国仅被海水腐蚀掉的钢,价值1.2万亿元,相当于每个中国人掏出1000元。
钱江晚报
金属跟干燥气体或非电解质液体直接接触。
不纯金属或合金跟电解质溶液接触
是
否
两者往往同时发生,
电化学腐蚀更普遍、速度更快。
金属腐蚀的分类
M - ne- = Mn+
金属腐蚀 化学腐蚀 电化学腐蚀
本质
是否形成原电池
条件
联系
1. 检查装置的气密性。
2. 在小烧杯中用稀酸盐浸泡6颗铁钉;在另一只小烧杯中用饱和的食盐水浸泡另6颗铁钉。
3. 按下图装好装置,试管均放在试管架上。
4. 注意观察毛细管中液面的变化 。
操作:
实验探究
实验探究
实验探究
操作:
实验探究
操作:
用稀盐酸浸泡过的铁钉 用饱和食盐水浸泡过的铁钉
装置
毛细管中液面上升
毛细管中液面下降
吸氧腐蚀
析氢腐蚀
水膜呈中性或酸性很弱
水膜酸性较强
吸氧腐蚀
析氢腐蚀
反应中生成了气体
反应中消耗了气体
用稀盐酸浸泡过的铁钉 用饱和食盐水浸泡过的铁钉
实验现象
结论
负极反应
正极反应
总反应
类别
条 件
普遍性 比 更普遍
1. 大桥上处于浪花飞溅区的钢发生电化学腐蚀,且由于干湿交替,氧供应充分,盐分不断浓缩,腐蚀最严重。请写出该腐蚀过程中的正、负极反应。
2. 某段时间,空气污染严重,酸雨腐蚀了钢,该腐蚀属于 腐蚀。
学以致用
二、金属的防护
2.改善金属的内部组成结构。
思路:抑制金属失去电子。
传统方法
1.在金属表面覆盖保护层。
桥梁用传统方法来防腐,防护寿命一般仅在10年左右。
金属的电化学防护
思考:请应用你所学电化学知识设计方案保护钢铁,画出示意图,并标出电子流动的方向。
牺牲阳极的阴极保护法
外加电流的阴极保护法
正极,被保护
电解池原理
原电池原理
阴极
阳极(惰性电极)
负极,被腐蚀
原理
被保护金属作哪极
另一电极
金属电化学防护
开拓视野
常用外加电流的阴极保护法防护航母,应用 原理,钢作 极,用惰性电极作 极。
电解池
阴
阳
燃气工程中钢管的防腐方法
对于城市燃气系统,由于地下管网密集,阴极保护的外加电源对其它管道干扰大,会造成自身受益、他家受害的局面。采用比钢活泼的金属材料与钢管相连则不会出现此类情况,该方法的名称叫 。
应用 原理,钢作 极,比钢活泼的金属作 极。
牺牲阳极的阴极保护法
开拓视野
原电池
正
负
桥梁的防护
电弧喷铝 +复合漆
三重保护,耐腐蚀寿命30年以上。
开拓视野
下列各情况,其中Fe片腐蚀由快到慢的顺序: 。
电解池的阳极>原电池的负极>化学腐蚀
>原电池的正极>电解池的阴极
(5)>(2)>(1)>(3)>(4)
学以致用
(1)
(2)
下列情况下,铁被腐蚀还是被保护?写出电极反应。
学以致用
(09年广东高考)出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。下列说法正确的是(双选)
A. 锡青铜的熔点比纯铜高。
B.在自然环境中,锡青铜中的锡对铜起保护作用。
C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快。
D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程。
学以致用
B C
课堂小结
一、金属腐蚀
1.本质:金属单质失去电子变成阳离子。
金属腐蚀
2.分类
(形成原电池)
二、金属电化学的防护
思路:抑制金属单质失去电子。
1.牺牲阳极的阴极保护法。(原电池原理)
2.外加电流的阴极保护法。(电解池原理)
