化学人教版高中选修4第三章第四节难溶电解质的溶解平衡PPT课件(共21张PPT)
文档属性
| 名称 | 化学人教版高中选修4第三章第四节难溶电解质的溶解平衡PPT课件(共21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 874.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-31 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
第四节 难溶电解质的溶解平衡
[复习]
1、什么叫饱和溶液?什么叫不饱和溶液?
一定温度下,不能再溶解溶质的溶液叫饱和溶液。
2.溶解性是指:_______________________________;
溶解性是物质的___________性质。物质溶解性的大小
跟___________________________有关。
一种物质溶解在另一种物质中的能力。
物理
溶质、溶剂的性质
溶解性 易溶 可溶 微溶 难溶
3、溶解度
在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量。叫做这种物质在这种溶剂里的溶解度。
注意:
①条件:一定温度; ②标准:100g溶剂
③状态:饱和状态 ④单位:g
⑤任何物质的溶解:是有条件的,在一定条件下
某物质的溶解量也是有限的,无限可溶解的物质不存在。
(1)20℃时100克水里,溶解了36克氯化钠达到饱和状态,20℃时NaCl的溶解度是多少?
(2)20℃时,KClO3在水里的溶解度是7.4g,这表示什 么含义?
此时,溶液中溶质、溶剂、溶液的质量比是 。
练习
36克
20℃时,100克水中最多溶解7.4 克KClO3
7.4 :100 :107.4
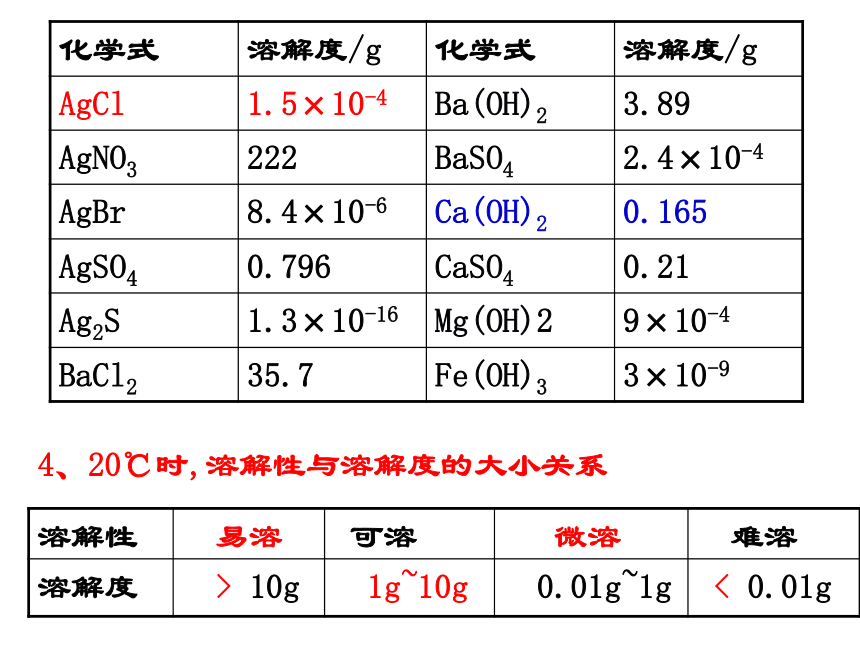
4、20℃时,溶解性与溶解度的大小关系
化学式 溶解度/g 化学式 溶解度/g
AgCl 1.5×10-4 Ba(OH)2 3.89
AgNO3 222 BaSO4 2.4×10-4
AgBr 8.4×10-6 Ca(OH)2 0.165
AgSO4 0.796 CaSO4 0.21
Ag2S 1.3×10-16 Mg(OH)2 9×10-4
BaCl2 35.7 Fe(OH)3 3×10-9
溶解性 易溶 可溶 微溶 难溶
溶解度 > 10g 1g~10g 0.01g~1g < 0.01g
讨论:
⑴ 向溶液中加入足量多的蔗糖,当观察到蔗糖的量不再减少时, 蔗糖是否还在溶解?
(2) 取4ml NaCl饱和溶液,滴加1—2ml 浓HCl,观察现象?
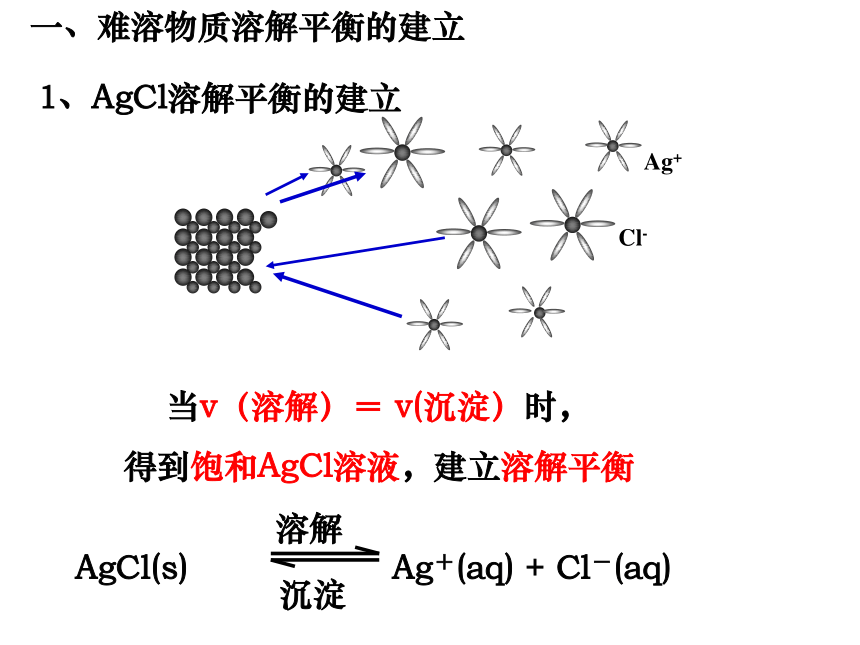
1、AgCl溶解平衡的建立
当v(溶解)= v(沉淀)时,
得到饱和AgCl溶液,建立溶解平衡
一、难溶物质溶解平衡的建立
2、溶解平衡的特征
逆、等、动、定、变
3、生成难溶电解质的离子反应的限度
当溶解度小于0.01g,或离子浓度小于1×10-5mol/L时,认为反应完全,但溶液中还有相应的离子。
溶解
AgCl(s) Ag+(aq) + Cl-(aq)
沉淀
4.影响因素:内因、外因(浓度、温度等)
【例1】:AgCl(s) Ag+(aq) + Cl-(aq) △H>0 的平衡体系,改变条件,溶解平衡怎样移动?
a.温度:
多数难溶电解质的溶解是吸热的, 升高温度,平衡正向移动。溶解度增大。
b.加入水:
平衡正向移动。
c.加入AgCl固体:
饱和溶液,平衡不移动。
d.加入NaCl晶体:
同离子效应,平衡逆向移动。
[例2]石灰乳中存在下列平衡: Ca(OH)2(s) Ca2+(aq) + 2OH-(aq),加入下列溶液,可使Ca(OH)2减少的是….....( )
A、Na2CO3溶液 B、AlCl3溶液 C、NaOH溶液 D、CaCl2溶液
AB
5、溶度积
⑴、溶度积(Ksp):
难溶电解质的溶解平衡中,离子浓度幂的乘积。
25℃时, Ksp = c(Pb2+).c(I-)2 = 7.1×10-9
mol3?l-3
练习:BaSO4、Fe(OH)3的溶度积表达式 。
Ksp[BaSO4] =c(Ba2+).c(SO42-) 单位: mol2?L-2
Ksp [Fe(OH)3]= c(Fe3+).c(OH-)3 单位: mol4?L-4
溶度积常数
化学式 Ksp 化学式 Ksp
AgCl 1.56×10-10 Cu2S 2×10-47
AgBr 7.7×10-13 CuCl 1.02×10-6
AgI 1.5×10-16 Fe(OH)2 1.64×10-14
Ag2S 6.3×10—50 Fe(OH)3 1.1×10-36
BaCO3 8.1×10-9 HgS 4×10-53
BaSO4 1.08×10-10 Li2CO3 1.7×10-3
CaCO3 8.7×10-9 MgCO3 2.6×10-5
CaF2 3.95×10—11 Mg(OH)2 1.2×10-11
CaSO4 1.96×10-4 PbSO4 1.06×10-8
CuS 8.5×10-45 ZnS 1.2×10-23
练1:在100mL 0.01mol/LKCl 溶液中,加入 1mL 0.01mol/L AgNO3溶液,下列说法正确的是(AgCl Ksp=1.8×10-10) ( )
A.有AgCl沉淀析出 B.无AgCl沉淀
C.无法确定 D.有沉淀但不是AgCl
A
⑶、溶度积规则
任意时刻:Qc = [c(Mn+)]m·[c(Am—)]n
当: Qc > Ksp 过饱和,析出沉淀,
Qc = Ksp 饱和,平衡状态
Qc < Ksp 未饱和。
如:工业原料氯化铵中混有氯化铁,加氨水调pH值至7-8
Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+
② 加沉淀剂
如:沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂
Cu2++S2-= CuS↓(黑色) Hg2++S2-= HgS↓
二、沉淀反应的应用
1、沉淀的生成
(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。
思考与交流
1、如果要除去某溶液中的SO42-,你选择加 入钡盐还是钙盐?为什么?
加入钡盐,因为BaSO4比CaSO4更难溶,使用钡盐可使SO42-沉淀更完全
2、是否可能使要除去的离子通过沉淀反应全部除去?说明原因。
不可能使要除去的离子通过沉淀完全除去
KSP(BaSO4) 1.08×10-10
KSP(CaSO4) 1.96×10-4
2. 沉淀的溶解
【例2】、用平衡移动的原理分析Mg(OH)2溶于盐酸和NH4Cl溶液的原因?并找出使沉淀溶解的规律。
解释:
在溶液中存在Mg(OH)2的溶解平衡: Mg(OH)2(s) ? Mg2+(aq)+2OH-(aq)
加入盐酸时,H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解;
加入NH4Cl时,NH4+水解,产生的H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。
滴加试剂 蒸馏水 盐酸 氯化铵溶液
现 象 不溶解 溶解 溶解
2. 沉淀的溶解
(1) 利用氧化还原方法降低某一离子的浓度。
(2) 生成弱电解质。如:
H2S
FeS(S) Fe2+ (aq) + S2- (aq)
S + NO + H2O
(3) 生成络合物,例:银铵溶液的配制
3、沉淀的转化
几种难熔电解质在25℃时的溶解平衡和溶度积:
AgCl(s) Ag+ + Cl-
Ksp= c(Ag+)c(Cl-) = 1.8×10-10mol2?L-2 AgBr(s) Ag+ + Br-
Ksp= c(Ag+)c(Br-) = 5.0×10-13mol2?L-2 AgI(s) Ag+ + I-
Ksp= c(Ag+)c(I-) = 8.3×10-17mol2?L-2
溶解能力大小有:AgCl > AgBr > AgI
沉淀的转化的实质:使溶液中的离子浓度更小
沉淀可以从溶解度小的向溶解度更小的方向转化,两者差别越大,转化越容易。
白色沉淀
黄色沉淀
黑色沉淀
步骤 NaCl和AgNO3 向所得固液中滴加KI 向新的固液混合物滴加Na2S
现象
[思考与交流]:
白色沉淀
白色沉淀转化为
红褐色沉淀
红褐色沉淀析出,溶液褪至无色
步骤 向MgCl2溶液中滴加NaOH溶液 向有白色沉淀的混合物液中滴加FeCl3溶液 静置
现象
共同进步!
第四节 难溶电解质的溶解平衡
[复习]
1、什么叫饱和溶液?什么叫不饱和溶液?
一定温度下,不能再溶解溶质的溶液叫饱和溶液。
2.溶解性是指:_______________________________;
溶解性是物质的___________性质。物质溶解性的大小
跟___________________________有关。
一种物质溶解在另一种物质中的能力。
物理
溶质、溶剂的性质
溶解性 易溶 可溶 微溶 难溶
3、溶解度
在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量。叫做这种物质在这种溶剂里的溶解度。
注意:
①条件:一定温度; ②标准:100g溶剂
③状态:饱和状态 ④单位:g
⑤任何物质的溶解:是有条件的,在一定条件下
某物质的溶解量也是有限的,无限可溶解的物质不存在。
(1)20℃时100克水里,溶解了36克氯化钠达到饱和状态,20℃时NaCl的溶解度是多少?
(2)20℃时,KClO3在水里的溶解度是7.4g,这表示什 么含义?
此时,溶液中溶质、溶剂、溶液的质量比是 。
练习
36克
20℃时,100克水中最多溶解7.4 克KClO3
7.4 :100 :107.4
4、20℃时,溶解性与溶解度的大小关系
化学式 溶解度/g 化学式 溶解度/g
AgCl 1.5×10-4 Ba(OH)2 3.89
AgNO3 222 BaSO4 2.4×10-4
AgBr 8.4×10-6 Ca(OH)2 0.165
AgSO4 0.796 CaSO4 0.21
Ag2S 1.3×10-16 Mg(OH)2 9×10-4
BaCl2 35.7 Fe(OH)3 3×10-9
溶解性 易溶 可溶 微溶 难溶
溶解度 > 10g 1g~10g 0.01g~1g < 0.01g
讨论:
⑴ 向溶液中加入足量多的蔗糖,当观察到蔗糖的量不再减少时, 蔗糖是否还在溶解?
(2) 取4ml NaCl饱和溶液,滴加1—2ml 浓HCl,观察现象?
1、AgCl溶解平衡的建立
当v(溶解)= v(沉淀)时,
得到饱和AgCl溶液,建立溶解平衡
一、难溶物质溶解平衡的建立
2、溶解平衡的特征
逆、等、动、定、变
3、生成难溶电解质的离子反应的限度
当溶解度小于0.01g,或离子浓度小于1×10-5mol/L时,认为反应完全,但溶液中还有相应的离子。
溶解
AgCl(s) Ag+(aq) + Cl-(aq)
沉淀
4.影响因素:内因、外因(浓度、温度等)
【例1】:AgCl(s) Ag+(aq) + Cl-(aq) △H>0 的平衡体系,改变条件,溶解平衡怎样移动?
a.温度:
多数难溶电解质的溶解是吸热的, 升高温度,平衡正向移动。溶解度增大。
b.加入水:
平衡正向移动。
c.加入AgCl固体:
饱和溶液,平衡不移动。
d.加入NaCl晶体:
同离子效应,平衡逆向移动。
[例2]石灰乳中存在下列平衡: Ca(OH)2(s) Ca2+(aq) + 2OH-(aq),加入下列溶液,可使Ca(OH)2减少的是….....( )
A、Na2CO3溶液 B、AlCl3溶液 C、NaOH溶液 D、CaCl2溶液
AB
5、溶度积
⑴、溶度积(Ksp):
难溶电解质的溶解平衡中,离子浓度幂的乘积。
25℃时, Ksp = c(Pb2+).c(I-)2 = 7.1×10-9
mol3?l-3
练习:BaSO4、Fe(OH)3的溶度积表达式 。
Ksp[BaSO4] =c(Ba2+).c(SO42-) 单位: mol2?L-2
Ksp [Fe(OH)3]= c(Fe3+).c(OH-)3 单位: mol4?L-4
溶度积常数
化学式 Ksp 化学式 Ksp
AgCl 1.56×10-10 Cu2S 2×10-47
AgBr 7.7×10-13 CuCl 1.02×10-6
AgI 1.5×10-16 Fe(OH)2 1.64×10-14
Ag2S 6.3×10—50 Fe(OH)3 1.1×10-36
BaCO3 8.1×10-9 HgS 4×10-53
BaSO4 1.08×10-10 Li2CO3 1.7×10-3
CaCO3 8.7×10-9 MgCO3 2.6×10-5
CaF2 3.95×10—11 Mg(OH)2 1.2×10-11
CaSO4 1.96×10-4 PbSO4 1.06×10-8
CuS 8.5×10-45 ZnS 1.2×10-23
练1:在100mL 0.01mol/LKCl 溶液中,加入 1mL 0.01mol/L AgNO3溶液,下列说法正确的是(AgCl Ksp=1.8×10-10) ( )
A.有AgCl沉淀析出 B.无AgCl沉淀
C.无法确定 D.有沉淀但不是AgCl
A
⑶、溶度积规则
任意时刻:Qc = [c(Mn+)]m·[c(Am—)]n
当: Qc > Ksp 过饱和,析出沉淀,
Qc = Ksp 饱和,平衡状态
Qc < Ksp 未饱和。
如:工业原料氯化铵中混有氯化铁,加氨水调pH值至7-8
Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+
② 加沉淀剂
如:沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂
Cu2++S2-= CuS↓(黑色) Hg2++S2-= HgS↓
二、沉淀反应的应用
1、沉淀的生成
(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。
思考与交流
1、如果要除去某溶液中的SO42-,你选择加 入钡盐还是钙盐?为什么?
加入钡盐,因为BaSO4比CaSO4更难溶,使用钡盐可使SO42-沉淀更完全
2、是否可能使要除去的离子通过沉淀反应全部除去?说明原因。
不可能使要除去的离子通过沉淀完全除去
KSP(BaSO4) 1.08×10-10
KSP(CaSO4) 1.96×10-4
2. 沉淀的溶解
【例2】、用平衡移动的原理分析Mg(OH)2溶于盐酸和NH4Cl溶液的原因?并找出使沉淀溶解的规律。
解释:
在溶液中存在Mg(OH)2的溶解平衡: Mg(OH)2(s) ? Mg2+(aq)+2OH-(aq)
加入盐酸时,H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解;
加入NH4Cl时,NH4+水解,产生的H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。
滴加试剂 蒸馏水 盐酸 氯化铵溶液
现 象 不溶解 溶解 溶解
2. 沉淀的溶解
(1) 利用氧化还原方法降低某一离子的浓度。
(2) 生成弱电解质。如:
H2S
FeS(S) Fe2+ (aq) + S2- (aq)
S + NO + H2O
(3) 生成络合物,例:银铵溶液的配制
3、沉淀的转化
几种难熔电解质在25℃时的溶解平衡和溶度积:
AgCl(s) Ag+ + Cl-
Ksp= c(Ag+)c(Cl-) = 1.8×10-10mol2?L-2 AgBr(s) Ag+ + Br-
Ksp= c(Ag+)c(Br-) = 5.0×10-13mol2?L-2 AgI(s) Ag+ + I-
Ksp= c(Ag+)c(I-) = 8.3×10-17mol2?L-2
溶解能力大小有:AgCl > AgBr > AgI
沉淀的转化的实质:使溶液中的离子浓度更小
沉淀可以从溶解度小的向溶解度更小的方向转化,两者差别越大,转化越容易。
白色沉淀
黄色沉淀
黑色沉淀
步骤 NaCl和AgNO3 向所得固液中滴加KI 向新的固液混合物滴加Na2S
现象
[思考与交流]:
白色沉淀
白色沉淀转化为
红褐色沉淀
红褐色沉淀析出,溶液褪至无色
步骤 向MgCl2溶液中滴加NaOH溶液 向有白色沉淀的混合物液中滴加FeCl3溶液 静置
现象
共同进步!
