人教版九年级化学下第八单元课题 2 金属的化学性质教学设计
文档属性
| 名称 | 人教版九年级化学下第八单元课题 2 金属的化学性质教学设计 |

|
|
| 格式 | zip | ||
| 文件大小 | 68.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-12-30 00:00:00 | ||
图片预览



文档简介
《金属的化学性质》教学设计
1、 教学分析
1.课程标准及相关内容分析
“金属的化学性质”属于九年制义务教育化学课程标准中一级主题“身边的化学物质”中的二级主题“金属与金属矿物”的知识内容,其标准是:(1)了解金属的物理性质,认识常见金属的化学性质。同时也属于九年制义务教育化学课程标准中一级主题“物质的化学变化”中的二级主题“认识几种化学反应”的知识内容,其标准是:“能用金属活动顺序对有关置换反应进行判断,并能解释日常生活中的一些化学现象”。还属于九年制义务教育化学课程标准中一级主题“科学探究”中的二级主题“增进对科学探究的理解、发展科学探究能力”的知识内容。
本节课的主要内容:(1)知道铁、铝、铜等常见金属与氧气的反应。(2)初步认识常见金属与盐酸、硫酸的置换反应,以及与盐溶液的置换反应,能用置换反应解释一些与日常生活有关的化学问题。(3)能用金属活动性顺序对有关的置换反应进行简单的判断,并能利用金属活动性顺序解释一些与日常生活有关的化学问题。
2.学生分析
(1)学生已有认识基础
通过前几章化学的学习,学生对于学习化学的方法有了初步的认识,知道几种基本反应类型,会判断置换反应。通过第八单元第一课题《金属材料》的学习,学生知道金属的物理性质;了解了金属与合金的用途。通过日常生活中铁生锈的生活现象,对金属的化学性质有一定的了解。学生在前一阶段的学习中已经做过镁条、铝箔、铁丝等在氧气中反应的实验,对于本节课的学习有了一定的认识基础,因此学生能够通过独立思考基本可以对反应的实验现象和结论进行预测和推断。再者,学生已经具备了一定的实验基本操作能力,根据反应的现象,可以初步归纳出大多数金属都能与氧气反应,反应的难易和剧烈程度不同的实验结论。同时,学生对于科学探究的方法和步骤有了一定的了解,这都是本节课能够顺利进行的保障。
⑵学生学习本课的困难或可能出现的问题
学生虽然知道金属的物理性质和用途等,但是金属与酸反应和金属与化合物反应会发生怎样的反应,生成什么物质,有怎样的实验现象学生不知道,这可以激发学生的学习热情。通过探究实验可以总结得出金属活动顺序表比较容易,但是对于金属活动顺序表的应用是学生的难点。再者,学生的实验操作能力和科学探究能力还有待于进一步提高。这正是本节课探究活动的切入点,可激发学生的探究兴趣,提高探究能力和实验能力。
二、教学目标
1.知识与技能
(1)知道铁、铝、铜等常见金属与氧气的反应。 ?
(2)初步认识常见金属与盐酸、硫酸的置换反应,以及与盐溶液的置换反应。
(3)能用金属活动性顺序对有关的置换反应进行简单的判断,并能利用金属活动性顺序解释一些与日常生活有关的化学问题。
(4)建立知识网络图、建立结构决定性质、性质影响用途的学科思想。
2、过程与方法 ?
(1)认识科学探究的基本过程,通过教师的组织、引导和点拔,进行实验探究和讨论交流,从而认识金属的化学性质及其活动性顺序。 ?
(2)通过实验探究和讨论交流,体验和掌握科学的方法,养成科学的态度;学会运用对比、分析、归纳、概括等方法对获取的信息进行加工和处理。
(3)初步学会运用比较、归纳、概括等方法对获取的信息进行加工,逐步形成良好学习习惯和方法。
3、情感态度与价值观 ?
(1)培养证唯物主义观点,保持和增强对化学现象的好奇心和探究欲,激发学习化学兴趣。 (2)培养合作意识以及勤于思考、严谨求实、勇于实践的科学精神。 ?
(3)了解化学与日常生活和生产的密切关系。
三、 教学重点与难点
重点:通过实验探究认识金属活动性顺序表、认识金属重要化学性质及置换反应、了解结构决定性质、性质影响用途的学科思想、构建知识网络。
难点:运用金属活动性顺序对置换反应作出判断
四、教学策略
教学策略:多媒体辅助教学法、探究实验、归纳总结、讲练结合、小组合作学习
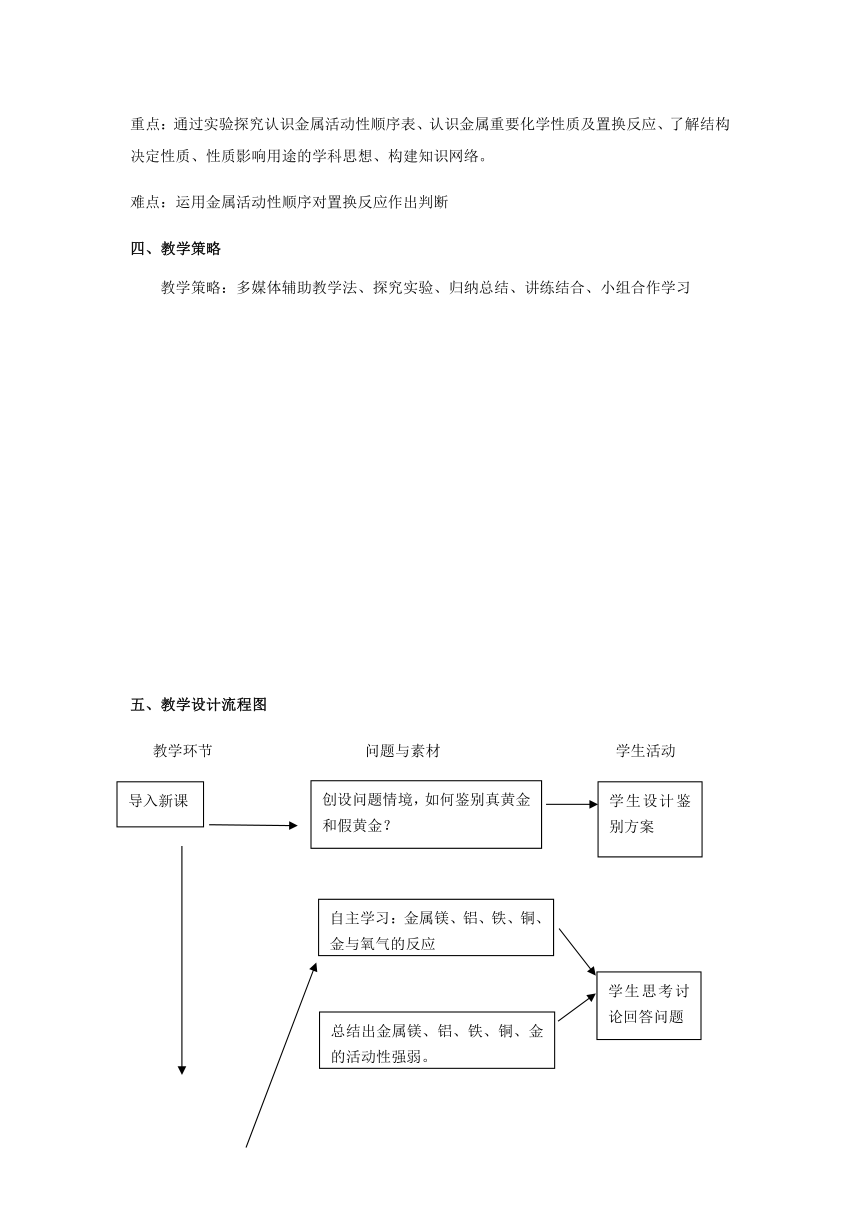
五、教学设计流程图
教学环节 问题与素材 学生活动
六、教学过程
教学环节 教师活动 学生活动 设计意图
导入新课 【创设问题情境】这是两枚真假不同的戒指。现在黄金饰品中的假黄金常常鱼目混珠,社会上有些不法分子时常以黄铜(铜和锌的混合物)冒充黄金进行诈骗活动。黄铜单纯从颜色、外型上看,与黄金极为相似,所以很难区分。我想请同学们根据你学过的化学知识设计一个实验方案鉴别真假黄金。 【总结】前两种方法利用金属物理性质,后一种则利用金属的化学性质。 【提问】还有没有别的方法区别黄金与假黄金?这就需要更多地了解金属的化学性质。本节课我们来学习金属的化学性质。 【板书】课题二 金属的化学性质 学生设计实验方案判断黄金的真假。通过测密度;硬度不同,相互刻画;根据已有的生活常识---用火烧(“真金不怕火炼”),变黑的为黄铜,不变色的为黄金 问题导思,激发学生的学习兴趣。 复习了金属的物理性质,培养理论联系实际的能力。 问题导思,激发学生的学习兴趣。
知识新授 【板书】一、金属与氧气反应【自主学习】金属与氧气反应【总结】通过氧气化学性质的学习我们知道,镁条在空气中就能剧烈的燃烧。通过预习我们也知道了铝在氧气中可以剧烈地燃烧。而铁在火柴引燃条件下,在氧气中能剧烈反应。铜在氧气中加热只能变黑。金在高温的条件下都不能与氧气发生反应。 这说明大多数金属都能与氧气反应,只是剧烈程度不同,而难易程度和剧烈程度反应出金属的活泼程度即金属的活动性。为什么金属与氧气反应的难易和剧烈程度不同? 金属的活动性强、有弱。在相同的条件下,金属与氧气反应越容易,金属的活泼性越强;金属的活动性越强,反应越剧烈。镁、铝、铁、铜、金几种金属的活动性顺序为:镁铝较活泼、铁铜次之、金不活泼。 学生讨论回答、总结规律 学生回答 本部分知识比较简单,在学习氧气的性质时已经学过镁、铁、铝、铜分别于氧气反应的实验现象。所以采用学生自主学习方式培养学生的学习能力。 培养技能,让学生在观察与讨论中发现问题、提出问题、解决问题,从中培养科学的观察、规范表达和综合分析问题的能力。 通过总结金属与氧气反应的难易程度总结得出金属活泼性有强有弱的结论,为总结金属活动顺序表做准备。激发学生思维和学习兴趣问题导思,激发兴趣,培养理论联系实际的能力。扩充学生知识面。
【提问】金属与氧气反应能体现金属活动性的不同。金属与其他物质反应能否也体现出金属活动性的不同呢?【探究实验】金属与盐酸或稀硫酸是否反应以及反应的剧烈程度,是否也可反映出金属的活泼程度。下面,我们就通过实验来比较镁、锌、铁、铜的活动性。 将学生分成A、B两大组:A组:在四支试管中分别放入两小块打磨光洁的镁条、锌粒、铁片、铜片,各加入约5 mL稀盐酸,观察现象,比较反应的剧烈程度;用燃着的木条放在试管口,观察并记录实验现象。B组:用稀硫酸代替稀盐酸进行实验,并比较发生的现象。通过以上实验,你观察到什么实验现象?得出什么结论?金属能与酸反应,如盐酸或稀硫酸等。【板书】二、金属与酸反应【总结】(1)镁、锌、铁可与盐酸或稀硫酸反应生成氢气,铜不能与盐酸或稀硫酸反应。(2)镁反应最剧烈,其次是锌,然后是铁。即镁、锌、铁与盐酸或稀硫酸反应时的剧烈程度不同。在生活中有这样一个现象绿豆在铁锅中煮了以后会变黑、苹果、梨子用铁刀切了以后,表面也会变黑。请同学们想一想这是为什么呢?这是因为绿豆、苹果、梨子与多种水果的细胞里?都含有鞣酸,鞣酸能和铁反应,生成黑色的鞣酸铁。(3)与酸反应时,能生成氢气的金属活动性强;否则,就较弱。(4)镁、锌、铁、铜的金属活动性由强到弱。【总结】这说明,通过金属与酸反应,在酸的种类相同、酸量相同、温度相同条件下,金属与酸反应的剧烈程度不同,也能体现出金属活动性的强和弱。镁锌铁铜四种金属的活动性由强到弱的顺序是镁>锌>铁>铜。这与金属与氧气反应得出的活动性顺序相一致。知道了金属的活动性顺序,大家能写出金属与酸反应的化学方程式吗?Mg+2HCl == MgCl2+ H2↑Zn+2HCl==ZnCl2 + H2↑Fe+2HCl== FeCl2 + H2↑请大家从反应物和生成物的物质类别如单质、化合物的角度分析,这些反应有什么特点?它与我们学习过的化合反应和分解反应的特点是否相同?置换反应:由一种单质与一种化合物反应,生成了另一种单质和另一种化合物的反应叫做置换反应。置换反应特点:A + BC = B + AC在金属活动性顺序里,位于氢前面的金属能置换出盐酸稀硫酸中的氢。【总结】金属+酸→ 金属化合物+H2↑ 【过渡】金属与氧气反应能体现金属的活动性顺序,与酸反应也能体现金属的活动性顺序,用其它方法能否比较出金属活动顺序吗?【回忆】铁和硫酸铜反应的实验现象和化学方程式。Fe+CuSO4=FeSO4+Cu“曾青得铁则化为铜”是现代湿法冶金的先驱,也是我国古代劳动人民辛勤智慧的结晶,我们应该加倍努力把我们祖先业绩发扬光大。【板书】三、金属与金属化合物溶液反应铁的活动性比铜强,说明活动性强的金属能把活动性弱的金属从其化合物溶液中置换出来。其它金属之间是否也存在这样的规律呢?活动与探究:把一段用砂纸打磨、擦亮的铝丝浸入盛有硫酸铜溶液的试管中,过一会儿取出,观察实验现象、写化学方程式2Al+3CuSO4=3Cu+ Al2(SO4)3(2) 把一段用砂纸打磨、擦亮的铜丝浸入盛有硝酸银溶液的试管中,过一会儿取出,观察实验现象、写化学方程式Cu+2AgNO3==Cu(NO3)2+2Ag(3) 把一段用砂纸打磨、擦亮的铜丝浸入盛有硫酸铝溶液的试管中,过一会儿取出,观察实验现象、写化学方程式。 学生思考 学生分组实验并仔细观察实验现象,记录并通过比较、分析,得出结论。 学生完成课堂学案学生口述实验现象学生讨论并回答 学生根据上网查阅的资料回答 学生分组实验并仔细观察实验现象,记录并通过比较、分析,得出结论。 学生写出化学方程式 思考回答:这些反应的特点是: 由一种单质跟一种化合物起反应生成另一种单质和另一种化合物。其特点不同于化合反应和分解反应。 学生分组实验并仔细观察实验现象,记录并通过比较、分析,得出结论。 学生回忆已有学过的知识不能回答,激发学生积极地思考,调动学生学习积极性。 通过学生动手实验加强对知识的理解和加深印象。 使学生在交流中互相启发,相互激励,发展和完善自我、培养团结协作、互助的精神。 培养学生的操作技能,让学生在观察与讨论中发现问题、提出问题、解决问题,从中培养科学的观察、规范表达和综合分析问题的能力通过反应现象判断产物并能书写化学方程式。 培养学生的归纳总结能力问题导思,激发兴趣,培养理论联系实际、规范表达的能力。 结合生活实际,解决生活实际问题,体现化学就在我们身边,激发学习化学积极性。 让学生在观察与讨论中发现问题、提出问题、解决问题,从中培养科学的观察、规范表达和综合分析问题的能力 为总结反应类型奠定基础。 使学生的思维从现象到本质产生飞跃。 问题激发兴趣培养学生处理和加工信息的能力 培养操作技能,让学生在观察与讨论中发现问题、提出问题、解决问题,从中培养科学的观察、规范表达和综合分析问题的能力 让学生在观察与讨论中发现问题、提出问题、解决问题,从中培养科学的观察、规范表达和综合分析问题的能力
通过以上实验,你观察到什么实验现象?可以得出什么结论?【投影】归纳总结实验现象、化学方程式【总结】活动性强的金属能把活动性弱的金属从它们的化合物溶液中反应出来。而活动性弱的金属不能把活动性强的金属从其化合物溶液中置换出来。即:金属与金属化合物反应:排在前面的金属能把排在后面的金属从其化合物溶液中反应出来,反之不行。(不考虑氢前氢后)三种金属活动性顺序为: Al> Cu> Ag 【总结】金属+金属化合物→ 新金属+新化合物通过探究活动,我们知道,很多金属不仅能与氧气反应,而且还能与盐酸或稀硫酸反应,还能把比它弱的金属从其化合物的溶液中置换出来。说明金属的活动性有强、有弱。经过了许多类似上述实验的探究过程,人们进行了认真的去伪存真、由表及里的分析,归纳和总结出了常见金属在溶液中的活动性顺序:【板书】四、金属活动顺序表K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au金属活动性:由强到弱【提问】我们家里都有铝锅、铁锅,为什么没有钾锅、镁锅?【总结】因为这些金属太活泼,不能以金属单质的形式存在。 学生改正书写化学反应方程式 金属活动性顺序:铝>铜>银 通过金属与金属化合物溶液反应鉴别。思考、理解、记忆、记录 思考、理解、记忆、记录 学生总结规律 通过反应现象判断产物并能书写化学方程式。 培养学生的归纳总结能力 问题导思,激发兴趣培养学生处理和加工信息的能力。 培养学生分析问题能力和实事求是的科学 总结规律,掌握学习方法
小结 通过本课题的学习,我们学习了金属的化学性质,与氧气发生反应,金属与酸反应和金属与另一种金属化合物溶液的反应,可以判断出金属活动性的强弱,得出金属活动顺序表。同时,我们也认识了一种新的反应类型──置换反应。用知识结构图的方法更加便于理解和记忆。 使本课知识再现,提高学生归纳总结能力通过介绍,增加学生生活常识,使学生认识到化学就在我们身边,激发学习化学积极性。
练习反馈: 1.下列物质能否发生反应?能反应的写出化学方程式(1)银与稀盐酸(2)锌与硫酸铜溶液(3)铜与硫酸锌溶液(4)铝与硝酸银溶液2.有X Y Z三种金属,如果把X和Y分别放入稀硫酸中, X 溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y的表面有银析出,而Z无变化.根据以上事实,判断X Y Z的金属活动顺序 ? 。3.芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的。下面是生产单质硅过程中的一个重要反应:SiO2 + 2C =Si +2CO↑,该反应的基本类型是 ( )A.化合反应 B.分解反应 C.置换反应 D.复分解反应4.若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是A.Mn+2HCl =MnC12+H2↑ B.Mg +MnSO4=MgSO4+MnC.Mn+Cu(NO3)2=Mn(NO3)2+Cu D.Fe+MnSO4 =FeSO4+Mn 通过课堂反馈了解学生对本节课知识的掌握情况
评价反思 通过本节课知识的学习,你怎样用化学方法鉴别真黄金和假黄金?你有哪些收获? 学生回答
作业 设计一个实验证明活泼性 Zn > Fe > Cu
6、板书设计
课题二 金属的化学性质
(1) 金属与氧气反应
(2) 金属与酸的反应
(3) 金属与金属化合物溶液的反应
(4) 置换反应
(5) 金属活动顺序表
七、学案或课堂练习设计
八、课后总结与反思
本节课采用了新的教学理念,通过有效地准备、有效地实施、有效地评价使学生从导入环节始终保持着浓厚的学习兴趣和学习的欲望,探究问题的热情高涨,很快进入学习“角色”,想学而乐学,顺利完成了教学任务。培养了学生的自学能力,小组合作意识浓厚。由现象推断产物,培养学生严密的逻辑思维能力和分析问题的能力,使学生进一步深化认识过程,学会探索知识的方法,提高思维品质和科学素养。提升解决实际问题、学以致用的能力。整节课学生们的学习都能有条不紊的进行,实验做的比较成功,教学互动进行的很好,以教师为主导,学生为主体,进行互动式教学。学生在回答问题过程中始终保持着积极的思维状态并积极举手回答问题。对教学内容中的重点知识和难点知识掌握情况较好。在课堂检测环节,正确率达到95%以上。同时,还建立了清晰的知识网络结构,使学生掌握了学习其它物质性质的学习方法。但是,由于本节课的课堂容量较大,个别学生还不能较好掌握。
导入新课
创设问题情境,如何鉴别真黄金和假黄金?
学生设计鉴别方案
自主学习:金属镁、铝、铁、铜、金与氧气的反应
学生思考讨论回答问题
总结出金属镁、铝、铁、铜、金的活动性强弱。
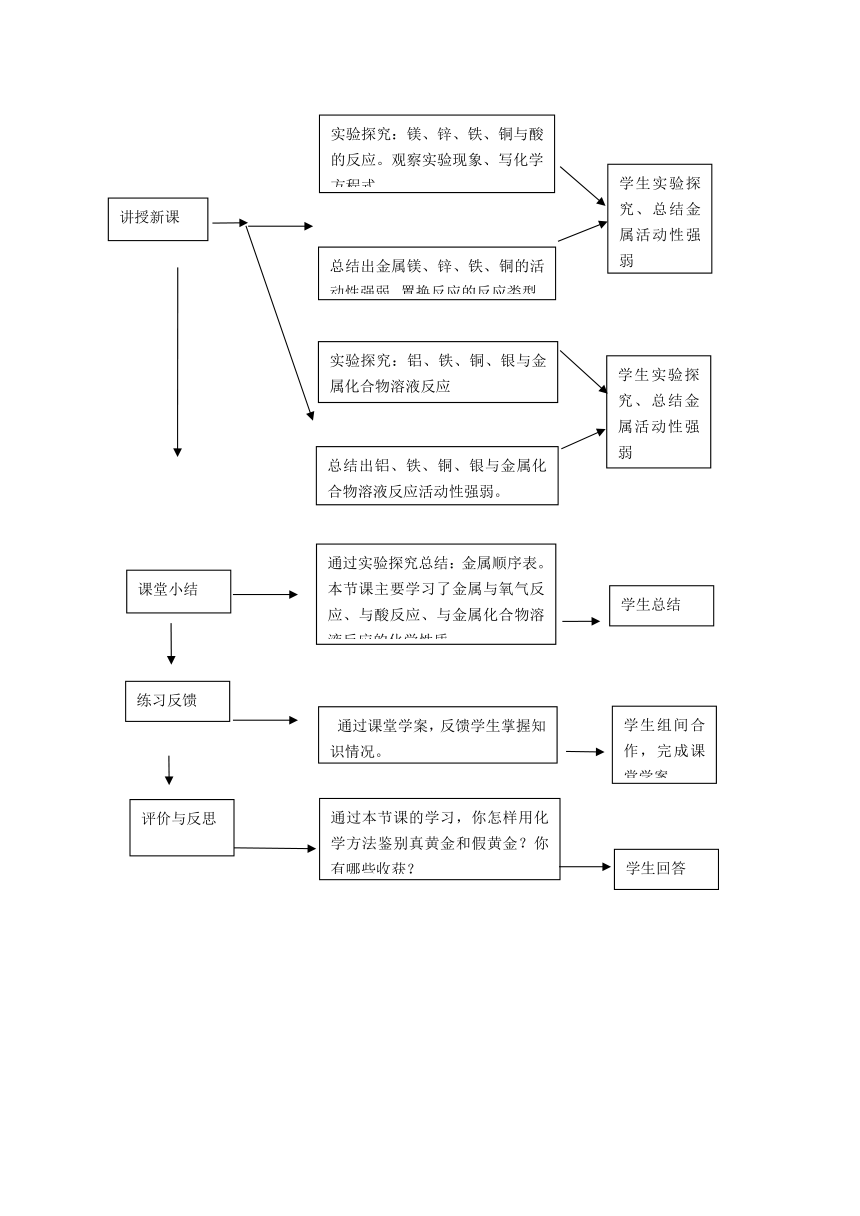
实验探究:镁、锌、铁、铜与酸的反应。观察实验现象、写化学方程式。
学生实验探究、总结金属活动性强弱
讲授新课
总结出金属镁、锌、铁、铜的活动性强弱、置换反应的反应类型。
实验探究:铝、铁、铜、银与金属化合物溶液反应
学生实验探究、总结金属活动性强弱
总结出铝、铁、铜、银与金属化合物溶液反应活动性强弱。
通过实验探究总结:金属顺序表。本节课主要学习了金属与氧气反应、与酸反应、与金属化合物溶液反应的化学性质。
学生总结
课堂小结
练习反馈
学生组间合作,完成课堂学案
通过课堂学案,反馈学生掌握知识情况。
通过本节课的学习,你怎样用化学方法鉴别真黄金和假黄金?你有哪些收获?
评价与反思
学生回答
同课章节目录
