1.5 物质的溶解 培优练习(含答案)
文档属性
| 名称 | 1.5 物质的溶解 培优练习(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 166.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-01-06 00:00:00 | ||
图片预览

文档简介
1.5 物质的溶解培优练习
一、选择题(共15题;共30分)
1.科学家用石墨烯膜制成"筛子",可以筛掉盐类物质.当海水流过该膜时,钠离子和氯离子被水分子包裹而不能通过,独立的水分子却能通过(如图).下列关于石墨烯膜“筛掉”氯化钠的说法错误的是( ???)
A.?该过程属于物理变化????????????????????????????????????????B.?该过程可应用于海水淡化 C.?“筛掉”氯化钠过程类似于过滤操作????????????????? D.?“筛掉”氯化钠后的海水溶质质量分数增大
第1题图 第2题图
2.在t℃时,某物质X、Y分别完全溶于水,溶液中X、Y与水的质量关系分别如图a、图b所示。下列说法正确的是( ???)
A.?X、Y都只能是固体??????????????????????????????????????????????B.?两种溶液一定是饱和溶液 C.?图示溶液的浓度:X3.今有60g溶质的质量分数为10%的食盐溶液,欲将其溶质的质量分数增大一倍,应采用的方法是(??? )
A.?把溶剂蒸发掉一半???????B.?加入6g食盐晶体???????C.?把溶剂蒸发掉30g???????D.?加入20%的食盐溶液30g
4.下列关于结晶和晶体的说法,正确的是(??? )
A.?饱和溶液降温析出晶体后的溶液仍然是饱和溶液?????B.?降低饱和溶液的温度一定有晶体析出 C.?从溶液中析出的晶体一定有结晶水??????????????????????????D.?把溶液的溶剂蒸发一些一定会有晶体析出
5.配制硝酸钾饱和溶液时得到下表数据,根据表中数据分析,不正确的是(??? )
序号
温度/℃
水的质量/g
所加硝酸钾的质量/g
所得溶液的质量/g
①
28
10
4
14
②
28
10
6
14
③
60
10
8
18
A.?60℃时10克水中最多能溶解硝酸钾8克???????????B.?60℃时等质量水中能溶解的硝酸钾比28℃时多 C.?①②所得溶液溶质的质量分数相等??????????????????? D.?③所得溶液不一定是硝酸钾的饱和溶液
6.硫酸镁在工农业以及医疗上有广泛应用,其溶解度如表所示.则下列说法正确的是(??? )
温度/℃
10
30
50
70
90
溶解度/g
27.7
39.3
49.0
54.1
51.1
A.?硫酸镁的溶解度随温度升高而减小 B.?10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液 C.?50℃时,100g硫酸镁饱和溶液中溶质和溶剂的质量比为49:100 D.?70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数不变
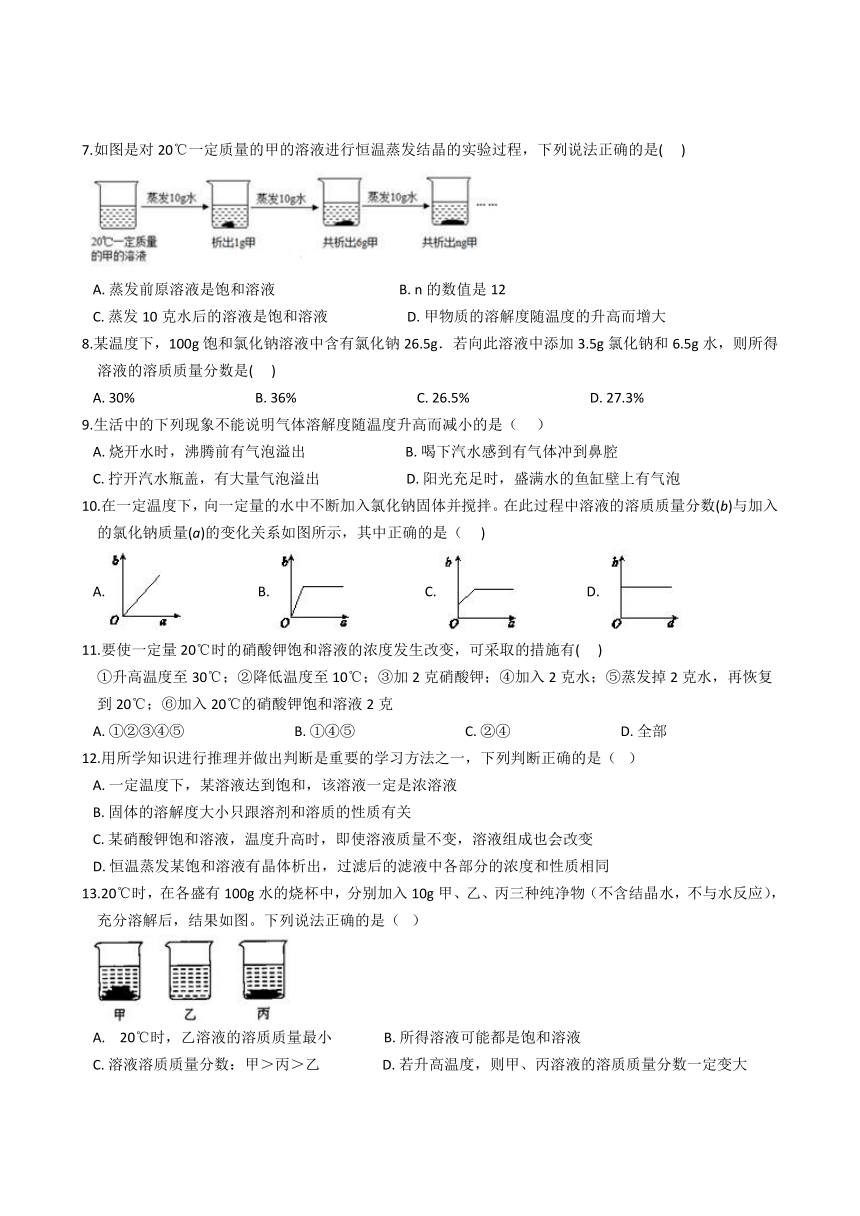
7.如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,下列说法正确的是(??? )
A.?蒸发前原溶液是饱和溶液????????????????????????????????????B.?n的数值是12 C.?蒸发10克水后的溶液是饱和溶液???????????????????????D.?甲物质的溶解度随温度的升高而增大
8.某温度下,100g饱和氯化钠溶液中含有氯化钠26.5g.若向此溶液中添加3.5g氯化钠和6.5g水,则所得溶液的溶质质量分数是(??? )
A.?30%???????????????????????????????????B.?36%???????????????????????????????????C.?26.5%???????????????????????????????????D.?27.3%
9.生活中的下列现象不能说明气体溶解度随温度升高而减小的是( ???)
A.?烧开水时,沸腾前有气泡溢出?????????????????????????????B.?喝下汽水感到有气体冲到鼻腔 C.?拧开汽水瓶盖,有大量气泡溢出?????????????????????????D.?阳光充足时,盛满水的鱼缸壁上有气泡
10.在一定温度下,向一定量的水中不断加入氯化钠固体并搅拌。在此过程中溶液的溶质质量分数(b)与加入的氯化钠质量(a)的变化关系如图所示,其中正确的是( ???)
A.???????????????????????B.???????????????????????C.?????????????????????D.?
11.要使一定量20℃时的硝酸钾饱和溶液的浓度发生改变,可采取的措施有(??? )
①升高温度至30℃;②降低温度至10℃;③加2克硝酸钾;④加入2克水;⑤蒸发掉2克水,再恢复到20℃;⑥加入20℃的硝酸钾饱和溶液2克
A.?①②③④⑤????????????????????????????????B.?①④⑤????????????????????????????????C.?②④????????????????????????????????D.?全部
12.用所学知识进行推理并做出判断是重要的学习方法之一,下列判断正确的是(? )
A.?一定温度下,某溶液达到饱和,该溶液一定是浓溶液 B.?固体的溶解度大小只跟溶剂和溶质的性质有关 C.?某硝酸钾饱和溶液,温度升高时,即使溶液质量不变,溶液组成也会改变 D.?恒温蒸发某饱和溶液有晶体析出,过滤后的滤液中各部分的浓度和性质相同
13.20℃时,在各盛有100g水的烧杯中,分别加入10g甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是(? )
A.?? 20℃时,乙溶液的溶质质量最小???????????????B.?所得溶液可能都是饱和溶液 C.?溶液溶质质量分数:甲>丙>乙??????????????????D.?若升高温度,则甲、丙溶液的溶质质量分数一定变大
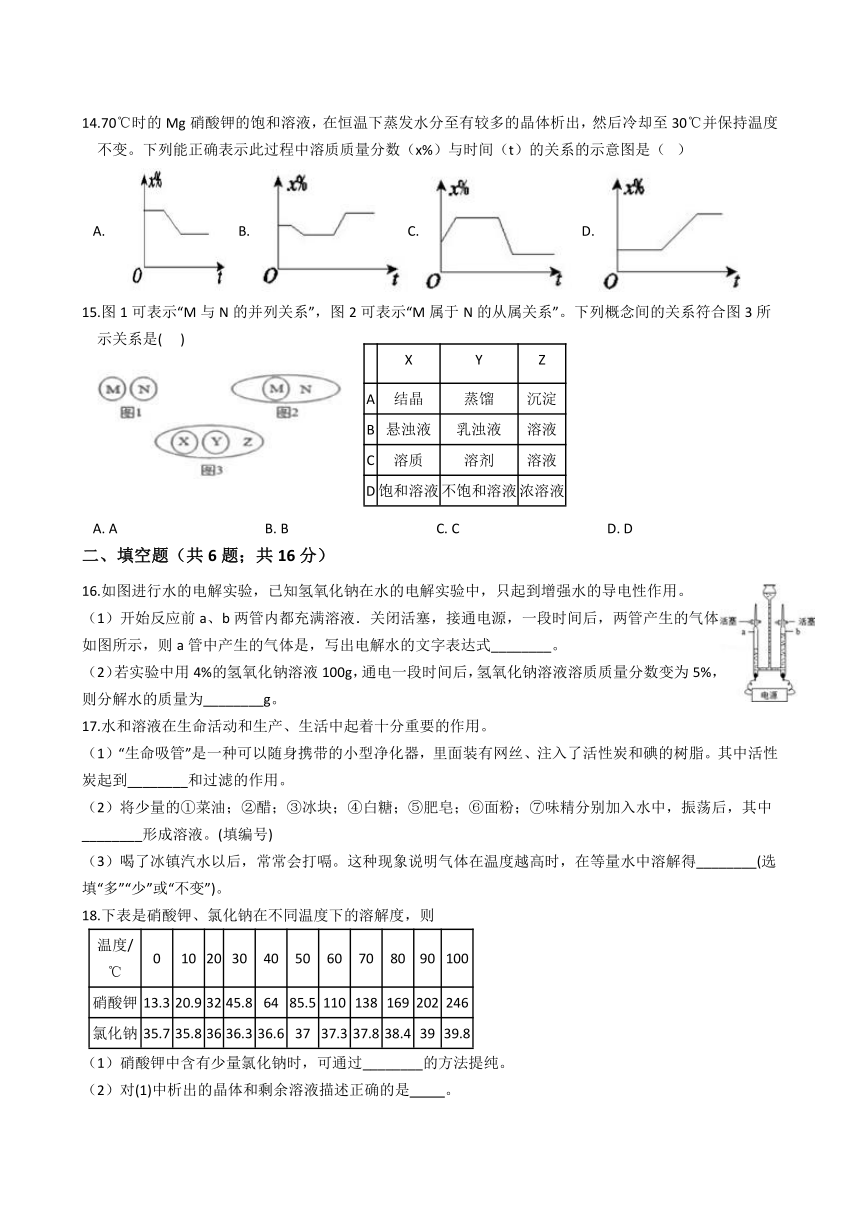
14.70℃时的Mg硝酸钾的饱和溶液,在恒温下蒸发水分至有较多的晶体析出,然后冷却至30℃并保持温度不变。下列能正确表示此过程中溶质质量分数(x%)与时间(t)的关系的示意图是(? )
A.?? ?B.?C.????D.?
X
Y
Z
A
结晶
蒸馏
沉淀
B
悬浊液
乳浊液
溶液
C
溶质
溶剂
溶液
D
饱和溶液
不饱和溶液
浓溶液
15.图1可表示“M与N的并列关系”,图2可表示“M属于N的从属关系”。下列概念间的关系符合图3所示关系是(??? )
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
二、填空题(共6题;共16分)
16.如图进行水的电解实验,已知氢氧化钠在水的电解实验中,只起到增强水的导电性作用。
(1)开始反应前a、b两管内都充满溶液.关闭活塞,接通电源,一段时间后,两管产生的气体如图所示,则a管中产生的气体是,写出电解水的文字表达式________。
(2)若实验中用4%的氢氧化钠溶液100g,通电一段时间后,氢氧化钠溶液溶质质量分数变为5%,则分解水的质量为________g。
17.水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)“生命吸管”是一种可以随身携带的小型净化器,里面装有网丝、注入了活性炭和碘的树脂。其中活性炭起到________和过滤的作用。
(2)将少量的①菜油;②醋;③冰块;④白糖;⑤肥皂;⑥面粉;⑦味精分别加入水中,振荡后,其中________形成溶液。(填编号)
(3)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体在温度越高时,在等量水中溶解得________(选填“多”“少”或“不变”)。
18.下表是硝酸钾、氯化钠在不同温度下的溶解度,则
温度/℃
0
10
20
30
40
50
60
70
80
90
100
硝酸钾
13.3
20.9
32
45.8
64
85.5
110
138
169
202
246
氯化钠
35.7
35.8
36
36.3
36.6
37
37.3
37.8
38.4
39
39.8
(1)硝酸钾中含有少量氯化钠时,可通过________的方法提纯。
(2)对(1)中析出的晶体和剩余溶液描述正确的是???????? 。
A.?剩余溶液一定是硝酸钾饱和溶液?????????????????????????B.?该过程溶液中硝酸钾的质量分数保持不变 C.?剩余的溶液一定是纯净物????????????????????????????????????D.?析出的晶体中只含有硝酸钾
(3)在一定温度下,将含69克硝酸钾、18克氯化钠的混合物完全溶解在50克水中。若要降低温度硝酸钾就开始析出,而氯化钠始终不能析出,则温度T(℃)的变化范围是________(硝酸钾和氯化钠溶解互不影响)。
19.某学生在一定温度下,向质量均为50g的四份水中分别加入一定质量的硝酸钾,搅拌至充分溶解(如有不溶的硝酸钾,则过滤除去),得到溶液.该学生在实验中记录数据如下
实验序号
实验1
实验2
实验3
实验4
水的质量(g)
50
50
50
50
加入硝酸钾的质量(g)
40
50
60
70
溶液的质量(g)
90
100
105
105
根据上述数据分析,实验??? ________(填实验序号)得到的溶液属于饱和溶液.该温度下硝酸钾的溶解度是________?克
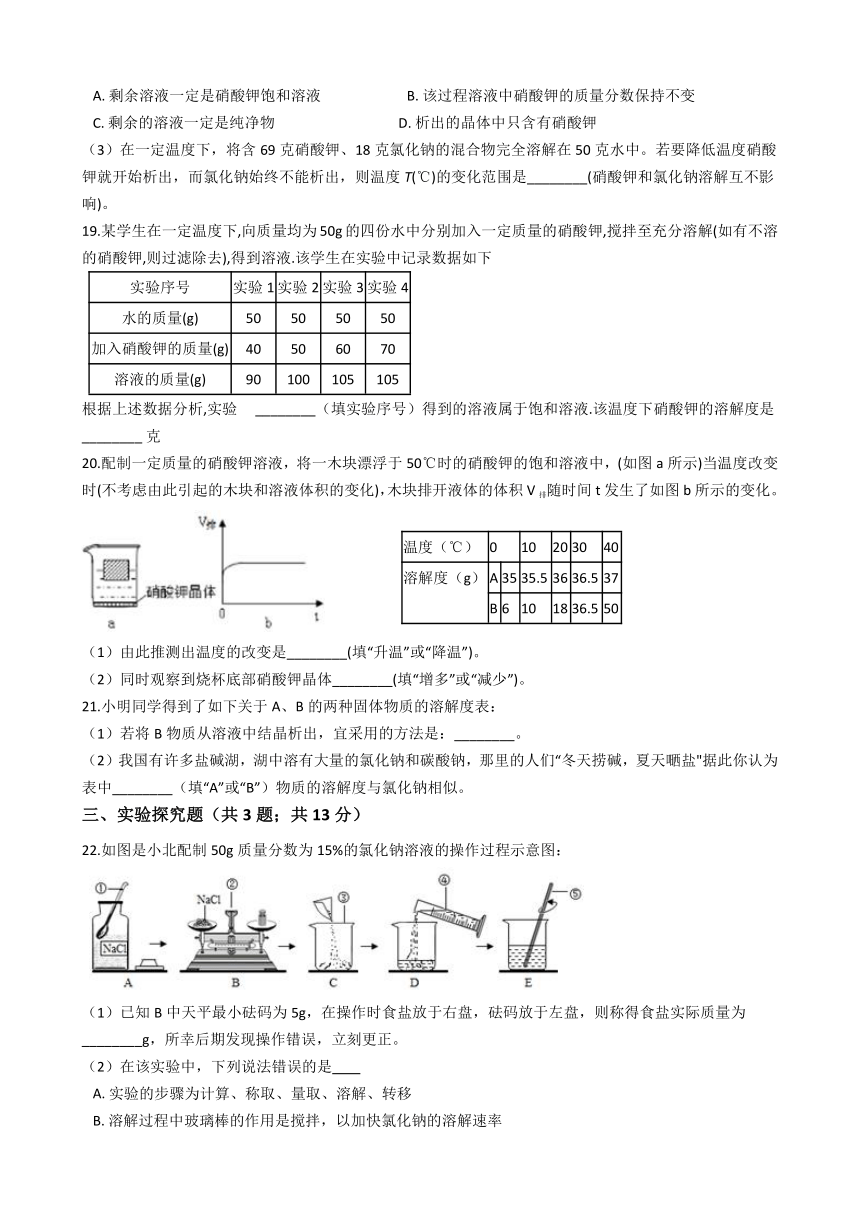
20.配制一定质量的硝酸钾溶液,将一木块漂浮于50℃时的硝酸钾的饱和溶液中,(如图a所示)当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积V排随时间t发生了如图b所示的变化。
温度(℃)
0
10
20
30
40
溶解度(g)
A
35
35.5
36
36.5
37
B
6
10
18
36.5
50
(1)由此推测出温度的改变是________(填“升温”或“降温”)。
(2)同时观察到烧杯底部硝酸钾晶体________(填“增多”或“减少”)。
21.小明同学得到了如下关于A、B的两种固体物质的溶解度表:
(1)若将B物质从溶液中结晶析出,宜采用的方法是:________。
(2)我国有许多盐碱湖,湖中溶有大量的氯化钠和碳酸钠,那里的人们“冬天捞碱,夏天嗮盐"据此你认为表中________(填“A”或“B”)物质的溶解度与氯化钠相似。
三、实验探究题(共3题;共13分)
22.如图是小北配制50g质量分数为15%的氯化钠溶液的操作过程示意图:
(1)已知B中天平最小砝码为5g,在操作时食盐放于右盘,砝码放于左盘,则称得食盐实际质量为________g,所幸后期发现操作错误,立刻更正。
(2)在该实验中,下列说法错误的是? ?????
A.?实验的步骤为计算、称取、量取、溶解、转移 B.?溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率 C.?把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签 D.?量取水时,用规格为50mL的量筒量取42.5mL蒸馏水
(3)如果配制过程中出现以下情况可能导致所配溶液的溶质质量分数偏大的是? ?????。
A.?所用氯化钠药品不纯???????????????????????????????????????????B.?量取水时俯视读数 C.?配完后将溶液转移至试剂瓶时洒出了一些???????????D.?量取水时仰视读数 E.?读数时,视线在游码偏右侧进行读数
(4)实验室若用15%的氯化钠溶液加水稀释成120g5%的氯化钠溶液,需要15%的氯化钠溶液________克,向其中加入________克水可配得5%的氯化钠溶液。
23.如图是实验室常用的一些仪器。
(1)根据以下实验要求,选择图中合适仪器,将对应的字母填在相应的横线上。
①用固体氯化钠配制50g溶质质量分数为10%的氯化钠溶液________;
②过滤粗盐水________。
(2)除了图中的仪器.(1)中的①、②两个实验都还要用到的一种仪器是________(填仪器名称)。
(3)若(1)中的①实验配制的氯化钠溶液溶质质量分数偏小,请你分析可能的原因是________(写一条即可)。
24.某科学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制一定质量分数的氯化钠溶液。
实验一:图1是同学们做粗盐提纯实验的操作示意图。请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是________。
(2)操作⑥中的错误是________。
(3)实验二:用提纯得到的精盐配制氯化钠溶液。小雪所取蒸馏水的体积如图3所示,则该实验小组原计划配制的氯化钠溶液中溶质的质量分数为________(水的密度约为1g/cm3)。进行正确实验后,经检测,所配制的溶液溶质质量分数偏小,其原因可能有________(填序号)。
①氯化钠固体仍然不纯? ?????????②烧杯先用少量蒸馏水润洗
③量取水时,仰视读数????? ?????④配好的溶液装瓶时,有少量溶液洒出
⑤量好的水倒入烧杯时,有少量水溅出
四、解答题(共3题;共33分)
25.硝酸钾在不同温度下的溶解度如下表所示:
温度/℃
0
10
20
30
40
50
溶解度/g
13.3
20.9
31.6
45.8
63.9
85.8
(1)分析表格可知,硝酸钾溶解度和温度的关系是________;
(2)30℃时,将12.5克硝酸钾加入到50克水中充分搅拌,求所得溶液的溶质质量分数;
(3)在温度不变时,能否将(2)中得到的溶液溶质质量分数增加一倍,请通过计算说明。
26.氯化钠俗名食盐是工业生产和生活的一种重要原料,也是实验室里常见的一种药品。下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题;
实验序号
水的质量(g)
加入氯化钠的质量(g)
溶液的质量(g)
①
10
2
12
②
10
3
13
③
10
4
13.6
④
10
5
m
(1)表中m=________;
(2)在这4次实验中,得到的是20℃氯化钠溶液属于饱和溶液的是________(填实验序号)
(3)计算第3次实验得到的氯化钠溶液的溶质质量分数。(写出过程)
(4)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?(写出过程)
27.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如下表所示。他从瓶中倒出100毫升用于配制稀硫酸。求:
浓硫酸(H2SO4)500mL
溶质的质量分数
98%
密度
1.84g/cm3
相对分子质量
98
强腐蚀性,阴冷、密封储藏
(1)这100毫升浓硫酸的质量是多少克?其中含溶质多少克?
(2)欲配制1000克质量分数为19.6%的稀硫酸,需要多少毫升这种浓硫酸?多少毫升水?
参考答案
一、选择题
1. D 2. C 3. C 4. A 5. A 6. C 7. C 8. C 9. C 10. B 11. C 12. D 13. B 14. A 15. C
二、填空题
16. (1)水 氢气+氧气(2)20
17. (1)吸附(2)②④⑦(3)少
18. (1)冷却热饱和溶液(2)A,D(3)70℃-20℃
19. 3、4;110
20. (1)降温(2)增多
21. (1)冷却热饱和溶液(2)A
三、实验探究题
22. (1)2.5g(2)C(3)B,E,G(4)40;80
23. (1)ACE;CD(2)玻璃棒(3)溶解时烧杯内壁有水珠(其他合理即可)
24. (1)加快溶解(2)没有用玻璃棒引流(3)19%;①②③
四、解答题
25. (1)硝酸钾溶解度随温度的升高而增大 (2)解:a%= ×100%=20%
答:所得溶液的溶质质量分数为20% (3)解:当温度为30℃时,在硝酸钾饱和溶液中
a%= ×100%=31.4%
∵31.4%<40%
∴不能将(2)中得到的溶液溶质质量分数增大一倍。
26. (1)13.6(2)③④3)第3次实验得到的氯化钠溶液的溶质质量分数为; (4)设释成5%的氯化钠溶液擀质量为x ?100×20% =5%x x=400g,所以所用水的质量为400g-100g=300g。
27. (1)100毫升浓硫酸的质量是:m=ρV=1.84g/cm3×100cm3=184g; 其中溶质的质量为:184g×98%=180.32g; (2)设需要98%的浓硫酸质量为x, 1000g×19.6%= x×98%; 解得:x=200g; 需要这种浓硫酸的体积:108.7g; 需要加水的质量:1000g-200g=800g; 需要加水的体积:。
一、选择题(共15题;共30分)
1.科学家用石墨烯膜制成"筛子",可以筛掉盐类物质.当海水流过该膜时,钠离子和氯离子被水分子包裹而不能通过,独立的水分子却能通过(如图).下列关于石墨烯膜“筛掉”氯化钠的说法错误的是( ???)
A.?该过程属于物理变化????????????????????????????????????????B.?该过程可应用于海水淡化 C.?“筛掉”氯化钠过程类似于过滤操作????????????????? D.?“筛掉”氯化钠后的海水溶质质量分数增大
第1题图 第2题图
2.在t℃时,某物质X、Y分别完全溶于水,溶液中X、Y与水的质量关系分别如图a、图b所示。下列说法正确的是( ???)
A.?X、Y都只能是固体??????????????????????????????????????????????B.?两种溶液一定是饱和溶液 C.?图示溶液的浓度:X
A.?把溶剂蒸发掉一半???????B.?加入6g食盐晶体???????C.?把溶剂蒸发掉30g???????D.?加入20%的食盐溶液30g
4.下列关于结晶和晶体的说法,正确的是(??? )
A.?饱和溶液降温析出晶体后的溶液仍然是饱和溶液?????B.?降低饱和溶液的温度一定有晶体析出 C.?从溶液中析出的晶体一定有结晶水??????????????????????????D.?把溶液的溶剂蒸发一些一定会有晶体析出
5.配制硝酸钾饱和溶液时得到下表数据,根据表中数据分析,不正确的是(??? )
序号
温度/℃
水的质量/g
所加硝酸钾的质量/g
所得溶液的质量/g
①
28
10
4
14
②
28
10
6
14
③
60
10
8
18
A.?60℃时10克水中最多能溶解硝酸钾8克???????????B.?60℃时等质量水中能溶解的硝酸钾比28℃时多 C.?①②所得溶液溶质的质量分数相等??????????????????? D.?③所得溶液不一定是硝酸钾的饱和溶液
6.硫酸镁在工农业以及医疗上有广泛应用,其溶解度如表所示.则下列说法正确的是(??? )
温度/℃
10
30
50
70
90
溶解度/g
27.7
39.3
49.0
54.1
51.1
A.?硫酸镁的溶解度随温度升高而减小 B.?10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液 C.?50℃时,100g硫酸镁饱和溶液中溶质和溶剂的质量比为49:100 D.?70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数不变
7.如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,下列说法正确的是(??? )
A.?蒸发前原溶液是饱和溶液????????????????????????????????????B.?n的数值是12 C.?蒸发10克水后的溶液是饱和溶液???????????????????????D.?甲物质的溶解度随温度的升高而增大
8.某温度下,100g饱和氯化钠溶液中含有氯化钠26.5g.若向此溶液中添加3.5g氯化钠和6.5g水,则所得溶液的溶质质量分数是(??? )
A.?30%???????????????????????????????????B.?36%???????????????????????????????????C.?26.5%???????????????????????????????????D.?27.3%
9.生活中的下列现象不能说明气体溶解度随温度升高而减小的是( ???)
A.?烧开水时,沸腾前有气泡溢出?????????????????????????????B.?喝下汽水感到有气体冲到鼻腔 C.?拧开汽水瓶盖,有大量气泡溢出?????????????????????????D.?阳光充足时,盛满水的鱼缸壁上有气泡
10.在一定温度下,向一定量的水中不断加入氯化钠固体并搅拌。在此过程中溶液的溶质质量分数(b)与加入的氯化钠质量(a)的变化关系如图所示,其中正确的是( ???)
A.???????????????????????B.???????????????????????C.?????????????????????D.?
11.要使一定量20℃时的硝酸钾饱和溶液的浓度发生改变,可采取的措施有(??? )
①升高温度至30℃;②降低温度至10℃;③加2克硝酸钾;④加入2克水;⑤蒸发掉2克水,再恢复到20℃;⑥加入20℃的硝酸钾饱和溶液2克
A.?①②③④⑤????????????????????????????????B.?①④⑤????????????????????????????????C.?②④????????????????????????????????D.?全部
12.用所学知识进行推理并做出判断是重要的学习方法之一,下列判断正确的是(? )
A.?一定温度下,某溶液达到饱和,该溶液一定是浓溶液 B.?固体的溶解度大小只跟溶剂和溶质的性质有关 C.?某硝酸钾饱和溶液,温度升高时,即使溶液质量不变,溶液组成也会改变 D.?恒温蒸发某饱和溶液有晶体析出,过滤后的滤液中各部分的浓度和性质相同
13.20℃时,在各盛有100g水的烧杯中,分别加入10g甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是(? )
A.?? 20℃时,乙溶液的溶质质量最小???????????????B.?所得溶液可能都是饱和溶液 C.?溶液溶质质量分数:甲>丙>乙??????????????????D.?若升高温度,则甲、丙溶液的溶质质量分数一定变大
14.70℃时的Mg硝酸钾的饱和溶液,在恒温下蒸发水分至有较多的晶体析出,然后冷却至30℃并保持温度不变。下列能正确表示此过程中溶质质量分数(x%)与时间(t)的关系的示意图是(? )
A.?? ?B.?C.????D.?
X
Y
Z
A
结晶
蒸馏
沉淀
B
悬浊液
乳浊液
溶液
C
溶质
溶剂
溶液
D
饱和溶液
不饱和溶液
浓溶液
15.图1可表示“M与N的并列关系”,图2可表示“M属于N的从属关系”。下列概念间的关系符合图3所示关系是(??? )
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
二、填空题(共6题;共16分)
16.如图进行水的电解实验,已知氢氧化钠在水的电解实验中,只起到增强水的导电性作用。
(1)开始反应前a、b两管内都充满溶液.关闭活塞,接通电源,一段时间后,两管产生的气体如图所示,则a管中产生的气体是,写出电解水的文字表达式________。
(2)若实验中用4%的氢氧化钠溶液100g,通电一段时间后,氢氧化钠溶液溶质质量分数变为5%,则分解水的质量为________g。
17.水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)“生命吸管”是一种可以随身携带的小型净化器,里面装有网丝、注入了活性炭和碘的树脂。其中活性炭起到________和过滤的作用。
(2)将少量的①菜油;②醋;③冰块;④白糖;⑤肥皂;⑥面粉;⑦味精分别加入水中,振荡后,其中________形成溶液。(填编号)
(3)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体在温度越高时,在等量水中溶解得________(选填“多”“少”或“不变”)。
18.下表是硝酸钾、氯化钠在不同温度下的溶解度,则
温度/℃
0
10
20
30
40
50
60
70
80
90
100
硝酸钾
13.3
20.9
32
45.8
64
85.5
110
138
169
202
246
氯化钠
35.7
35.8
36
36.3
36.6
37
37.3
37.8
38.4
39
39.8
(1)硝酸钾中含有少量氯化钠时,可通过________的方法提纯。
(2)对(1)中析出的晶体和剩余溶液描述正确的是???????? 。
A.?剩余溶液一定是硝酸钾饱和溶液?????????????????????????B.?该过程溶液中硝酸钾的质量分数保持不变 C.?剩余的溶液一定是纯净物????????????????????????????????????D.?析出的晶体中只含有硝酸钾
(3)在一定温度下,将含69克硝酸钾、18克氯化钠的混合物完全溶解在50克水中。若要降低温度硝酸钾就开始析出,而氯化钠始终不能析出,则温度T(℃)的变化范围是________(硝酸钾和氯化钠溶解互不影响)。
19.某学生在一定温度下,向质量均为50g的四份水中分别加入一定质量的硝酸钾,搅拌至充分溶解(如有不溶的硝酸钾,则过滤除去),得到溶液.该学生在实验中记录数据如下
实验序号
实验1
实验2
实验3
实验4
水的质量(g)
50
50
50
50
加入硝酸钾的质量(g)
40
50
60
70
溶液的质量(g)
90
100
105
105
根据上述数据分析,实验??? ________(填实验序号)得到的溶液属于饱和溶液.该温度下硝酸钾的溶解度是________?克
20.配制一定质量的硝酸钾溶液,将一木块漂浮于50℃时的硝酸钾的饱和溶液中,(如图a所示)当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积V排随时间t发生了如图b所示的变化。
温度(℃)
0
10
20
30
40
溶解度(g)
A
35
35.5
36
36.5
37
B
6
10
18
36.5
50
(1)由此推测出温度的改变是________(填“升温”或“降温”)。
(2)同时观察到烧杯底部硝酸钾晶体________(填“增多”或“减少”)。
21.小明同学得到了如下关于A、B的两种固体物质的溶解度表:
(1)若将B物质从溶液中结晶析出,宜采用的方法是:________。
(2)我国有许多盐碱湖,湖中溶有大量的氯化钠和碳酸钠,那里的人们“冬天捞碱,夏天嗮盐"据此你认为表中________(填“A”或“B”)物质的溶解度与氯化钠相似。
三、实验探究题(共3题;共13分)
22.如图是小北配制50g质量分数为15%的氯化钠溶液的操作过程示意图:
(1)已知B中天平最小砝码为5g,在操作时食盐放于右盘,砝码放于左盘,则称得食盐实际质量为________g,所幸后期发现操作错误,立刻更正。
(2)在该实验中,下列说法错误的是? ?????
A.?实验的步骤为计算、称取、量取、溶解、转移 B.?溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率 C.?把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签 D.?量取水时,用规格为50mL的量筒量取42.5mL蒸馏水
(3)如果配制过程中出现以下情况可能导致所配溶液的溶质质量分数偏大的是? ?????。
A.?所用氯化钠药品不纯???????????????????????????????????????????B.?量取水时俯视读数 C.?配完后将溶液转移至试剂瓶时洒出了一些???????????D.?量取水时仰视读数 E.?读数时,视线在游码偏右侧进行读数
(4)实验室若用15%的氯化钠溶液加水稀释成120g5%的氯化钠溶液,需要15%的氯化钠溶液________克,向其中加入________克水可配得5%的氯化钠溶液。
23.如图是实验室常用的一些仪器。
(1)根据以下实验要求,选择图中合适仪器,将对应的字母填在相应的横线上。
①用固体氯化钠配制50g溶质质量分数为10%的氯化钠溶液________;
②过滤粗盐水________。
(2)除了图中的仪器.(1)中的①、②两个实验都还要用到的一种仪器是________(填仪器名称)。
(3)若(1)中的①实验配制的氯化钠溶液溶质质量分数偏小,请你分析可能的原因是________(写一条即可)。
24.某科学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制一定质量分数的氯化钠溶液。
实验一:图1是同学们做粗盐提纯实验的操作示意图。请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是________。
(2)操作⑥中的错误是________。
(3)实验二:用提纯得到的精盐配制氯化钠溶液。小雪所取蒸馏水的体积如图3所示,则该实验小组原计划配制的氯化钠溶液中溶质的质量分数为________(水的密度约为1g/cm3)。进行正确实验后,经检测,所配制的溶液溶质质量分数偏小,其原因可能有________(填序号)。
①氯化钠固体仍然不纯? ?????????②烧杯先用少量蒸馏水润洗
③量取水时,仰视读数????? ?????④配好的溶液装瓶时,有少量溶液洒出
⑤量好的水倒入烧杯时,有少量水溅出
四、解答题(共3题;共33分)
25.硝酸钾在不同温度下的溶解度如下表所示:
温度/℃
0
10
20
30
40
50
溶解度/g
13.3
20.9
31.6
45.8
63.9
85.8
(1)分析表格可知,硝酸钾溶解度和温度的关系是________;
(2)30℃时,将12.5克硝酸钾加入到50克水中充分搅拌,求所得溶液的溶质质量分数;
(3)在温度不变时,能否将(2)中得到的溶液溶质质量分数增加一倍,请通过计算说明。
26.氯化钠俗名食盐是工业生产和生活的一种重要原料,也是实验室里常见的一种药品。下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题;
实验序号
水的质量(g)
加入氯化钠的质量(g)
溶液的质量(g)
①
10
2
12
②
10
3
13
③
10
4
13.6
④
10
5
m
(1)表中m=________;
(2)在这4次实验中,得到的是20℃氯化钠溶液属于饱和溶液的是________(填实验序号)
(3)计算第3次实验得到的氯化钠溶液的溶质质量分数。(写出过程)
(4)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?(写出过程)
27.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如下表所示。他从瓶中倒出100毫升用于配制稀硫酸。求:
浓硫酸(H2SO4)500mL
溶质的质量分数
98%
密度
1.84g/cm3
相对分子质量
98
强腐蚀性,阴冷、密封储藏
(1)这100毫升浓硫酸的质量是多少克?其中含溶质多少克?
(2)欲配制1000克质量分数为19.6%的稀硫酸,需要多少毫升这种浓硫酸?多少毫升水?
参考答案
一、选择题
1. D 2. C 3. C 4. A 5. A 6. C 7. C 8. C 9. C 10. B 11. C 12. D 13. B 14. A 15. C
二、填空题
16. (1)水 氢气+氧气(2)20
17. (1)吸附(2)②④⑦(3)少
18. (1)冷却热饱和溶液(2)A,D(3)70℃-20℃
19. 3、4;110
20. (1)降温(2)增多
21. (1)冷却热饱和溶液(2)A
三、实验探究题
22. (1)2.5g(2)C(3)B,E,G(4)40;80
23. (1)ACE;CD(2)玻璃棒(3)溶解时烧杯内壁有水珠(其他合理即可)
24. (1)加快溶解(2)没有用玻璃棒引流(3)19%;①②③
四、解答题
25. (1)硝酸钾溶解度随温度的升高而增大 (2)解:a%= ×100%=20%
答:所得溶液的溶质质量分数为20% (3)解:当温度为30℃时,在硝酸钾饱和溶液中
a%= ×100%=31.4%
∵31.4%<40%
∴不能将(2)中得到的溶液溶质质量分数增大一倍。
26. (1)13.6(2)③④3)第3次实验得到的氯化钠溶液的溶质质量分数为; (4)设释成5%的氯化钠溶液擀质量为x ?100×20% =5%x x=400g,所以所用水的质量为400g-100g=300g。
27. (1)100毫升浓硫酸的质量是:m=ρV=1.84g/cm3×100cm3=184g; 其中溶质的质量为:184g×98%=180.32g; (2)设需要98%的浓硫酸质量为x, 1000g×19.6%= x×98%; 解得:x=200g; 需要这种浓硫酸的体积:108.7g; 需要加水的质量:1000g-200g=800g; 需要加水的体积:。
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
