课题 2 金属的化学性质(第1课时)(共20张PPT)
文档属性
| 名称 | 课题 2 金属的化学性质(第1课时)(共20张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 3.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-08 10:04:56 | ||
图片预览








文档简介
(共20张PPT)
课 题 2 金属的化学性质
第 八 单 元 金属和金属材料
第 1 课时
第八单元 金属和金属材料
1.知道铁、铝、铜等常见金属与氧气的反应。
2.知道常见金属能与盐酸、稀硫酸发生化学反应,并能解释一些与日常生活有关的化学问题。
3.初步认识置换反应的概念,能够判断常见的化学反应是否属于置换反应。
学 习 目 标
自 主 探 究
为什么出土的文物里,金器保存的基本完好,铜器表面有锈迹,而铁器却锈迹斑斑?
东周鹿型金怪兽
东汉晚期青铜奔马
春秋金柄铁剑
一、金属与氧气的反应
〖思考〗说出镁在空气中燃烧的现象和铁在氧气中燃烧
的现象,写出反应的化学方程式。
〖思考〗请同学们阅读教材第9页,回答为什么铝具有
良好的抗腐蚀性?能否用钢刷去刷洗铝锅呢?写出反应
的化学方程式。
铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化,铝具有很好的抗腐蚀性能。
若用钢刷擦洗铝制品,容易把氧化薄膜除掉,从而起不到保护作用。
〖实验〗用坩埚钳夹持铜片在酒精灯上加热。仔细观察
金属表面的变化。
现象
化学方程式
铜片由紫红色变成黑色
真金不怕火炼
金即使在高温条件下也不与氧气反应
结论:大多数金属能与氧气反应,但是反应的难易和剧烈程度不同。
应用:判断金属活动性的方法一
活动性:镁、铝>铁、铜>金
二、金属与盐酸、稀硫酸的反应
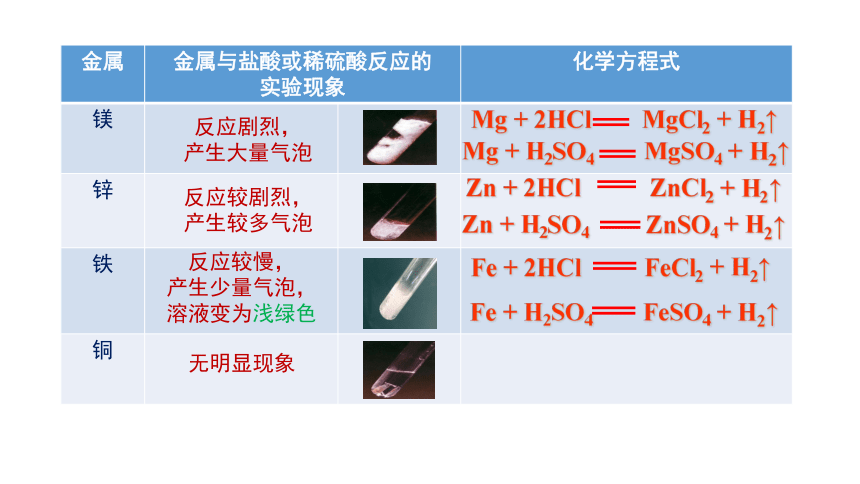
〖探究〗试管中分别放有镁条、锌粒、铁钉、铜片,分别向其中加入少量盐酸(或稀硫酸),观察现象,比较反应的剧烈程度。
金属 金属与盐酸或稀硫酸反应的
实验现象 化学方程式
镁
锌
铁
铜
无明显现象
反应较慢,
产生少量气泡,
溶液变为浅绿色
反应较剧烈,
产生较多气泡
反应剧烈,
产生大量气泡
Mg + 2HCl MgCl2 + H2↑
Mg + H2SO4 MgSO4 + H2↑
Zn + 2HCl ZnCl2 + H2↑
Zn + H2SO4 ZnSO4 + H2↑
Fe + 2HCl FeCl2 + H2↑
Fe + H2SO4 FeSO4 + H2↑
盐酸
金属与盐酸的反应
结论:很多金属能与盐酸或稀硫酸反应,但是反应的剧烈程度不同。
应用:判断金属活动性的方法二,根据金属与盐酸或稀硫酸能否反应以及反应的剧烈程度判断金属活动性
活动性:镁>锌>铁>铜
(1)为什么实验室常用锌和稀硫酸反应制氢气?
〖讨论〗
锌与酸反应速率适中,镁反应快,铁反应较慢。
盐酸具有挥发性,硫酸不挥发。
(2)为什么用铁锅炒菜时常加入食醋?
〖讨论〗
铁锅炒菜时加入食醋(含有醋酸),铁能与醋酸反应,增加食物中的含铁量,为人体补充铁元素。
(3)请大家从反应物和生成物的物质类别的角度分析,金属与盐酸、稀硫酸的反应有什么特点?
〖讨论〗
置换反应:一种单质和一种化合物反应,生成另一种单质和另一化合物的反应
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
1.把一支洁净的铁钉放入稀硫酸中,下列说法错误的是( )
A.铁钉表面产生气泡 B.溶液由无色变成浅绿色
C.铁钉质量变轻 D.液体质量变轻
2.下列关于金属与氧气反应的观点中不正确的是( )
A.大多数金属都能与氧气反应?????????
B.镁在点燃时能与空气中的氧气反应
C.“真金不怕火炼”说明金即使在高温下也不与氧气反应?????????????
D.铁在氧气中燃烧生成氧化铁
D
D
课 堂 达 标
3.下列各组物质,由金属跟同一种稀酸直接作用生成的是( )
A.ZnCl2 和ZnSO4 B. ZnSO4和 FeSO4
C.FeCl2 和 FeCl3 D. ZnSO4 和 CuSO4
4.生铁和足量的稀盐酸充分反应后,总会有一些残渣剩余,残渣的成分主要是( )
A.铁 B.氯化铁 C.氯化亚铁 D.碳
B
D
C
5.为了适应火车提速,我国铁路线上的短轨(25m)已经链接为长轨,一方面火车得到了提速,另一方面降低了火车经过时的噪音。铁路部门的技术工人用下列反应焊接原钢轨间的缝隙:
该反应的基本类型是( )
A.分解反应 B.化合反应 C.置换反应
2Al+Fe2O3 2Fe +Al2O3
高温
6、黄金是一种贵重金属,在人类漫长的历史中,素有“沙里淘金”“真金不怕火炼”之说。 这说明黄金在自然界中主要是以 (填“单质”或“化合物”)形式存在,也说明黄金的化学性质在自然条件下化学性质非常 。
7、铝的金属活动性比较强,但铝制品却比较耐用,请用化学方程式解释原因。
单质
稳定
序号 实验过程 实验现象
1 镁粉和铁粉分别与 5% 盐酸反应 镁粉产生气体快?
2? 铁粉和铁片分别与 10%盐酸反应? 铁粉产生气体快
3? 铁片分别与 5% 盐酸和10% 盐酸反应? 10%盐酸产生气体快?
8.为了探究影响金属与酸反应剧烈程度的因素,进行了以下实验:
因素一: ;
因素二: ;
因素三: 。
金属活动性强弱
金属颗粒的大小(或反应物接触面积的大小)
酸溶液中溶质的质量分数(或酸溶液的浓度)
由此得出影响金属与酸反应剧烈程度的因素有:
再见
课 题 2 金属的化学性质
第 八 单 元 金属和金属材料
第 1 课时
第八单元 金属和金属材料
1.知道铁、铝、铜等常见金属与氧气的反应。
2.知道常见金属能与盐酸、稀硫酸发生化学反应,并能解释一些与日常生活有关的化学问题。
3.初步认识置换反应的概念,能够判断常见的化学反应是否属于置换反应。
学 习 目 标
自 主 探 究
为什么出土的文物里,金器保存的基本完好,铜器表面有锈迹,而铁器却锈迹斑斑?
东周鹿型金怪兽
东汉晚期青铜奔马
春秋金柄铁剑
一、金属与氧气的反应
〖思考〗说出镁在空气中燃烧的现象和铁在氧气中燃烧
的现象,写出反应的化学方程式。
〖思考〗请同学们阅读教材第9页,回答为什么铝具有
良好的抗腐蚀性?能否用钢刷去刷洗铝锅呢?写出反应
的化学方程式。
铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化,铝具有很好的抗腐蚀性能。
若用钢刷擦洗铝制品,容易把氧化薄膜除掉,从而起不到保护作用。
〖实验〗用坩埚钳夹持铜片在酒精灯上加热。仔细观察
金属表面的变化。
现象
化学方程式
铜片由紫红色变成黑色
真金不怕火炼
金即使在高温条件下也不与氧气反应
结论:大多数金属能与氧气反应,但是反应的难易和剧烈程度不同。
应用:判断金属活动性的方法一
活动性:镁、铝>铁、铜>金
二、金属与盐酸、稀硫酸的反应
〖探究〗试管中分别放有镁条、锌粒、铁钉、铜片,分别向其中加入少量盐酸(或稀硫酸),观察现象,比较反应的剧烈程度。
金属 金属与盐酸或稀硫酸反应的
实验现象 化学方程式
镁
锌
铁
铜
无明显现象
反应较慢,
产生少量气泡,
溶液变为浅绿色
反应较剧烈,
产生较多气泡
反应剧烈,
产生大量气泡
Mg + 2HCl MgCl2 + H2↑
Mg + H2SO4 MgSO4 + H2↑
Zn + 2HCl ZnCl2 + H2↑
Zn + H2SO4 ZnSO4 + H2↑
Fe + 2HCl FeCl2 + H2↑
Fe + H2SO4 FeSO4 + H2↑
盐酸
金属与盐酸的反应
结论:很多金属能与盐酸或稀硫酸反应,但是反应的剧烈程度不同。
应用:判断金属活动性的方法二,根据金属与盐酸或稀硫酸能否反应以及反应的剧烈程度判断金属活动性
活动性:镁>锌>铁>铜
(1)为什么实验室常用锌和稀硫酸反应制氢气?
〖讨论〗
锌与酸反应速率适中,镁反应快,铁反应较慢。
盐酸具有挥发性,硫酸不挥发。
(2)为什么用铁锅炒菜时常加入食醋?
〖讨论〗
铁锅炒菜时加入食醋(含有醋酸),铁能与醋酸反应,增加食物中的含铁量,为人体补充铁元素。
(3)请大家从反应物和生成物的物质类别的角度分析,金属与盐酸、稀硫酸的反应有什么特点?
〖讨论〗
置换反应:一种单质和一种化合物反应,生成另一种单质和另一化合物的反应
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
1.把一支洁净的铁钉放入稀硫酸中,下列说法错误的是( )
A.铁钉表面产生气泡 B.溶液由无色变成浅绿色
C.铁钉质量变轻 D.液体质量变轻
2.下列关于金属与氧气反应的观点中不正确的是( )
A.大多数金属都能与氧气反应?????????
B.镁在点燃时能与空气中的氧气反应
C.“真金不怕火炼”说明金即使在高温下也不与氧气反应?????????????
D.铁在氧气中燃烧生成氧化铁
D
D
课 堂 达 标
3.下列各组物质,由金属跟同一种稀酸直接作用生成的是( )
A.ZnCl2 和ZnSO4 B. ZnSO4和 FeSO4
C.FeCl2 和 FeCl3 D. ZnSO4 和 CuSO4
4.生铁和足量的稀盐酸充分反应后,总会有一些残渣剩余,残渣的成分主要是( )
A.铁 B.氯化铁 C.氯化亚铁 D.碳
B
D
C
5.为了适应火车提速,我国铁路线上的短轨(25m)已经链接为长轨,一方面火车得到了提速,另一方面降低了火车经过时的噪音。铁路部门的技术工人用下列反应焊接原钢轨间的缝隙:
该反应的基本类型是( )
A.分解反应 B.化合反应 C.置换反应
2Al+Fe2O3 2Fe +Al2O3
高温
6、黄金是一种贵重金属,在人类漫长的历史中,素有“沙里淘金”“真金不怕火炼”之说。 这说明黄金在自然界中主要是以 (填“单质”或“化合物”)形式存在,也说明黄金的化学性质在自然条件下化学性质非常 。
7、铝的金属活动性比较强,但铝制品却比较耐用,请用化学方程式解释原因。
单质
稳定
序号 实验过程 实验现象
1 镁粉和铁粉分别与 5% 盐酸反应 镁粉产生气体快?
2? 铁粉和铁片分别与 10%盐酸反应? 铁粉产生气体快
3? 铁片分别与 5% 盐酸和10% 盐酸反应? 10%盐酸产生气体快?
8.为了探究影响金属与酸反应剧烈程度的因素,进行了以下实验:
因素一: ;
因素二: ;
因素三: 。
金属活动性强弱
金属颗粒的大小(或反应物接触面积的大小)
酸溶液中溶质的质量分数(或酸溶液的浓度)
由此得出影响金属与酸反应剧烈程度的因素有:
再见
同课章节目录
