上海市2020届浦东新区九年级第一学期期末考试暨中考化学一模试卷(PDF)
文档属性
| 名称 | 上海市2020届浦东新区九年级第一学期期末考试暨中考化学一模试卷(PDF) |

|
|
| 格式 | zip | ||
| 文件大小 | 493.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-08 00:00:00 | ||
图片预览


文档简介
第 1 页 / 共 7 页
浦东新区 2019 学年第一学期初中学业质量监测
初三理化 试卷
化学部分
相对原子质量:H-1 C-12 O-16 Ca-40 Cu-64
六、选择题
27. 地壳中含量最多的元素是( )
A. O B. Si C. Al D. Fe
28. 属于物理变化的是( )
A.蜡烛燃烧 B. 火药爆炸 C. 粮食酿酒 D. 海水晒盐
29. 属于纯净物的是( )
A. 石灰水 B. 蒸馏水 C. 大理石 D. 稀盐酸
30. 属于浊液的是( )
A. 糖水 B. 泥水 C. 盐水 D. 汽水
31. 表示 2 个氢分子的是( )
A. H2 B. 2H C. 2H2 D. 2H2O
32. 硫在氧气中燃烧的现象是( )
A. 发出白光 B. 淡蓝色火焰 C. 产生白烟 D. 蓝紫色火焰
33. 取用固体药品的正确操作是( )
34. 铕(Eu)是有“工业维生素”美誉的稀土元素,Eu2O3 中铕元素的化合价为( )
A. +1 B. +2 C. +3 D. +4
35. 不属于碳元素同素异形体的是( )
A. C60 B. 金刚石 C. 石墨 D. 二氧化碳
36. 正确的化学用语是( )
A. 碳酸根:CO3 B. 汞原子:Ag C. 氧化铁:FeO D. 胆矾:CuSO4
第 2 页 / 共 7 页
37.“酒精温度计遇热液面上升”的微观解释是( )
A. 分子质量增大 B. 分子间隔增大 C. 分子体积增大 D. 分子个数增多
38. 水是生命之源,关于水的说法正确的是( )
A. 水是最常见的溶剂 B. 实验室废液不经处理直接排放
C. 水变成冰体积减小 D. 明矾在净水过程中起消毒作用
39. 有关空气的说法错误的是( )
A. 氮气约占空气体积的 78% B. 空气质量指数反映空气质量状况
C. 空气中二氧化碳会造成酸雨 D. 分离液态空气可用于工业制氧气
40. 有关燃烧和灭火的说法正确的是( )
A. 可燃物在空气中才能燃烧 B. 煤炭粉碎能使燃烧更充分
C. 降低可燃物着火点可灭火 D. 天然气燃烧符合“低碳”理念
41. 过氧乙酸(C2H4O3)是常用的消毒剂,有关过氧乙酸说法正确的是( )
A. 摩尔质量为 76g B. 碳、氢、氧元素的质量比为 2:4:3
C. 一个分子中有 9 个原子 D. 0.1mol 过氧乙酸中约含 6.02×1023个分子
42. 已知:2KClO3 2
MnO
?
???→ 2KCl+3O2?,有关说法错误的是( )
A. 属于分解反应
B. 钾元素的存在形态不变
C. 从化学方程式可知氧气是无色的
D. MnO2和 KCl 的混合物可通过溶解、过滤分离
43. 化学基本观念说法错误的是( )
A. 微粒观:金刚石由分子构成 B. 转化观:二氧化碳可转化为碳酸
C. 元素观:氧气由氧元素组成 D. 守恒观:化学反应前后元素种类不变
44. 硝酸钾溶解度曲线如图Ⅱ所示,图Ⅰ中“操作 X”前后溶液状态变化过程可以在图Ⅱ中表示为( )
A. b 点→a 点 B. c 点→a 点 C. c 点→b 点 D. c 点→d 点
45. 一个碳原子的质量为 mg,一个氧原子的质量为 ng,氧的相对原子质量可表示为( )
A.
12n
m
B.
12
m
n
C.
16n
m
D.
16
m
n
第 3 页 / 共 7 页
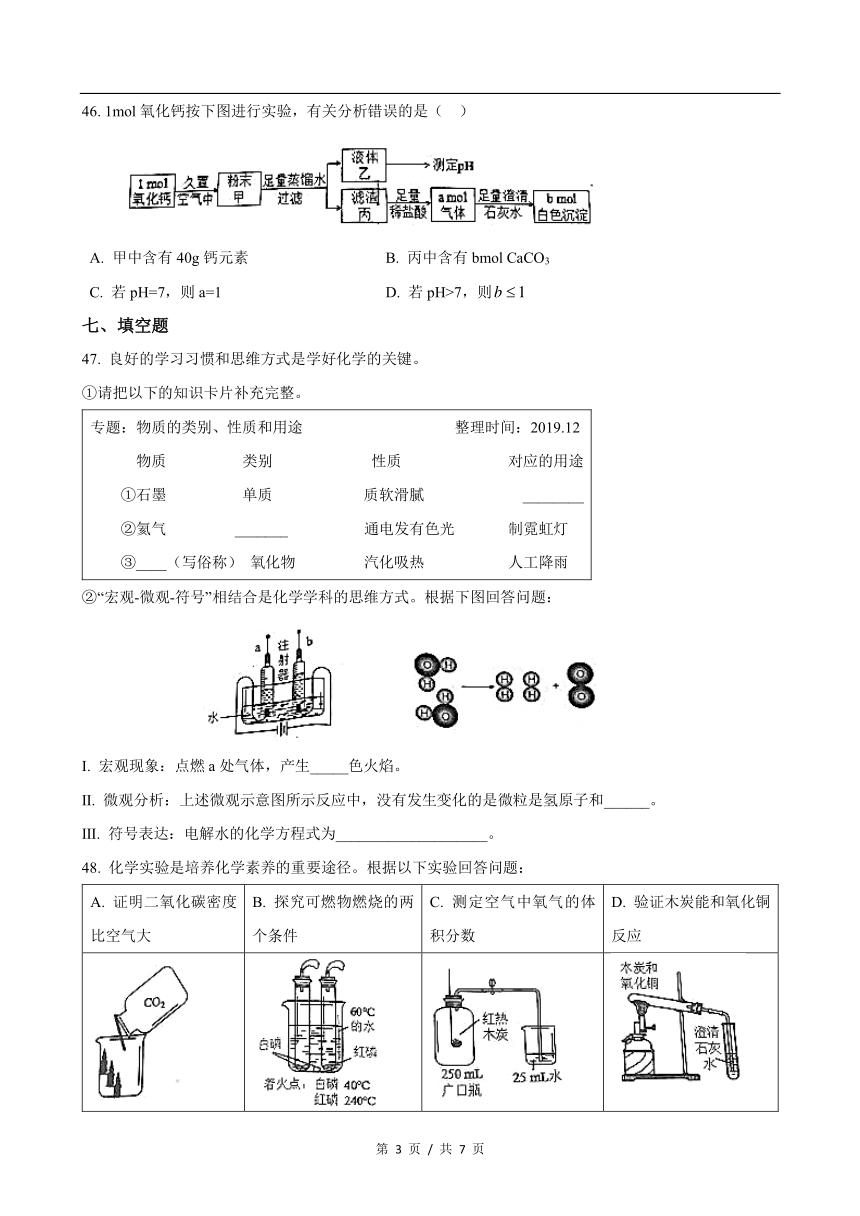
46. 1mol 氧化钙按下图进行实验,有关分析错误的是( )
A. 甲中含有 40g 钙元素 B. 丙中含有 bmol CaCO3
C. 若 pH=7,则 a=1 D. 若 pH>7,则 1b ?
七、填空题
47. 良好的学习习惯和思维方式是学好化学的关键。
①请把以下的知识卡片补充完整。
专题:物质的类别、性质和用途 整理时间:2019.12
物质 类别 性质 对应的用途
①石墨 单质 质软滑腻 ________
②氦气 _______ 通电发有色光 制霓虹灯
③____(写俗称) 氧化物 汽化吸热 人工降雨
②“宏观-微观-符号”相结合是化学学科的思维方式。根据下图回答问题:
Ⅰ. 宏观现象:点燃 a 处气体,产生_____色火焰。
Ⅱ. 微观分析:上述微观示意图所示反应中,没有发生变化的是微粒是氢原子和______。
Ⅲ. 符号表达:电解水的化学方程式为____________________。
48. 化学实验是培养化学素养的重要途径。根据以下实验回答问题:
A. 证明二氧化碳密度
比空气大
B. 探究可燃物燃烧的两
个条件
C. 测定空气中氧气的体
积分数
D. 验证木炭能和氧化铜
反应
第 4 页 / 共 7 页
①A 中观察到的现象是______________。
②B 中水的作用是隔绝空气和_________。
③C 中红热木炭和氧气反应的化学方程式为_____________________。
④D 中实验结束时,应先______(选填“取出导管”或“停止加热”)。
⑤对不能达到目的的实验,你的改进措施是______________________。
49. 氯化钠和碳酸钠在不同温度下的溶解度见下表:
温度(℃) 0 10 20 30 40
溶解度(g/100g 水) 氯化钠 35.7 35.8 36 36.3 36.6
碳酸钠 7 12.5 22 40 48.8
①30℃时碳酸钠的溶解度为_____g/100g 水,该温度下碳酸钠饱和溶液的溶质质量分数为________。
②氯化钠的溶解度随温度的升高而______(选填“增大”或“减小”)。
③碳酸钠中混有少量氯化钠,提纯碳酸钠的方法是_________(选填“降温结晶”或“蒸发结晶”)。
④区分氯化钠和碳酸钠两种白色固体,可采用以下方法:
A 是_______(选填“氯化钠”或“碳酸钠”),m 的取值范围是__________。
Ⅱ. 化学方法
查阅资料:氯化钠溶液呈中性,碳酸钠溶液呈碱性。
实验药品:蒸馏水,紫色石蕊试液,无色酚酞试液。
实验步骤 现象和结论
_____________ _____________
⑤资料显示,碳酸钠溶液的浓度越大,电导率(物质传导电流的能力)越大。用数字化仪器测得溶液中投
入无水碳酸钠固体后电导率的变化如右下图所示:
第 5 页 / 共 7 页
关于 a、b、c 三点所处溶液的分析正确的是_____。
A. 溶质质量:a=b=c B. 溶剂质量:a
50. 根据题意回答。
①写出仪器名称:w_________。
②用氯酸钾和二氧化锰制取较纯氧气的装置组合是_______。
③实验室用大理石和稀盐酸反应制取二氧化碳的化学方程式为________,若要随时控制反应的发生与停止,
选择的发生装置是___________。
④用装置 F 收集氧气(从 n 端进入),该如何操作__________。
⑤铁丝在氧气中燃烧的实验操作顺序是_______(用字母排序)。
⑥气体 X 可能是 O2、CO2 中的一种或两种,用下图所示装置进行实验(忽略气体的溶解)。
Ⅰ. 若观察到甲中石灰水变浑浊,乙中石灰水始终未变浑浊,最终有 10mL 液体进入丙中,则气体 X 的成分
是________。
Ⅱ. 若气体 X 中只含有 O2,则观察到的现象是__________________。
⑦含溶质 0.1mol 的过氧化氢溶液在二氧化锰的催化作用下,完全分解能生成氧气______mol。(根据化学方
程式列式计算)
第 6 页 / 共 7 页
51. 兴趣小组对“一氧化碳还原氧化铜”的实验进行改进。
【查阅资料及准备】
Ⅰ. 甲酸在 98%硫酸溶液催化下的反应为:HCOOH
98%
80 90?
?????→
硫酸溶液
℃
H2O+CO? 。
Ⅱ. 一氧化碳的爆炸极限(混合气体中的体积分数)为:12.5%-75%。
Ⅲ. 经测量,下图装置中试管、干燥管和 D 处前导管的总体积为 80mL。在广口瓶的适当位置绘制放置爆
炸的安全线。
【设计方案】实验装置如下(固定装置略):
实验步骤 现象 分析和结论
Ⅰ. 检查气密性。按上图连接装置,D 处瓶中装满水,
推动空注射器
D 处导管口产生气
泡
说明整套装置_____(选填
“漏气”或“不漏气”)
Ⅱ. 装入药品,进行反应。把 B 装置放入 A 中,逐滴
滴入甲酸,待 D 处液面下降至安全线处,点燃酒精
灯。反应完成后,熄灭酒精灯。装置冷却后取出 B
C 处黑色粉末变为
红色
C 处反应的化学方程式为
__________________
Ⅲ. 尾气处理,打开 D 处瓶塞,点燃瓶内气体 瓶口出现蓝色火焰 尾气处理的目的是_____
【实验分析】
①待 D 处液面下降至安全线处,再点燃酒精灯是为了_______________。
②能证明 CuO 已知 CO 发生反应的现象有_____________。
③若 B 处有 a mol 甲酸参加反应,D 处生成 b mol 碳酸钙,则 a>b,理由是________________。
④假设装置内空气已全部排入 D 处瓶中,当瓶内气体体积为 400mL 时,点燃是否发生爆炸?
通过计算说明理由(不考虑药品的体积)____________。
⑤逐滴滴入甲酸后,符合右图变量 y 的是_______
a. B 处水的物质的量
b. B 处生成一氧化碳的质量
c. C 处生成金属铜的物质的量
d. D 处碳酸钙的质量
第 7 页 / 共 7 页
参考答案
六、选择题
27 28 29 30 31 32 33 34 35 36
A D B B C D C C D A
37 38 39 40 41 42 43 44 45 46
B A C B C C A B A D
七、填空题
47.①润滑材料;单质;干冰 ②淡蓝;氧原子;2H2O ===
通电
2H2? +O2?
48.①烧杯中蜡烛从下到上依次熄灭 ②提供热量 ③C+O2===
点燃
CO2 ④取出导管
⑤C 实验,在集气瓶中预先加入适量氢氧化钠溶液(或把木炭换为红磷,并在瓶内加入少量水),并在右侧
烧杯中再加至少 25mL 水(合理即可)
49.①40;28.6%(2/7) ②增大 ③降温结晶
④碳酸钠;2.2 3.6m? ? ;取等质量的碳酸钠和氯化钠于试管中,分别加入适量的水溶解,再滴加几滴
无色酚酞试液:溶液变红,说明为碳酸钠固体;溶液不变色,说明为氯化钠固体
⑤C
八、简答题
50. ①试管 ②AE ③CaCO3+2HCl=CaCl2+H2O+CO2?;C
④在集气瓶内装满水,并延长 m 导管,在导管口接一个烧杯 ⑤badc
⑥10mLO2和 90mLCO2;甲乙中石灰水不变浑浊,且乙中石灰水流入丙中,约 100mL ⑦0.05
51.【设计方案】不漏气;CO+CuO
?
=== Cu+CO2;防止 CO 排出污染环境
①防止 CO 与空气混合加热发生爆炸 ②C 中黑色固体变红 ③部分 CO 未参与反应
④不爆炸;CO 的体积分数为 80%,不在爆炸极限范围内 ⑤b
同课章节目录
