第三章第四节-难溶电解质的溶解平衡(共23张PPT)
文档属性
| 名称 | 第三章第四节-难溶电解质的溶解平衡(共23张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 371.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-10 00:00:00 | ||
图片预览








文档简介
(共23张PPT)
第四节难溶电解质的溶解平衡
第三章水溶液中的离子平衡
1、盐类的水解实质:
2、水解规律:
3、影响因素
有弱才水解,无弱不水解;
谁弱谁水解,谁强显谁性;
越弱越水解,都弱双水解。
盐电离出来的离子与水电离出来的H + 或OH –
结合,从而使水的电离平衡发生移动的过程。
思考与讨论
(1)NaCl在水溶液里达到溶液平衡状态时有何特征?
(2)要使NaCl饱和溶液中析出NaCl固体,可采取什么措施?
加热浓缩
降温
(3)在饱和NaCl溶液中加入浓盐酸有何现象?
可溶的电解质溶液中存在溶解平衡,难溶的电解质在水中是否也存在溶解平衡呢?
一、Ag+和Cl-的反应能进行到底吗?
阅读课本P65~66思考与交流
大于10g,易溶
1g~10g,可溶
0.01g~1g,微溶
小于0.01g,难溶
20℃时,溶解度:
讨论1、谈谈对部分酸、碱和盐的溶解度表中“溶”与”不溶“的理解。
讨论2、根据对溶解度及反应限度、化学平衡原理的认识,说明生成沉淀的离子反应是否能真正进行到底。
1、生成沉淀的离子反应能发生的原因
生成物的溶解度很小
2、AgCl溶解平衡的建立
当v(溶解)=v(沉淀)时,得到饱和AgCl溶液,建立溶解平衡
3、溶解平衡的特征
逆、等、动、定、变
4、生成难溶电解质的离子反应的限度
难溶电解质的溶解度小于0.01g,离子反应生成难溶电解质,离子浓度小于1×10-5mol/L时,认为反应完全,但溶液中还有相应的离子。
党日活动总结 “解放思想大讨论”活动工作计划总结
党日活动总结“解放思想大讨论”活动工
作总结
信访局严格按照省、市委和区工委的部署,扎实开展解放思想学习讨论活动,经过学习宣传、讨论研究和问题查摆三个阶段,着力在“开”、“实”上做文章,解决影响和制约科学发展的突出问题,解决群众迫切希望解决的突出问题,着力形成有利于科学发展的工作机制,基本完成了各项任务,取得了良好成效,现将活动开展情况汇报如下:
一、统一思想,提高认识
为把全局思想统一到区工委、管委会解放思想大讨论活动精神上来,我们先后组织召开了学习动员会、学习讨论会、学习交流会等会议,全面传达贯彻省、市、区解放思想大讨论活动精神,明确大讨论活动的目的、意义、方法、步骤及有关要求,结合信访工作实际,进一步统一思想,明确目标,在全局范围积极开展解放思想学习讨论“五个一”活动,即:制定一份活动方案、写好一篇学习心得、落实一篇以上的调研文章、进行一次深刻的问题查摆剖析、组织一次专题讨论学习活动。以扎实的工作业绩,在信访维稳和推进区域经济更好更快的发展上做文章。
二、加强领导,明确责任
信访局两位局领导坚持带头学习、带头交流讨论、带头
调查研
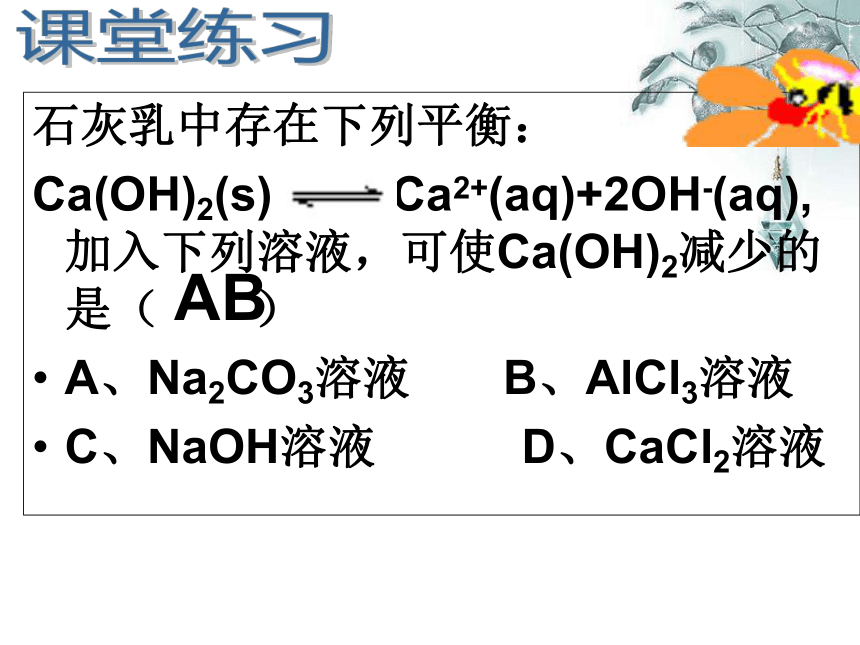
石灰乳中存在下列平衡:
Ca(OH)2(s) Ca2+(aq)+2OH-(aq),加入下列溶液,可使Ca(OH)2减少的是( )
A、Na2CO3溶液 B、AlCl3溶液
C、NaOH溶液 D、CaCl2溶液
AB
1、溶度积(Ksp):在一定温度下,在难溶电解质的饱和溶液中,各离子浓度幂之乘积为一常数.
2、表达式:(MmAn的饱和溶液) Ksp=[c(Mn+)]m · [c(Am-)]n
3、溶度积规则:离子积Qc=c(Mn+)m · c(Am-)n
Qc > Ksp,溶液处于过饱和溶液状态,生成沉淀.
Qc = Ksp,沉淀和溶解达到平衡,溶液为饱和溶液.
Qc < Ksp,溶液未达饱和,沉淀发生溶解.
二.溶度积和溶度积规则
阅读课本P70(科学视野)
课堂练习
2.铬酸银(Ag2CrO4)在298K时的溶解度为0.0045g,求其溶度积。
1.在100mL 0.01mol/LKCl 溶液中,加入 1mL 0.01mol/L AgNO3 溶液,有沉淀(已知AgCl KSP=1.8×10-10) ?
Ag+沉淀是否完全?
第四节难溶电解质的溶解平衡
(第二课时)
第三章水溶液中的离子平衡
三、沉淀反应的应用
1、沉淀的生成
(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。
阅读课本P66~68
(2)方法
a 、调pH值
如:工业原料氯化铵中混有氯化铁,
加氨水调pH值至7-8
Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+
b 、加沉淀剂:如沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂
Cu2++S2-=CuS↓ Hg2++S2-=HgS↓
思考与交流
1、如果要除去某溶液中的SO42-,你选择加 入钡盐还是钙盐?为什么?
加入钡盐,因为BaSO4比CaSO4更难溶,使用钡盐可使SO42-沉淀更完全
2、以你现有的知识,你认为判断沉淀能否生成可从哪方面考虑?是否可能使要除去的离子通过沉淀反应全部除去?说明原因。
从溶解度方面可判断沉淀能否生成
不可能使要除去的离子通过沉淀完全除去
要除去MgCl2酸性溶液中少量的FeCl3,不宜选用的试剂是( )
A、MgO B、MgCO3
C、NaOH D、Mg(OH)2
c
2、沉淀的溶解
(1)原理
设法不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动
(2)举例
a 、难溶于水的盐溶于酸中
如:CaCO3溶于盐酸,FeS、Al(OH)3、Cu(OH)2溶于强酸
b 、难溶于水的电解质溶于某些盐溶液
如:Mg(OH)2溶于NH4Cl溶液
思考与交流
用平衡移动的原理分析Mg(OH)2溶于盐酸和NH4Cl溶液的原因
解释
在溶液中存在Mg(OH)2的溶解平衡:
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq)
加入盐酸时,H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解
加入NH4Cl时,
1、NH4+直接结合OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解
2、NH4+水解,产生的H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解
小结:难溶电解质溶解的规律
不断减小溶解平衡体系中的相应离子,平衡就向沉淀溶解的方向移动,从而使沉淀溶解
牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡: Ca5(PO4)3OH(s) 5Ca2++3PO43-+OH- 进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是
。
已知Ca5(PO4)3F(s)的溶解度比上面的矿化产物更小、质地更坚固。用离子方程表示当牙膏中配有氟化物添加剂后能防止龋齿的原因 。
生成的有机酸能中和OH-,使平衡向脱矿方向移动,加速腐蚀牙齿
5Ca2++3PO43-+F-=Ca5(PO4)3F↓
(1)沉淀转化的方法
对于一些用酸或其他方法也不能溶解的沉淀,可以先将其转化为另一种用酸或其他方法能溶解的沉淀。
(2)沉淀转化的实质
沉淀转化的实质是沉淀溶解平衡移动。一般溶解度小的沉淀转化成溶解度更小的沉淀容易实现。
(3)沉淀转化的应用
沉淀的转化在科研和生产中具有重要的应用价值。
①锅炉除水垢
二、沉淀反应的应用
3、沉淀的转化
锅炉中水垢中含有CaSO4 ,可先用Na2CO3溶液处理,使 之转化为疏松、易溶于酸的CaCO3。
CaSO4 SO42- + Ca2+
+
CO32-
CaCO3
②对一些自然现象的解释
科学视野:溶度积
资料:氟化物防治龋齿的化学原理
第四节难溶电解质的溶解平衡
第三章水溶液中的离子平衡
1、盐类的水解实质:
2、水解规律:
3、影响因素
有弱才水解,无弱不水解;
谁弱谁水解,谁强显谁性;
越弱越水解,都弱双水解。
盐电离出来的离子与水电离出来的H + 或OH –
结合,从而使水的电离平衡发生移动的过程。
思考与讨论
(1)NaCl在水溶液里达到溶液平衡状态时有何特征?
(2)要使NaCl饱和溶液中析出NaCl固体,可采取什么措施?
加热浓缩
降温
(3)在饱和NaCl溶液中加入浓盐酸有何现象?
可溶的电解质溶液中存在溶解平衡,难溶的电解质在水中是否也存在溶解平衡呢?
一、Ag+和Cl-的反应能进行到底吗?
阅读课本P65~66思考与交流
大于10g,易溶
1g~10g,可溶
0.01g~1g,微溶
小于0.01g,难溶
20℃时,溶解度:
讨论1、谈谈对部分酸、碱和盐的溶解度表中“溶”与”不溶“的理解。
讨论2、根据对溶解度及反应限度、化学平衡原理的认识,说明生成沉淀的离子反应是否能真正进行到底。
1、生成沉淀的离子反应能发生的原因
生成物的溶解度很小
2、AgCl溶解平衡的建立
当v(溶解)=v(沉淀)时,得到饱和AgCl溶液,建立溶解平衡
3、溶解平衡的特征
逆、等、动、定、变
4、生成难溶电解质的离子反应的限度
难溶电解质的溶解度小于0.01g,离子反应生成难溶电解质,离子浓度小于1×10-5mol/L时,认为反应完全,但溶液中还有相应的离子。
党日活动总结 “解放思想大讨论”活动工作计划总结
党日活动总结“解放思想大讨论”活动工
作总结
信访局严格按照省、市委和区工委的部署,扎实开展解放思想学习讨论活动,经过学习宣传、讨论研究和问题查摆三个阶段,着力在“开”、“实”上做文章,解决影响和制约科学发展的突出问题,解决群众迫切希望解决的突出问题,着力形成有利于科学发展的工作机制,基本完成了各项任务,取得了良好成效,现将活动开展情况汇报如下:
一、统一思想,提高认识
为把全局思想统一到区工委、管委会解放思想大讨论活动精神上来,我们先后组织召开了学习动员会、学习讨论会、学习交流会等会议,全面传达贯彻省、市、区解放思想大讨论活动精神,明确大讨论活动的目的、意义、方法、步骤及有关要求,结合信访工作实际,进一步统一思想,明确目标,在全局范围积极开展解放思想学习讨论“五个一”活动,即:制定一份活动方案、写好一篇学习心得、落实一篇以上的调研文章、进行一次深刻的问题查摆剖析、组织一次专题讨论学习活动。以扎实的工作业绩,在信访维稳和推进区域经济更好更快的发展上做文章。
二、加强领导,明确责任
信访局两位局领导坚持带头学习、带头交流讨论、带头
调查研
石灰乳中存在下列平衡:
Ca(OH)2(s) Ca2+(aq)+2OH-(aq),加入下列溶液,可使Ca(OH)2减少的是( )
A、Na2CO3溶液 B、AlCl3溶液
C、NaOH溶液 D、CaCl2溶液
AB
1、溶度积(Ksp):在一定温度下,在难溶电解质的饱和溶液中,各离子浓度幂之乘积为一常数.
2、表达式:(MmAn的饱和溶液) Ksp=[c(Mn+)]m · [c(Am-)]n
3、溶度积规则:离子积Qc=c(Mn+)m · c(Am-)n
Qc > Ksp,溶液处于过饱和溶液状态,生成沉淀.
Qc = Ksp,沉淀和溶解达到平衡,溶液为饱和溶液.
Qc < Ksp,溶液未达饱和,沉淀发生溶解.
二.溶度积和溶度积规则
阅读课本P70(科学视野)
课堂练习
2.铬酸银(Ag2CrO4)在298K时的溶解度为0.0045g,求其溶度积。
1.在100mL 0.01mol/LKCl 溶液中,加入 1mL 0.01mol/L AgNO3 溶液,有沉淀(已知AgCl KSP=1.8×10-10) ?
Ag+沉淀是否完全?
第四节难溶电解质的溶解平衡
(第二课时)
第三章水溶液中的离子平衡
三、沉淀反应的应用
1、沉淀的生成
(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。
阅读课本P66~68
(2)方法
a 、调pH值
如:工业原料氯化铵中混有氯化铁,
加氨水调pH值至7-8
Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+
b 、加沉淀剂:如沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂
Cu2++S2-=CuS↓ Hg2++S2-=HgS↓
思考与交流
1、如果要除去某溶液中的SO42-,你选择加 入钡盐还是钙盐?为什么?
加入钡盐,因为BaSO4比CaSO4更难溶,使用钡盐可使SO42-沉淀更完全
2、以你现有的知识,你认为判断沉淀能否生成可从哪方面考虑?是否可能使要除去的离子通过沉淀反应全部除去?说明原因。
从溶解度方面可判断沉淀能否生成
不可能使要除去的离子通过沉淀完全除去
要除去MgCl2酸性溶液中少量的FeCl3,不宜选用的试剂是( )
A、MgO B、MgCO3
C、NaOH D、Mg(OH)2
c
2、沉淀的溶解
(1)原理
设法不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动
(2)举例
a 、难溶于水的盐溶于酸中
如:CaCO3溶于盐酸,FeS、Al(OH)3、Cu(OH)2溶于强酸
b 、难溶于水的电解质溶于某些盐溶液
如:Mg(OH)2溶于NH4Cl溶液
思考与交流
用平衡移动的原理分析Mg(OH)2溶于盐酸和NH4Cl溶液的原因
解释
在溶液中存在Mg(OH)2的溶解平衡:
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq)
加入盐酸时,H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解
加入NH4Cl时,
1、NH4+直接结合OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解
2、NH4+水解,产生的H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解
小结:难溶电解质溶解的规律
不断减小溶解平衡体系中的相应离子,平衡就向沉淀溶解的方向移动,从而使沉淀溶解
牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡: Ca5(PO4)3OH(s) 5Ca2++3PO43-+OH- 进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是
。
已知Ca5(PO4)3F(s)的溶解度比上面的矿化产物更小、质地更坚固。用离子方程表示当牙膏中配有氟化物添加剂后能防止龋齿的原因 。
生成的有机酸能中和OH-,使平衡向脱矿方向移动,加速腐蚀牙齿
5Ca2++3PO43-+F-=Ca5(PO4)3F↓
(1)沉淀转化的方法
对于一些用酸或其他方法也不能溶解的沉淀,可以先将其转化为另一种用酸或其他方法能溶解的沉淀。
(2)沉淀转化的实质
沉淀转化的实质是沉淀溶解平衡移动。一般溶解度小的沉淀转化成溶解度更小的沉淀容易实现。
(3)沉淀转化的应用
沉淀的转化在科研和生产中具有重要的应用价值。
①锅炉除水垢
二、沉淀反应的应用
3、沉淀的转化
锅炉中水垢中含有CaSO4 ,可先用Na2CO3溶液处理,使 之转化为疏松、易溶于酸的CaCO3。
CaSO4 SO42- + Ca2+
+
CO32-
CaCO3
②对一些自然现象的解释
科学视野:溶度积
资料:氟化物防治龋齿的化学原理
