8.1:金属材料(含解析)
图片预览


文档简介
中小学教育资源及组卷应用平台
初中化学人教版九年级下学期第八单元课题1:金属材料
一、单选题(共7题;共14分)
1.咱国庆70年阅兵你看了吗?下列相关叙述的物质不含有金属材料的是(?? )
A.?五星红旗—国旗??????????????????????????B.?钢铁怪兽—坦克
C.?空中战鹰—飞机???????????????????????????D.?便携战斗部—导弹
2.下列关于钢铁的说法中,正确的是()
A.?生铁的含碳量比钢的少???????????????????????????????????????B.?生铁和钢都是铁的合金
C.?纯铁较软,而生铁比铁更软????????????????????????????????D.?工业上用高炉炼制出的纯铁
3.下列有关金属的说法中,错误的是(?? )
A.?铜制插头是利用铜的导电性????????????????????????????????B.?钨制灯丝是利用钨的熔点低
C.?铝制成铝箔是利用铝的延展性?????????????????????????????D.?用铁锅炒菜是利用铁的导热性
4.下面是某同学对主题内容进行的归纳情况,你认为其中一组错误的是(?? )
A.?化学与安全:进入山洞先做“灯火实验”,点燃可燃性气体前先验纯
B.?环保与使用:加快“煤改气”,多使用清洁能源:推行共享单车,打造绿色交通
C.?微粒与构成:氧气由氧分子构成,氯化钠由氯离子和钠离子构成
D.?元素与组成:地壳中含量最多的是铝元素,空气中含量最多的是氮元素
5.金属的用途主要由性质决定的,下面有关用途和性质的对应关系错误的是(?? )
A.?用铝合金门窗代替铁门窗是因为铝的密度比铁小、更轻便,且比铁抗腐蚀性强
B.?用钨制灯丝而不用锡,是因为锡的熔点低
C.?电线用铜制而不用银,是因为铜的导电性优于银
D.?铁制品表面镀铬是因为铬的硬度大,耐磨且不易生锈
6.下列关于“合金”的叙述①合金中至少含有两种金属;②合金中元素以化合态的形式存在;③合金中一定含有金属;④合金一定为混合物;⑤合金依然具有金属特性,其中正确的是(?? )
A.?④????????????????????????????????????B.?①②③????????????????????????????????????C.?③④????????????????????????????????????D.?③④⑤
7.下列实验操作能达成实验目的是(?? )
选项 实验目的 实验操作
A 比较合金与纯金属的硬度 用黄铜片和纯铜片相互刻划
B 检验CO2是否集满 向集气瓶中加入澄清石灰水,振荡
C 验证质量守恒定律 称量镁条在空气中点燃前、后固体的质量
D 证明CO2能与水反应 向盛满CO2的塑料瓶中倒水,拧紧瓶盖并振荡
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
二、填空题(共4题;共25分)
8.写出下列金属元素的符号:
热水瓶内胆上镀的金属 ________?;地壳中含量最多的金属________?;闪光灯中使用的金属________?;水银温度计里的金属________ ;导电性最好的金属是________?.
9.生铁和钢都是________?合金.要使生铁变成钢,必须降低生铁中的________?含量,调整________的含量,除去________等有害杂质.纯铁________?,不宜用来制造机械和其他用品;生铁中的白口铁缺点是________?,不宜铸造和机械加工;灰口铁强度________?,不能煅轧;钢较硬,具有良好________?性、________?性、________?性,可以煅轧和铸造.
10.我们的日常生活用品,很多都是由金属材料制成的.例如:体温计中的液体是________;制造导线一般是用________;水龙头表面镀的一般是________;炒菜锅最好用________制作;灯泡里的灯丝是________;一种合金与人体具有很好的“相容性”,可以用来制造“人造骨”的是________.(以上空格均写物质的名称)
11.如图为优盘的外观和内部结构示意图。
(1)图中含有的金属材料是________(填1种,下同)。
(2)利用铝合金做保护套的材料与用铁相比具有的优点是________(填一点即可)。
(3)将铜加工成铜箔基板利用的铜的性质是________。
(4)闪存芯片通常用高纯硅(纯度高达99.99%以上的Si单质)做原料。工业上利用碳与SiO2反应得到粗硅:再在粗硅中通入Cl2 , 得到SiCl4;最后在高温的条件下,让SiCl4与氢反应,得到高纯硅和一种化合物。请写出由SiCl4得到高纯硅的化学方程式________。
三、解答题(共2题;共18分)
12.回答下列的问题:?????????????????????????????
(1)金刚石和石墨物理性质存在差异的原因是________;
(2)黄铜片和纯铜片互相刻划,纯铜片上有痕迹原因是________;
(3)从微观角度分析,O2和O3化学性质不同的原因是________.
13.金属材料在生活、生产中应用十分广泛。
(1)图①是金属的一个应用实例,请说出利用了金属的什么物理性质。(答出一点即可)
(2)图②中两块金属片互相刻划后,在纯铜片上有明显的划痕。该实验探究的目的是什么?得到什么结论?
(3)请你举一实例说明合金的用途比纯金属更广泛。
四、实验探究题(共1题;共10分)
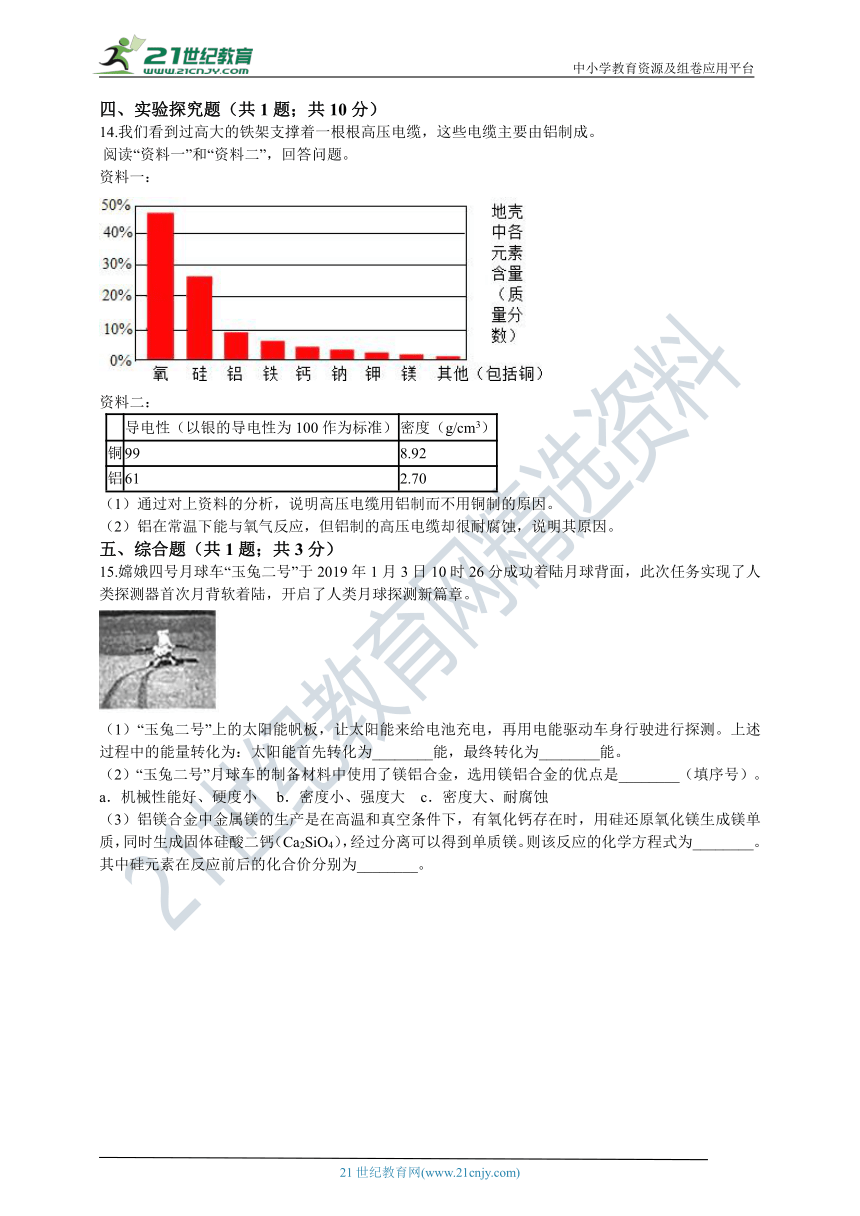
14.我们看到过高大的铁架支撑着一根根高压电缆,这些电缆主要由铝制成。
?阅读“资料一”和“资料二”,回答问题。
资料一:
资料二:
导电性(以银的导电性为100作为标准) 密度(g/cm3)
铜 99 8.92
铝 61 2.70
(1)通过对上资料的分析,说明高压电缆用铝制而不用铜制的原因。
(2)铝在常温下能与氧气反应,但铝制的高压电缆却很耐腐蚀,说明其原因。
五、综合题(共1题;共3分)
15.嫦娥四号月球车“玉兔二号”于2019年1月3日10时26分成功着陆月球背面,此次任务实现了人类探测器首次月背软着陆,开启了人类月球探测新篇章。
(1)“玉兔二号”上的太阳能帆板,让太阳能来给电池充电,再用电能驱动车身行驶进行探测。上述过程中的能量转化为:太阳能首先转化为________能,最终转化为________能。
(2)“玉兔二号”月球车的制备材料中使用了镁铝合金,选用镁铝合金的优点是________(填序号)。
a.机械性能好、硬度小??? b.密度小、强度大 ??c.密度大、耐腐蚀
(3)铝镁合金中金属镁的生产是在高温和真空条件下,有氧化钙存在时,用硅还原氧化镁生成镁单质,同时生成固体硅酸二钙(Ca2SiO4),经过分离可以得到单质镁。则该反应的化学方程式为________。其中硅元素在反应前后的化合价分别为________。
答案解析部分
一、单选题
1.答案: A
解析:A. 五星红旗的材料主要是纤维材质,不属于金属材料,故符合题意;
B. 坦克的外壳用的是合金,合金属于金属材料,故不符合题意;
C. 飞机的外壳用的是合金,合金属于金属材料,故不符合题意;
D. 导弹的外壳用的是合金,合金属于金属材料,故不符合题意;
故答案为:A。
金属材料包括纯金属、合金、金属间化合物和特种金属材料等。
2.答案: B
解析:A、生铁的含碳量在2~4.3%,钢的含碳量在0.03~2%,故生铁的含碳量比钢的多,而不是少,A不符合题意,
B、生铁和钢都是铁的合金,B符合题意,
C、纯铁较软,而生铁因为含碳,所以纯铁更硬,C不符合题意,
D、工业上用高炉炼制出的是生铁,D不符合题意,
故答案为:B
A、根据生铁和钢的组成分析
B 、根据合金的概念分析
C、根据合金的特性分析
D、根据高炉炼铁得到的是生铁分析
3.答案: B
解析:A、铜质插头是利用铜的导电性是正确的叙述;
B、是不符合题意的叙述,钨制灯丝是利用钨的熔点高,不易熔化;
C、铝制成铝箔是利用铝的延展性,是正确的叙述;
D、用铁锅炒菜时利用铁的导热性,是正确的叙述;
故答案为:B。
A.根据性质决定用途考虑,做导线需要具有导电性;
B.根据金属钨的熔点高进行解答;
C.根据金属具有延展性考虑;
D.根据金属具有良好的导热性进行分析判断。
4.答案: D
解析:A、进入山洞先做“灯火实验”,以防二氧化碳浓度过高,造成人缺氧窒息;可燃性气体与空气混合后点燃可能发生爆炸,点燃可燃性气体之前,为防止发生爆炸,应先检验气体的纯度,故A不符合题意;
B、加快“煤改气”,多使用清洁能源:推行共享单车,打造绿色交通可以节约化石燃料,防治环境污染,故B不符合题意;
C、氧气是由氧分子构成的;氯化钠是由钠离子与氯离子构成的,故C不符合题意;
D、地壳中含量最多的是氧元素,空气中含量最多的是氮元素,故D符合题意。
故答案为:D。
地壳中元素含量的排列顺序为O>Si>Al>Fe>Ca>Na>K>Mg。
5.答案: C
解析:A、用铝合金门窗代替铁门窗,是因为铝的密度比铁小、更轻便,且比铁耐腐蚀,不符合题意;
B、灯丝的材料应具有熔点高的性质,用钨制灯丝而不用锡,是因为锡的熔点低,不符合题意;
C、电线用铜制而不用银,并不是因为铜的导电性优于银,是因为银的价格较高,符合题意;
D、铁制品表面镀铬是因为铬的硬度大,耐磨且具有优良的抗腐蚀性,不易生锈,不符合题意。
故答案为:C。
本题难度不大,物质的性质决定用途,可以根据物质的性质方面进行分析、判断,从而得出正确的结论。?
6.答案: D
解析:合金是指一种金属中加热融合其他金属或非金属形成具有金属特性的物质,因此合金是金属和其他金属或非金属的混合物,在合金中金属或非金属以单质形式存在,
故答案为:D
合金是指一种金属中加热融合其他金属或非金属形成具有金属特性的物质,据此分析解答
7.答案: A
解析:A、合金的硬度大于其组成金属的硬度,用相互刻画的方法可以比较合金与纯金属的硬度,A符合题意;
B、排空气法收集时,检验二氧化碳是否集满可用燃着的木条放在集气瓶口,观察木条是否熄灭来判断是否集满,B不符合题意;
C、有气体参与或生成的反应用来验证质量守恒定律时,反应应该在密封体系中进行,C不符合题意;
D、二氧化碳可溶于水也能和水反应,向盛满CO2的塑料瓶中倒水,拧紧瓶盖并振荡,塑料瓶变瘪也可能是二氧化碳溶于水造成的,要证明CO2能与水反应,需要证明有新物质生成,D不符合题意。
故答案为:A。
纯金属的硬度比合金的硬度小,熔点比合金高。
二、填空题
8.答案:Ag;Al;Mg;Hg;Ag
解析:热水瓶内胆上镀的金属是银,银的元素符号为Ag;地球上含量最多的金属铝,铝的元素符号为Al;闪光灯中使用的金属是镁,镁的元素符号为Mg;水银温度计里的金属是汞,汞的元素符号是Hg;导电性最好的金属是,银的元素符号为Ag.
故答案为:银(Ag);铝(Al);镁(Mg);汞(Hg);银(Ag).
只有熟悉元素的名称和元素符号的写法,才能正确解答本题.
9.答案:铁、碳;碳;硅、锰;硫、磷;机械性能和可加工性能差;硬而脆;差;韧;可加工;耐腐蚀
解析:生铁和钢是指铁与碳融合一起得到的铁合金,含C量在0.03%﹣2%之间的铁合金称为钢、2%﹣4.3%之间称为生铁,通过降低生铁的含C量可以把生铁变成钢,生铁因含C量高性能呈现硬而脆、机械性能差,钢含C量低,有较好地韧性,具有良好的机械性能.
故答:铁、碳;碳;硅、锰;硫、磷;机械性能和可加工性能差;硬而脆;差;韧;可加工;耐腐蚀.
合金是生活中使用广泛的金属材料,生铁和钢又是生活中应用最多的合金,通过生铁和钢组成上、性能上、应用上的对比,可细化对这两种材料的认识.
10.答案:汞;铜;铬;铁;钨;钛
解析:解:家里的日常生活用品,它们有很多都是由金属材料制成的,汞是常温下唯一的液态金属,体温计中的液体是汞;铜具有优良的导电性,作导线的一般是铜;铬的硬度大,耐腐蚀,水龙头表面镀的金属一般是铬;铁具有导热性,炒菜的锅一般是铁.钨的熔点最高,灯泡的灯丝是钨;钛合金与人体具有很好的“相容性”,可以用来制造“人造骨”
故答为:汞,铜,铬,铁,钨,钛;
物质的性质决定物质的用途,根据常见金属的性质和用途分析回答.
11.答案: (1)铜或铝合金
(2)质轻(或硬度大,耐腐蚀等)
(3)延展性
(4)
解析:(1)金属材料包括纯金属单质以及它们的合金,铜和铝合金属于金属材料;(2)铝铁合金与铁相比具有的优点是质轻、硬度大,耐腐蚀等;(3)铜具有良好的延展性,所以可将铜加工成铜箔;(4)在高温的条件下,SiCl4与氢气反应,得到高纯硅和氯化氢气体,所以反应的化学方程式为: 。
(2)合金比组成它的纯金属硬度大、熔点低、耐腐蚀性强。
三、解答题
12.答案:(1)碳原子的排列顺序不同
(2)黄铜片比纯铜片硬度大
(3)分子构成不同
解析:解:(1)金刚石和石墨物理性质存在差异的原因是碳原子的排列顺序不同;(2)黄铜片和纯铜片互相刻划,纯铜片上有痕迹原因是黄铜片比纯铜片硬度大;(3)从微观角度分析,O2和O3化学性质不同的原因是分子构成不同;
故答案为:碳原子的排列顺序不同;黄铜片比纯铜片硬度大;分子构成不同.
根据金刚石和石墨物理性质不同的原因,氧气和臭氧分子构成不同去分析判断,根据合金的用途分析回答.
13.答案:(1)解:导电性(或延展性)
(2)解:目的是比较黄铜和铜的硬度,结论是黄铜的硬度比铜大
(3)解:医疗器械、炊具、反应釜等都是用不锈钢,而不用纯铁,因不锈钢的抗腐蚀性优于纯铁(其它合理答案均可)
解析:(1)图1金属做电线利用了金属的导电性和延展性;(2)纯铜的硬度小于合金的硬度,所以用两块金属片互相刻划,比较硬度,会在纯铜片上有明显的划痕;(3)纯铁易被锈蚀,医疗器械、炊具、反应釜等都是用不锈钢,而不用纯铁,因为不锈钢的抗腐蚀性优于纯铁。
根据金属的物理性质和用途分析,金属都有导电性和延展性;根据合金的性质分析,合金的硬度比纯金属硬度大,应用广泛。
四、实验探究题
14.答案:(1)铝在地壳中含量比铜在地壳中含量高,铝比铜的密度小,避免铁架承受过大的压力和电缆承受过大的拉力;
(2)铝表面易形成致密的氧化膜,可阻止铝进一步被氧化。
解析:(1)铝在地壳中含量比铜在地壳中含量高;铝的导电性大约是铜的导电性的2/3,但密度不到铜的1/3,制相同长度、相同导电能力的电缆,铝的质量比铜小,避免铁架承受过大的压力和电缆承爱过的拉力。
(2)铝在常温下与空气中的氧气反应,其表面生成一层致密的氧化铝薄膜,隔绝了与空气的接触,阻止了铝的进一步反应。
本题主要考查了物质的性质决定物质的用途方面的内容。
五、综合题
15.答案: (1)电;机械
(2)b
(3)2CaO+2MgO+Si Ca2SiO4+2Mg;0价和+4价
解析:(1)“玉兔二号”上的太阳能帆板,让太阳能来给电池充电,再用电能驱动车身行驶进行探测。上述过程中的能量转化为:太阳能首先转化为电能,最终转化为机械能;故填:电;机械;(2)镁铝合金的优点是密度小,硬度大,机械性能好等;故填:b;(3)在高温和真空条件下,有氧化钙存在时,用硅还原氧化镁生成镁单质,同时生成固体硅酸二钙(Ca2SiO4),反应前,硅是单质,硅元素的化合价为零,在生成物Ca2SiO4中,钙元素显+2价,氧元素显-2价,所以其中硅元素显+4价;故填:2CaO+2MgO+Si Ca2SiO4+2Mg;0价和+4价。
(1)根据 太阳能帆板的工作原理分析
(2)根据合金的特点分析
(3)根据氧化钙和氧化镁和硅在高温真空下生成硅酸钙和镁,化合物中各元素的化合价为零分析
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
