2019—2020年人教版化学高一必修一第四章第一节4.1无机非金属材料的主角——硅(共26张PPT)
文档属性
| 名称 | 2019—2020年人教版化学高一必修一第四章第一节4.1无机非金属材料的主角——硅(共26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-13 00:00:00 | ||
图片预览







文档简介
(共26张PPT)
必修一 第四章
无机非金属材料的主角——硅
晶体硅
二氧化硅
硅胶
1.1硅的原子结构示意图
硅原子和碳原子的最外电子层均有4个电子,其原子既不易失去也不易得到电子,主要形成四价的化合物。
Si
+14
8
4
2
+6
4
2
C
1硅元素与硅单质
结构决定性质
1.2硅的结构、物理性质和用途
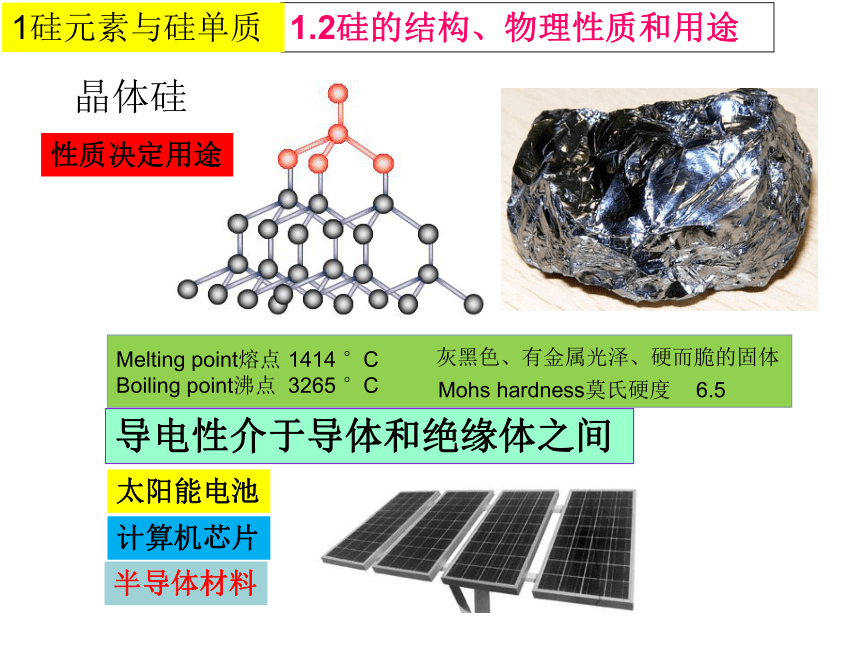
晶体硅
1硅元素与硅单质
导电性介于导体和绝缘体之间
Mohs hardness莫氏硬度 6.5
Melting point熔点 1414 °C
Boiling point沸点 3265 °C
灰黑色、有金属光泽、硬而脆的固体
太阳能电池
计算机芯片
半导体材料
性质决定用途
1.3.2在高温条件下,单质硅能与O2和Cl2等非金属单质反应。
1.3.1常温下化学性质不活泼,只能跟F2、HF和 NaOH溶液反应。
Si+4HF=SiF4↑+2H2↑
Si+2NaOH+H2O=Na2SiO3+2H2↑
Si+O2 SiO2
Si + 2Cl2 ==== SiCl4
1.3硅的化学性质
1硅元素与硅单质
Si是否具有两性?
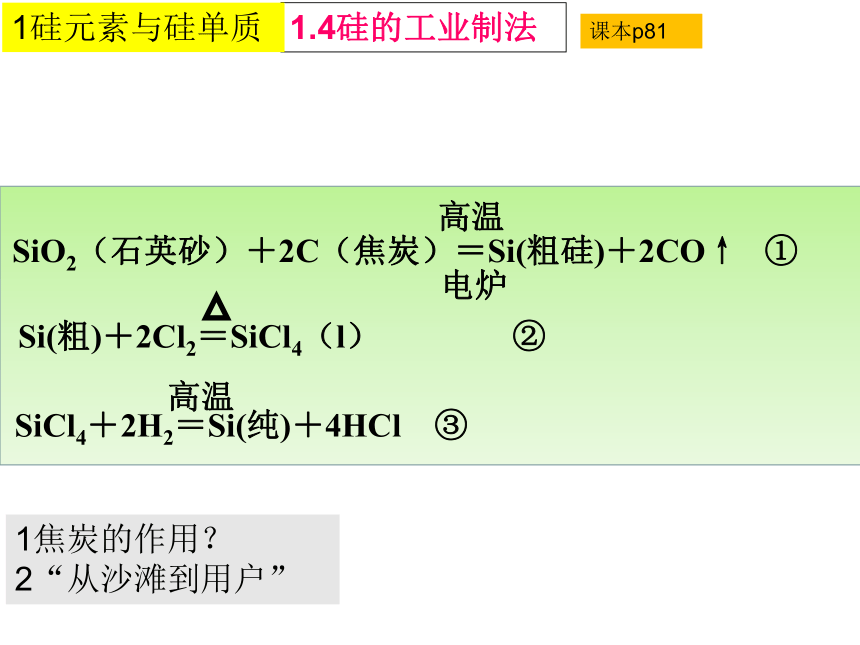
SiO2(石英砂)+2C(焦炭)=Si(粗硅)+2CO↑ ①
高温
SiCl4+2H2=Si(纯)+4HCl ③
高温
Si(粗)+2Cl2=SiCl4(l) ②
1.4硅的工业制法
1硅元素与硅单质
电炉
课本p81
1焦炭的作用?
2“从沙滩到用户”
结晶形和无定形。通称硅石。
石英
水晶
紫水晶
蔷薇石英
茶晶
黄水晶
2.1存在形态
2二氧化硅
水晶
开采注意粉尘
玛瑙
结晶形和无定形。通称硅石。
2.1存在形态
2二氧化硅
工艺品、饰品
2二氧化硅
实验仪器
2.2用途
光导纤维
2.3结构与物理性质
2二氧化硅
Melting point熔点 1,713 °C
Boiling point沸点 2,950 °C
SiO2是由Si和O按1:2的比例组成的立体空间网状结构,没有SiO2 分子存在,只存在硅氧原子。 因此性质很稳定
很不活泼,氢氟酸( HF)是唯一与之反应的酸。
SiO2+4HF=SiF4?+2H2O
1.玻璃中含有SiO2,用HF来刻蚀玻璃。
2.4.1特性
2.4化学性质
2二氧化硅
性质决定用途
2.实验室能不能用玻璃瓶盛装氢氟酸。
2.4.2酸性氧化物
SiO2 + 2NaOH = Na2SiO3 +H2O
硅酸钠(粘合剂)
不能用磨口玻璃塞盛碱性溶液,如NaOH、KOH、Na2CO3、Na2SiO3等溶液。
应用
应用
SiO2+ CaO === CaSiO3
高温
某同学根据SiO2既可与碱反应,也能与氢氟酸反应,推断SiO2为两性氧化物,是否正确?
?Na2CO3+SiO2===Na2SiO3+CO2↑
CaCO3 +SiO2 === CaSiO3 + CO2↑
高温
高温
SiO2 + 2C = Si + 2CO↑
高温
高沸点制低沸点——普通玻璃
2.4.3高沸点
2.4化学性质
2二氧化硅
性质决定用途
2.4.4弱氧化性
硅酸是一种白色粉末状的固体,它不溶于水;
H2SiO3
3.1物理性质
3硅酸
性质决定用途
H2SiO3 + 2NaOH == Na2SiO3 + 2H2O
3.2.2不稳定(比H2CO3稳定),受热易分解
?
H2SiO3 == H2O + SiO2
3.2.1一种很弱的酸,不能使指示剂变色、只能与强碱发生中和反应
3.2化学性质
3.3用途
3.3.1硅胶多孔,吸附水份能力强,常用作实验室和袋装食品、瓶装药品等的干燥剂。
3.3.2也可以用作催化剂的载体。
现 象
结 论
方程式
离子
方程式
①滴入酚酞溶液呈红色
Na2SiO3+2HCl = H2SiO3(胶体)+2NaCl
②再滴入稀盐酸,溶液红色变浅至无色,有透明胶冻状物质产生
SiO32- + 2H+ == H2SiO3 (胶体)
a、Na2SiO3溶液呈碱性,b、可溶性
硅酸盐与盐酸反应生成不溶于水的硅酸,
c、先形成硅酸溶胶,后形成硅酸凝胶
3.4制备方法
3硅酸
1、定义:
由硅、氧和金属组成的化合物的总称
2、性质:
硅酸盐种类很多,是一大类结构复杂的固态物质,大多数不溶于水,化学性质很稳定。
3、表示方法:
(1)化学式法:
Na2SiO3,CaSiO3
4.1表示方法
4硅酸盐
(2)氧化物法:
活泼金属氧化物→较活泼金属氧化物→二氧化硅→水
高岭石:Al2(Si2O5)(OH)4
Al2O3·2SiO2·2H2O
正长石:KAlSi3O8
硅酸钠是白色固体,可溶于水,其水溶液俗称水玻璃。
4.2硅酸钠(Na2SiO3)物理性质、用途
4硅酸盐
用途
1制备硅胶
2作肥皂填料
3做建筑、纸张的黏合剂
4木材、织物的防腐剂及防火剂
4.3硅酸钠(Na2SiO3)化学性质
4硅酸盐
②与盐反应
①与酸反应
Na2SiO3 + 2HCl =2NaCl + H2SiO3↓
CaCl2+Na2SiO3=CaSiO3↓+2NaCl
无机非金属材料
硅酸盐产品
陶瓷
水泥
玻璃
粘土
黏土和石灰石
硅酸三钙(3CaO·SiO2)
硅酸二钙(2CaO·SiO2) 混合物
铝酸三钙(3CaO·Al2O3)
陶都江苏宜兴 瓷都江西景德镇
CHINA
水硬性
具有抗氧化、抗酸碱腐蚀、耐高温、绝缘、易成型
有色玻璃
钢化玻璃
纯碱、石灰石和石英
?Na2CO3+SiO2===Na2SiO3+CO2↑
CaCO3 +SiO2===CaSiO3 + CO2↑
高温
高温
无固定的熔沸点,
在一定温度范围内软化
5硅酸盐工业
5.1传统无机非金属材料
5硅酸盐工业
Silicon carbide碳化硅(金刚砂)SiC
具有金刚石结构、硬度大,用作砂纸、砂轮的磨料。
Melting point熔点 2,830 °C
Solubility:Insoluble in water
5.2新型无机非金属材料
5硅酸盐工业
硅橡胶耐高温、低温 -60—250℃
高弹性(火箭、导弹、飞机的零件和绝缘材料)
5.2新型无机非金属材料
5硅酸盐工业
分子筛:具有均匀微孔结构的铝硅酸盐
用作吸附剂、催化剂
Molecular sieve
5.2新型无机非金属材料
新型陶瓷
高温结构陶瓷、压电陶瓷
透明陶瓷、超导陶瓷等
5硅酸盐工业
5.2新型无机非金属材料
人造骨骼
氮化硅陶瓷在1200℃左右的高温下,仍具有很高的强度,
可用来制造汽轮机叶片、轴承、永久性模具等。
5硅酸盐工业
5.2新型无机非金属材料
Silicon nitride氮化硅陶瓷
Melting point熔点:1,900 °C
F-117是一种单座战斗轰炸机。设计目的是凭隐身性能,突破敌火力网,压制敌方防空系统,摧毁严密防守的指挥所、战略要地、重要工业目标,还可执行侦察任务,具有一定空战能力。
练习:
1.下列说法正确的是( )
A.二氧化硅溶于水显酸性
B.二氧化碳通入水玻璃(Na2SiO3的水溶液)可以得到原硅酸.
C.因为高温时,二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强.
D.二氧化硅是酸性氧化物,它不溶于任何酸
2.硅酸钠溶液俗称水玻璃,呈碱性.下列物质中,能用带磨口玻璃塞的试剂瓶盛放的是( )
A.浓硫酸 B.水玻璃 C.氢氟酸 D 苛性碱
3.下列物质中能跟SiO2发生反应的是( )
A 盐酸 B 硝酸 C 硫酸 D 烧碱溶液
4.光纤通讯是光作为信息的载体,让光在光导纤维中传输,制造光导纤维的基本原料是( )
A 铜 B 钢 C 石英 D 铝
5.除去二氧化硅固体中混有的CaCO3固体,方法正确的是( )
A 加水,过滤 B 加热
C 加盐酸,过滤 D 加NaOH溶液,过滤
必修一 第四章
无机非金属材料的主角——硅
晶体硅
二氧化硅
硅胶
1.1硅的原子结构示意图
硅原子和碳原子的最外电子层均有4个电子,其原子既不易失去也不易得到电子,主要形成四价的化合物。
Si
+14
8
4
2
+6
4
2
C
1硅元素与硅单质
结构决定性质
1.2硅的结构、物理性质和用途
晶体硅
1硅元素与硅单质
导电性介于导体和绝缘体之间
Mohs hardness莫氏硬度 6.5
Melting point熔点 1414 °C
Boiling point沸点 3265 °C
灰黑色、有金属光泽、硬而脆的固体
太阳能电池
计算机芯片
半导体材料
性质决定用途
1.3.2在高温条件下,单质硅能与O2和Cl2等非金属单质反应。
1.3.1常温下化学性质不活泼,只能跟F2、HF和 NaOH溶液反应。
Si+4HF=SiF4↑+2H2↑
Si+2NaOH+H2O=Na2SiO3+2H2↑
Si+O2 SiO2
Si + 2Cl2 ==== SiCl4
1.3硅的化学性质
1硅元素与硅单质
Si是否具有两性?
SiO2(石英砂)+2C(焦炭)=Si(粗硅)+2CO↑ ①
高温
SiCl4+2H2=Si(纯)+4HCl ③
高温
Si(粗)+2Cl2=SiCl4(l) ②
1.4硅的工业制法
1硅元素与硅单质
电炉
课本p81
1焦炭的作用?
2“从沙滩到用户”
结晶形和无定形。通称硅石。
石英
水晶
紫水晶
蔷薇石英
茶晶
黄水晶
2.1存在形态
2二氧化硅
水晶
开采注意粉尘
玛瑙
结晶形和无定形。通称硅石。
2.1存在形态
2二氧化硅
工艺品、饰品
2二氧化硅
实验仪器
2.2用途
光导纤维
2.3结构与物理性质
2二氧化硅
Melting point熔点 1,713 °C
Boiling point沸点 2,950 °C
SiO2是由Si和O按1:2的比例组成的立体空间网状结构,没有SiO2 分子存在,只存在硅氧原子。 因此性质很稳定
很不活泼,氢氟酸( HF)是唯一与之反应的酸。
SiO2+4HF=SiF4?+2H2O
1.玻璃中含有SiO2,用HF来刻蚀玻璃。
2.4.1特性
2.4化学性质
2二氧化硅
性质决定用途
2.实验室能不能用玻璃瓶盛装氢氟酸。
2.4.2酸性氧化物
SiO2 + 2NaOH = Na2SiO3 +H2O
硅酸钠(粘合剂)
不能用磨口玻璃塞盛碱性溶液,如NaOH、KOH、Na2CO3、Na2SiO3等溶液。
应用
应用
SiO2+ CaO === CaSiO3
高温
某同学根据SiO2既可与碱反应,也能与氢氟酸反应,推断SiO2为两性氧化物,是否正确?
?Na2CO3+SiO2===Na2SiO3+CO2↑
CaCO3 +SiO2 === CaSiO3 + CO2↑
高温
高温
SiO2 + 2C = Si + 2CO↑
高温
高沸点制低沸点——普通玻璃
2.4.3高沸点
2.4化学性质
2二氧化硅
性质决定用途
2.4.4弱氧化性
硅酸是一种白色粉末状的固体,它不溶于水;
H2SiO3
3.1物理性质
3硅酸
性质决定用途
H2SiO3 + 2NaOH == Na2SiO3 + 2H2O
3.2.2不稳定(比H2CO3稳定),受热易分解
?
H2SiO3 == H2O + SiO2
3.2.1一种很弱的酸,不能使指示剂变色、只能与强碱发生中和反应
3.2化学性质
3.3用途
3.3.1硅胶多孔,吸附水份能力强,常用作实验室和袋装食品、瓶装药品等的干燥剂。
3.3.2也可以用作催化剂的载体。
现 象
结 论
方程式
离子
方程式
①滴入酚酞溶液呈红色
Na2SiO3+2HCl = H2SiO3(胶体)+2NaCl
②再滴入稀盐酸,溶液红色变浅至无色,有透明胶冻状物质产生
SiO32- + 2H+ == H2SiO3 (胶体)
a、Na2SiO3溶液呈碱性,b、可溶性
硅酸盐与盐酸反应生成不溶于水的硅酸,
c、先形成硅酸溶胶,后形成硅酸凝胶
3.4制备方法
3硅酸
1、定义:
由硅、氧和金属组成的化合物的总称
2、性质:
硅酸盐种类很多,是一大类结构复杂的固态物质,大多数不溶于水,化学性质很稳定。
3、表示方法:
(1)化学式法:
Na2SiO3,CaSiO3
4.1表示方法
4硅酸盐
(2)氧化物法:
活泼金属氧化物→较活泼金属氧化物→二氧化硅→水
高岭石:Al2(Si2O5)(OH)4
Al2O3·2SiO2·2H2O
正长石:KAlSi3O8
硅酸钠是白色固体,可溶于水,其水溶液俗称水玻璃。
4.2硅酸钠(Na2SiO3)物理性质、用途
4硅酸盐
用途
1制备硅胶
2作肥皂填料
3做建筑、纸张的黏合剂
4木材、织物的防腐剂及防火剂
4.3硅酸钠(Na2SiO3)化学性质
4硅酸盐
②与盐反应
①与酸反应
Na2SiO3 + 2HCl =2NaCl + H2SiO3↓
CaCl2+Na2SiO3=CaSiO3↓+2NaCl
无机非金属材料
硅酸盐产品
陶瓷
水泥
玻璃
粘土
黏土和石灰石
硅酸三钙(3CaO·SiO2)
硅酸二钙(2CaO·SiO2) 混合物
铝酸三钙(3CaO·Al2O3)
陶都江苏宜兴 瓷都江西景德镇
CHINA
水硬性
具有抗氧化、抗酸碱腐蚀、耐高温、绝缘、易成型
有色玻璃
钢化玻璃
纯碱、石灰石和石英
?Na2CO3+SiO2===Na2SiO3+CO2↑
CaCO3 +SiO2===CaSiO3 + CO2↑
高温
高温
无固定的熔沸点,
在一定温度范围内软化
5硅酸盐工业
5.1传统无机非金属材料
5硅酸盐工业
Silicon carbide碳化硅(金刚砂)SiC
具有金刚石结构、硬度大,用作砂纸、砂轮的磨料。
Melting point熔点 2,830 °C
Solubility:Insoluble in water
5.2新型无机非金属材料
5硅酸盐工业
硅橡胶耐高温、低温 -60—250℃
高弹性(火箭、导弹、飞机的零件和绝缘材料)
5.2新型无机非金属材料
5硅酸盐工业
分子筛:具有均匀微孔结构的铝硅酸盐
用作吸附剂、催化剂
Molecular sieve
5.2新型无机非金属材料
新型陶瓷
高温结构陶瓷、压电陶瓷
透明陶瓷、超导陶瓷等
5硅酸盐工业
5.2新型无机非金属材料
人造骨骼
氮化硅陶瓷在1200℃左右的高温下,仍具有很高的强度,
可用来制造汽轮机叶片、轴承、永久性模具等。
5硅酸盐工业
5.2新型无机非金属材料
Silicon nitride氮化硅陶瓷
Melting point熔点:1,900 °C
F-117是一种单座战斗轰炸机。设计目的是凭隐身性能,突破敌火力网,压制敌方防空系统,摧毁严密防守的指挥所、战略要地、重要工业目标,还可执行侦察任务,具有一定空战能力。
练习:
1.下列说法正确的是( )
A.二氧化硅溶于水显酸性
B.二氧化碳通入水玻璃(Na2SiO3的水溶液)可以得到原硅酸.
C.因为高温时,二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强.
D.二氧化硅是酸性氧化物,它不溶于任何酸
2.硅酸钠溶液俗称水玻璃,呈碱性.下列物质中,能用带磨口玻璃塞的试剂瓶盛放的是( )
A.浓硫酸 B.水玻璃 C.氢氟酸 D 苛性碱
3.下列物质中能跟SiO2发生反应的是( )
A 盐酸 B 硝酸 C 硫酸 D 烧碱溶液
4.光纤通讯是光作为信息的载体,让光在光导纤维中传输,制造光导纤维的基本原料是( )
A 铜 B 钢 C 石英 D 铝
5.除去二氧化硅固体中混有的CaCO3固体,方法正确的是( )
A 加水,过滤 B 加热
C 加盐酸,过滤 D 加NaOH溶液,过滤
