仁爱湘教版九下化学 实验8 金属的性质 同步练习(含解析)
文档属性
| 名称 | 仁爱湘教版九下化学 实验8 金属的性质 同步练习(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 112.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-13 00:00:00 | ||
图片预览



文档简介
仁爱湘教版九年级下册化学训练 实验8 金属的性质
一、单选题
1.近来市场上出现了能补充人体盐分的饮品﹣﹣盐汽水,你认为盐汽水的成分和普通汽水最大的不同是增加了( )
A.?水?????????????????????????????????B.?氯化钠??????????????????????????????????C.?二氧化碳?????????????????????????????????D.?碳酸钙
2. 下列有关实验操作及分析均合理的是( )
A.?排水法收集O2:导气管口刚有气泡冒出立即收集,收集到的O2更纯净 B.?去除粗盐中难溶性杂质:将粗盐全部加入水中立即过滤,导致产率偏低 C.?测定空气里O2含量:点燃红磷慢慢伸入集气瓶并塞紧瓶塞,导致测定结果偏低 D.?探究CO2性质:将CO2快速倒入盛有燃着蜡烛的烧杯中,便于观察低处蜡烛先熄灭
3.在“粗盐的提纯”实验中,下列仪器用到的次数最多的是( )
A.?漏斗??????????????????????????????????B.?烧杯??????????????????????????????????C.?玻璃棒???????????????????????????????????D.?酒精灯
4. 某粗盐样品中除含有不溶性固体杂质外,可能还含有少量氯化镁、氯化钙、硫酸钠.某化学兴趣小组开展如下探究活动:
探究一:除去粗盐中不溶性杂质
探究二:从滤液1中提取氯化钠固体(该探究中,微溶物不沉淀)
关于以上探究活动,有下列说法:
①试剂甲是碳酸钠溶液,试剂乙是氯化钡溶液
②滤液1中的溶质一定有氯化钠,可能有氯化钙
③若向探究二所得的白色滤渣中加入过量的稀盐酸,滤渣不溶解
④往滤液4中加入适量的试剂丙时有中和反应发生
上述说法中正确的是(? )
A.?①③?????????????????????????????????????B.?①④?????????????????????????????????????C.?②③?????????????????????????????????????D.?②④
5.如图是利用海水提取粗盐的过程,下列说法中错误的是( )
A.?图中①是结晶池???????????????????????????????????????B.?图中②的操作过程是溶解、过滤、结晶 C.?析出晶体后的母液是氯化钠的饱和溶液????D.?蒸发池是利用氯化钠的溶解度受温度影响变化大的原理
6.除去难溶性杂质后的食盐中往往含有少量的Na2SO4、MgCl2、CaCl2等杂质,为了将这些杂质除去,可向食盐溶液中加入过量的NaOH、Na2CO3、BaCl2溶液,然后过滤除去沉淀,再加入盐酸调至溶液pH=7,最后蒸发得到精盐.下列操作及加入溶液顺序不正确的是(?? )
A.?BaCl2、Na2CO3、NaOH、过滤、HCl???????????????B.?BaCl2、NaOH、Na2CO3、过滤、HCl C.?Na2CO3、BaCl2、NaOH、过滤、HCl???????????????D.?NaOH、BaCl2、Na2CO3、过滤、HCl
7. 根据实践经验,你认为下列课外实验不能成功的是(?? )
A.?用灼烧法鉴别羊毛和化纤????????????????????????????????????B.?用肥皂水鉴别硬水和软水 C.?用食盐水制作叶脉书签???????????????????????????????????????D.?用紫甘蓝和酒精溶液制酸碱指示剂
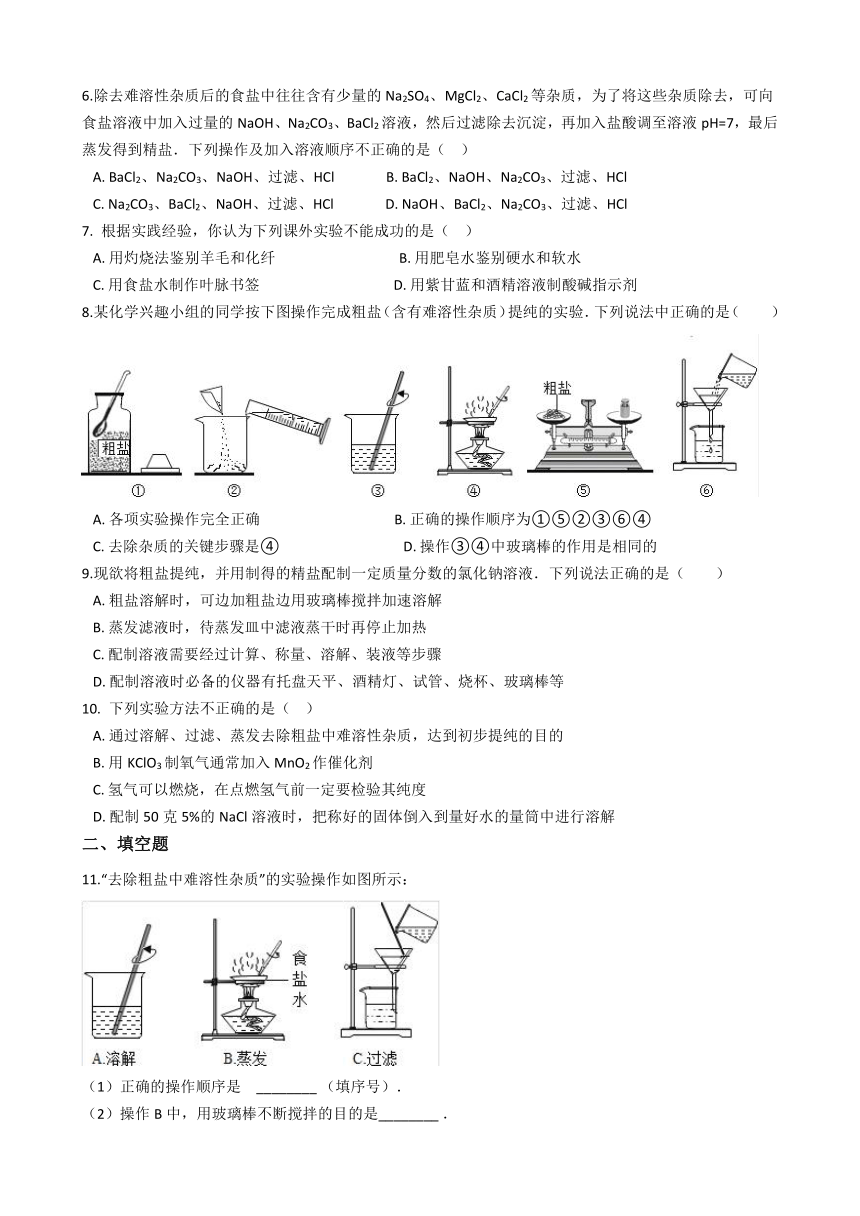
8.某化学兴趣小组的同学按下图操作完成粗盐(含有难溶性杂质)提纯的实验.下列说法中正确的是( )
A.?各项实验操作完全正确???????????????????????????????????????B.?正确的操作顺序为①⑤②③⑥④ C.?去除杂质的关键步骤是④????????????????????????????????????D.?操作③④中玻璃棒的作用是相同的
9.现欲将粗盐提纯,并用制得的精盐配制一定质量分数的氯化钠溶液.下列说法正确的是( )
A.?粗盐溶解时,可边加粗盐边用玻璃棒搅拌加速溶解 B.?蒸发滤液时,待蒸发皿中滤液蒸干时再停止加热 C.?配制溶液需要经过计算、称量、溶解、装液等步骤 D.?配制溶液时必备的仪器有托盘天平、酒精灯、试管、烧杯、玻璃棒等
10. 下列实验方法不正确的是(?? )
A.?通过溶解、过滤、蒸发去除粗盐中难溶性杂质,达到初步提纯的目的 B.?用KClO3制氧气通常加入MnO2作催化剂 C.?氢气可以燃烧,在点燃氢气前一定要检验其纯度 D.?配制50克5%的NaCl溶液时,把称好的固体倒入到量好水的量筒中进行溶解
二、填空题
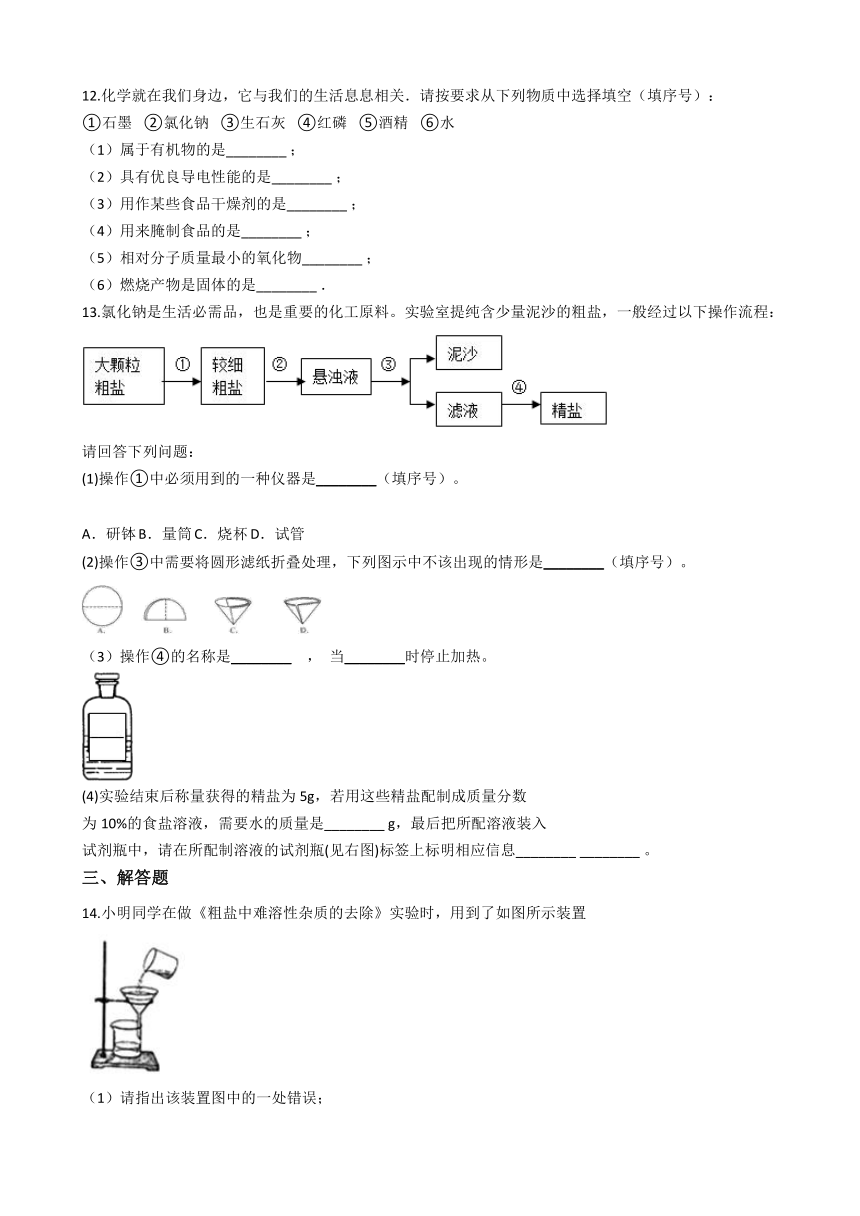
11.“去除粗盐中难溶性杂质”的实验操作如图所示: (1)正确的操作顺序是 ________?(填序号). (2)操作B中,用玻璃棒不断搅拌的目的是________?.
12.化学就在我们身边,它与我们的生活息息相关.请按要求从下列物质中选择填空(填序号): ①石墨? ②氯化钠? ③生石灰? ④红磷? ⑤酒精? ⑥水 (1)属于有机物的是________?;??????? (2)具有优良导电性能的是________?; (3)用作某些食品干燥剂的是________?;? (4)用来腌制食品的是________?; (5)相对分子质量最小的氧化物________?; (6)燃烧产物是固体的是________?.
13.氯化钠是生活必需品,也是重要的化工原料。实验室提纯含少量泥沙的粗盐,一般经过以下操作流程: 请回答下列问题: (1)操作①中必须用到的一种仪器是________(填序号)。
A.研钵
B.量筒
C.烧杯
D.试管
(2)操作③中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是________(填序号)。 (3)操作④的名称是________ , 当________时停止加热。 (4)实验结束后称量获得的精盐为5g,若用这些精盐配制成质量分数 为10%的食盐溶液,需要水的质量是________?g,最后把所配溶液装入 试剂瓶中,请在所配制溶液的试剂瓶(见右图)标签上标明相应信息________?________?。
三、解答题
14.小明同学在做《粗盐中难溶性杂质的去除》实验时,用到了如图所示装置
(1)请指出该装置图中的一处错误;
(2)改进装置后过滤,发现滤液仍然浑浊,其原因可能是什么?(写出一条即可)
(3)经初步提纯所得精盐是否为纯净物?请写出你的判断和理由.
四、综合题
15.某化学兴趣小组进行粗盐提纯、溶液配制实验的探究.
(1)粗盐提纯的实验操作步骤为________、________、蒸发,在蒸发操作中,玻璃棒的作用是________。
(2)用得到的精盐配制100g质量分数为2%的氯化钠溶液.
①计算:需要氯化钠固体的质量为________g;水的体积为________mL(水的密度近似看作1g/cm3)
②称量:用托盘天平称得所需质量的氯化钠并转移到烧杯中.③量取:用到的玻璃仪器有________ 、________。在量取水的过程中,如果仰视读数,则配制得到的氯化钠溶液中氯化钠的质量分数 ________(填“大于”或“小于”或“等于”)2%
④溶解:用________搅拌,作用是________ 。
16.粗盐提纯的基本操作步骤是:①溶解、②、③、④转移并计算精盐产率.
(1)操作②的名称是________,目的是________,该操作过程中玻璃棒的作用是________.
(2)操作③的过程中停止加热的最佳时刻为________.
答案解析部分
一、单选题
1.【答案】 B
【解析】【解答】根据题意,近来市场上出现了能补充人体盐分的饮品﹣﹣盐汽水,该饮料能及时补充大量运动所流失的水分和盐分,可知该饮料与普通汽水的不同是增加了盐.
A、水是氧化物,不属于盐,故选项错误;
B、氯化钠属于盐,易溶于水,可用于制作补充人体盐分的饮品﹣﹣盐汽水,故选项正确;
C、二氧化碳是氧化物,不属于盐,故选项错误;
D、碳酸钙属于盐,但难溶于水,故选项错误;
故选:B.
【分析】近来市场上出现了能补充人体盐分的饮品﹣﹣盐汽水,该饮料能及时补充大量运动所流失的水分和盐分,可知该饮料与普通汽水的不同是增加了盐,据此进行分析判断.
2.【答案】 B
【解析】【解答】解:A、导管口刚有气泡冒出立即收集,此时收集的气体中混有空气,会影响气体的性质实验,故错误;
B、去除粗盐中难溶性杂质:将粗盐全部加入水中,立即过滤,可能没有全部溶解,导致产率偏低,正确;
C、由于插入燃烧匙太慢,在塞紧瓶塞之前,瓶内部分空气受热逸出,使瓶内的气体除氧气之外的气体也跑到了瓶外,会导致液体水面上升超过;
D、探究CO2性质:将CO2慢慢倒入盛有燃着蜡烛的烧杯中,便于观察低处蜡烛先熄灭,故错误;
答案:B.
【分析】A、根据刚有气泡冒出时,收集的气体不纯解答;
B、根据去除粗盐中难溶性杂质:将粗盐全部加入水中,立即过滤,可能没有全部溶解解答;
C、根据由于插入燃烧匙太慢,在塞紧瓶塞之前,瓶内部分空气受热逸出,使瓶内的气体除氧气之外的气体也跑到了瓶外解答;
D、根据探究CO2性质:将CO2慢慢倒入盛有燃着蜡烛的烧杯中解答.
3.【答案】 C
【解析】【解答】解:根据精盐提纯实验的步骤确定每步中用到的仪器:溶解:烧杯、玻璃棒;过滤:漏斗、烧杯、玻璃棒、铁架台带铁圈;蒸发:蒸发皿、玻璃棒、铁架台带铁圈、酒精灯.因此用到次数最多的是玻璃棒,每步操作中都用到.
故选C
【分析】根据精盐提纯的步骤进行解答.精盐提纯步骤是溶解、过滤、蒸发
4.【答案】 D
【解析】【解答】解:某粗盐样品中除含有不溶性固体杂质外,可能还含有少量氯化镁、氯化钙、硫酸钠.溶解过滤的滤液1,则滤液1一定有氯化钠.
往滤液1中加过量的氢氧化钠溶液,若含氢氧化钠溶液和氯化镁反应生成氢氧化镁沉淀和氯化钠,无明显现象,说明没有氯化镁.
硫酸根离子可用钡离子来除去,钙离子可用碳酸根离子来除去,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡.往滤液2中加过量的试剂甲,试剂甲是氯化钡溶液,试剂乙是碳酸钠溶液;由反应现象是无明显现象,说明不含硫酸钠.
往滤液3中加过量的试剂乙(碳酸钠溶液),出现白色沉淀,可能是过量的氯化钡与碳酸钠溶液反应生成白色沉淀,也可能是氯化钙与碳酸钠反应生成白色沉淀,滤液1中的溶质一定有氯化钠,可能有氯化钙.
若向探究二所得的白色滤渣中加入过量的稀盐酸,由于不存在硫酸钠,沉淀可能是碳酸钡或碳酸钙,加入过量的稀盐酸,滤渣全部溶解.
往滤液4中加入适量的试剂丙,丙应为稀盐酸,过量的氢氧化钠语言稀盐酸反应生成氯化钠和水,属于中和反应.
由上述分析,②④说法正确.
故选:D.
【分析】根据某粗盐样品中除含有不溶性固体杂质外,可能还含有少量氯化镁、氯化钙、硫酸钠.溶解过滤的滤液1,则滤液1一定有氯化钠.
根据氢氧化钠溶液和氯化镁反应生成氢氧化镁沉淀和氯化钠;硫酸根离子可用钡离子来除杂,钙离子可用碳酸根离子来除杂,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀;完全反应后,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,据此进行分析解答.
本题难度较大,考查了粗盐提纯中离子的除杂,除去多种杂质离子时,要考虑除杂的顺序、后面加入的试剂要能除去前面加入的过量的试剂.
5.【答案】 D
【解析】【解答】A、氯化钠的溶解度受温度影响变化不大,可用蒸发结晶的方法进行分离,故图中①是结晶池,故A正确;
B、粗盐中含有泥沙等难溶性杂质,所以图中②的操作过程是溶解、过滤、结晶,得到氯化钠晶体,故B正确;
C、析出晶体后的母液是氯化钠的饱和溶液,故C正确;
D、氯化钠的溶解度受温度影响变化不大,可用蒸发结晶的方法进行分离,而不是氯化钠的溶解度受温度影响变化大的原理,故D错误.
故选:D.
【分析】根据海水晒盐的原理是:利用阳光和风力的作用,使水不断蒸发,氯化钠溶液越来越浓,当水蒸发到一定程度时,形成氯化钠的饱和溶液,再继续蒸发时,就会有氯化钠晶体析出进行解答.
6.【答案】C
【解析】【解答】解:镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,如果加反了,过量的钡离子就没法除去;离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,除去CaCl2用的是碳酸钠溶液,所以碳酸钠必须放在氯化钡之后,故选:C.
【分析】根据镁离子会与氢氧根离子和碳酸根离子生成沉淀,钙离子会与碳酸根离子生成沉淀,硫酸根离子会与钡离子生成沉淀,加入盐酸可以除去过量的碳酸钠和氢氧化钠等进行分析.
7.【答案】C
【解析】【解答】解:A、羊毛和化纤属于蛋白质,在燃烧时有烧焦羽毛气味,故A正确;
B、用肥皂水可以鉴别硬水和软水,泡沫多的是软水,泡沫少的是硬水,故B正确;
C、叶脉书签就是除去表皮和叶肉组织,而只由叶脉做成;植物的叶、叶脉由坚韧的纤维素构成,在碱液中不易煮烂,而叶脉四周的叶肉在碱液中容易煮烂,食盐不具有碱性,故不能制作叶脉书签,故C错误;
D、由于紫甘蓝的汁液在不同的酸碱性溶液中会出现不同的颜色,所以酒精浸泡捣烂的紫甘蓝可制酸碱指示剂,故D正确.
故选C.
【分析】A、根据蛋白质的特点考虑;
B、根据软水和硬水的鉴别方法考虑;
C、叶脉书签就是除去表皮和叶肉组织,而只由叶脉做成;植物的叶、叶脉由坚韧的纤维素构成,在碱液中不易煮烂,而叶脉四周的叶肉在碱液中容易煮烂;
D、紫甘蓝的汁液在不同的酸碱性溶液中会出现不同的颜色,所以能作指示剂.
8.【答案】 B
【解析】【解答】A、⑥过滤操作中需要玻璃棒引流,故A错误;
B、粗盐提纯的步骤为:①从瓶内取出粗盐样品,⑤称取粗盐样品,②加入量取好的水,③溶解,⑥过滤,④蒸发,所以正确的操作顺序为:①⑤②③⑥④,故B正确;
C、粗盐提纯的关键操作是过滤,故C错误;
D、操作③中玻璃棒的作用是加速溶解,操作④中玻璃棒搅拌,防止局部过热,造成液滴飞溅,故D错误;
故选:B.
【分析】A、根据粗盐提纯的正确操作进行分析;
B、根据粗盐提纯的步骤为:①从瓶内取出粗盐样品,⑤称取粗盐样品,②加入量取好的水,③溶解,⑥过滤,④蒸发进行分析;
C、根据粗盐提纯的关键操作是过滤进行分析;
D、根据玻璃棒在粗盐提纯中的作用进行分析.
9.【答案】 C
【解析】【解答】解:A、当需要固体和液体加到一个容器内时,先固体后液体,防止迸溅,所以“粗盐溶解时,用药匙将粗盐逐渐加入水中,边加边用玻璃棒搅拌以加速溶解”错误,故A错误;
B、蒸发滤液时,待蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干;故B错误;
C、配制溶液需要经过计算、称量(称固体,量液体)、溶解、装液等步骤,故C正确;
D、配制溶液时必备的仪器有托盘天平、量筒、烧杯、玻璃棒等,不需要酒精灯,故说法错误;
故选C.
【分析】A、当需要固体和液体加到一个容器内时,先固体后液体,防止迸溅;
B、蒸发滤液时,待蒸发皿中出现较多固体时,便应停止加热,利用余热蒸干;
C、配制溶液需要经过计算、称量、溶解、装液等步骤;
D、配制溶液时必备的仪器有托盘天平、量筒、烧杯、玻璃棒等.
10.【答案】D
【解析】【解答】解:A、粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐)得到精盐的过程,故选项实验方法正确.
B、用KClO3制氧气通常加入MnO2作催化剂,能加快反应速率,故选项实验方法正确.
C、氢气可以燃烧,具有可燃性,为防止发生爆炸,在点燃氢气前一定要检验其纯度,故选项实验方法正确.
D、配制50克5%的NaCl溶液时,把称好的固体倒入到量好水的烧杯中进行溶解,不能在量筒内进行溶解操作,故选项实验方法错误.
故选:D.
【分析】A、根据粗盐提纯是将粗盐中含有的泥沙等不溶物除去,进行分析判断.
B、根据实验室制取氧气的反应原理,进行分析判断.
C、根据可燃性气体与空气混合后点燃可能发生爆炸,进行分析判断.
D、根据溶解操作的方法,进行分析判断.
二、填空题
11.【答案】ACB;搅拌,使液体受热均匀
【解析】【解答】(1)粗盐的主要成分是氯化钠,氯化钠易溶于水,盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程),故正确的操作顺序是ACB. (2)B操作是蒸发操作,蒸发操作中,玻璃棒起到搅拌而使液体受热均匀,以防液体受热不均匀,造成液体飞溅. 故答案为:(1)ACB;(2)搅拌,使液体受热均匀. 【分析】(1)粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程),进行分析判断; (2)B操作是蒸发操作,由蒸发操作中玻璃棒的作用,进行分析解答.
12.【答案】⑤;①;③;②;⑥;④
【解析】【解答】解:(1)酒精,学名叫乙醇,含有碳元素的化合物,属于有机物; (2)石墨是一种具有优良导电性能的碳的单质; (3)生石灰能与水反应生成熟石灰,可以做干燥剂; (4)氯化钠一种盐,可以做调味品,用来腌制食品; (5)氢元素是相对原子质量最小的元素,因此水是相对分子质量最小的氧化物; (6)磷在空气中燃烧生成白色的五氧化二磷固体. 故答案为:(1)⑤;(2)①;(3)③;(4)②;(5)⑥;(6)④. 【分析】可以从物质的性质着手分析物质的用途,酒精属于有机物;石墨具有很好的导电性;生石灰能与水反应生成氢氧化钙;氯化钠是一种常用的调味品;氢是相对原子质量最小的元素;红磷燃烧后生成的五氧化二磷是固体.
13.【答案】A ;D ;蒸发 ;出现较多固体 ;45g ;氯化钠溶液 ;10%
【解析】【解答】(1)根据图示操作,结合选项分析,由于操作①是将大颗粒粗盐变成较细的粗盐,故需研钵来研磨,而量筒只能用来量取液体的体积,烧杯一般被用来做大量液体的反应容器,试管则可用来加热少量的液体等用途,这三种仪器都不能用来研磨。故选A (2)A、B、C 是滤纸的正确的折叠方法的步骤,而D中的滤纸,在接口处出现缝隙,过滤时,待滤液会直接从此处进入下面的烧杯,影响过滤效果,错误。故选D (3)根据题意,操作④是将氯化钠溶液变为氯化钠晶体,故为蒸发结晶;当蒸发皿中出现较多固体时,应停止加热,要利用余热将其蒸干。 (4)根据溶质质量分数计算公式:溶质质量分数=×100%可知,溶液质量=溶质质量÷溶质质量分数,故5g食盐可配制10%的食盐溶液=5g÷10%=50g,所以需要水的质量=50g-5g=45g。根据题意,标签上标明氯化钠的名称、化学式和溶质质量分数即可。 【分析】本题主要考查了有关粗盐提纯的实验的相关知识,难度不大,只要同学们在平时的学习中注意相关基础知识和基本技能的积累和储备,即可轻松解答。
三、解答题
14.【答案】(1)缺少玻璃棒引流 (2)滤纸破损(或滤液高于滤纸边缘或盛接滤液的烧杯不干净等) (3)不是纯净物;精盐中含有氯化钠、氯化钙、氯化镁等。
【解析】【解答】解:(1)过滤液体时,注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流; (2)过滤后发现滤液仍然浑浊,可能原因是滤纸破损(会使得液体中的不溶物进入下面的烧杯,从而使得滤液浑浊)、液面高于滤纸边缘(会使部分液体未经过滤纸的过滤直接流下,该操作会使滤液仍然浑浊)或盛接滤液的烧杯不干净等; (3)经初步提纯所得精盐中含有氯化钠、氯化钙、氯化镁等多种物质,属于混合物. 故答案为:(1)缺少玻璃棒引流;(2)滤纸破损(或滤液高于滤纸边缘或盛接滤液的烧杯不干净等);(3)不是纯净物;精盐中含有氯化钠、氯化钙、氯化镁等.
【分析】(1)过滤液体时,要遵循“一贴、二低、三靠”的原则; (2)过滤液体时,要遵循“一贴、二低、三靠”的原则,凡是不经滤纸的过滤就直接进入滤液的操作,都能造成滤液浑浊;另外接滤液的烧杯不干净也会造成同样的结果; (3)经初步提纯所得精盐中含有氯化钠、氯化钙、氯化镁等.
四、综合题
15.【答案】(1)溶解;过滤;搅拌,防止因局部温度过高,造成液滴飞溅 (2)2;98;量筒;胶头滴管;小于;玻璃棒;加速溶解
【解析】【解答】(1)粗盐提纯的实验操作步骤为溶解、过滤、蒸发,在蒸发操作中,玻璃棒的作是搅拌,防止因局部温度过高,造成液滴飞溅;(2)①需要氯化钠固体的质量为100g×2%=2g;需要水的体积为(100g-2g)÷1g/cm3=98mL;③量取过程中用到的玻璃仪器有量筒、胶头滴管。在量取水的过程中,如果仰视读数,所得数据偏小,量筒中水的体积偏大。则配制得到的氯化钠溶液中氯化钠的质量分数小于2%;④溶解过程中用玻璃棒搅拌,作用是加速溶解。
【分析】根据盐提纯的实验操作步骤为溶解、过滤、蒸发分析;根据一定溶质质量分数的溶液配制方法分析,其中在量取水的过程中,如果仰视读数,所得数据偏小,量筒中水的体积偏大。
16.【答案】(1)过滤;除去不溶性物质;引流 (2)待蒸发皿中出现较多量的固体时
【解析】【解答】解:(1)粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程)、转移并计算精盐产率,则操作②的名称是过滤,以除去除去不溶性物质;该操作过程中玻璃棒的作用是引流.(2)蒸发时,待蒸发皿中出现较多量的固体时,应停止加热,利用余热将剩余液体蒸干.故答案为:(1)过滤;除去不溶性物质;引流;(2)待蒸发皿中出现较多量的固体时.
【分析】(1)根据粗盐提纯是将粗盐中含有的泥沙等不溶物除去,进行分析解答.(2)根据蒸发操作中停止加热的时机,进行分析解答.
一、单选题
1.近来市场上出现了能补充人体盐分的饮品﹣﹣盐汽水,你认为盐汽水的成分和普通汽水最大的不同是增加了( )
A.?水?????????????????????????????????B.?氯化钠??????????????????????????????????C.?二氧化碳?????????????????????????????????D.?碳酸钙
2. 下列有关实验操作及分析均合理的是( )
A.?排水法收集O2:导气管口刚有气泡冒出立即收集,收集到的O2更纯净 B.?去除粗盐中难溶性杂质:将粗盐全部加入水中立即过滤,导致产率偏低 C.?测定空气里O2含量:点燃红磷慢慢伸入集气瓶并塞紧瓶塞,导致测定结果偏低 D.?探究CO2性质:将CO2快速倒入盛有燃着蜡烛的烧杯中,便于观察低处蜡烛先熄灭
3.在“粗盐的提纯”实验中,下列仪器用到的次数最多的是( )
A.?漏斗??????????????????????????????????B.?烧杯??????????????????????????????????C.?玻璃棒???????????????????????????????????D.?酒精灯
4. 某粗盐样品中除含有不溶性固体杂质外,可能还含有少量氯化镁、氯化钙、硫酸钠.某化学兴趣小组开展如下探究活动:
探究一:除去粗盐中不溶性杂质
探究二:从滤液1中提取氯化钠固体(该探究中,微溶物不沉淀)
关于以上探究活动,有下列说法:
①试剂甲是碳酸钠溶液,试剂乙是氯化钡溶液
②滤液1中的溶质一定有氯化钠,可能有氯化钙
③若向探究二所得的白色滤渣中加入过量的稀盐酸,滤渣不溶解
④往滤液4中加入适量的试剂丙时有中和反应发生
上述说法中正确的是(? )
A.?①③?????????????????????????????????????B.?①④?????????????????????????????????????C.?②③?????????????????????????????????????D.?②④
5.如图是利用海水提取粗盐的过程,下列说法中错误的是( )
A.?图中①是结晶池???????????????????????????????????????B.?图中②的操作过程是溶解、过滤、结晶 C.?析出晶体后的母液是氯化钠的饱和溶液????D.?蒸发池是利用氯化钠的溶解度受温度影响变化大的原理
6.除去难溶性杂质后的食盐中往往含有少量的Na2SO4、MgCl2、CaCl2等杂质,为了将这些杂质除去,可向食盐溶液中加入过量的NaOH、Na2CO3、BaCl2溶液,然后过滤除去沉淀,再加入盐酸调至溶液pH=7,最后蒸发得到精盐.下列操作及加入溶液顺序不正确的是(?? )
A.?BaCl2、Na2CO3、NaOH、过滤、HCl???????????????B.?BaCl2、NaOH、Na2CO3、过滤、HCl C.?Na2CO3、BaCl2、NaOH、过滤、HCl???????????????D.?NaOH、BaCl2、Na2CO3、过滤、HCl
7. 根据实践经验,你认为下列课外实验不能成功的是(?? )
A.?用灼烧法鉴别羊毛和化纤????????????????????????????????????B.?用肥皂水鉴别硬水和软水 C.?用食盐水制作叶脉书签???????????????????????????????????????D.?用紫甘蓝和酒精溶液制酸碱指示剂
8.某化学兴趣小组的同学按下图操作完成粗盐(含有难溶性杂质)提纯的实验.下列说法中正确的是( )
A.?各项实验操作完全正确???????????????????????????????????????B.?正确的操作顺序为①⑤②③⑥④ C.?去除杂质的关键步骤是④????????????????????????????????????D.?操作③④中玻璃棒的作用是相同的
9.现欲将粗盐提纯,并用制得的精盐配制一定质量分数的氯化钠溶液.下列说法正确的是( )
A.?粗盐溶解时,可边加粗盐边用玻璃棒搅拌加速溶解 B.?蒸发滤液时,待蒸发皿中滤液蒸干时再停止加热 C.?配制溶液需要经过计算、称量、溶解、装液等步骤 D.?配制溶液时必备的仪器有托盘天平、酒精灯、试管、烧杯、玻璃棒等
10. 下列实验方法不正确的是(?? )
A.?通过溶解、过滤、蒸发去除粗盐中难溶性杂质,达到初步提纯的目的 B.?用KClO3制氧气通常加入MnO2作催化剂 C.?氢气可以燃烧,在点燃氢气前一定要检验其纯度 D.?配制50克5%的NaCl溶液时,把称好的固体倒入到量好水的量筒中进行溶解
二、填空题
11.“去除粗盐中难溶性杂质”的实验操作如图所示: (1)正确的操作顺序是 ________?(填序号). (2)操作B中,用玻璃棒不断搅拌的目的是________?.
12.化学就在我们身边,它与我们的生活息息相关.请按要求从下列物质中选择填空(填序号): ①石墨? ②氯化钠? ③生石灰? ④红磷? ⑤酒精? ⑥水 (1)属于有机物的是________?;??????? (2)具有优良导电性能的是________?; (3)用作某些食品干燥剂的是________?;? (4)用来腌制食品的是________?; (5)相对分子质量最小的氧化物________?; (6)燃烧产物是固体的是________?.
13.氯化钠是生活必需品,也是重要的化工原料。实验室提纯含少量泥沙的粗盐,一般经过以下操作流程: 请回答下列问题: (1)操作①中必须用到的一种仪器是________(填序号)。
A.研钵
B.量筒
C.烧杯
D.试管
(2)操作③中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是________(填序号)。 (3)操作④的名称是________ , 当________时停止加热。 (4)实验结束后称量获得的精盐为5g,若用这些精盐配制成质量分数 为10%的食盐溶液,需要水的质量是________?g,最后把所配溶液装入 试剂瓶中,请在所配制溶液的试剂瓶(见右图)标签上标明相应信息________?________?。
三、解答题
14.小明同学在做《粗盐中难溶性杂质的去除》实验时,用到了如图所示装置
(1)请指出该装置图中的一处错误;
(2)改进装置后过滤,发现滤液仍然浑浊,其原因可能是什么?(写出一条即可)
(3)经初步提纯所得精盐是否为纯净物?请写出你的判断和理由.
四、综合题
15.某化学兴趣小组进行粗盐提纯、溶液配制实验的探究.
(1)粗盐提纯的实验操作步骤为________、________、蒸发,在蒸发操作中,玻璃棒的作用是________。
(2)用得到的精盐配制100g质量分数为2%的氯化钠溶液.
①计算:需要氯化钠固体的质量为________g;水的体积为________mL(水的密度近似看作1g/cm3)
②称量:用托盘天平称得所需质量的氯化钠并转移到烧杯中.③量取:用到的玻璃仪器有________ 、________。在量取水的过程中,如果仰视读数,则配制得到的氯化钠溶液中氯化钠的质量分数 ________(填“大于”或“小于”或“等于”)2%
④溶解:用________搅拌,作用是________ 。
16.粗盐提纯的基本操作步骤是:①溶解、②、③、④转移并计算精盐产率.
(1)操作②的名称是________,目的是________,该操作过程中玻璃棒的作用是________.
(2)操作③的过程中停止加热的最佳时刻为________.
答案解析部分
一、单选题
1.【答案】 B
【解析】【解答】根据题意,近来市场上出现了能补充人体盐分的饮品﹣﹣盐汽水,该饮料能及时补充大量运动所流失的水分和盐分,可知该饮料与普通汽水的不同是增加了盐.
A、水是氧化物,不属于盐,故选项错误;
B、氯化钠属于盐,易溶于水,可用于制作补充人体盐分的饮品﹣﹣盐汽水,故选项正确;
C、二氧化碳是氧化物,不属于盐,故选项错误;
D、碳酸钙属于盐,但难溶于水,故选项错误;
故选:B.
【分析】近来市场上出现了能补充人体盐分的饮品﹣﹣盐汽水,该饮料能及时补充大量运动所流失的水分和盐分,可知该饮料与普通汽水的不同是增加了盐,据此进行分析判断.
2.【答案】 B
【解析】【解答】解:A、导管口刚有气泡冒出立即收集,此时收集的气体中混有空气,会影响气体的性质实验,故错误;
B、去除粗盐中难溶性杂质:将粗盐全部加入水中,立即过滤,可能没有全部溶解,导致产率偏低,正确;
C、由于插入燃烧匙太慢,在塞紧瓶塞之前,瓶内部分空气受热逸出,使瓶内的气体除氧气之外的气体也跑到了瓶外,会导致液体水面上升超过;
D、探究CO2性质:将CO2慢慢倒入盛有燃着蜡烛的烧杯中,便于观察低处蜡烛先熄灭,故错误;
答案:B.
【分析】A、根据刚有气泡冒出时,收集的气体不纯解答;
B、根据去除粗盐中难溶性杂质:将粗盐全部加入水中,立即过滤,可能没有全部溶解解答;
C、根据由于插入燃烧匙太慢,在塞紧瓶塞之前,瓶内部分空气受热逸出,使瓶内的气体除氧气之外的气体也跑到了瓶外解答;
D、根据探究CO2性质:将CO2慢慢倒入盛有燃着蜡烛的烧杯中解答.
3.【答案】 C
【解析】【解答】解:根据精盐提纯实验的步骤确定每步中用到的仪器:溶解:烧杯、玻璃棒;过滤:漏斗、烧杯、玻璃棒、铁架台带铁圈;蒸发:蒸发皿、玻璃棒、铁架台带铁圈、酒精灯.因此用到次数最多的是玻璃棒,每步操作中都用到.
故选C
【分析】根据精盐提纯的步骤进行解答.精盐提纯步骤是溶解、过滤、蒸发
4.【答案】 D
【解析】【解答】解:某粗盐样品中除含有不溶性固体杂质外,可能还含有少量氯化镁、氯化钙、硫酸钠.溶解过滤的滤液1,则滤液1一定有氯化钠.
往滤液1中加过量的氢氧化钠溶液,若含氢氧化钠溶液和氯化镁反应生成氢氧化镁沉淀和氯化钠,无明显现象,说明没有氯化镁.
硫酸根离子可用钡离子来除去,钙离子可用碳酸根离子来除去,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡.往滤液2中加过量的试剂甲,试剂甲是氯化钡溶液,试剂乙是碳酸钠溶液;由反应现象是无明显现象,说明不含硫酸钠.
往滤液3中加过量的试剂乙(碳酸钠溶液),出现白色沉淀,可能是过量的氯化钡与碳酸钠溶液反应生成白色沉淀,也可能是氯化钙与碳酸钠反应生成白色沉淀,滤液1中的溶质一定有氯化钠,可能有氯化钙.
若向探究二所得的白色滤渣中加入过量的稀盐酸,由于不存在硫酸钠,沉淀可能是碳酸钡或碳酸钙,加入过量的稀盐酸,滤渣全部溶解.
往滤液4中加入适量的试剂丙,丙应为稀盐酸,过量的氢氧化钠语言稀盐酸反应生成氯化钠和水,属于中和反应.
由上述分析,②④说法正确.
故选:D.
【分析】根据某粗盐样品中除含有不溶性固体杂质外,可能还含有少量氯化镁、氯化钙、硫酸钠.溶解过滤的滤液1,则滤液1一定有氯化钠.
根据氢氧化钠溶液和氯化镁反应生成氢氧化镁沉淀和氯化钠;硫酸根离子可用钡离子来除杂,钙离子可用碳酸根离子来除杂,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀;完全反应后,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,据此进行分析解答.
本题难度较大,考查了粗盐提纯中离子的除杂,除去多种杂质离子时,要考虑除杂的顺序、后面加入的试剂要能除去前面加入的过量的试剂.
5.【答案】 D
【解析】【解答】A、氯化钠的溶解度受温度影响变化不大,可用蒸发结晶的方法进行分离,故图中①是结晶池,故A正确;
B、粗盐中含有泥沙等难溶性杂质,所以图中②的操作过程是溶解、过滤、结晶,得到氯化钠晶体,故B正确;
C、析出晶体后的母液是氯化钠的饱和溶液,故C正确;
D、氯化钠的溶解度受温度影响变化不大,可用蒸发结晶的方法进行分离,而不是氯化钠的溶解度受温度影响变化大的原理,故D错误.
故选:D.
【分析】根据海水晒盐的原理是:利用阳光和风力的作用,使水不断蒸发,氯化钠溶液越来越浓,当水蒸发到一定程度时,形成氯化钠的饱和溶液,再继续蒸发时,就会有氯化钠晶体析出进行解答.
6.【答案】C
【解析】【解答】解:镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,如果加反了,过量的钡离子就没法除去;离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,除去CaCl2用的是碳酸钠溶液,所以碳酸钠必须放在氯化钡之后,故选:C.
【分析】根据镁离子会与氢氧根离子和碳酸根离子生成沉淀,钙离子会与碳酸根离子生成沉淀,硫酸根离子会与钡离子生成沉淀,加入盐酸可以除去过量的碳酸钠和氢氧化钠等进行分析.
7.【答案】C
【解析】【解答】解:A、羊毛和化纤属于蛋白质,在燃烧时有烧焦羽毛气味,故A正确;
B、用肥皂水可以鉴别硬水和软水,泡沫多的是软水,泡沫少的是硬水,故B正确;
C、叶脉书签就是除去表皮和叶肉组织,而只由叶脉做成;植物的叶、叶脉由坚韧的纤维素构成,在碱液中不易煮烂,而叶脉四周的叶肉在碱液中容易煮烂,食盐不具有碱性,故不能制作叶脉书签,故C错误;
D、由于紫甘蓝的汁液在不同的酸碱性溶液中会出现不同的颜色,所以酒精浸泡捣烂的紫甘蓝可制酸碱指示剂,故D正确.
故选C.
【分析】A、根据蛋白质的特点考虑;
B、根据软水和硬水的鉴别方法考虑;
C、叶脉书签就是除去表皮和叶肉组织,而只由叶脉做成;植物的叶、叶脉由坚韧的纤维素构成,在碱液中不易煮烂,而叶脉四周的叶肉在碱液中容易煮烂;
D、紫甘蓝的汁液在不同的酸碱性溶液中会出现不同的颜色,所以能作指示剂.
8.【答案】 B
【解析】【解答】A、⑥过滤操作中需要玻璃棒引流,故A错误;
B、粗盐提纯的步骤为:①从瓶内取出粗盐样品,⑤称取粗盐样品,②加入量取好的水,③溶解,⑥过滤,④蒸发,所以正确的操作顺序为:①⑤②③⑥④,故B正确;
C、粗盐提纯的关键操作是过滤,故C错误;
D、操作③中玻璃棒的作用是加速溶解,操作④中玻璃棒搅拌,防止局部过热,造成液滴飞溅,故D错误;
故选:B.
【分析】A、根据粗盐提纯的正确操作进行分析;
B、根据粗盐提纯的步骤为:①从瓶内取出粗盐样品,⑤称取粗盐样品,②加入量取好的水,③溶解,⑥过滤,④蒸发进行分析;
C、根据粗盐提纯的关键操作是过滤进行分析;
D、根据玻璃棒在粗盐提纯中的作用进行分析.
9.【答案】 C
【解析】【解答】解:A、当需要固体和液体加到一个容器内时,先固体后液体,防止迸溅,所以“粗盐溶解时,用药匙将粗盐逐渐加入水中,边加边用玻璃棒搅拌以加速溶解”错误,故A错误;
B、蒸发滤液时,待蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干;故B错误;
C、配制溶液需要经过计算、称量(称固体,量液体)、溶解、装液等步骤,故C正确;
D、配制溶液时必备的仪器有托盘天平、量筒、烧杯、玻璃棒等,不需要酒精灯,故说法错误;
故选C.
【分析】A、当需要固体和液体加到一个容器内时,先固体后液体,防止迸溅;
B、蒸发滤液时,待蒸发皿中出现较多固体时,便应停止加热,利用余热蒸干;
C、配制溶液需要经过计算、称量、溶解、装液等步骤;
D、配制溶液时必备的仪器有托盘天平、量筒、烧杯、玻璃棒等.
10.【答案】D
【解析】【解答】解:A、粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐)得到精盐的过程,故选项实验方法正确.
B、用KClO3制氧气通常加入MnO2作催化剂,能加快反应速率,故选项实验方法正确.
C、氢气可以燃烧,具有可燃性,为防止发生爆炸,在点燃氢气前一定要检验其纯度,故选项实验方法正确.
D、配制50克5%的NaCl溶液时,把称好的固体倒入到量好水的烧杯中进行溶解,不能在量筒内进行溶解操作,故选项实验方法错误.
故选:D.
【分析】A、根据粗盐提纯是将粗盐中含有的泥沙等不溶物除去,进行分析判断.
B、根据实验室制取氧气的反应原理,进行分析判断.
C、根据可燃性气体与空气混合后点燃可能发生爆炸,进行分析判断.
D、根据溶解操作的方法,进行分析判断.
二、填空题
11.【答案】ACB;搅拌,使液体受热均匀
【解析】【解答】(1)粗盐的主要成分是氯化钠,氯化钠易溶于水,盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程),故正确的操作顺序是ACB. (2)B操作是蒸发操作,蒸发操作中,玻璃棒起到搅拌而使液体受热均匀,以防液体受热不均匀,造成液体飞溅. 故答案为:(1)ACB;(2)搅拌,使液体受热均匀. 【分析】(1)粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程),进行分析判断; (2)B操作是蒸发操作,由蒸发操作中玻璃棒的作用,进行分析解答.
12.【答案】⑤;①;③;②;⑥;④
【解析】【解答】解:(1)酒精,学名叫乙醇,含有碳元素的化合物,属于有机物; (2)石墨是一种具有优良导电性能的碳的单质; (3)生石灰能与水反应生成熟石灰,可以做干燥剂; (4)氯化钠一种盐,可以做调味品,用来腌制食品; (5)氢元素是相对原子质量最小的元素,因此水是相对分子质量最小的氧化物; (6)磷在空气中燃烧生成白色的五氧化二磷固体. 故答案为:(1)⑤;(2)①;(3)③;(4)②;(5)⑥;(6)④. 【分析】可以从物质的性质着手分析物质的用途,酒精属于有机物;石墨具有很好的导电性;生石灰能与水反应生成氢氧化钙;氯化钠是一种常用的调味品;氢是相对原子质量最小的元素;红磷燃烧后生成的五氧化二磷是固体.
13.【答案】A ;D ;蒸发 ;出现较多固体 ;45g ;氯化钠溶液 ;10%
【解析】【解答】(1)根据图示操作,结合选项分析,由于操作①是将大颗粒粗盐变成较细的粗盐,故需研钵来研磨,而量筒只能用来量取液体的体积,烧杯一般被用来做大量液体的反应容器,试管则可用来加热少量的液体等用途,这三种仪器都不能用来研磨。故选A (2)A、B、C 是滤纸的正确的折叠方法的步骤,而D中的滤纸,在接口处出现缝隙,过滤时,待滤液会直接从此处进入下面的烧杯,影响过滤效果,错误。故选D (3)根据题意,操作④是将氯化钠溶液变为氯化钠晶体,故为蒸发结晶;当蒸发皿中出现较多固体时,应停止加热,要利用余热将其蒸干。 (4)根据溶质质量分数计算公式:溶质质量分数=×100%可知,溶液质量=溶质质量÷溶质质量分数,故5g食盐可配制10%的食盐溶液=5g÷10%=50g,所以需要水的质量=50g-5g=45g。根据题意,标签上标明氯化钠的名称、化学式和溶质质量分数即可。 【分析】本题主要考查了有关粗盐提纯的实验的相关知识,难度不大,只要同学们在平时的学习中注意相关基础知识和基本技能的积累和储备,即可轻松解答。
三、解答题
14.【答案】(1)缺少玻璃棒引流 (2)滤纸破损(或滤液高于滤纸边缘或盛接滤液的烧杯不干净等) (3)不是纯净物;精盐中含有氯化钠、氯化钙、氯化镁等。
【解析】【解答】解:(1)过滤液体时,注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流; (2)过滤后发现滤液仍然浑浊,可能原因是滤纸破损(会使得液体中的不溶物进入下面的烧杯,从而使得滤液浑浊)、液面高于滤纸边缘(会使部分液体未经过滤纸的过滤直接流下,该操作会使滤液仍然浑浊)或盛接滤液的烧杯不干净等; (3)经初步提纯所得精盐中含有氯化钠、氯化钙、氯化镁等多种物质,属于混合物. 故答案为:(1)缺少玻璃棒引流;(2)滤纸破损(或滤液高于滤纸边缘或盛接滤液的烧杯不干净等);(3)不是纯净物;精盐中含有氯化钠、氯化钙、氯化镁等.
【分析】(1)过滤液体时,要遵循“一贴、二低、三靠”的原则; (2)过滤液体时,要遵循“一贴、二低、三靠”的原则,凡是不经滤纸的过滤就直接进入滤液的操作,都能造成滤液浑浊;另外接滤液的烧杯不干净也会造成同样的结果; (3)经初步提纯所得精盐中含有氯化钠、氯化钙、氯化镁等.
四、综合题
15.【答案】(1)溶解;过滤;搅拌,防止因局部温度过高,造成液滴飞溅 (2)2;98;量筒;胶头滴管;小于;玻璃棒;加速溶解
【解析】【解答】(1)粗盐提纯的实验操作步骤为溶解、过滤、蒸发,在蒸发操作中,玻璃棒的作是搅拌,防止因局部温度过高,造成液滴飞溅;(2)①需要氯化钠固体的质量为100g×2%=2g;需要水的体积为(100g-2g)÷1g/cm3=98mL;③量取过程中用到的玻璃仪器有量筒、胶头滴管。在量取水的过程中,如果仰视读数,所得数据偏小,量筒中水的体积偏大。则配制得到的氯化钠溶液中氯化钠的质量分数小于2%;④溶解过程中用玻璃棒搅拌,作用是加速溶解。
【分析】根据盐提纯的实验操作步骤为溶解、过滤、蒸发分析;根据一定溶质质量分数的溶液配制方法分析,其中在量取水的过程中,如果仰视读数,所得数据偏小,量筒中水的体积偏大。
16.【答案】(1)过滤;除去不溶性物质;引流 (2)待蒸发皿中出现较多量的固体时
【解析】【解答】解:(1)粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程)、转移并计算精盐产率,则操作②的名称是过滤,以除去除去不溶性物质;该操作过程中玻璃棒的作用是引流.(2)蒸发时,待蒸发皿中出现较多量的固体时,应停止加热,利用余热将剩余液体蒸干.故答案为:(1)过滤;除去不溶性物质;引流;(2)待蒸发皿中出现较多量的固体时.
【分析】(1)根据粗盐提纯是将粗盐中含有的泥沙等不溶物除去,进行分析解答.(2)根据蒸发操作中停止加热的时机,进行分析解答.
