选修4期末综合复习(带答案)
文档属性
| 名称 | 选修4期末综合复习(带答案) |  | |
| 格式 | zip | ||
| 文件大小 | 301.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-17 21:24:32 | ||
图片预览


文档简介
2019—2020学年高二化学选修4期末综合复习
一、选择题(本题包括16小题,每小题3分,共48分)
1. 下列过程中ΔH小于零的是( )
A.Ba(OH)2与NH4Cl固体混合
B.氯化铵分解得氨气
C.碳酸钙分解得二氧化碳
D.实验室制备氢气
2. 下列说法中,可以证明反应N2(g)+3H2(g)2NH3(g)已达到平衡状态的是( )
A.1个N≡N键断裂的同时,有3个H—H键形成
B.1个N≡N键断裂的同时,有3个H—H键断裂
C.3个H—H键形成的同时,有6个N—H键断裂
D.1个N≡N键断裂的同时,有6个N—H键形成
3根据碘与氢气反应的热化学方程式:
①I2(g)+H2(g)2HI(g) ΔH=-9.48 kJ·mol-1
②I2(s)+H2(g) 2HI(g) ΔH=+26.48 kJ·mol-1
下列判断正确的是( )
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应②的反应物总能量比反应①的反应物总能量低
D.反应①的生成物比反应②的生成物稳定
4.下列说法正确的是( )
A.S(g)+O2(g)===SO2 (g)可用该反应的ΔH表示燃烧热
B.通过直接蒸发MgCl2溶液的方法获取无水氯化镁固体
C.除去CuCl2溶液中的Fe3+离子,选用氢氧化钠溶液作沉淀剂
D.测定中和热的实验中,参与反应的酸或碱,无论谁过量,都不影响中和热的数值
5. 下列热化学方程式中的反应热能表示燃烧热的是(a、b、c、d均大于0)( )
A.C6H12O6(s)+6O2(g)===6CO2(g)+6H2O(l)ΔH=-a kJ·mol-1
B.CH3CH2OH(l)+O2(g)===CH3CHO(l)+H2O(l)ΔH=-b kJ·mol-1
C.C(s)+O2(g)===CO(g) ΔH=-c kJ·mol-1
D.NH3(g)+O2(g)===NO(g)+H2O(g)ΔH=-d kJ·mol-1
6.下列方程式书写正确的是( )
A.H2S的电离方程式:H2S+H2OH3O++HS-
B.NaHCO3在水溶液中的电离方程式:NaHCO3===Na++H++CO
C.CO的水解方程式:CO+2H2OH2CO3+2OH-
D.HS-的水解方程式:HS-+H2OS2-+H3O+
7.在稀硫酸与锌反应制取氢气的实验中,探究加入硫酸铜溶液的量对氢气生成速率的影响。实验中Zn粒过量且颗粒大小相同,饱和硫酸铜溶液用量0~4.0 mL,保持溶液总体积为100.0mL,记录获得相同体积(336mL)的气体所需时间,实验结果如图所示(气体体积均转化为标况下)。据图分析,下列说法不正确的是( )
A.饱和硫酸铜溶液用量过多不利于更快收集氢气
B.a、c两点对应的氢气生成速率相等
C.b点对应的反应速率为v(H2SO4)=1.0×10-3mol·L-1·s-1
D.d点没有构成原电池,反应速率减慢
8.将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡NH2COONH4(s)2NH3(g)+CO2(g),若保持温度和容器体积不变,再充入n(NH3)∶n(CO2)=2∶1,则再次达到平衡时c(NH3)( )
A.增大 B.不变
C.变小 D.因条件不足无法判断
9. 常温下,将a L 0.1 mol·L-1的NaOH溶液与 b L 0.1 mol·L-1的CH3COOH溶液混合。下列有关混合溶液的说法一定不正确是( )
A.ac(Na+)>c(H+)>c(OH-)
B.a>b时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.a=b时,c(CH3COOH)+c(H+)=c(OH-)
D.无论a、b有何关系,均有c(H+)+c(Na+)=c(CH3COO-)+c(OH-)
10.下列说法正确的是( )
A.pH=1的醋酸加水稀释到原体积的100倍,稀释后pH=3
B.室温下pH=3的醋酸溶液和pH=11的Ba(OH)2溶液等体积混合后溶液呈酸性
C.室温下pH相同的NH4Cl溶液和CH3COOH溶液,由水电离产生的c(H+)相同
D.某温度下,水的离子积常数为1×10-12,该温度下pH=7的溶液呈中性
11. .为探究钢铁的吸氧腐蚀原理设计了如图所示的装置,下列有关说法中错误的是( )
A.正极的电极反应式为O2+2H2O+4e-===4OH-
B.将石墨电极改成镁电极,难以观察到铁锈生成
C.若向自来水中加入少量的氯化钠固体,可较快地看到铁锈
D.分别向铁、石墨电极附近吹入氧气,前者铁锈出现得快
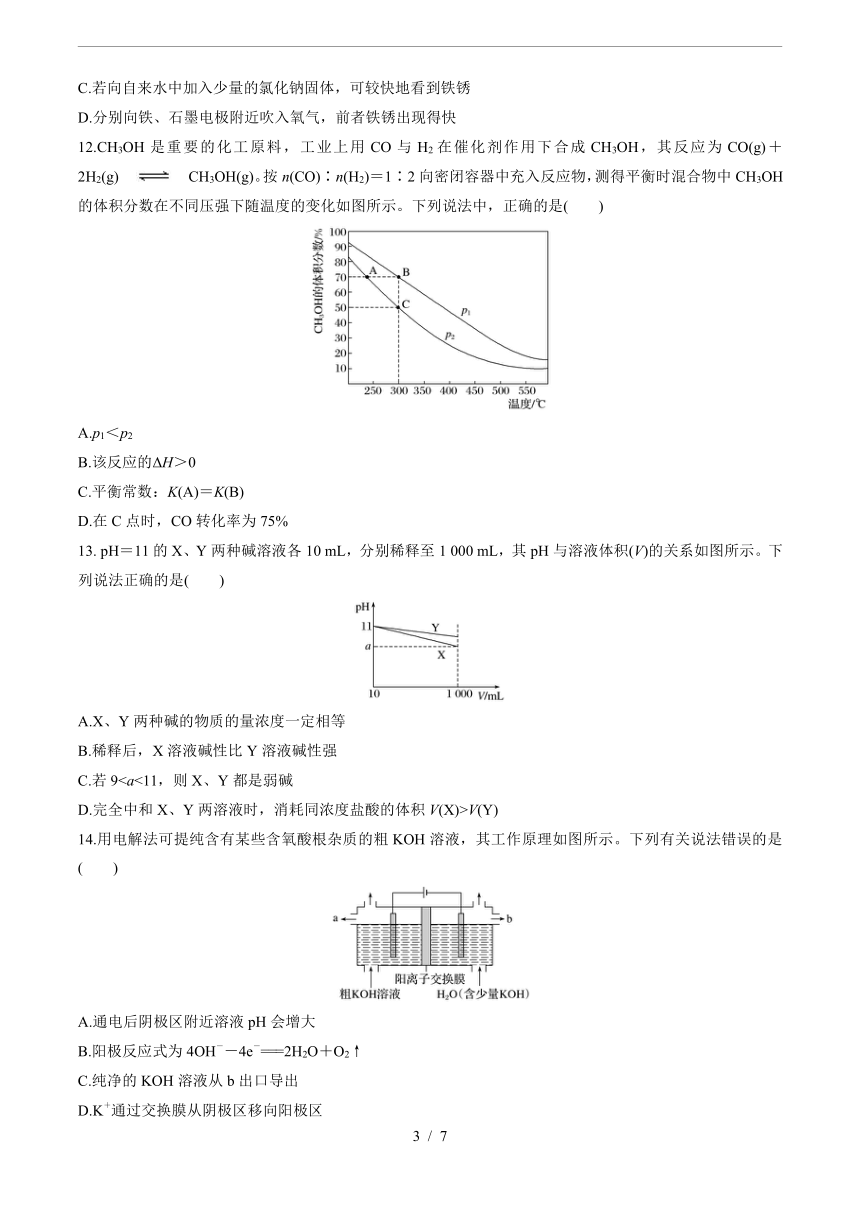
12.CH3OH是重要的化工原料,工业上用CO与H2在催化剂作用下合成CH3OH,其反应为CO(g)+2H2(g)CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是( )
A.p1<p2
B.该反应的ΔH>0
C.平衡常数:K(A)=K(B)
D.在C点时,CO转化率为75%
13. pH=11的X、Y两种碱溶液各10 mL,分别稀释至1 000 mL,其pH与溶液体积(V)的关系如图所示。下列说法正确的是( )
A.X、Y两种碱的物质的量浓度一定相等
B.稀释后,X溶液碱性比Y溶液碱性强
C.若9D.完全中和X、Y两溶液时,消耗同浓度盐酸的体积V(X)>V(Y)
14.用电解法可提纯含有某些含氧酸根杂质的粗KOH溶液,其工作原理如图所示。下列有关说法错误的是( )
A.通电后阴极区附近溶液pH会增大
B.阳极反应式为4OH--4e-===2H2O+O2↑
C.纯净的KOH溶液从b出口导出
D.K+通过交换膜从阴极区移向阳极区
15室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1 mol·L-1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示。下列判断错误的是( )
A.三种酸的电离常数关系:KHA>KHB>KHD
B.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
16. 已知常温下:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述正确的是( )
A.AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小
B.已知Ksp(AgBr)C.将0.001 mol·L-1的AgNO3溶液滴入0.001 mol·L-1的KCl和0.001 mol·L-1的K2CrO4溶液中先产生Ag2CrO4沉淀
D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动
二、非选择题(本题包括5小题,共52分)
17.(8分)(1)已知:①Fe(s)+1/2O2(g)===FeO(s) ΔH1=-272.0kJ·mol-1;
②2Al(s)+3/2O2(g)===Al2O3(s) ΔH2=-1675.7kJ·mol-1。
Al和FeO发生铝热反应的热化学方程式是_____________________________________
________________________________________________________________________。
某同学认为,铝热反应可用于工业炼铁,你的判断是________(填“能”或“不能”),你的理由是________________________________________________________________________
________________________________________________________________________。
(2)反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示。
①据图判断该反应是________(填“吸”或“放”)热反应
②其中B历程表明此反应采用的条件为______(填字母)。
A.升高温度 B.增大反应物的浓度
C.降低温度 D.使用催化剂
18.(12分) CO可用于合成甲醇,化学方程式为CO(g)+2H2(g)CH3OH(g)。
(1)图1是反应CO(g)+2H2(g)CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。
①该反应的焓变ΔH________(填“>”“<”或“=”)0。
②T1和T2温度下的平衡常数大小关系是K1________(填“>”“<”或“=”)K2。在T1温度下,往体积为1 L的密闭容器中,充入1 mol CO和2 mol H2,经测得CO和CH3OH(g)的浓度随时间变化如图2所示。则该反应的平衡常数为______________。
③若容器容积不变,下列措施可增加CO转化率的是________(填字母)。
a.升高温度
b.将CH3OH(g)从体系中分离
c.使用合适的催化剂
d.充入He,使体系总压强增大
(2)在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线z对应的温度是________℃;该温度下上述反应的化学平衡常数为________。曲线上a、b、c点对应的化学平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为________________________。
19.(12分)结合下表回答下列问题(均为常温下的数据):
酸 电离常数(Ka)
CH3COOH 1.8×10-5
HClO 3×10-8
H2CO3 K1=4.4×10-7 K2=4.7×10-11
H2C2O4 K1=5.4×10-2 K2=5.4×10-5
H2S K1=1.3×10-7 K2=7.1×10-15
请回答下列问题:
(1)同浓度的CH3COO-、HCO、CO、HC2O、ClO-、S2-中结合H+的能力最弱的是____________。
(2)常温下0.1mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是____(填字母)。
A.c(H+)B.c(H+)/c(CH3COOH)C.c(H+)/c(OH-)D.c(OH-)
(3)0.1mol·L-1的H2C2O4溶液与0.1mol·L-1的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为__________________。
(4)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是CH3COONa________NaClO,两溶液中:c(Na+)-c(ClO-)__________c(K+)-c(CH3COO-)(填“>”“<”或“=”)。
(5)向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=______________。
20.(10分) 硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
(1)步骤②中发生反应的离子方程式为__________________________________________
________________________________________________________________________。
(2)步骤④中调节pH=6.0~6.5的目的是_______________________________________
________________________________________________________________________。
(3)步骤⑤的操作为________________________________________________________。
(4)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH <8.0 8.0~9.6 >9.6
颜色 黄色 绿色 蓝色
25 ℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为____________(25 ℃时 ,Ksp[Mg(OH)2]=5.6×10-12)。
参考答案
1.答案 D
2.答案 A
3.答案 C
4.答案 D
5.答案 A
6.答案 A
7.答案 D
8.答案 B
9.答案 B
10.答案 B
11.答案 D
12.答案 D
13.答案 C
14.答案 D
15.答案 C
16.答案 D
17.答案 (1)3FeO(s)+2Al(s)===Al2O3(s)+3Fe(s) ΔH=-859.7kJ·mol-1 不能 该反应为引发反应,需消耗大量能量,成本较高 (2)①吸 ②D
解析 (1)②-①×3即得:3FeO(s)+2Al(s)===Al2O3(s)+3Fe(s) ΔH=-859.7 kJ·mol-1。利用铝热反应在工业上大面积炼铁时,为了引发反应需要消耗大量能源,冶炼Fe的成本就太高了,所以不能使用铝热反应炼铁。(2)①反应物能量低于最后的生成物能量,所以该反应为吸热反应。②从A到B明显反应的活化能降低了,所以是加入了催化剂。
18.答案 (1)①< ②> 12 ③b (2)270 4 K1=K219.答案 (1)HC2O (2)AC (3)c(K+)>c(HC2O)>c(H+)>c(C2O)>c(OH-) (4)> = (5)5
20.答案 (1)2NH+MgOMg2++2NH3↑+H2O
(2)抑制Mg2+水解,以便得到较纯的产品
(3)蒸发浓缩、冷却结晶 (4)蓝色
/
一、选择题(本题包括16小题,每小题3分,共48分)
1. 下列过程中ΔH小于零的是( )
A.Ba(OH)2与NH4Cl固体混合
B.氯化铵分解得氨气
C.碳酸钙分解得二氧化碳
D.实验室制备氢气
2. 下列说法中,可以证明反应N2(g)+3H2(g)2NH3(g)已达到平衡状态的是( )
A.1个N≡N键断裂的同时,有3个H—H键形成
B.1个N≡N键断裂的同时,有3个H—H键断裂
C.3个H—H键形成的同时,有6个N—H键断裂
D.1个N≡N键断裂的同时,有6个N—H键形成
3根据碘与氢气反应的热化学方程式:
①I2(g)+H2(g)2HI(g) ΔH=-9.48 kJ·mol-1
②I2(s)+H2(g) 2HI(g) ΔH=+26.48 kJ·mol-1
下列判断正确的是( )
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应②的反应物总能量比反应①的反应物总能量低
D.反应①的生成物比反应②的生成物稳定
4.下列说法正确的是( )
A.S(g)+O2(g)===SO2 (g)可用该反应的ΔH表示燃烧热
B.通过直接蒸发MgCl2溶液的方法获取无水氯化镁固体
C.除去CuCl2溶液中的Fe3+离子,选用氢氧化钠溶液作沉淀剂
D.测定中和热的实验中,参与反应的酸或碱,无论谁过量,都不影响中和热的数值
5. 下列热化学方程式中的反应热能表示燃烧热的是(a、b、c、d均大于0)( )
A.C6H12O6(s)+6O2(g)===6CO2(g)+6H2O(l)ΔH=-a kJ·mol-1
B.CH3CH2OH(l)+O2(g)===CH3CHO(l)+H2O(l)ΔH=-b kJ·mol-1
C.C(s)+O2(g)===CO(g) ΔH=-c kJ·mol-1
D.NH3(g)+O2(g)===NO(g)+H2O(g)ΔH=-d kJ·mol-1
6.下列方程式书写正确的是( )
A.H2S的电离方程式:H2S+H2OH3O++HS-
B.NaHCO3在水溶液中的电离方程式:NaHCO3===Na++H++CO
C.CO的水解方程式:CO+2H2OH2CO3+2OH-
D.HS-的水解方程式:HS-+H2OS2-+H3O+
7.在稀硫酸与锌反应制取氢气的实验中,探究加入硫酸铜溶液的量对氢气生成速率的影响。实验中Zn粒过量且颗粒大小相同,饱和硫酸铜溶液用量0~4.0 mL,保持溶液总体积为100.0mL,记录获得相同体积(336mL)的气体所需时间,实验结果如图所示(气体体积均转化为标况下)。据图分析,下列说法不正确的是( )
A.饱和硫酸铜溶液用量过多不利于更快收集氢气
B.a、c两点对应的氢气生成速率相等
C.b点对应的反应速率为v(H2SO4)=1.0×10-3mol·L-1·s-1
D.d点没有构成原电池,反应速率减慢
8.将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡NH2COONH4(s)2NH3(g)+CO2(g),若保持温度和容器体积不变,再充入n(NH3)∶n(CO2)=2∶1,则再次达到平衡时c(NH3)( )
A.增大 B.不变
C.变小 D.因条件不足无法判断
9. 常温下,将a L 0.1 mol·L-1的NaOH溶液与 b L 0.1 mol·L-1的CH3COOH溶液混合。下列有关混合溶液的说法一定不正确是( )
A.a
B.a>b时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.a=b时,c(CH3COOH)+c(H+)=c(OH-)
D.无论a、b有何关系,均有c(H+)+c(Na+)=c(CH3COO-)+c(OH-)
10.下列说法正确的是( )
A.pH=1的醋酸加水稀释到原体积的100倍,稀释后pH=3
B.室温下pH=3的醋酸溶液和pH=11的Ba(OH)2溶液等体积混合后溶液呈酸性
C.室温下pH相同的NH4Cl溶液和CH3COOH溶液,由水电离产生的c(H+)相同
D.某温度下,水的离子积常数为1×10-12,该温度下pH=7的溶液呈中性
11. .为探究钢铁的吸氧腐蚀原理设计了如图所示的装置,下列有关说法中错误的是( )
A.正极的电极反应式为O2+2H2O+4e-===4OH-
B.将石墨电极改成镁电极,难以观察到铁锈生成
C.若向自来水中加入少量的氯化钠固体,可较快地看到铁锈
D.分别向铁、石墨电极附近吹入氧气,前者铁锈出现得快
12.CH3OH是重要的化工原料,工业上用CO与H2在催化剂作用下合成CH3OH,其反应为CO(g)+2H2(g)CH3OH(g)。按n(CO)∶n(H2)=1∶2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是( )
A.p1<p2
B.该反应的ΔH>0
C.平衡常数:K(A)=K(B)
D.在C点时,CO转化率为75%
13. pH=11的X、Y两种碱溶液各10 mL,分别稀释至1 000 mL,其pH与溶液体积(V)的关系如图所示。下列说法正确的是( )
A.X、Y两种碱的物质的量浓度一定相等
B.稀释后,X溶液碱性比Y溶液碱性强
C.若9
14.用电解法可提纯含有某些含氧酸根杂质的粗KOH溶液,其工作原理如图所示。下列有关说法错误的是( )
A.通电后阴极区附近溶液pH会增大
B.阳极反应式为4OH--4e-===2H2O+O2↑
C.纯净的KOH溶液从b出口导出
D.K+通过交换膜从阴极区移向阳极区
15室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1 mol·L-1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示。下列判断错误的是( )
A.三种酸的电离常数关系:KHA>KHB>KHD
B.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
16. 已知常温下:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述正确的是( )
A.AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小
B.已知Ksp(AgBr)
D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动
二、非选择题(本题包括5小题,共52分)
17.(8分)(1)已知:①Fe(s)+1/2O2(g)===FeO(s) ΔH1=-272.0kJ·mol-1;
②2Al(s)+3/2O2(g)===Al2O3(s) ΔH2=-1675.7kJ·mol-1。
Al和FeO发生铝热反应的热化学方程式是_____________________________________
________________________________________________________________________。
某同学认为,铝热反应可用于工业炼铁,你的判断是________(填“能”或“不能”),你的理由是________________________________________________________________________
________________________________________________________________________。
(2)反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示。
①据图判断该反应是________(填“吸”或“放”)热反应
②其中B历程表明此反应采用的条件为______(填字母)。
A.升高温度 B.增大反应物的浓度
C.降低温度 D.使用催化剂
18.(12分) CO可用于合成甲醇,化学方程式为CO(g)+2H2(g)CH3OH(g)。
(1)图1是反应CO(g)+2H2(g)CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。
①该反应的焓变ΔH________(填“>”“<”或“=”)0。
②T1和T2温度下的平衡常数大小关系是K1________(填“>”“<”或“=”)K2。在T1温度下,往体积为1 L的密闭容器中,充入1 mol CO和2 mol H2,经测得CO和CH3OH(g)的浓度随时间变化如图2所示。则该反应的平衡常数为______________。
③若容器容积不变,下列措施可增加CO转化率的是________(填字母)。
a.升高温度
b.将CH3OH(g)从体系中分离
c.使用合适的催化剂
d.充入He,使体系总压强增大
(2)在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线z对应的温度是________℃;该温度下上述反应的化学平衡常数为________。曲线上a、b、c点对应的化学平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为________________________。
19.(12分)结合下表回答下列问题(均为常温下的数据):
酸 电离常数(Ka)
CH3COOH 1.8×10-5
HClO 3×10-8
H2CO3 K1=4.4×10-7 K2=4.7×10-11
H2C2O4 K1=5.4×10-2 K2=5.4×10-5
H2S K1=1.3×10-7 K2=7.1×10-15
请回答下列问题:
(1)同浓度的CH3COO-、HCO、CO、HC2O、ClO-、S2-中结合H+的能力最弱的是____________。
(2)常温下0.1mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是____(填字母)。
A.c(H+)B.c(H+)/c(CH3COOH)C.c(H+)/c(OH-)D.c(OH-)
(3)0.1mol·L-1的H2C2O4溶液与0.1mol·L-1的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为__________________。
(4)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是CH3COONa________NaClO,两溶液中:c(Na+)-c(ClO-)__________c(K+)-c(CH3COO-)(填“>”“<”或“=”)。
(5)向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=______________。
20.(10分) 硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
(1)步骤②中发生反应的离子方程式为__________________________________________
________________________________________________________________________。
(2)步骤④中调节pH=6.0~6.5的目的是_______________________________________
________________________________________________________________________。
(3)步骤⑤的操作为________________________________________________________。
(4)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH <8.0 8.0~9.6 >9.6
颜色 黄色 绿色 蓝色
25 ℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为____________(25 ℃时 ,Ksp[Mg(OH)2]=5.6×10-12)。
参考答案
1.答案 D
2.答案 A
3.答案 C
4.答案 D
5.答案 A
6.答案 A
7.答案 D
8.答案 B
9.答案 B
10.答案 B
11.答案 D
12.答案 D
13.答案 C
14.答案 D
15.答案 C
16.答案 D
17.答案 (1)3FeO(s)+2Al(s)===Al2O3(s)+3Fe(s) ΔH=-859.7kJ·mol-1 不能 该反应为引发反应,需消耗大量能量,成本较高 (2)①吸 ②D
解析 (1)②-①×3即得:3FeO(s)+2Al(s)===Al2O3(s)+3Fe(s) ΔH=-859.7 kJ·mol-1。利用铝热反应在工业上大面积炼铁时,为了引发反应需要消耗大量能源,冶炼Fe的成本就太高了,所以不能使用铝热反应炼铁。(2)①反应物能量低于最后的生成物能量,所以该反应为吸热反应。②从A到B明显反应的活化能降低了,所以是加入了催化剂。
18.答案 (1)①< ②> 12 ③b (2)270 4 K1=K2
20.答案 (1)2NH+MgOMg2++2NH3↑+H2O
(2)抑制Mg2+水解,以便得到较纯的产品
(3)蒸发浓缩、冷却结晶 (4)蓝色
/
