人教版九年级下化学教学讲义,复习补习资料(含知识讲解,巩固练习):51【提高】溶解度和溶质的质量分数
文档属性
| 名称 | 人教版九年级下化学教学讲义,复习补习资料(含知识讲解,巩固练习):51【提高】溶解度和溶质的质量分数 |

|
|
| 格式 | zip | ||
| 文件大小 | 89.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-23 00:00:00 | ||
图片预览



文档简介
溶解度和溶质的质量分数(提高)
【学习目标】
1.掌握饱和溶液、不饱和溶液、溶解度等概念及相互关系;掌握溶解度曲线的意义及应用。
2.认识一种溶液组成的表示方法——溶质的质量分数;掌握溶质质量分数的有关计算。 3.初步学会配制一定溶质质量分数的溶液。
【典型例题】
类型一、考查饱和溶液、不饱和溶液、溶解度及溶解度曲线的应用 1.(2019?重庆中考)如图是甲、乙两种固体物质在水中的溶解度曲线,下列说法不正确的是( )
A. 10℃时,甲、乙两种物质的饱和溶液浓度相同 B. 保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液
C. 30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80g D. 10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大
【思路点拨】固体溶解度曲线所能表示的意义:①根据已知的温度可以查出有关物质的溶解度;②根据物质的溶解度也可以查出它所对应的温度;③可以判断或比较相同温度下,不同物质溶解度的大小(或饱和溶液中溶质的质量分数的大小);④根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶、升温结晶);并且,还可以判断或比较析出晶体的质量大小,即曲线越陡,析出的晶体就越多;⑤两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;并且,此时两种物质饱和溶液的溶质质量分数也相同的。
【答案】D 【解析】10℃时,甲、乙两种物质的溶解度相同,故饱和溶液浓度相同,A选项正确。保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液,B选项正确。30℃时,甲的溶解度为60g,将40g甲物质加入50g水中,充分溶解只能溶解30g,溶液的质量为80g,C选项正确。10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数不变,D选项错误。
【总结升华】解答这类题目时,首先,要熟记和理解固体溶解度曲线及其使用,固体溶解度的概念和意义,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法;然后结合所学的相关知识和技能,细致地阅读、分析题意等,最后按照题目的要求,认真地进行选择或解答即可。
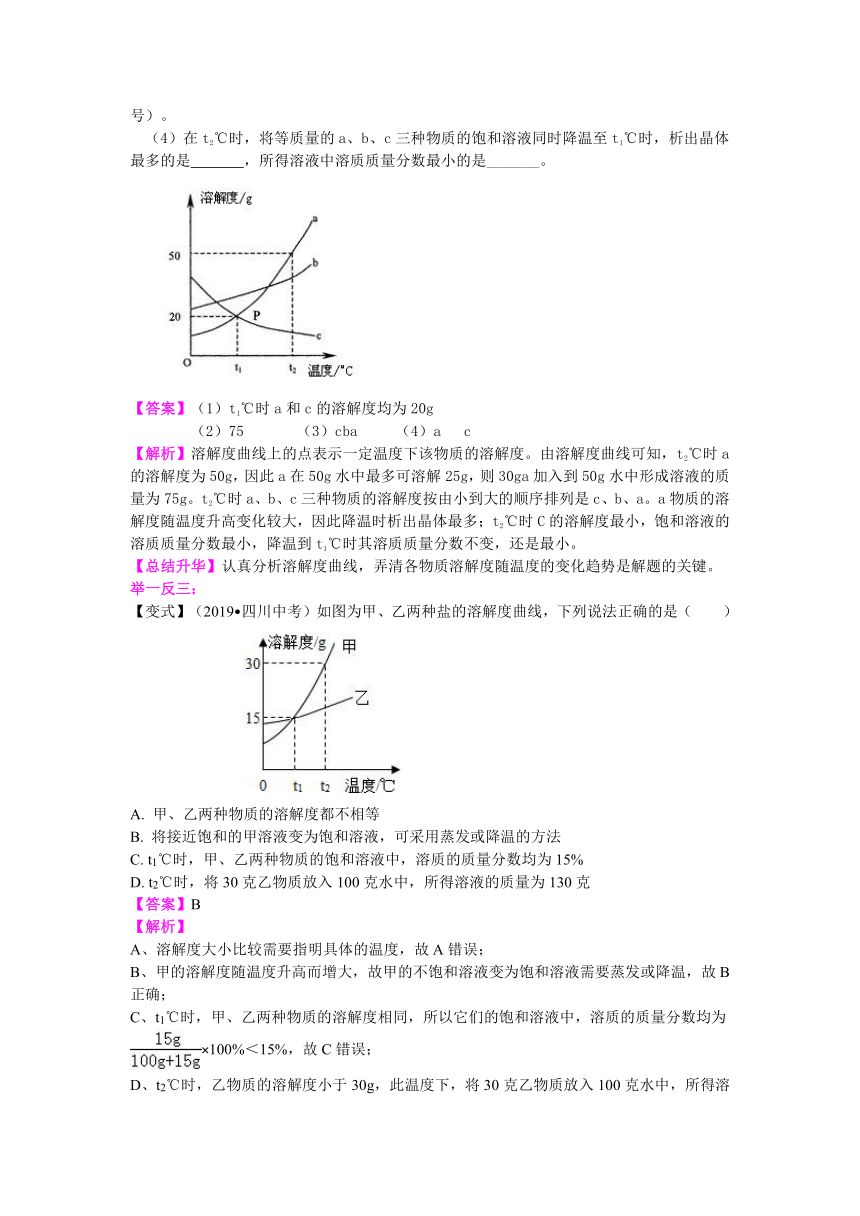
2.下图是a、b、c三种物质的溶解度曲线。请回答: (1)P点的含义是_____________________。 (2)t2℃时30g a物质加入到50g水中不断搅拌,形成的溶液质量是______g。 (3)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是________(填写物质序号)。 (4)在t2℃时,将等质量的a、b、c三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是 ,所得溶液中溶质质量分数最小的是_______。
【答案】(1)t1℃时a和c的溶解度均为20g
(2)75 (3)cba (4)a c
【解析】溶解度曲线上的点表示一定温度下该物质的溶解度。由溶解度曲线可知,t2℃时a的溶解度为50g,因此a在50g水中最多可溶解25g,则30ga加入到50g水中形成溶液的质量为75g。t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是c、b、a。a物质的溶解度随温度升高变化较大,因此降温时析出晶体最多;t2℃时C的溶解度最小,饱和溶液的溶质质量分数最小,降温到t1℃时其溶质质量分数不变,还是最小。
【总结升华】认真分析溶解度曲线,弄清各物质溶解度随温度的变化趋势是解题的关键。 举一反三: 【变式】(2019?四川中考)如图为甲、乙两种盐的溶解度曲线,下列说法正确的是( )
A. 甲、乙两种物质的溶解度都不相等 B. 将接近饱和的甲溶液变为饱和溶液,可采用蒸发或降温的方法
C. t1℃时,甲、乙两种物质的饱和溶液中,溶质的质量分数均为15% D. t2℃时,将30克乙物质放入100克水中,所得溶液的质量为130克 【答案】B 【解析】
A、溶解度大小比较需要指明具体的温度,故A错误;
B、甲的溶解度随温度升高而增大,故甲的不饱和溶液变为饱和溶液需要蒸发或降温,故B正确;
C、t1℃时,甲、乙两种物质的溶解度相同,所以它们的饱和溶液中,溶质的质量分数均为×100%<15%,故C错误;
D、t2℃时,乙物质的溶解度小于30g,此温度下,将30克乙物质放入100克水中,所得溶液的质量小于130克,故D错误。
类型二、考查溶液的配制、溶质质量分数和溶液的稀释等有关计算
3.双氧水(H2O2)既是工业上的重要的绿色氧化剂,又是常用的医药消毒剂。小明从试剂商店购得一瓶质量分数为30%的双氧水,用于制取氧气。若要配制5%的双氧水600g,需要30%的双氧水的质量为___________。需加水的体积是___________。 【答案】100g 500mL 【解析】用浓溶液配置稀溶液的过程中溶质质量不变。根据溶质质量分数的定义可知:溶质的质量=溶液质量×溶质的质量分数。设需要30%的双氧水的质量为X,根据题意可列等式
30%X=600g×5%
解得X=100g
则水的质量为600g-100g=500g,即需加水的体积为500mL。 【总结升华】此题的解题关键是记住溶液稀释前后溶质的质量不变。
4.小明利用家庭小实验粗略测定食醋中醋酸的质量分数。方法是:用注射器吸取20mL食醋,逐滴加入到5.3g 10%的碳酸钠溶液中,至不再产生气泡为止,此时注射器中剩余的食醋为8mL。请计算食醋中醋酸的质量分数。(已知食醋的密度近似为1g/cm3,Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑) 【答案】
解:滴加食醋的质量为(20ml-8ml)×1g/cm3=12g ? 参加反应的碳酸钠质量为5.3g×10%=0.53g 设反应消耗醋酸的质量为x。 ? Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑ 106 120 0.53g x ? ? 食醋中醋酸的质量分数为:
答:食醋中醋酸的质量分数为5%。 【解析】想计算食醋中醋酸的质量分数,需要知道食醋的质量以及所含醋酸的质量。已知所用食醋的体积为12mL,即12g;12g食醋中含醋酸的质量可以根据化学方程式求出。 【总结升华】解关于化学方程式和溶质质量分数结合的计算题,要注意参加反应的或者生成的物质的质量是溶液中的溶质质量。 举一反三:
【变式1】现欲将粗盐提纯,并用制得的精盐配制质量分数一定的氯化钠溶液。下列说法不正确的是( ) A.粗盐溶解时,可边加粗盐边用玻璃棒搅拌加速溶解 B.过滤滤液时,可以直接把溶有粗盐的液体直接倒入漏斗? C.配制溶液需要经过计算、称量、溶解、装液等步骤? D.配制溶液时必备的仪器有托盘天平、量筒、烧杯、玻璃棒等
【答案】B 【解析】粗盐提纯需要先溶解,用玻璃棒搅拌可以加速溶解;过滤时不能直接把液体倒入漏斗,必须用玻璃棒引流。A、C、D三个选项的说法都是正确的。 【变式2】四川汶川抗震救灾期间,为了防止灾后疫情的发生,每天需要喷洒大量的消毒液。 (1)800Kg 质量分数为0.5% 的过氧乙酸消毒液中,过氧乙酸的质量为__________kg。 (2)要配制 800Kg 质量分数为0.5% 的过氧乙酸消毒液,需要质量分数为16% 的过氧乙酸溶液的质量是多少?
【答案】
解:(1)800kg×0.5%=4kg (2)解:设需要质量分数为16%过氧乙酸溶液的质量为X。 X·16% = 4 Kg? X = 25 Kg? 答:需要质量分数为16%的过氧乙酸溶液的质量是25kg。 【变式3】过氧化氢溶液长期保存会自然分解,使得溶质质量分数
减小。小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一
起测定溶质质量分数。他们取出该溶液51g,加入适量二氧化锰,
生成氧气的质量与反应时间的关系如图所示。 (1)求完全反应后生成氧气的质量为________。 (2)计算该溶液中溶质的质量分数。 【答案】 (1)0.48g (2)解:设51g过氧化氢溶液中含过氧化氢的质量为x。 2H2O22H2O + O2↑ 68 32 x 0.48g 过氧化氢溶液中溶质的质量分数为
答:该溶液中溶质的质量分数为2%。 【解析】根据图中数据可知反应后生成氧气的质量是0.48g。溶液中溶质的质量分数为溶质质量和溶液质量之比。分析已知数据,需要求出溶质过氧化氢的质量;根据氧气的质量,利用化学方程式就可计算出反应中分解的过氧化氢质量。
溶解度和溶质的质量分数(提高)
【巩固练习】
选择题 (每小题只有一个选项符合题意)
1.下列有关溶液的说法错误的是( )? ①碘酒中的溶质是酒精;②改变条件,饱和溶液与不饱和溶液可相互转化;③氢氧化钙的饱和溶液一定是浓溶液;④析出晶体后的溶液是该温度下的饱和溶液
A.①② B.②③ C.①③ D.③④
2.小红同学在一定温度下进行KNO3的溶解实验,实验数据如下:? ? 根据上述实验数据,下列叙述正确的是( )
A.实验1所得溶液的溶质质量分数=80g÷100g×100%
B.实验2所得溶液为饱和溶液
C.实验4所得溶液的溶质质量分数比实验3大
D.该温度下,KNO3饱和溶液的溶质质量分数=110g÷210g×100%
3.对“20℃时,硝酸钾溶解度为31.6g”这句话解释正确的是( ) A.20℃时,100g硝酸钾溶液中含有31.6g硝酸钾 B.在100g水中溶解31.6g硝酸钾就达到饱和状态
C.20℃时,100g水中溶解31.6g硝酸钾就达到饱和状态
D.20℃时,31.6g硝酸钾被131.6g水溶解就达到饱和状态 4.下列关于溶液的说法正确的是( )
A.20℃时,在100g水中溶解了30g氯化钠,则20℃时氯化钠的溶解度是30g
B.气体物质的溶解度,随温度的升高而减小,随压强的增大而增大
C.在20℃时,向一定量的饱和石灰水中加入少量生石灰,若恢复到原温度时,溶液中溶质的质量不变
D.饱和硝酸钠溶液一定比不饱和硝酸钠溶液的溶质质量分数大
5.取70g某温度下的氯化钾饱和溶液,将其恒温蒸发10g水,析出4g氯化钾固体,则剩余溶液中所含溶质质量为( )
A.16g B.20g C.40g D.56g
6.下列说法中正确的是( )
A.无色透明的液体一定是溶液
B.配制溶液时,搅拌可以增大溶质的溶解度
C.将10%的氯化钠溶液倒出一半,剩余溶液中溶质的质量分数仍为10%
D.同种溶质的饱和溶液,一定比它的不饱和溶液的溶质质量分数大
7.(2019?四川中考)20℃时,取甲、乙、丙、丁四种纯净物各40 g,分别加入到四个各盛有100g水的烧杯中,充分溶解,其溶解情况如下表:
物质
甲
乙
丙
丁
未溶解固体的质量/g
8.4
4
0
18.4
下列说法正确的是( )
A. 所得四杯溶液都是饱和溶液 B. 丁溶液的溶质质量分数最大
C. 20℃时四种物质溶解度的关系为:丁>甲>乙>丙
D. 四杯溶液中各加入20℃的100 g水后,溶液质量相等,且均为不饱和溶液
8.(2019?浙江中考)下表是固体甲和乙在不同温度时的溶解度。下列说法中正确的是( )
温度/℃
0
20
40
100
甲溶解度/克
0.73
0.165
0.121
0.076
乙溶解度/克
13.3
31.6
63.9
246
A.20℃时甲物质的饱和溶液升高温度会变为不饱和溶液 B.100℃时乙物质的饱和溶液冷却到室温会析出晶体,但溶液仍饱和
C.20℃时.甲溶液的溶质质量分数一定小于乙溶液的溶质质量分数
D.20℃时,100克乙物质加入100克水中.所得溶液的溶质质量分数等于50%
9.有40g质量分数为5%的氯化钙溶液,若将其质量分数增加到10%,应采用的方法是( )
A.把溶剂蒸发掉一半 B.加入40g质量分数为20%的氯化钙溶液
C.把溶剂蒸发掉20g D.加入2g氯化钙固体
二、填空题
10.如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题:
(1)A、B两种物质的溶解度受温度影响较大的是_______;
(2)t1℃时,A物质的溶解度___________ B物质的溶解度(填“>”、“=”或“<”);t2℃时,把80g B物质放入100g 水中,充分搅拌,得到溶液的质量________g。
11.如图是甲、乙两种物质的溶解度曲线,下列说法不正确的是 。
①升高温度,可使甲的不饱和溶液变为饱和溶液;②50℃时甲的饱和溶液溶质的质量分数为40%;③20℃时,甲、乙两种物质的溶解度相等;④要使乙从其浓溶液中析出,可冷却乙的热浓溶液
12.60℃时,硝酸钾的溶解度为110g。在60℃时,将70g硝酸钾放入50g水中,充分溶解后所得溶液的质量为 。
13.20℃时,食盐的溶解度为36g。该温度下将20g食盐投入50g水中,溶液的溶质质量分数为 。若将15g食盐投入50g水中,所得溶液的溶质质量分数为 。
14.(2019?山东中考)如图是甲、乙两种固体物质的溶解度曲线。据图回答:
(1)10℃时,甲物质的溶解度 乙物质的溶解度.(填“>”或“=”或“<”)。
(2)把30℃时等质量的甲、乙两物质饱和溶液降温到10℃,析出晶体较多的是 。
(3)20℃时,将50g甲物质放入盛有100g水的烧杯中,最终所得溶液的质量为 g;若将烧杯内物质升温到30℃(不考虑水蒸发),溶液中不变的是 (填序号)。
A.溶剂的质量 B.溶液的质量 C.溶质的质量分数 D.以上都不变
三、计算题
15.(2019?福建中考)一定量的锌与200g硫酸溶液恰好反应,生成氢气0.4g,计算:(1)参加反应的锌的质量。(2)硫酸溶液溶质的质量分数。(3)反应后所得溶液的溶质质量分数。(4)将此硫酸溶液100g稀释成5%的硫酸溶液,需要加水的质量。
【答案与解析】
1.【答案】C?
【解析】碘酒中的溶质是碘,酒精是溶剂,故①不正确;饱和溶液和不饱和溶液在一定条件下可相互转化,故②正确;氢氧化钙微溶于水,其饱和溶液浓度很小,属于稀溶液,故③不正确;有晶体析出的溶液是该温度下的饱和溶液,故④正确。?
2.【答案】D? 【解析】实验1所得溶液溶质质量分数=80g÷(100g+80g)×100%,故A错;由实验3提供数据知,实验2为不饱和溶液,故B错;由于实验3和实验4都是饱和溶液,在100 g水中最多能溶解110 gKNO3,故它们的溶质质量分数相等,故C错;该温度下KNO3饱和溶液的溶质质量分数=110g÷210g×100%,故D正确。 ??
3.【答案】C
【解析】20℃时,硝酸钾溶解度为31.6g,是表示20℃时100g水中溶解31.6g硝酸钾就达到饱和状态。A应该是131.6g硝酸钾溶液中含31.6g的硝酸钾;B没有指明温度;D没说明达到饱和状态。C是正确的。
4.【答案】B
【解析】物质的溶解度要指明四要素,选项A中,没有指明溶液状态,故是错误的;20℃时,向一定量的饱和石灰水中加入生石灰,生石灰就会消耗溶液中的水生成氢氧化钙,故溶液中的氢氧化钙会结晶析出,因此,恢复到原来温度时,溶液中溶质的质量减少,故C错误;同一温度时同种溶质的饱和溶液比其不饱和溶液的质量分数大,但选项D没有指明温度,故是错误的。
5.【答案】A
【解析】该溶液恒温蒸发10g水,析出4g氯化钾固体,则该温度下氯化钾的溶解度为40g。设70g饱和溶液中氯化钾的质量为X,列式140g :40g=70g :X,可得X=20g,则剩余溶液中所含溶质质量为20g-4g=16g。
6.【答案】C 【解析】溶液是一种或几种物质分散到另一种物质里形成的均一、稳定的混合物。无色透明的液体不一定是溶液,如水是无色透明的,但水不是混合物。固体物质的溶解度主要受温度的影响,搅拌可以加快溶质溶解的速度,但不能增大溶质的溶解度。溶液是均一的混合物,故C答案正确。不少学生因没有注意温度而误选D。如20℃时KNO3的溶解度是31.6g,60℃时它的溶解度是110g。这样在20℃时把31.6gKNO3放到100g水中,却还是不饱和溶液,很显然后者的质量分数比前者的大。因此只有在相同温度下,同种溶质的饱和溶液才比它的不饱和溶液的溶质质量分数大。?
7.【答案】D
【解析】
A、丙物质未溶解固体的质量为0,可知丙溶液可能为饱和溶液,也可能为不饱和溶液,故A错误;
B、溶剂质量相同而丁溶液的溶质质量最小,所以丁溶液的溶质质量分数最小,故B错误;
C、溶剂质量相同而甲、乙、丙、丁四种溶液中溶质质量的大小关系为丙>乙>甲>丁,所以20℃时四种物质溶解度的关系为:丙>乙>甲>丁,故C错误;
D.四杯溶液中各加入20℃的100 g水后,未溶解的固体全部溶解,故溶质的质量和溶剂的质量相等,溶液质量相等,且均为不饱和溶液。故选D。
8.【答案】B
【解析】
A、甲物质的溶解度随温度的升高而减小,所以20℃时甲物质的饱和溶液升高温度还是饱和溶液,故A错误;
B、乙物质的溶解度随温度的升高而增大,所以100℃时乙物质的饱和溶液冷却到室温会析出晶体,但溶液仍饱和,故B正确;
C、甲、乙两种物质的溶液状态不能确定,所以20℃时,甲、乙溶液的溶质质量分数不能确定,故C错误;
D、20℃时,乙物质的溶解度是31.6g,100克乙物质不能全部溶解,溶质质量分数为:×100%=24%,故D错误。
9.【答案】C
【解析】关于溶液稀释或浓缩(无溶质析出)的计算一定要抓住:溶液稀释或浓缩(无溶质析出)前后,溶质的质量不变。关于溶液浓缩(无溶质析出)的计算,要根据浓缩的具体类型来具体分析找出等量关系来解决。
10.【答案】A = 160g ? 【解析】观察AB的溶解度曲线可以看出A的溶解度随温度升高变化的多。t1℃时AB的溶解度曲线交于一点,也就是t1℃时二者的溶解度相等。t2℃时B的溶解度是60g,把80gB放入100g水中只能溶解60g,因此得到的溶液质量为160g。
11.【答案】①②④
12.【答案】105g
【解析】60℃时,50g水最多能溶解硝酸钾55g,所得溶液的质量为50g+55g=105g。
13.【答案】26.5% 23.1%
14.【答案】(1)= (2)甲 (3)140 A
【解析】
(1)10℃时,甲物质的溶解度曲线和乙物质的溶解度曲线交于一点,二者的溶解度相等;
(2)把30℃时等质量的甲、乙两物质饱和溶液降温到10℃,由于甲的溶解度变化幅度大于乙,所以甲析出晶体较多;
(3)20℃时甲的溶解度是40g,即100g水中最多溶解40g的甲,所以将50g甲物质放入盛有100g水的烧杯中,最终所得溶液的质量为140g;若将烧杯内物质升温到30℃(不考虑水蒸发),溶剂质量不变,溶解度变大,溶质会继续溶解,则溶液中不变的是溶剂的质量,所以升温溶质的质量分数增大。
15.【答案】(1)13g (2)9.8% (3)15.1% (4)96g
【学习目标】
1.掌握饱和溶液、不饱和溶液、溶解度等概念及相互关系;掌握溶解度曲线的意义及应用。
2.认识一种溶液组成的表示方法——溶质的质量分数;掌握溶质质量分数的有关计算。 3.初步学会配制一定溶质质量分数的溶液。
【典型例题】
类型一、考查饱和溶液、不饱和溶液、溶解度及溶解度曲线的应用 1.(2019?重庆中考)如图是甲、乙两种固体物质在水中的溶解度曲线,下列说法不正确的是( )
A. 10℃时,甲、乙两种物质的饱和溶液浓度相同 B. 保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液
C. 30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80g D. 10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大
【思路点拨】固体溶解度曲线所能表示的意义:①根据已知的温度可以查出有关物质的溶解度;②根据物质的溶解度也可以查出它所对应的温度;③可以判断或比较相同温度下,不同物质溶解度的大小(或饱和溶液中溶质的质量分数的大小);④根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶、升温结晶);并且,还可以判断或比较析出晶体的质量大小,即曲线越陡,析出的晶体就越多;⑤两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;并且,此时两种物质饱和溶液的溶质质量分数也相同的。
【答案】D 【解析】10℃时,甲、乙两种物质的溶解度相同,故饱和溶液浓度相同,A选项正确。保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液,B选项正确。30℃时,甲的溶解度为60g,将40g甲物质加入50g水中,充分溶解只能溶解30g,溶液的质量为80g,C选项正确。10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数不变,D选项错误。
【总结升华】解答这类题目时,首先,要熟记和理解固体溶解度曲线及其使用,固体溶解度的概念和意义,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法;然后结合所学的相关知识和技能,细致地阅读、分析题意等,最后按照题目的要求,认真地进行选择或解答即可。
2.下图是a、b、c三种物质的溶解度曲线。请回答: (1)P点的含义是_____________________。 (2)t2℃时30g a物质加入到50g水中不断搅拌,形成的溶液质量是______g。 (3)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是________(填写物质序号)。 (4)在t2℃时,将等质量的a、b、c三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是 ,所得溶液中溶质质量分数最小的是_______。
【答案】(1)t1℃时a和c的溶解度均为20g
(2)75 (3)cba (4)a c
【解析】溶解度曲线上的点表示一定温度下该物质的溶解度。由溶解度曲线可知,t2℃时a的溶解度为50g,因此a在50g水中最多可溶解25g,则30ga加入到50g水中形成溶液的质量为75g。t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是c、b、a。a物质的溶解度随温度升高变化较大,因此降温时析出晶体最多;t2℃时C的溶解度最小,饱和溶液的溶质质量分数最小,降温到t1℃时其溶质质量分数不变,还是最小。
【总结升华】认真分析溶解度曲线,弄清各物质溶解度随温度的变化趋势是解题的关键。 举一反三: 【变式】(2019?四川中考)如图为甲、乙两种盐的溶解度曲线,下列说法正确的是( )
A. 甲、乙两种物质的溶解度都不相等 B. 将接近饱和的甲溶液变为饱和溶液,可采用蒸发或降温的方法
C. t1℃时,甲、乙两种物质的饱和溶液中,溶质的质量分数均为15% D. t2℃时,将30克乙物质放入100克水中,所得溶液的质量为130克 【答案】B 【解析】
A、溶解度大小比较需要指明具体的温度,故A错误;
B、甲的溶解度随温度升高而增大,故甲的不饱和溶液变为饱和溶液需要蒸发或降温,故B正确;
C、t1℃时,甲、乙两种物质的溶解度相同,所以它们的饱和溶液中,溶质的质量分数均为×100%<15%,故C错误;
D、t2℃时,乙物质的溶解度小于30g,此温度下,将30克乙物质放入100克水中,所得溶液的质量小于130克,故D错误。
类型二、考查溶液的配制、溶质质量分数和溶液的稀释等有关计算
3.双氧水(H2O2)既是工业上的重要的绿色氧化剂,又是常用的医药消毒剂。小明从试剂商店购得一瓶质量分数为30%的双氧水,用于制取氧气。若要配制5%的双氧水600g,需要30%的双氧水的质量为___________。需加水的体积是___________。 【答案】100g 500mL 【解析】用浓溶液配置稀溶液的过程中溶质质量不变。根据溶质质量分数的定义可知:溶质的质量=溶液质量×溶质的质量分数。设需要30%的双氧水的质量为X,根据题意可列等式
30%X=600g×5%
解得X=100g
则水的质量为600g-100g=500g,即需加水的体积为500mL。 【总结升华】此题的解题关键是记住溶液稀释前后溶质的质量不变。
4.小明利用家庭小实验粗略测定食醋中醋酸的质量分数。方法是:用注射器吸取20mL食醋,逐滴加入到5.3g 10%的碳酸钠溶液中,至不再产生气泡为止,此时注射器中剩余的食醋为8mL。请计算食醋中醋酸的质量分数。(已知食醋的密度近似为1g/cm3,Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑) 【答案】
解:滴加食醋的质量为(20ml-8ml)×1g/cm3=12g ? 参加反应的碳酸钠质量为5.3g×10%=0.53g 设反应消耗醋酸的质量为x。 ? Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑ 106 120 0.53g x ? ? 食醋中醋酸的质量分数为:
答:食醋中醋酸的质量分数为5%。 【解析】想计算食醋中醋酸的质量分数,需要知道食醋的质量以及所含醋酸的质量。已知所用食醋的体积为12mL,即12g;12g食醋中含醋酸的质量可以根据化学方程式求出。 【总结升华】解关于化学方程式和溶质质量分数结合的计算题,要注意参加反应的或者生成的物质的质量是溶液中的溶质质量。 举一反三:
【变式1】现欲将粗盐提纯,并用制得的精盐配制质量分数一定的氯化钠溶液。下列说法不正确的是( ) A.粗盐溶解时,可边加粗盐边用玻璃棒搅拌加速溶解 B.过滤滤液时,可以直接把溶有粗盐的液体直接倒入漏斗? C.配制溶液需要经过计算、称量、溶解、装液等步骤? D.配制溶液时必备的仪器有托盘天平、量筒、烧杯、玻璃棒等
【答案】B 【解析】粗盐提纯需要先溶解,用玻璃棒搅拌可以加速溶解;过滤时不能直接把液体倒入漏斗,必须用玻璃棒引流。A、C、D三个选项的说法都是正确的。 【变式2】四川汶川抗震救灾期间,为了防止灾后疫情的发生,每天需要喷洒大量的消毒液。 (1)800Kg 质量分数为0.5% 的过氧乙酸消毒液中,过氧乙酸的质量为__________kg。 (2)要配制 800Kg 质量分数为0.5% 的过氧乙酸消毒液,需要质量分数为16% 的过氧乙酸溶液的质量是多少?
【答案】
解:(1)800kg×0.5%=4kg (2)解:设需要质量分数为16%过氧乙酸溶液的质量为X。 X·16% = 4 Kg? X = 25 Kg? 答:需要质量分数为16%的过氧乙酸溶液的质量是25kg。 【变式3】过氧化氢溶液长期保存会自然分解,使得溶质质量分数
减小。小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一
起测定溶质质量分数。他们取出该溶液51g,加入适量二氧化锰,
生成氧气的质量与反应时间的关系如图所示。 (1)求完全反应后生成氧气的质量为________。 (2)计算该溶液中溶质的质量分数。 【答案】 (1)0.48g (2)解:设51g过氧化氢溶液中含过氧化氢的质量为x。 2H2O22H2O + O2↑ 68 32 x 0.48g 过氧化氢溶液中溶质的质量分数为
答:该溶液中溶质的质量分数为2%。 【解析】根据图中数据可知反应后生成氧气的质量是0.48g。溶液中溶质的质量分数为溶质质量和溶液质量之比。分析已知数据,需要求出溶质过氧化氢的质量;根据氧气的质量,利用化学方程式就可计算出反应中分解的过氧化氢质量。
溶解度和溶质的质量分数(提高)
【巩固练习】
选择题 (每小题只有一个选项符合题意)
1.下列有关溶液的说法错误的是( )? ①碘酒中的溶质是酒精;②改变条件,饱和溶液与不饱和溶液可相互转化;③氢氧化钙的饱和溶液一定是浓溶液;④析出晶体后的溶液是该温度下的饱和溶液
A.①② B.②③ C.①③ D.③④
2.小红同学在一定温度下进行KNO3的溶解实验,实验数据如下:? ? 根据上述实验数据,下列叙述正确的是( )
A.实验1所得溶液的溶质质量分数=80g÷100g×100%
B.实验2所得溶液为饱和溶液
C.实验4所得溶液的溶质质量分数比实验3大
D.该温度下,KNO3饱和溶液的溶质质量分数=110g÷210g×100%
3.对“20℃时,硝酸钾溶解度为31.6g”这句话解释正确的是( ) A.20℃时,100g硝酸钾溶液中含有31.6g硝酸钾 B.在100g水中溶解31.6g硝酸钾就达到饱和状态
C.20℃时,100g水中溶解31.6g硝酸钾就达到饱和状态
D.20℃时,31.6g硝酸钾被131.6g水溶解就达到饱和状态 4.下列关于溶液的说法正确的是( )
A.20℃时,在100g水中溶解了30g氯化钠,则20℃时氯化钠的溶解度是30g
B.气体物质的溶解度,随温度的升高而减小,随压强的增大而增大
C.在20℃时,向一定量的饱和石灰水中加入少量生石灰,若恢复到原温度时,溶液中溶质的质量不变
D.饱和硝酸钠溶液一定比不饱和硝酸钠溶液的溶质质量分数大
5.取70g某温度下的氯化钾饱和溶液,将其恒温蒸发10g水,析出4g氯化钾固体,则剩余溶液中所含溶质质量为( )
A.16g B.20g C.40g D.56g
6.下列说法中正确的是( )
A.无色透明的液体一定是溶液
B.配制溶液时,搅拌可以增大溶质的溶解度
C.将10%的氯化钠溶液倒出一半,剩余溶液中溶质的质量分数仍为10%
D.同种溶质的饱和溶液,一定比它的不饱和溶液的溶质质量分数大
7.(2019?四川中考)20℃时,取甲、乙、丙、丁四种纯净物各40 g,分别加入到四个各盛有100g水的烧杯中,充分溶解,其溶解情况如下表:
物质
甲
乙
丙
丁
未溶解固体的质量/g
8.4
4
0
18.4
下列说法正确的是( )
A. 所得四杯溶液都是饱和溶液 B. 丁溶液的溶质质量分数最大
C. 20℃时四种物质溶解度的关系为:丁>甲>乙>丙
D. 四杯溶液中各加入20℃的100 g水后,溶液质量相等,且均为不饱和溶液
8.(2019?浙江中考)下表是固体甲和乙在不同温度时的溶解度。下列说法中正确的是( )
温度/℃
0
20
40
100
甲溶解度/克
0.73
0.165
0.121
0.076
乙溶解度/克
13.3
31.6
63.9
246
A.20℃时甲物质的饱和溶液升高温度会变为不饱和溶液 B.100℃时乙物质的饱和溶液冷却到室温会析出晶体,但溶液仍饱和
C.20℃时.甲溶液的溶质质量分数一定小于乙溶液的溶质质量分数
D.20℃时,100克乙物质加入100克水中.所得溶液的溶质质量分数等于50%
9.有40g质量分数为5%的氯化钙溶液,若将其质量分数增加到10%,应采用的方法是( )
A.把溶剂蒸发掉一半 B.加入40g质量分数为20%的氯化钙溶液
C.把溶剂蒸发掉20g D.加入2g氯化钙固体
二、填空题
10.如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题:
(1)A、B两种物质的溶解度受温度影响较大的是_______;
(2)t1℃时,A物质的溶解度___________ B物质的溶解度(填“>”、“=”或“<”);t2℃时,把80g B物质放入100g 水中,充分搅拌,得到溶液的质量________g。
11.如图是甲、乙两种物质的溶解度曲线,下列说法不正确的是 。
①升高温度,可使甲的不饱和溶液变为饱和溶液;②50℃时甲的饱和溶液溶质的质量分数为40%;③20℃时,甲、乙两种物质的溶解度相等;④要使乙从其浓溶液中析出,可冷却乙的热浓溶液
12.60℃时,硝酸钾的溶解度为110g。在60℃时,将70g硝酸钾放入50g水中,充分溶解后所得溶液的质量为 。
13.20℃时,食盐的溶解度为36g。该温度下将20g食盐投入50g水中,溶液的溶质质量分数为 。若将15g食盐投入50g水中,所得溶液的溶质质量分数为 。
14.(2019?山东中考)如图是甲、乙两种固体物质的溶解度曲线。据图回答:
(1)10℃时,甲物质的溶解度 乙物质的溶解度.(填“>”或“=”或“<”)。
(2)把30℃时等质量的甲、乙两物质饱和溶液降温到10℃,析出晶体较多的是 。
(3)20℃时,将50g甲物质放入盛有100g水的烧杯中,最终所得溶液的质量为 g;若将烧杯内物质升温到30℃(不考虑水蒸发),溶液中不变的是 (填序号)。
A.溶剂的质量 B.溶液的质量 C.溶质的质量分数 D.以上都不变
三、计算题
15.(2019?福建中考)一定量的锌与200g硫酸溶液恰好反应,生成氢气0.4g,计算:(1)参加反应的锌的质量。(2)硫酸溶液溶质的质量分数。(3)反应后所得溶液的溶质质量分数。(4)将此硫酸溶液100g稀释成5%的硫酸溶液,需要加水的质量。
【答案与解析】
1.【答案】C?
【解析】碘酒中的溶质是碘,酒精是溶剂,故①不正确;饱和溶液和不饱和溶液在一定条件下可相互转化,故②正确;氢氧化钙微溶于水,其饱和溶液浓度很小,属于稀溶液,故③不正确;有晶体析出的溶液是该温度下的饱和溶液,故④正确。?
2.【答案】D? 【解析】实验1所得溶液溶质质量分数=80g÷(100g+80g)×100%,故A错;由实验3提供数据知,实验2为不饱和溶液,故B错;由于实验3和实验4都是饱和溶液,在100 g水中最多能溶解110 gKNO3,故它们的溶质质量分数相等,故C错;该温度下KNO3饱和溶液的溶质质量分数=110g÷210g×100%,故D正确。 ??
3.【答案】C
【解析】20℃时,硝酸钾溶解度为31.6g,是表示20℃时100g水中溶解31.6g硝酸钾就达到饱和状态。A应该是131.6g硝酸钾溶液中含31.6g的硝酸钾;B没有指明温度;D没说明达到饱和状态。C是正确的。
4.【答案】B
【解析】物质的溶解度要指明四要素,选项A中,没有指明溶液状态,故是错误的;20℃时,向一定量的饱和石灰水中加入生石灰,生石灰就会消耗溶液中的水生成氢氧化钙,故溶液中的氢氧化钙会结晶析出,因此,恢复到原来温度时,溶液中溶质的质量减少,故C错误;同一温度时同种溶质的饱和溶液比其不饱和溶液的质量分数大,但选项D没有指明温度,故是错误的。
5.【答案】A
【解析】该溶液恒温蒸发10g水,析出4g氯化钾固体,则该温度下氯化钾的溶解度为40g。设70g饱和溶液中氯化钾的质量为X,列式140g :40g=70g :X,可得X=20g,则剩余溶液中所含溶质质量为20g-4g=16g。
6.【答案】C 【解析】溶液是一种或几种物质分散到另一种物质里形成的均一、稳定的混合物。无色透明的液体不一定是溶液,如水是无色透明的,但水不是混合物。固体物质的溶解度主要受温度的影响,搅拌可以加快溶质溶解的速度,但不能增大溶质的溶解度。溶液是均一的混合物,故C答案正确。不少学生因没有注意温度而误选D。如20℃时KNO3的溶解度是31.6g,60℃时它的溶解度是110g。这样在20℃时把31.6gKNO3放到100g水中,却还是不饱和溶液,很显然后者的质量分数比前者的大。因此只有在相同温度下,同种溶质的饱和溶液才比它的不饱和溶液的溶质质量分数大。?
7.【答案】D
【解析】
A、丙物质未溶解固体的质量为0,可知丙溶液可能为饱和溶液,也可能为不饱和溶液,故A错误;
B、溶剂质量相同而丁溶液的溶质质量最小,所以丁溶液的溶质质量分数最小,故B错误;
C、溶剂质量相同而甲、乙、丙、丁四种溶液中溶质质量的大小关系为丙>乙>甲>丁,所以20℃时四种物质溶解度的关系为:丙>乙>甲>丁,故C错误;
D.四杯溶液中各加入20℃的100 g水后,未溶解的固体全部溶解,故溶质的质量和溶剂的质量相等,溶液质量相等,且均为不饱和溶液。故选D。
8.【答案】B
【解析】
A、甲物质的溶解度随温度的升高而减小,所以20℃时甲物质的饱和溶液升高温度还是饱和溶液,故A错误;
B、乙物质的溶解度随温度的升高而增大,所以100℃时乙物质的饱和溶液冷却到室温会析出晶体,但溶液仍饱和,故B正确;
C、甲、乙两种物质的溶液状态不能确定,所以20℃时,甲、乙溶液的溶质质量分数不能确定,故C错误;
D、20℃时,乙物质的溶解度是31.6g,100克乙物质不能全部溶解,溶质质量分数为:×100%=24%,故D错误。
9.【答案】C
【解析】关于溶液稀释或浓缩(无溶质析出)的计算一定要抓住:溶液稀释或浓缩(无溶质析出)前后,溶质的质量不变。关于溶液浓缩(无溶质析出)的计算,要根据浓缩的具体类型来具体分析找出等量关系来解决。
10.【答案】A = 160g ? 【解析】观察AB的溶解度曲线可以看出A的溶解度随温度升高变化的多。t1℃时AB的溶解度曲线交于一点,也就是t1℃时二者的溶解度相等。t2℃时B的溶解度是60g,把80gB放入100g水中只能溶解60g,因此得到的溶液质量为160g。
11.【答案】①②④
12.【答案】105g
【解析】60℃时,50g水最多能溶解硝酸钾55g,所得溶液的质量为50g+55g=105g。
13.【答案】26.5% 23.1%
14.【答案】(1)= (2)甲 (3)140 A
【解析】
(1)10℃时,甲物质的溶解度曲线和乙物质的溶解度曲线交于一点,二者的溶解度相等;
(2)把30℃时等质量的甲、乙两物质饱和溶液降温到10℃,由于甲的溶解度变化幅度大于乙,所以甲析出晶体较多;
(3)20℃时甲的溶解度是40g,即100g水中最多溶解40g的甲,所以将50g甲物质放入盛有100g水的烧杯中,最终所得溶液的质量为140g;若将烧杯内物质升温到30℃(不考虑水蒸发),溶剂质量不变,溶解度变大,溶质会继续溶解,则溶液中不变的是溶剂的质量,所以升温溶质的质量分数增大。
15.【答案】(1)13g (2)9.8% (3)15.1% (4)96g
同课章节目录
