人教版高中化学选修5教学讲义,复习补习资料(含知识讲解,巩固练习):19【基础】糖类
文档属性
| 名称 | 人教版高中化学选修5教学讲义,复习补习资料(含知识讲解,巩固练习):19【基础】糖类 |

|
|
| 格式 | zip | ||
| 文件大小 | 269.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-26 00:00:00 | ||
图片预览



文档简介
糖类
【学习目标】
1、了解糖类的组成和分类以及糖类在工农业生产和社会生活中的广泛方法应用和重要意义;
2、掌握糖类中重要的代表物葡萄糖、蔗糖、淀粉、纤维素的组成和主要性质,它们之间的相互转化关系以及与烃的衍生物的关系。
【要点梳理】
要点一、糖类的组成和分类
1.糖类的组成。
(1)糖类是由碳、氢、氧三种元素组成的一类有机化合物,大多数糖类的分子组成可用通式Cm(H2O)n来表示(m、n可以相同,也可以不同)。
注意:对糖类的通式的理解应注意两点:
①该通式只表明糖类由C、H、O三种元素组成,并未反映糖类的结构特点。
②有些属于糖类的物质不符合该通式,如脱氧核糖C5H10O4;而有些符合该通式的物质却不属于糖类。如乙酸CH3COOH、乳酸。
(2)从结构上看,糖类可定义为多羟基醛或多羟基酮,以及水解后可以生成多羟基醛或多羟基酮的化合物。
2.糖类的分类。
(1)根据能否水解以及水解后的产物,糖类可分为单糖、低聚糖和多糖。
单糖是不能水解的糖,一般为多羟基醛或多羟基酮,如葡萄糖、果糖、核糖及脱氧核糖等。
低聚糖是1 mol糖水解后能产生2 mol~10 mol单糖的糖类。其中以二糖最为重要,常见的二糖有麦芽糖、蔗糖和乳糖等。
多糖是1 mol糖水解后能产生很多摩尔单糖的糖类。如淀粉、纤维素等。多糖属于天然高分子化合物。
(2)单糖、低聚糖、多糖之间的相互转化关系为:
(3)糖类是绿色植物光合作用的产物,是一切生命体维持生命活动所需能量的主要来源。
要点二、糖类的结构和性质
1.葡萄糖的结构、性质和用途。
葡萄糖是自然界中分布最广的单糖,主要存在于葡萄及其他带有甜味的水果、蜂蜜中,植物的种子、叶、根、花中,动物的血液、脑脊液和淋巴液中。
(1)分子结构。
葡萄糖的分子式为C6H12O6,结构简式为CH2OH(CHOH)4CHO。它是一种多羟基醛。
(2)物理性质。
葡萄糖是无色晶体,熔点为146℃,有甜味,但甜度不如蔗糖,易溶于水,稍溶于乙醇,不溶于乙醚。
(3)化学性质。
葡萄糖分子中含有醛基和醇羟基,可发生氧化、加成、酯化等反应。
①氧化反应。
a.燃烧。
C6H12O6(s)+6O2(g)—→6CO2(g)+6H2O(1) ΔH=-2804kJ·mol-1
b.被银氨溶液或新制的Cu(OH)2氧化。
CH2OH(CHOH)4CHO+2Ag(NH3)2OHCH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
CH2OH(CHOH)4CHO+2Cu(OH)2CH2OH(CHOH)4COOH+Cu2O↓+2H2O
②加成反应。
CH2OH(CHOH)4CHO+H2CH2OH(CHOH)4CH2OH(己六醇)
③酯化反应。
特别提示:葡萄糖是单糖,不能发生水解反应。
(4)主要用途。
葡萄糖用于糖果制造业,还可用于医药工业。
2.果糖简介。
(1)果糖是最甜的糖,广泛分布在植物中,在水果和蜂蜜中含量较高。
(2)果糖的分子式为C6H12O6,结构简式为,它是一种多羟基酮。果糖与葡萄糖互为同分异构体。
(3)纯净的果糖为无色晶体,熔点为103 ~105℃,它不易结晶,通常为黏稠性液体,易溶于水、乙醇和乙醚。果糖是最甜的糖。
(4)果糖分子中含有酮基和醇羟基,能发生加成、酯化反应。
3.蔗糖与麦芽糖。
蔗糖与麦芽糖都是重要的二糖,蔗糖为白色晶体,麦芽糖为无色晶体,两者都易溶于水,都有甜味。
蔗糖与麦芽糖的比较
蔗糖
麦芽糖
相似点
①组成相同,化学式均为C12H22O11,互为同分异构体
②都属于二糖,每摩尔水解后生成两摩尔单糖
③水解产物都能发生银镜反应,都能还原新制Cu(OH)2
④都具有甜味(蔗糖更甜)
不
同
点
官能团
不含醛基(非还原性糖)
含有醛基(还原性糖)
化学性质
不能发生银镜反应,也不能还原新制Cu(OH)2
能发生银镜反应,能还原新制Cu(OH)2
水解产物
葡萄糖和果糖各半
仅有葡萄糖
来源
以甘蔗和甜菜含量最多
淀粉在酶作用下的水解产物
用途
甜味食物、制红糖、白糖等
甜味食物、制饴糖
4.淀粉与纤维素。
淀粉和纤维素是最重要的多糖。两者具有相同的分子通式(C6H10O5)n。它们都是由许多个单糖单元(C6H10O5)构成的天然高分子化合物。但由于n值不同,两者不是同分异构体关系,又由于结构不同,两者也不是同系物关系。
(1)淀粉与纤维素的比较
名称
淀粉
纤维素
存在
存在于植物种子、块根、谷类等中
存在于棉花、木材等中
通式
(C6H10O5)n
(C6H10O5)n
结构特点
由几百个到几千个单糖单元构成的高分子化合物
由比淀粉更多的单糠单元构成的高分子化合物
物理性质
白色粉末,不溶于冷水,一部分可溶于热水,无甜味
白色、无嗅、无味的物质,不溶于水,无甜味
化
学
性
质
加碘水
淀粉与碘作用呈现蓝色
纤维素与碘不作用,不变蓝,可用于鉴别淀粉和纤维素
水解
在淀粉酶作用下水解成麦芽糖,在无机酸作用下水解成葡萄糖
在无机酸催化作用下水解,最后生成葡萄糖,比淀粉水解困难
酯化
不能发生酯化反应
生成火棉、胶棉和醋酝纤维
用途
作工业原料,制取葡萄糖、酒精等
可用于纺织工业、造纸工业,制硝酸纤维、醋酸纤维和黏胶纤维等
(2)淀粉和纤维素的主要化学性质。
①都无还原性。
淀粉和纤维素都不能被银氨溶液或新制的Cu(OH)2氧化,因而都没有还原性。
②都能水解,其水解的最终产物都是葡萄糖,但纤维素比淀粉更难水解。
(C6H10O5)n +nH2OnC6H12O6
(淀粉或纤维素) (葡萄糖)
③淀粉遇碘单质变蓝色,纤维素遇碘单质不变色,因此可用碘单质来鉴定淀粉的存在或区分淀粉和纤维素。
④纤维素分子的每个单糖单元有3个醇羟基,其分子通式可表示为[C6H7O2(OH)3]n,能表现出醇的性质。如能与HNO3、CH3COOH等发生酯化反应。
要点三、糖类之间的相互转化关系
注:C6H12O62C2H5OH+2CO2。
【典型例题】
类型一:糖类的结构和性质
例1 下列物质中,在一定条件下既能发生银镜反应,能发生水解反应的是( )。
①甲酸甲酯 ②蔗糖 ③葡萄糖 ④麦芽糖
A.①④ B.②③ C.①③ D.③④
【思路点拨】本题考查物质的结构以及有机物官能团的性质。能发生银镜反应的是醛基,能发生水解反应的是卤素原子或者酯基。
【答案】A
【解析】能发生银镜反应,说明有机物结构中含有醛基已学过的能发生水解反应的有机物有卤代烃、酯及低聚糖或糖等。甲酸甲酯中有和;蔗糖能发生水解反应,但无;葡萄糖能发生银镜反应,但不能水解麦芽糖是还原性糖,能发生银镜反应,同时也能发生水解反应。故答案为A。
【总结升华】在总结有机化学内容时,注意整理有机官能团可以发生的反应,以及发生有机反应的官能团。比如醛基可以与银氨溶液、新制氢氧化铜发生氧化反应,也可以与氢气发生还原(或加成)反应;发生水解反应的有卤代烃中的卤素原子及酯基。
举一反三:
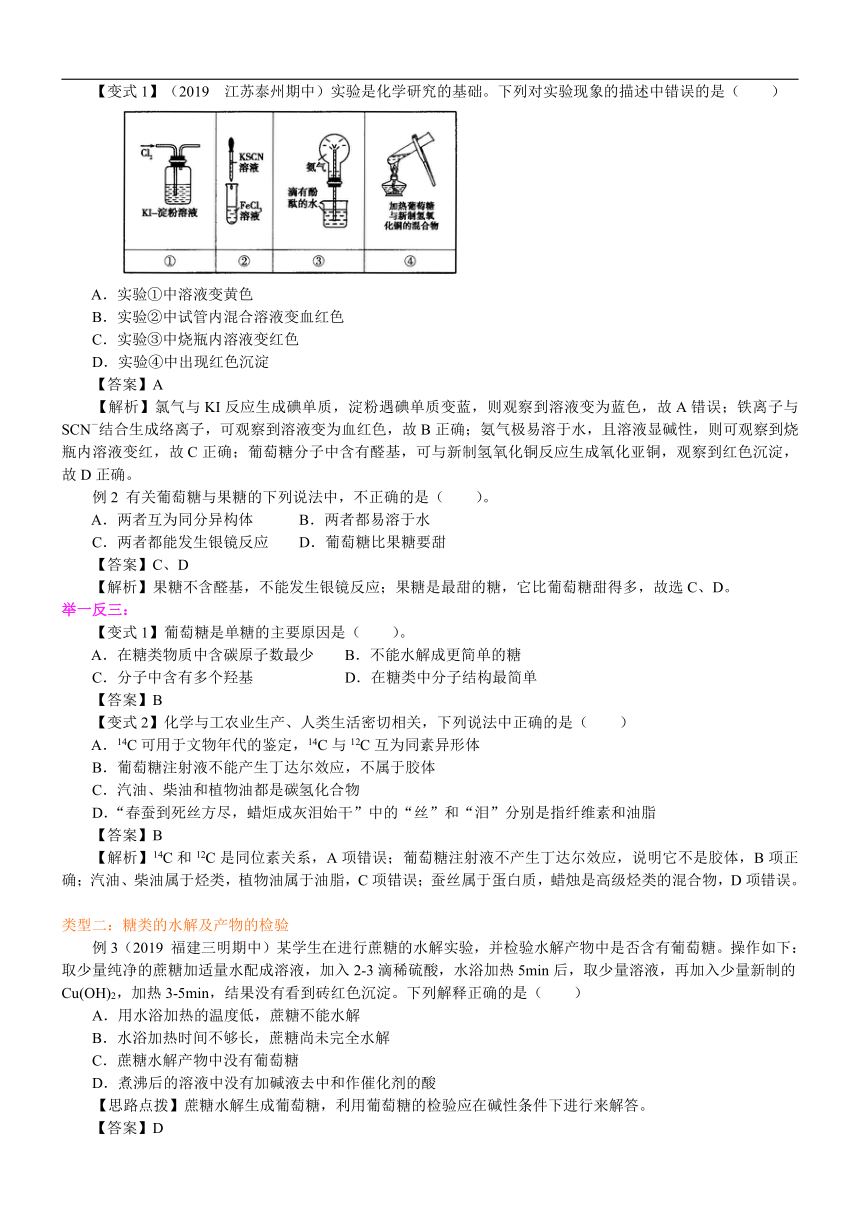
【变式1】(2019 江苏泰州期中)实验是化学研究的基础。下列对实验现象的描述中错误的是( )
A.实验①中溶液变黄色
B.实验②中试管内混合溶液变血红色
C.实验③中烧瓶内溶液变红色
D.实验④中出现红色沉淀
【答案】A
【解析】氯气与KI反应生成碘单质,淀粉遇碘单质变蓝,则观察到溶液变为蓝色,故A错误;铁离子与SCN-结合生成络离子,可观察到溶液变为血红色,故B正确;氨气极易溶于水,且溶液显碱性,则可观察到烧瓶内溶液变红,故C正确;葡萄糖分子中含有醛基,可与新制氢氧化铜反应生成氧化亚铜,观察到红色沉淀,故D正确。
例2 有关葡萄糖与果糖的下列说法中,不正确的是( )。
A.两者互为同分异构体 B.两者都易溶于水
C.两者都能发生银镜反应 D.葡萄糖比果糖要甜
【答案】C、D
【解析】果糖不含醛基,不能发生银镜反应;果糖是最甜的糖,它比葡萄糖甜得多,故选C、D。
举一反三:
【变式1】葡萄糖是单糖的主要原因是( )。
A.在糖类物质中含碳原子数最少 B.不能水解成更简单的糖
C.分子中含有多个羟基 D.在糖类中分子结构最简单
【答案】B
【变式2】化学与工农业生产、人类生活密切相关,下列说法中正确的是( )
A.14C可用于文物年代的鉴定,14C与12C互为同素异形体
B.葡萄糖注射液不能产生丁达尔效应,不属于胶体
C.汽油、柴油和植物油都是碳氢化合物
D.“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是指纤维素和油脂
【答案】B
【解析】14C和12C是同位素关系,A项错误;葡萄糖注射液不产生丁达尔效应,说明它不是胶体,B项正确;汽油、柴油属于烃类,植物油属于油脂,C项错误;蚕丝属于蛋白质,蜡烛是高级烃类的混合物,D项错误。
类型二:糖类的水解及产物的检验
例3(2019 福建三明期中)某学生在进行蔗糖的水解实验,并检验水解产物中是否含有葡萄糖。操作如下:取少量纯净的蔗糖加适量水配成溶液,加入2-3滴稀硫酸,水浴加热5min后,取少量溶液,再加入少量新制的Cu(OH)2,加热3-5min,结果没有看到砖红色沉淀。下列解释正确的是( )
A.用水浴加热的温度低,蔗糖不能水解
B.水浴加热时间不够长,蔗糖尚未完全水解
C.蔗糖水解产物中没有葡萄糖
D.煮沸后的溶液中没有加碱液去中和作催化剂的酸
【思路点拨】蔗糖水解生成葡萄糖,利用葡萄糖的检验应在碱性条件下进行来解答。
【答案】D
【解析】取少量纯蔗糖加适量水配成溶液,在蔗糖溶液中加入3-5滴稀硫酸,将混合液煮沸几分钟、冷却,则蔗糖在酸性条件下水解生成葡萄糖,而葡萄糖的检验应在碱性条件下进行,应先加碱中和至碱性,再加入适量的新制Cu(OH)2并加热至沸腾,可观察到砖红色沉淀生成,所以在酸性条件下不能生成Cu2O,故没有观察到砖红色沉淀生成,故选D。
【总结升华】检验糖类的水解产物除可用银氨溶液外,还可使用新制的Cu(OH)2悬浊液,和银镜反应一样,使用Cu(OH)2之前也要先加入NaOH中和作为催化剂的酸,同时所配制的Cu(OH)2中NaOH必须过量,配制的方法是:在洁净的试管中加入10%的NaOH溶液2 mL,然后滴入5%的CuSO4溶液5滴,振荡后即可使用。
举一反三:
【变式1】将蔗糖溶于水,配成10%的溶液,分装在两个试管中,在第一支试管中加入银氨溶液,在水浴中加热,没有变化,原因是蔗糖分子中________;在第二支试管中,加入几滴稀H2SO4,再在水浴中加热,加NaOH中和酸后也加入银氨溶液,现象________,原因是________,稀硫酸的作用是________。
【答案】无醛基 有光亮的银镜产生 蔗糖发生水解,生成葡萄糖 催化剂
【巩固练习】
一、选择题
1.有关糖类物质的叙述中,正确的是( )。
A.凡符合通式Cm(H2O)n的化合物都属于糖类,不符合通式Cm(H2O)n的化合物都不是糖类
B.凡具有甜味的物质都属于糖类,凡不具有甜味的物质都不属于糖类
C.糖类物质只含碳、氢、氧三种元素,但含碳、氢、氧三种元素的有机物不一定是糖类
D.糖类物质有的有还原性,有的没有还原性
2.下列有关葡萄糖的叙述中,错误的是( )。
A.能加氢生成六元醇 B.能发生银镜反应
C.能与醇发生酯化反应 D.能被氧化为CO2与H2O
3.崇明米酒既有酒味又有甜味,其中甜味来源的途径是( )。
A.淀粉→蔗糖→葡萄糖 B.淀粉→麦芽糖→葡萄糖
C.淀粉→麦芽糖→果糖 D.淀粉→蔗糖→果糖
4.(2019 延边州期末)蔬菜、水果中富含纤维素,纤维素被食入人体后的作用是( )
A.为人体内的化学反应提供原料
B.为维持人体生命活动提供能量
C.加强胃肠蠕动,具有通便功能
D.人体中没有水解纤维素的酶,所以纤维素在人体中没有任何作用
5.关于葡萄糖和蔗糖的比较,下列说法不正确的是( )。
A.葡萄糖不能水解,蔗糖能水解
B.蔗糖的相对分子质量是葡萄糖的2倍
C.葡萄糖是还原性糖,蔗糖是非还原性糖
D.浓硫酸能使它们都发生炭化现象
6.下列有关麦芽糖的叙述中,错误的是( )。
A.纯净的麦芽糖是白色晶体,易溶于水,有甜味
B.麦芽糖能发生银镜反应,是一种还原性糖
C.1 mol麦芽糖水解得到1 mol葡萄糖和1 mol果糖
D.麦芽糖和蔗糖互为同分异构体
7.将淀粉水解并用Cu(OH)2碱性溶液检验水解产物的实验中,要进行的主要操作有:①加热;②滴入稀硫酸;③加入新制的Cu(OH)2溶液;④加入NaOH溶液中和。以上各步操作的先后顺序的正确排列是( )。
A.①②③④① B.②①④③① C.②①④③ D.④③①②①
8.(2019 北京西城期末)下列鉴别实验中,所选试剂不合理的是( )
A.用水鉴别乙醇和苯
B.用碳酸氢钠溶液鉴别乙酸和乙醇
C.用新制的氢氧化铜鉴别葡萄糖和蔗糖
D.用高锰酸钾酸性溶液鉴别甲苯和己烯
9.(2019 西安模拟)新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述不正确的是( )。
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质
C.防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖
10.已知有如下过程:
根据上图,a、b、c可分别表示( )。
A.淀粉、酶、葡萄糖 B.蔗糖、酶、果糖
C.纤维素、酶、葡萄糖 D.麦芽糖、酶、葡萄糖
二、填空题
1.有A、B、C、D四种有机物,均由碳、氢、氧三种元素组成。A、B的实验式相同,B、C的分子式相同,B、c在一定条件下相互作用可生成D。常温常压下,A是气体,B、C、D是固体,四种物质均易溶于水,A、B可发生银镜反应,B的相对分子质量是A的6倍。
(1)写出四种有机物的名称:A________、B________、C________。
(2)写出D的一种同分异构体发生水解的化学方程式:________________。
2.淀粉和纤维素的分子组成都可用通式________表示,但二者的n值________同。它们都属于________糖,在性质上与单糖、二糖不同,没有________味,都________(填“能”或“不能”)发生银镜反应,但在硫酸的催化作用下,都能发生________反应,其反应的最终产物都是________。纤维素在硫酸催化作用下发生反应的化学方程式是________________。
3.聚乳酸是一种新型可被生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料。聚乳酸材料废弃后,先水解成乳酸(),乳酸在微生物作用下分解为CO2和H2O。
(1)乳酸的工业生产可以采用生物发酵法。
①检验淀粉是否完全水解,可以选用的一种试剂是________(填序号)。
a.溴水 b.银氨溶液 c.碘酒 d.碘化钾淀粉溶液
②用18吨葡萄糖发酵,理论上可以得到乳酸的质量是________吨。
(2)乳酸的生产也可以采用有机合成法,其中的一种方法是丙酸法。
①反应Ⅰ的反应类型是________反应。
②进行反应Ⅱ时,需要加入过量的乙醇,这样做的目的是________。
(3)两个乳酸分子之间可以形成环状的酯,该环状酯的结构简式是________。乳酸在一定条件下发生反应得到聚乳酸的化学方程式是________。
4.某酒精厂用含淀粉50%的白薯干制取酒精,如果发酵过程中有20%的淀粉损失掉,计算生产含水量8%的酒精10 t,理论上需用这种白薯干多少吨?
【参考答案与解析】
一、选择题
1.C、D
【解析】C2H4O2、CH2O等不属于糖类,而C5H10O4(脱氧核糖)却是糖类;糖类有的有甜味,有的没有甜味;含C、H、O的有机物还可能是其他烃的含氧衍生物,如醇、酚、醛、羧酸、酯等;葡萄糖、麦芽糖等有还原性,而蔗糖、淀粉等没有还原性。
2.C
【解析】葡萄糖的分子结构为CH2OH(CHOH)4CHO,其分子中含有5个醇羟基和一个醛基,含有醛基,可与氢加成得到六元醇,与银氨溶液反应可生成银镜;含有醇羟基,可与羧基反应生成酯;葡萄糖由C、H、O三种元素组成,可燃烧生成CO2和H2O(在人体中被氧化为CO2和H2O)。
3.B
【解析】米中含有大量的淀粉,在微生物的作用下,淀粉首先水解生成麦芽糖,然后再水解成人的味觉敏感的葡萄糖,从而产生甜味。本题如果知道蔗糖、麦芽糖水解的产物及淀粉水解的最终产物是葡萄糖等知识,也可正确进行判断。
4.C
【解析】A项人不能消化纤维素,纤维素在人体内不能发生反应,故A错误;B项人不能消化纤维素,纤维素不能为人体生命活动提供能量,故B错误;C项纤维素可以促进大肠蠕动,从而促进消化吸收其他营养物质,所以纤维素在防止便秘方面是有利的,故C正确;D项纤维素加强胃肠蠕动,具有通便功能,故D错误。故选C。
5.B
【解析】蔗糖的分子式为C12H22O11,葡萄糖的分子式为C6H12O6,蔗糖的相对分子质量比葡萄糖的2倍略小。
6.C
【解析】麦芽糖是白色晶体;麦芽糖分子中含有醛基,能发生银镜反应,是一种还原性糖;1 mol麦芽糖水解生成2 mol葡萄糖;麦芽糖与蔗糖的分子式相同,而结构不同,两者互为同分异构体。
7.B
【解析】加热既是淀粉在酸催化作用下水解反应的条件,也是其水解产物葡萄糖与新制Cu(OH)2发生反应的条件。滴入稀硫酸用来催化淀粉水解,加入NaOH溶液是为了中和用作催化剂的硫酸。
8.D
【解析】A项,乙醇可以与水互溶,不会分层;苯不溶于水,密度比水小,有机层在上层,故可用水鉴别乙醇和苯。B项,乙酸可以和碳酸氢钠溶液反应生成二氧化碳气体,乙醇不能和碳酸氢钠溶液反应,故可以用碳酸氢钠溶液鉴别乙酸和乙醇。C项,葡萄糖中含有醛基,能够和新制的氢氧化铜反应产生红色沉淀,蔗糖不能和新制的氢氧化铜反应,故可以用新制的氢氧化铜鉴别葡萄糖和蔗糖。D项,甲苯和己烯都能使高锰酸钾酸性溶液褪色,故不能用高锰酸钾酸性溶液鉴别甲苯和己烯。
9.D
【解析】A项棉花、优质针叶木等原料的主要成分是纤维素,故A正确;B项Fe3O4是磁性物质,有磁性,故B正确;C项树脂相对分子质量很大,属于有机高分子材料,故C正确;D项葡萄糖遇碘不变蓝,故D错误。故选D。
10.D
【解析】反应最终结果是1分子a生成2分子c,且b的量不变,这表明b是催化剂(如酶),而a与c应是二糖与单糖的关系。
二、填空题
1.(1)甲醛 葡萄糖 果糖 蔗糖
(2)C12H22O11+H2O2C6H12O6
(麦芽糖) (葡萄糖)
【解析】由C、H、O组成的有机物中仅有HCHO(甲醛)在常温下是气体,则A是甲醛;而B的相对分子质量是A的6倍,其分子式为C6H12O6,可能是葡萄糖,而C与B互为同分异构体,则C是果糖;B、C作用生成D,则D为蔗糖,它的同分异构体是麦芽糖。
2.(C6H10O5)n 不 多 甜 不能 水解 葡萄糖
(C6H10O5)n +nH2OnC6H12O6
(纤维素) (葡萄糖)
【解析】淀粉和纤维素的分子通式都可表示为(C6H10O5)n,但n值不同,它们不是同分异构体;淀粉和纤维素都是多糖,都没有甜味,也不能发生银镜反应,但能水解,其水解的最终产物都是葡萄糖。
3.(1)①c ②18
(2)①取代 ②提高乳酸的转化率
【解析】(1)淀粉若是完全水解,则溶液中已没有淀粉剩余。向溶液中滴加碘酒观察,若不变蓝,则水解完全。由关系式C6H12O6(葡萄糖)~2C3H6O3(乳酸),根据质量守恒定律得m(葡萄糖)=m(乳酸)=18吨。
(2)②加入过量的乙醇,使平衡向生成乳酸乙酯的方向移动,从而提高乳酸的转化率。
(3)抓住酯化反应的原理“酸脱羟基,醇脱氢,生成酯和水”,结合题给要求,即可得出答案。
4.40.5 t。
【解析】解:设理论上需用白薯干的质量为m。由关系式
(C6H10O5)n ~ 2nC2H5OH
162n 92n
50%×(1-20%)·m 10 t×(1-8%)
,
解得m=40.5 t。
答:需用这种白薯干40.5 t。
【学习目标】
1、了解糖类的组成和分类以及糖类在工农业生产和社会生活中的广泛方法应用和重要意义;
2、掌握糖类中重要的代表物葡萄糖、蔗糖、淀粉、纤维素的组成和主要性质,它们之间的相互转化关系以及与烃的衍生物的关系。
【要点梳理】
要点一、糖类的组成和分类
1.糖类的组成。
(1)糖类是由碳、氢、氧三种元素组成的一类有机化合物,大多数糖类的分子组成可用通式Cm(H2O)n来表示(m、n可以相同,也可以不同)。
注意:对糖类的通式的理解应注意两点:
①该通式只表明糖类由C、H、O三种元素组成,并未反映糖类的结构特点。
②有些属于糖类的物质不符合该通式,如脱氧核糖C5H10O4;而有些符合该通式的物质却不属于糖类。如乙酸CH3COOH、乳酸。
(2)从结构上看,糖类可定义为多羟基醛或多羟基酮,以及水解后可以生成多羟基醛或多羟基酮的化合物。
2.糖类的分类。
(1)根据能否水解以及水解后的产物,糖类可分为单糖、低聚糖和多糖。
单糖是不能水解的糖,一般为多羟基醛或多羟基酮,如葡萄糖、果糖、核糖及脱氧核糖等。
低聚糖是1 mol糖水解后能产生2 mol~10 mol单糖的糖类。其中以二糖最为重要,常见的二糖有麦芽糖、蔗糖和乳糖等。
多糖是1 mol糖水解后能产生很多摩尔单糖的糖类。如淀粉、纤维素等。多糖属于天然高分子化合物。
(2)单糖、低聚糖、多糖之间的相互转化关系为:
(3)糖类是绿色植物光合作用的产物,是一切生命体维持生命活动所需能量的主要来源。
要点二、糖类的结构和性质
1.葡萄糖的结构、性质和用途。
葡萄糖是自然界中分布最广的单糖,主要存在于葡萄及其他带有甜味的水果、蜂蜜中,植物的种子、叶、根、花中,动物的血液、脑脊液和淋巴液中。
(1)分子结构。
葡萄糖的分子式为C6H12O6,结构简式为CH2OH(CHOH)4CHO。它是一种多羟基醛。
(2)物理性质。
葡萄糖是无色晶体,熔点为146℃,有甜味,但甜度不如蔗糖,易溶于水,稍溶于乙醇,不溶于乙醚。
(3)化学性质。
葡萄糖分子中含有醛基和醇羟基,可发生氧化、加成、酯化等反应。
①氧化反应。
a.燃烧。
C6H12O6(s)+6O2(g)—→6CO2(g)+6H2O(1) ΔH=-2804kJ·mol-1
b.被银氨溶液或新制的Cu(OH)2氧化。
CH2OH(CHOH)4CHO+2Ag(NH3)2OHCH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
CH2OH(CHOH)4CHO+2Cu(OH)2CH2OH(CHOH)4COOH+Cu2O↓+2H2O
②加成反应。
CH2OH(CHOH)4CHO+H2CH2OH(CHOH)4CH2OH(己六醇)
③酯化反应。
特别提示:葡萄糖是单糖,不能发生水解反应。
(4)主要用途。
葡萄糖用于糖果制造业,还可用于医药工业。
2.果糖简介。
(1)果糖是最甜的糖,广泛分布在植物中,在水果和蜂蜜中含量较高。
(2)果糖的分子式为C6H12O6,结构简式为,它是一种多羟基酮。果糖与葡萄糖互为同分异构体。
(3)纯净的果糖为无色晶体,熔点为103 ~105℃,它不易结晶,通常为黏稠性液体,易溶于水、乙醇和乙醚。果糖是最甜的糖。
(4)果糖分子中含有酮基和醇羟基,能发生加成、酯化反应。
3.蔗糖与麦芽糖。
蔗糖与麦芽糖都是重要的二糖,蔗糖为白色晶体,麦芽糖为无色晶体,两者都易溶于水,都有甜味。
蔗糖与麦芽糖的比较
蔗糖
麦芽糖
相似点
①组成相同,化学式均为C12H22O11,互为同分异构体
②都属于二糖,每摩尔水解后生成两摩尔单糖
③水解产物都能发生银镜反应,都能还原新制Cu(OH)2
④都具有甜味(蔗糖更甜)
不
同
点
官能团
不含醛基(非还原性糖)
含有醛基(还原性糖)
化学性质
不能发生银镜反应,也不能还原新制Cu(OH)2
能发生银镜反应,能还原新制Cu(OH)2
水解产物
葡萄糖和果糖各半
仅有葡萄糖
来源
以甘蔗和甜菜含量最多
淀粉在酶作用下的水解产物
用途
甜味食物、制红糖、白糖等
甜味食物、制饴糖
4.淀粉与纤维素。
淀粉和纤维素是最重要的多糖。两者具有相同的分子通式(C6H10O5)n。它们都是由许多个单糖单元(C6H10O5)构成的天然高分子化合物。但由于n值不同,两者不是同分异构体关系,又由于结构不同,两者也不是同系物关系。
(1)淀粉与纤维素的比较
名称
淀粉
纤维素
存在
存在于植物种子、块根、谷类等中
存在于棉花、木材等中
通式
(C6H10O5)n
(C6H10O5)n
结构特点
由几百个到几千个单糖单元构成的高分子化合物
由比淀粉更多的单糠单元构成的高分子化合物
物理性质
白色粉末,不溶于冷水,一部分可溶于热水,无甜味
白色、无嗅、无味的物质,不溶于水,无甜味
化
学
性
质
加碘水
淀粉与碘作用呈现蓝色
纤维素与碘不作用,不变蓝,可用于鉴别淀粉和纤维素
水解
在淀粉酶作用下水解成麦芽糖,在无机酸作用下水解成葡萄糖
在无机酸催化作用下水解,最后生成葡萄糖,比淀粉水解困难
酯化
不能发生酯化反应
生成火棉、胶棉和醋酝纤维
用途
作工业原料,制取葡萄糖、酒精等
可用于纺织工业、造纸工业,制硝酸纤维、醋酸纤维和黏胶纤维等
(2)淀粉和纤维素的主要化学性质。
①都无还原性。
淀粉和纤维素都不能被银氨溶液或新制的Cu(OH)2氧化,因而都没有还原性。
②都能水解,其水解的最终产物都是葡萄糖,但纤维素比淀粉更难水解。
(C6H10O5)n +nH2OnC6H12O6
(淀粉或纤维素) (葡萄糖)
③淀粉遇碘单质变蓝色,纤维素遇碘单质不变色,因此可用碘单质来鉴定淀粉的存在或区分淀粉和纤维素。
④纤维素分子的每个单糖单元有3个醇羟基,其分子通式可表示为[C6H7O2(OH)3]n,能表现出醇的性质。如能与HNO3、CH3COOH等发生酯化反应。
要点三、糖类之间的相互转化关系
注:C6H12O62C2H5OH+2CO2。
【典型例题】
类型一:糖类的结构和性质
例1 下列物质中,在一定条件下既能发生银镜反应,能发生水解反应的是( )。
①甲酸甲酯 ②蔗糖 ③葡萄糖 ④麦芽糖
A.①④ B.②③ C.①③ D.③④
【思路点拨】本题考查物质的结构以及有机物官能团的性质。能发生银镜反应的是醛基,能发生水解反应的是卤素原子或者酯基。
【答案】A
【解析】能发生银镜反应,说明有机物结构中含有醛基已学过的能发生水解反应的有机物有卤代烃、酯及低聚糖或糖等。甲酸甲酯中有和;蔗糖能发生水解反应,但无;葡萄糖能发生银镜反应,但不能水解麦芽糖是还原性糖,能发生银镜反应,同时也能发生水解反应。故答案为A。
【总结升华】在总结有机化学内容时,注意整理有机官能团可以发生的反应,以及发生有机反应的官能团。比如醛基可以与银氨溶液、新制氢氧化铜发生氧化反应,也可以与氢气发生还原(或加成)反应;发生水解反应的有卤代烃中的卤素原子及酯基。
举一反三:
【变式1】(2019 江苏泰州期中)实验是化学研究的基础。下列对实验现象的描述中错误的是( )
A.实验①中溶液变黄色
B.实验②中试管内混合溶液变血红色
C.实验③中烧瓶内溶液变红色
D.实验④中出现红色沉淀
【答案】A
【解析】氯气与KI反应生成碘单质,淀粉遇碘单质变蓝,则观察到溶液变为蓝色,故A错误;铁离子与SCN-结合生成络离子,可观察到溶液变为血红色,故B正确;氨气极易溶于水,且溶液显碱性,则可观察到烧瓶内溶液变红,故C正确;葡萄糖分子中含有醛基,可与新制氢氧化铜反应生成氧化亚铜,观察到红色沉淀,故D正确。
例2 有关葡萄糖与果糖的下列说法中,不正确的是( )。
A.两者互为同分异构体 B.两者都易溶于水
C.两者都能发生银镜反应 D.葡萄糖比果糖要甜
【答案】C、D
【解析】果糖不含醛基,不能发生银镜反应;果糖是最甜的糖,它比葡萄糖甜得多,故选C、D。
举一反三:
【变式1】葡萄糖是单糖的主要原因是( )。
A.在糖类物质中含碳原子数最少 B.不能水解成更简单的糖
C.分子中含有多个羟基 D.在糖类中分子结构最简单
【答案】B
【变式2】化学与工农业生产、人类生活密切相关,下列说法中正确的是( )
A.14C可用于文物年代的鉴定,14C与12C互为同素异形体
B.葡萄糖注射液不能产生丁达尔效应,不属于胶体
C.汽油、柴油和植物油都是碳氢化合物
D.“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是指纤维素和油脂
【答案】B
【解析】14C和12C是同位素关系,A项错误;葡萄糖注射液不产生丁达尔效应,说明它不是胶体,B项正确;汽油、柴油属于烃类,植物油属于油脂,C项错误;蚕丝属于蛋白质,蜡烛是高级烃类的混合物,D项错误。
类型二:糖类的水解及产物的检验
例3(2019 福建三明期中)某学生在进行蔗糖的水解实验,并检验水解产物中是否含有葡萄糖。操作如下:取少量纯净的蔗糖加适量水配成溶液,加入2-3滴稀硫酸,水浴加热5min后,取少量溶液,再加入少量新制的Cu(OH)2,加热3-5min,结果没有看到砖红色沉淀。下列解释正确的是( )
A.用水浴加热的温度低,蔗糖不能水解
B.水浴加热时间不够长,蔗糖尚未完全水解
C.蔗糖水解产物中没有葡萄糖
D.煮沸后的溶液中没有加碱液去中和作催化剂的酸
【思路点拨】蔗糖水解生成葡萄糖,利用葡萄糖的检验应在碱性条件下进行来解答。
【答案】D
【解析】取少量纯蔗糖加适量水配成溶液,在蔗糖溶液中加入3-5滴稀硫酸,将混合液煮沸几分钟、冷却,则蔗糖在酸性条件下水解生成葡萄糖,而葡萄糖的检验应在碱性条件下进行,应先加碱中和至碱性,再加入适量的新制Cu(OH)2并加热至沸腾,可观察到砖红色沉淀生成,所以在酸性条件下不能生成Cu2O,故没有观察到砖红色沉淀生成,故选D。
【总结升华】检验糖类的水解产物除可用银氨溶液外,还可使用新制的Cu(OH)2悬浊液,和银镜反应一样,使用Cu(OH)2之前也要先加入NaOH中和作为催化剂的酸,同时所配制的Cu(OH)2中NaOH必须过量,配制的方法是:在洁净的试管中加入10%的NaOH溶液2 mL,然后滴入5%的CuSO4溶液5滴,振荡后即可使用。
举一反三:
【变式1】将蔗糖溶于水,配成10%的溶液,分装在两个试管中,在第一支试管中加入银氨溶液,在水浴中加热,没有变化,原因是蔗糖分子中________;在第二支试管中,加入几滴稀H2SO4,再在水浴中加热,加NaOH中和酸后也加入银氨溶液,现象________,原因是________,稀硫酸的作用是________。
【答案】无醛基 有光亮的银镜产生 蔗糖发生水解,生成葡萄糖 催化剂
【巩固练习】
一、选择题
1.有关糖类物质的叙述中,正确的是( )。
A.凡符合通式Cm(H2O)n的化合物都属于糖类,不符合通式Cm(H2O)n的化合物都不是糖类
B.凡具有甜味的物质都属于糖类,凡不具有甜味的物质都不属于糖类
C.糖类物质只含碳、氢、氧三种元素,但含碳、氢、氧三种元素的有机物不一定是糖类
D.糖类物质有的有还原性,有的没有还原性
2.下列有关葡萄糖的叙述中,错误的是( )。
A.能加氢生成六元醇 B.能发生银镜反应
C.能与醇发生酯化反应 D.能被氧化为CO2与H2O
3.崇明米酒既有酒味又有甜味,其中甜味来源的途径是( )。
A.淀粉→蔗糖→葡萄糖 B.淀粉→麦芽糖→葡萄糖
C.淀粉→麦芽糖→果糖 D.淀粉→蔗糖→果糖
4.(2019 延边州期末)蔬菜、水果中富含纤维素,纤维素被食入人体后的作用是( )
A.为人体内的化学反应提供原料
B.为维持人体生命活动提供能量
C.加强胃肠蠕动,具有通便功能
D.人体中没有水解纤维素的酶,所以纤维素在人体中没有任何作用
5.关于葡萄糖和蔗糖的比较,下列说法不正确的是( )。
A.葡萄糖不能水解,蔗糖能水解
B.蔗糖的相对分子质量是葡萄糖的2倍
C.葡萄糖是还原性糖,蔗糖是非还原性糖
D.浓硫酸能使它们都发生炭化现象
6.下列有关麦芽糖的叙述中,错误的是( )。
A.纯净的麦芽糖是白色晶体,易溶于水,有甜味
B.麦芽糖能发生银镜反应,是一种还原性糖
C.1 mol麦芽糖水解得到1 mol葡萄糖和1 mol果糖
D.麦芽糖和蔗糖互为同分异构体
7.将淀粉水解并用Cu(OH)2碱性溶液检验水解产物的实验中,要进行的主要操作有:①加热;②滴入稀硫酸;③加入新制的Cu(OH)2溶液;④加入NaOH溶液中和。以上各步操作的先后顺序的正确排列是( )。
A.①②③④① B.②①④③① C.②①④③ D.④③①②①
8.(2019 北京西城期末)下列鉴别实验中,所选试剂不合理的是( )
A.用水鉴别乙醇和苯
B.用碳酸氢钠溶液鉴别乙酸和乙醇
C.用新制的氢氧化铜鉴别葡萄糖和蔗糖
D.用高锰酸钾酸性溶液鉴别甲苯和己烯
9.(2019 西安模拟)新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述不正确的是( )。
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质
C.防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖
10.已知有如下过程:
根据上图,a、b、c可分别表示( )。
A.淀粉、酶、葡萄糖 B.蔗糖、酶、果糖
C.纤维素、酶、葡萄糖 D.麦芽糖、酶、葡萄糖
二、填空题
1.有A、B、C、D四种有机物,均由碳、氢、氧三种元素组成。A、B的实验式相同,B、C的分子式相同,B、c在一定条件下相互作用可生成D。常温常压下,A是气体,B、C、D是固体,四种物质均易溶于水,A、B可发生银镜反应,B的相对分子质量是A的6倍。
(1)写出四种有机物的名称:A________、B________、C________。
(2)写出D的一种同分异构体发生水解的化学方程式:________________。
2.淀粉和纤维素的分子组成都可用通式________表示,但二者的n值________同。它们都属于________糖,在性质上与单糖、二糖不同,没有________味,都________(填“能”或“不能”)发生银镜反应,但在硫酸的催化作用下,都能发生________反应,其反应的最终产物都是________。纤维素在硫酸催化作用下发生反应的化学方程式是________________。
3.聚乳酸是一种新型可被生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料。聚乳酸材料废弃后,先水解成乳酸(),乳酸在微生物作用下分解为CO2和H2O。
(1)乳酸的工业生产可以采用生物发酵法。
①检验淀粉是否完全水解,可以选用的一种试剂是________(填序号)。
a.溴水 b.银氨溶液 c.碘酒 d.碘化钾淀粉溶液
②用18吨葡萄糖发酵,理论上可以得到乳酸的质量是________吨。
(2)乳酸的生产也可以采用有机合成法,其中的一种方法是丙酸法。
①反应Ⅰ的反应类型是________反应。
②进行反应Ⅱ时,需要加入过量的乙醇,这样做的目的是________。
(3)两个乳酸分子之间可以形成环状的酯,该环状酯的结构简式是________。乳酸在一定条件下发生反应得到聚乳酸的化学方程式是________。
4.某酒精厂用含淀粉50%的白薯干制取酒精,如果发酵过程中有20%的淀粉损失掉,计算生产含水量8%的酒精10 t,理论上需用这种白薯干多少吨?
【参考答案与解析】
一、选择题
1.C、D
【解析】C2H4O2、CH2O等不属于糖类,而C5H10O4(脱氧核糖)却是糖类;糖类有的有甜味,有的没有甜味;含C、H、O的有机物还可能是其他烃的含氧衍生物,如醇、酚、醛、羧酸、酯等;葡萄糖、麦芽糖等有还原性,而蔗糖、淀粉等没有还原性。
2.C
【解析】葡萄糖的分子结构为CH2OH(CHOH)4CHO,其分子中含有5个醇羟基和一个醛基,含有醛基,可与氢加成得到六元醇,与银氨溶液反应可生成银镜;含有醇羟基,可与羧基反应生成酯;葡萄糖由C、H、O三种元素组成,可燃烧生成CO2和H2O(在人体中被氧化为CO2和H2O)。
3.B
【解析】米中含有大量的淀粉,在微生物的作用下,淀粉首先水解生成麦芽糖,然后再水解成人的味觉敏感的葡萄糖,从而产生甜味。本题如果知道蔗糖、麦芽糖水解的产物及淀粉水解的最终产物是葡萄糖等知识,也可正确进行判断。
4.C
【解析】A项人不能消化纤维素,纤维素在人体内不能发生反应,故A错误;B项人不能消化纤维素,纤维素不能为人体生命活动提供能量,故B错误;C项纤维素可以促进大肠蠕动,从而促进消化吸收其他营养物质,所以纤维素在防止便秘方面是有利的,故C正确;D项纤维素加强胃肠蠕动,具有通便功能,故D错误。故选C。
5.B
【解析】蔗糖的分子式为C12H22O11,葡萄糖的分子式为C6H12O6,蔗糖的相对分子质量比葡萄糖的2倍略小。
6.C
【解析】麦芽糖是白色晶体;麦芽糖分子中含有醛基,能发生银镜反应,是一种还原性糖;1 mol麦芽糖水解生成2 mol葡萄糖;麦芽糖与蔗糖的分子式相同,而结构不同,两者互为同分异构体。
7.B
【解析】加热既是淀粉在酸催化作用下水解反应的条件,也是其水解产物葡萄糖与新制Cu(OH)2发生反应的条件。滴入稀硫酸用来催化淀粉水解,加入NaOH溶液是为了中和用作催化剂的硫酸。
8.D
【解析】A项,乙醇可以与水互溶,不会分层;苯不溶于水,密度比水小,有机层在上层,故可用水鉴别乙醇和苯。B项,乙酸可以和碳酸氢钠溶液反应生成二氧化碳气体,乙醇不能和碳酸氢钠溶液反应,故可以用碳酸氢钠溶液鉴别乙酸和乙醇。C项,葡萄糖中含有醛基,能够和新制的氢氧化铜反应产生红色沉淀,蔗糖不能和新制的氢氧化铜反应,故可以用新制的氢氧化铜鉴别葡萄糖和蔗糖。D项,甲苯和己烯都能使高锰酸钾酸性溶液褪色,故不能用高锰酸钾酸性溶液鉴别甲苯和己烯。
9.D
【解析】A项棉花、优质针叶木等原料的主要成分是纤维素,故A正确;B项Fe3O4是磁性物质,有磁性,故B正确;C项树脂相对分子质量很大,属于有机高分子材料,故C正确;D项葡萄糖遇碘不变蓝,故D错误。故选D。
10.D
【解析】反应最终结果是1分子a生成2分子c,且b的量不变,这表明b是催化剂(如酶),而a与c应是二糖与单糖的关系。
二、填空题
1.(1)甲醛 葡萄糖 果糖 蔗糖
(2)C12H22O11+H2O2C6H12O6
(麦芽糖) (葡萄糖)
【解析】由C、H、O组成的有机物中仅有HCHO(甲醛)在常温下是气体,则A是甲醛;而B的相对分子质量是A的6倍,其分子式为C6H12O6,可能是葡萄糖,而C与B互为同分异构体,则C是果糖;B、C作用生成D,则D为蔗糖,它的同分异构体是麦芽糖。
2.(C6H10O5)n 不 多 甜 不能 水解 葡萄糖
(C6H10O5)n +nH2OnC6H12O6
(纤维素) (葡萄糖)
【解析】淀粉和纤维素的分子通式都可表示为(C6H10O5)n,但n值不同,它们不是同分异构体;淀粉和纤维素都是多糖,都没有甜味,也不能发生银镜反应,但能水解,其水解的最终产物都是葡萄糖。
3.(1)①c ②18
(2)①取代 ②提高乳酸的转化率
【解析】(1)淀粉若是完全水解,则溶液中已没有淀粉剩余。向溶液中滴加碘酒观察,若不变蓝,则水解完全。由关系式C6H12O6(葡萄糖)~2C3H6O3(乳酸),根据质量守恒定律得m(葡萄糖)=m(乳酸)=18吨。
(2)②加入过量的乙醇,使平衡向生成乳酸乙酯的方向移动,从而提高乳酸的转化率。
(3)抓住酯化反应的原理“酸脱羟基,醇脱氢,生成酯和水”,结合题给要求,即可得出答案。
4.40.5 t。
【解析】解:设理论上需用白薯干的质量为m。由关系式
(C6H10O5)n ~ 2nC2H5OH
162n 92n
50%×(1-20%)·m 10 t×(1-8%)
,
解得m=40.5 t。
答:需用这种白薯干40.5 t。
