人教版九年级化学11.2 化学肥料(共32张PPT)
文档属性
| 名称 | 人教版九年级化学11.2 化学肥料(共32张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 763.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-28 00:00:00 | ||
图片预览









文档简介
课件32张PPT。课题2 化学肥料阅读教材P79-80完成下列问题:1、什么是化肥?
2、农业生产中为什么要使用化肥?
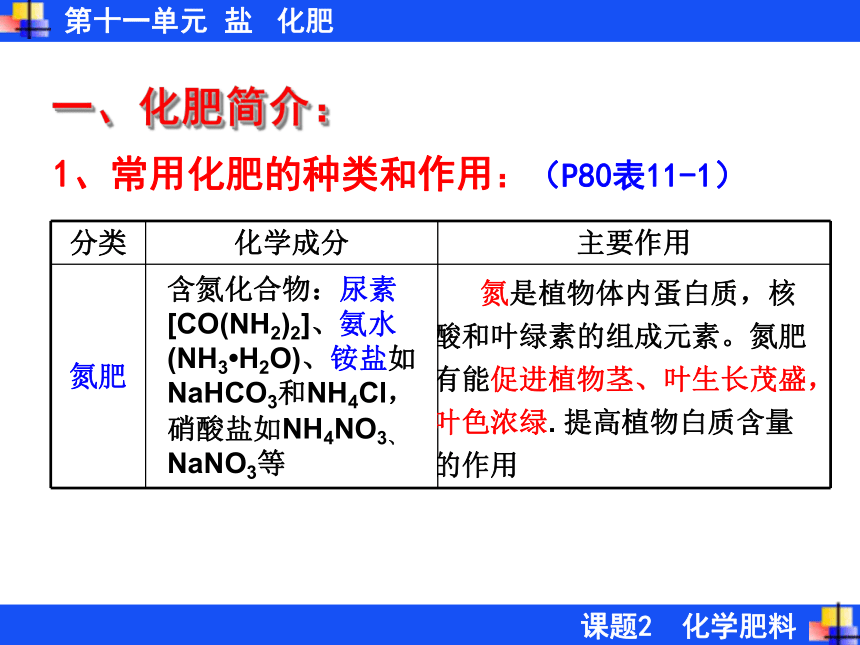
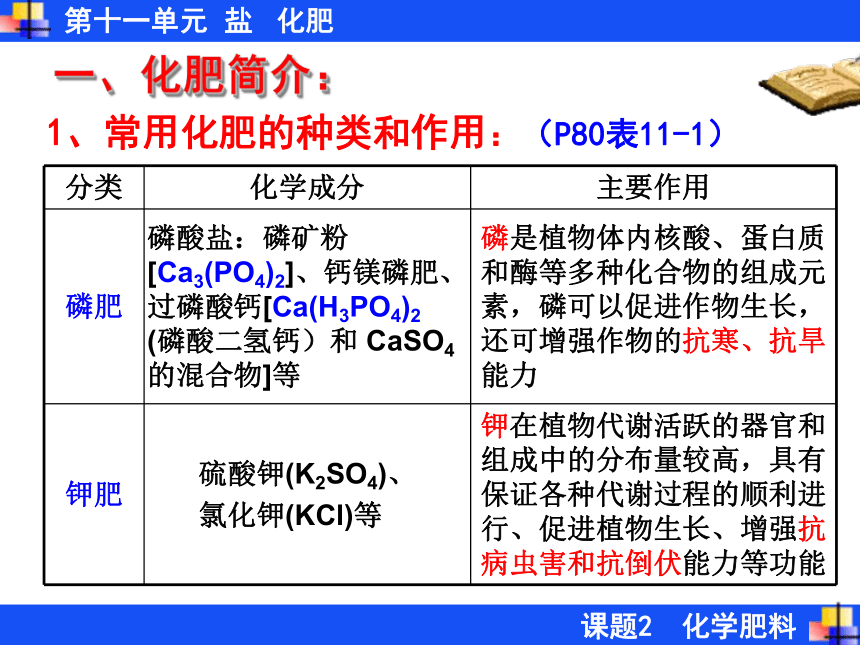
3、主要的化学肥料有哪些? 导 入 植物生长需要养分,土壤所能提供的养分是有限的,因此要靠施肥来补充,施肥是使农业增产的重要手段。 人类最初使用的肥料是人畜粪便、植物体等沤制的天然有机肥料。18世纪中期,随着人们对化学元素与植物生长关系的了解,出现了以化学和物理方法制成的含农作物生长所需营养元素的化学肥料(简称化肥)。之后,随着世界人口的增长,人类对农产品需求增加,增施化肥已经成为了农作物增产的最有力措施,施用化肥的增产作用占各增产因素总和的30%—60%。农业生产中为什么要使用化肥 农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,其中氮、磷、钾需要量较大,因此氮肥、磷肥和钾肥是最主要的化学肥料。一、化肥简介:常用化肥的种类和作用1、常用化肥的种类和作用:(P80表11-1)一、化肥简介:1、常用化肥的种类和作用:(P80表11-1)一、化肥简介: 1.将下列化学成分、化学肥料,主要作用连起来. 磷肥
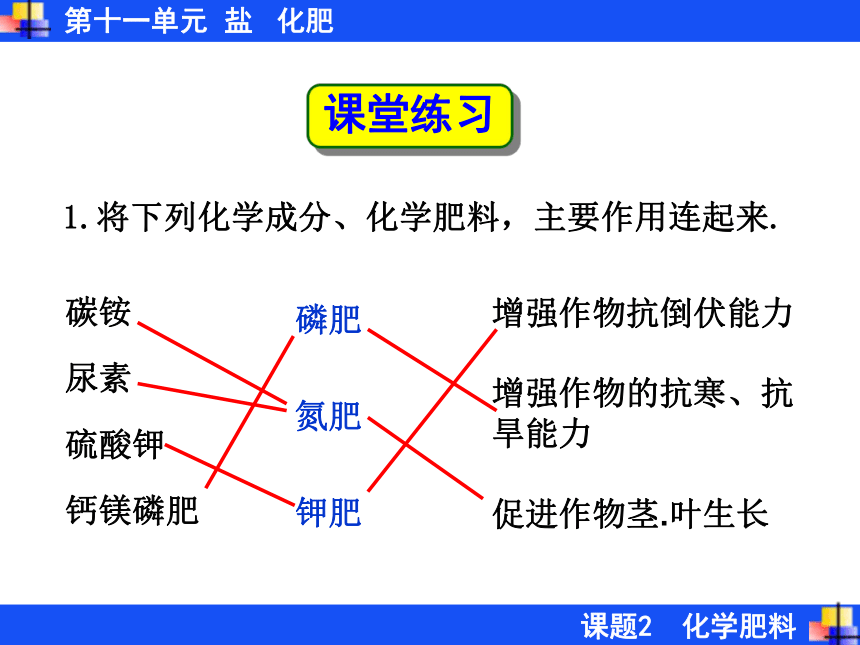
氮肥
钾肥 碳铵
尿素
硫酸钾
钙镁磷肥 增强作物抗倒伏能力
增强作物的抗寒、抗旱能力
促进作物茎.叶生长 课堂练习(1)缺氮:生长迟缓,叶片发黄。缺氮的棉花2、常用化肥缺乏时的表现:缺氮的棉花缺氮的玉米缺氮的马铃薯(2)缺磷:植株矮小,产量下降。2、常用化肥缺乏时的表现:正常与缺磷的小麦(3)缺钾:茎干软弱,容易倒伏,叶尖发黄2、常用化肥缺乏时的表现:缺钾的大豆 缺钾的甘蓝缺钾的包菜2、常用化肥缺乏时的表现:(1)缺氮:(2)缺磷:(3)缺钾:茎干软弱,容易倒伏,叶尖发黄植株矮小,产量下降。生长迟缓,叶片发黄。1、常用化肥的种类和作用:(P80表11-1)一、化肥简介:1、氮气含氮元素是否属于氮肥?为什么? 2、大豆、蚕豆等豆科植物为什么无需或只需
少量施用氮肥? 不属于,大多数植物不能直接吸收氮气,只能吸收含氮化合物 因为它们根部有根瘤菌能把空气中氮转化成含氮化合物被植物吸收。(氮的固定)交流讨论 空气中的N2在打雷闪电的时候被高能激发.并且与氧气发生反应,氮气被氧化为一氧化氮,进而被氧化为二氧化氮 N2+O2=2NO 2NO+O2=2NO2 二氧化氮溶于水生成硝酸和一氧化氮 3NO2+H2O=2HNO3+NO 硝酸又和别的不溶盐类反应生成可溶的硝酸盐,而硝酸盐是植物可以吸收的 氮肥 知识拓展 夏天,雷阵雨特别多,总是打雷、闪电的,可是爷爷总说雷雨天好,雷雨发庄稼,这是为什么呢?磷酸二氢铵:NH4H2PO4
磷酸铵氢 :(NH4)2HPO4
硝酸钾:KNO33、复合肥料:(1)定义:同时含两种或两种以上营养元素的化肥。(2)种类:(3)特点:能够同时均匀地供给作物几种营养成分。2、某星期天,小明同学回家发现自家田里的小麦出现大面积倒伏现象,你认为缺少的化肥是( )
A.NH4NO3 B.CO(NH2)2
C.Ca(H2PO4)2 D.KCl
3、林强家种的花出现叶子发黄的现象,老师告诉他
需要施肥,他应该施用以下肥料中的( )
A、NH4HCO3 B、Ca3(PO4)2 C、KCl D、K2SO4
4、下列化学肥料属于复合肥的是( )
A.氯化钾 B.尿素 C.碳酸氢铵 D.硝酸钾DAD课堂练习阅读讨论1、使用化肥的利与弊:2、使用农药的利与弊:利:弊:利:弊:提高农作物的产量具有重要作用 由于化肥中常含有一些重金属元素、有毒有机物和放射性物质,施入土壤后形成潜在的土壤污染;另外化肥在施用过程中因某些成分的积累、流失或变化,引起土壤酸化、水域氮和磷的升高、氮化物和硫化物气体排放等,造成土壤退化、大气环境和污染。 对农业的高产丰收具有重要作用 农药本身是有毒物质,使用不当会带来对自然环境的污染和对人体健康的危害。 农药在自然环境中的转移【总结】要合理施用化肥和农药,提高利用率,减少污染。①有针对性、均衡适度地施用化肥,提高施用效率,
减少负面作用②以最少量的农药获得最高的防治效果,同时又延缓或防止抗药性的产生,从而减少农药对农产品和环境的污染。交流讨论 使用化肥和农药会带来这么多的环境问题,哪
我们就不用了吗?怎么用才能减少对环境的污染呢?不合理使用会带来环境问题。4、化肥、农药使用的利与弊:对提高农产品的产量有重要作用。(1)利:(2)弊:①土壤污染②水体污染③大气污染。【总结】要合理施用化肥和农药,提高利用率,减少污染。5、合理使用化肥,有利于农作物的生长和减少环境污染。下列有关化肥的说法正确的是( )
A.为保证高产尽量多施用化肥
B.将氯化铵与碱性物质混合施用
C.CO(NH2)2是一种常用的复合肥料
D.提倡将农家肥与化肥综合使用
6、见课本85页选择题第(1)题巩固练习D白色晶体白色晶体白色晶体白色晶体灰白色
粉末灰白色
粉末无味无味无味无味无味易溶易溶易溶易溶难溶难溶有刺激性气味二、化肥的简易鉴别探究初步区分氮肥、磷肥和钾肥的方法1、比较氮肥、磷肥、钾肥的外观,气味和在水中的溶解性.归纳它们的性质。探究无气味无气味无气味2、取上述化肥少量,分别加入少量熟石灰粉末,混合、研磨,能否嗅到气味?有刺激性气味有刺激性气味探究二、化肥的简易鉴别:1.初步区分常见化肥的方法:P84(1)看外观:可区分出磷肥(2)加 水:可区分出磷肥(灰白色)(大多不溶于水)(3)加熟石灰研磨:可区分出铵态氮肥(铵盐)(有氨味)7、下列化肥从外观即可与其他化肥相区别的是( )
A、硝酸钾 B、碳酸铵
C、氯化钾 D、磷矿粉
8.下列化肥通过加水溶解就可以鉴别出来的是( )
A.碳酸氢 B.硫酸铵
C.磷矿粉 D.硝酸铵
9.下列化肥通过与熟石灰混合、研磨就可以鉴别出来
的是( )
A.硫酸铵 B.尿素
C.硝酸铵 D.氯化铵C课堂练习BD氮肥尿 素(NH4)2SO4、NH4Cl、NH4NO3(NH4)2SO4NH4Cl 、 NH4NO3加碱有氨味加硝酸钡溶液有白色沉淀无沉淀无氨味加硝酸银溶液有白色沉淀无沉淀NH4NO3NH4Cl氮肥的简易鉴别(1)氮肥中氨水是液态,碳酸氢铵有强烈的氨味。(2)其他常见氮肥可按下列步骤鉴别:资料卡片(NH4)2SO4 + NaOH=
NH4Cl + Ca(OH)2=
NH4NO3 + NaOH=例如:NaNO3 + H2O + NH3 ↑Na2SO4 + 2H2O + 2NH3 ↑思考 铵盐能与碱反应,放出氨气,据此如何来检验NH4+ 的 存在?? 2CaCl2 + 2H2O + 2NH3 ↑23、NH4+的检验:(1)原理:NH4+ + OH- = NH3 + H2O(3)方法:向样品中加入碱溶液(微热),将湿润的红色石蕊试纸放在试管口,观察现象。(2)试剂:碱溶液[ NaOH 、Ca(OH)2 ]闻到刺激性气味,试纸变蓝色,
则证明含有NH4+。(4)现象:8、下列化肥不能与熟石灰混合施用的是( )
A. 氯化钾
B. 碳酸氢铵
C. 氨水
D. 硝酸钾
9、见课本85页第3题B课堂练习3、NH4+的检验:(1)原理:NH4+ + OH- = NH3 + H2O(3)方法:向样品中加入碱溶液(微热),将湿润的红色石蕊试纸放在试管口,观察现象。(2)试剂:碱溶液[ NaOH 、Ca(OH)2 ]闻到刺激性气味,试纸变蓝色,
则证明含有NH4+。(4)现象:[注意事项]:铵态氮肥(铵盐)不能与碱性物质混合使用1.氯化铵、硫酸铵、硝酸铵、尿素都是白色固体,也是重要的化肥。下列物质能够将尿素从这四种化肥中鉴别出来的是( )
A.HCl B.NaCl
C.H2O D.Ca(OH)2D巩固练习 2、某化肥包装袋上的部分说明如右图所示。
(1)硝酸铵属化学肥料中的?????? ?
A.钾肥???B.氮肥????C.磷肥
(2)硝酸铵应具有的性质是???? ?
A.易溶于水 B.有挥发性 C.受热易分解
(3)硝酸铵能与强碱反应,其中与烧碱反应的方程式:
NH4NO3 + NaOH=NaNO3 + NH3↑+ X,
则X的化学式是:??? ? ;施用该类肥料时,要避免与? ? (填“酸”或“碱”)性物质混用,否则会减低肥效。硝酸铵
化学式 NH4NO3
净重 50Kg
含氮量 ≥30%
注意事项 密封贮存
防潮防晒
隔绝热源
BAC H2O碱 巩固练习谢谢指导
2、农业生产中为什么要使用化肥?
3、主要的化学肥料有哪些? 导 入 植物生长需要养分,土壤所能提供的养分是有限的,因此要靠施肥来补充,施肥是使农业增产的重要手段。 人类最初使用的肥料是人畜粪便、植物体等沤制的天然有机肥料。18世纪中期,随着人们对化学元素与植物生长关系的了解,出现了以化学和物理方法制成的含农作物生长所需营养元素的化学肥料(简称化肥)。之后,随着世界人口的增长,人类对农产品需求增加,增施化肥已经成为了农作物增产的最有力措施,施用化肥的增产作用占各增产因素总和的30%—60%。农业生产中为什么要使用化肥 农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,其中氮、磷、钾需要量较大,因此氮肥、磷肥和钾肥是最主要的化学肥料。一、化肥简介:常用化肥的种类和作用1、常用化肥的种类和作用:(P80表11-1)一、化肥简介:1、常用化肥的种类和作用:(P80表11-1)一、化肥简介: 1.将下列化学成分、化学肥料,主要作用连起来. 磷肥
氮肥
钾肥 碳铵
尿素
硫酸钾
钙镁磷肥 增强作物抗倒伏能力
增强作物的抗寒、抗旱能力
促进作物茎.叶生长 课堂练习(1)缺氮:生长迟缓,叶片发黄。缺氮的棉花2、常用化肥缺乏时的表现:缺氮的棉花缺氮的玉米缺氮的马铃薯(2)缺磷:植株矮小,产量下降。2、常用化肥缺乏时的表现:正常与缺磷的小麦(3)缺钾:茎干软弱,容易倒伏,叶尖发黄2、常用化肥缺乏时的表现:缺钾的大豆 缺钾的甘蓝缺钾的包菜2、常用化肥缺乏时的表现:(1)缺氮:(2)缺磷:(3)缺钾:茎干软弱,容易倒伏,叶尖发黄植株矮小,产量下降。生长迟缓,叶片发黄。1、常用化肥的种类和作用:(P80表11-1)一、化肥简介:1、氮气含氮元素是否属于氮肥?为什么? 2、大豆、蚕豆等豆科植物为什么无需或只需
少量施用氮肥? 不属于,大多数植物不能直接吸收氮气,只能吸收含氮化合物 因为它们根部有根瘤菌能把空气中氮转化成含氮化合物被植物吸收。(氮的固定)交流讨论 空气中的N2在打雷闪电的时候被高能激发.并且与氧气发生反应,氮气被氧化为一氧化氮,进而被氧化为二氧化氮 N2+O2=2NO 2NO+O2=2NO2 二氧化氮溶于水生成硝酸和一氧化氮 3NO2+H2O=2HNO3+NO 硝酸又和别的不溶盐类反应生成可溶的硝酸盐,而硝酸盐是植物可以吸收的 氮肥 知识拓展 夏天,雷阵雨特别多,总是打雷、闪电的,可是爷爷总说雷雨天好,雷雨发庄稼,这是为什么呢?磷酸二氢铵:NH4H2PO4
磷酸铵氢 :(NH4)2HPO4
硝酸钾:KNO33、复合肥料:(1)定义:同时含两种或两种以上营养元素的化肥。(2)种类:(3)特点:能够同时均匀地供给作物几种营养成分。2、某星期天,小明同学回家发现自家田里的小麦出现大面积倒伏现象,你认为缺少的化肥是( )
A.NH4NO3 B.CO(NH2)2
C.Ca(H2PO4)2 D.KCl
3、林强家种的花出现叶子发黄的现象,老师告诉他
需要施肥,他应该施用以下肥料中的( )
A、NH4HCO3 B、Ca3(PO4)2 C、KCl D、K2SO4
4、下列化学肥料属于复合肥的是( )
A.氯化钾 B.尿素 C.碳酸氢铵 D.硝酸钾DAD课堂练习阅读讨论1、使用化肥的利与弊:2、使用农药的利与弊:利:弊:利:弊:提高农作物的产量具有重要作用 由于化肥中常含有一些重金属元素、有毒有机物和放射性物质,施入土壤后形成潜在的土壤污染;另外化肥在施用过程中因某些成分的积累、流失或变化,引起土壤酸化、水域氮和磷的升高、氮化物和硫化物气体排放等,造成土壤退化、大气环境和污染。 对农业的高产丰收具有重要作用 农药本身是有毒物质,使用不当会带来对自然环境的污染和对人体健康的危害。 农药在自然环境中的转移【总结】要合理施用化肥和农药,提高利用率,减少污染。①有针对性、均衡适度地施用化肥,提高施用效率,
减少负面作用②以最少量的农药获得最高的防治效果,同时又延缓或防止抗药性的产生,从而减少农药对农产品和环境的污染。交流讨论 使用化肥和农药会带来这么多的环境问题,哪
我们就不用了吗?怎么用才能减少对环境的污染呢?不合理使用会带来环境问题。4、化肥、农药使用的利与弊:对提高农产品的产量有重要作用。(1)利:(2)弊:①土壤污染②水体污染③大气污染。【总结】要合理施用化肥和农药,提高利用率,减少污染。5、合理使用化肥,有利于农作物的生长和减少环境污染。下列有关化肥的说法正确的是( )
A.为保证高产尽量多施用化肥
B.将氯化铵与碱性物质混合施用
C.CO(NH2)2是一种常用的复合肥料
D.提倡将农家肥与化肥综合使用
6、见课本85页选择题第(1)题巩固练习D白色晶体白色晶体白色晶体白色晶体灰白色
粉末灰白色
粉末无味无味无味无味无味易溶易溶易溶易溶难溶难溶有刺激性气味二、化肥的简易鉴别探究初步区分氮肥、磷肥和钾肥的方法1、比较氮肥、磷肥、钾肥的外观,气味和在水中的溶解性.归纳它们的性质。探究无气味无气味无气味2、取上述化肥少量,分别加入少量熟石灰粉末,混合、研磨,能否嗅到气味?有刺激性气味有刺激性气味探究二、化肥的简易鉴别:1.初步区分常见化肥的方法:P84(1)看外观:可区分出磷肥(2)加 水:可区分出磷肥(灰白色)(大多不溶于水)(3)加熟石灰研磨:可区分出铵态氮肥(铵盐)(有氨味)7、下列化肥从外观即可与其他化肥相区别的是( )
A、硝酸钾 B、碳酸铵
C、氯化钾 D、磷矿粉
8.下列化肥通过加水溶解就可以鉴别出来的是( )
A.碳酸氢 B.硫酸铵
C.磷矿粉 D.硝酸铵
9.下列化肥通过与熟石灰混合、研磨就可以鉴别出来
的是( )
A.硫酸铵 B.尿素
C.硝酸铵 D.氯化铵C课堂练习BD氮肥尿 素(NH4)2SO4、NH4Cl、NH4NO3(NH4)2SO4NH4Cl 、 NH4NO3加碱有氨味加硝酸钡溶液有白色沉淀无沉淀无氨味加硝酸银溶液有白色沉淀无沉淀NH4NO3NH4Cl氮肥的简易鉴别(1)氮肥中氨水是液态,碳酸氢铵有强烈的氨味。(2)其他常见氮肥可按下列步骤鉴别:资料卡片(NH4)2SO4 + NaOH=
NH4Cl + Ca(OH)2=
NH4NO3 + NaOH=例如:NaNO3 + H2O + NH3 ↑Na2SO4 + 2H2O + 2NH3 ↑思考 铵盐能与碱反应,放出氨气,据此如何来检验NH4+ 的 存在?? 2CaCl2 + 2H2O + 2NH3 ↑23、NH4+的检验:(1)原理:NH4+ + OH- = NH3 + H2O(3)方法:向样品中加入碱溶液(微热),将湿润的红色石蕊试纸放在试管口,观察现象。(2)试剂:碱溶液[ NaOH 、Ca(OH)2 ]闻到刺激性气味,试纸变蓝色,
则证明含有NH4+。(4)现象:8、下列化肥不能与熟石灰混合施用的是( )
A. 氯化钾
B. 碳酸氢铵
C. 氨水
D. 硝酸钾
9、见课本85页第3题B课堂练习3、NH4+的检验:(1)原理:NH4+ + OH- = NH3 + H2O(3)方法:向样品中加入碱溶液(微热),将湿润的红色石蕊试纸放在试管口,观察现象。(2)试剂:碱溶液[ NaOH 、Ca(OH)2 ]闻到刺激性气味,试纸变蓝色,
则证明含有NH4+。(4)现象:[注意事项]:铵态氮肥(铵盐)不能与碱性物质混合使用1.氯化铵、硫酸铵、硝酸铵、尿素都是白色固体,也是重要的化肥。下列物质能够将尿素从这四种化肥中鉴别出来的是( )
A.HCl B.NaCl
C.H2O D.Ca(OH)2D巩固练习 2、某化肥包装袋上的部分说明如右图所示。
(1)硝酸铵属化学肥料中的?????? ?
A.钾肥???B.氮肥????C.磷肥
(2)硝酸铵应具有的性质是???? ?
A.易溶于水 B.有挥发性 C.受热易分解
(3)硝酸铵能与强碱反应,其中与烧碱反应的方程式:
NH4NO3 + NaOH=NaNO3 + NH3↑+ X,
则X的化学式是:??? ? ;施用该类肥料时,要避免与? ? (填“酸”或“碱”)性物质混用,否则会减低肥效。硝酸铵
化学式 NH4NO3
净重 50Kg
含氮量 ≥30%
注意事项 密封贮存
防潮防晒
隔绝热源
BAC H2O碱 巩固练习谢谢指导
同课章节目录
