人教版九年级化学下第九单元课题3溶液的浓度教学课件 (共26张PPT)
文档属性
| 名称 | 人教版九年级化学下第九单元课题3溶液的浓度教学课件 (共26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 44.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-28 00:00:00 | ||
图片预览







文档简介
课件26张PPT。课题3 溶液的浓度探究内容溶质种类相同的不同溶液,如
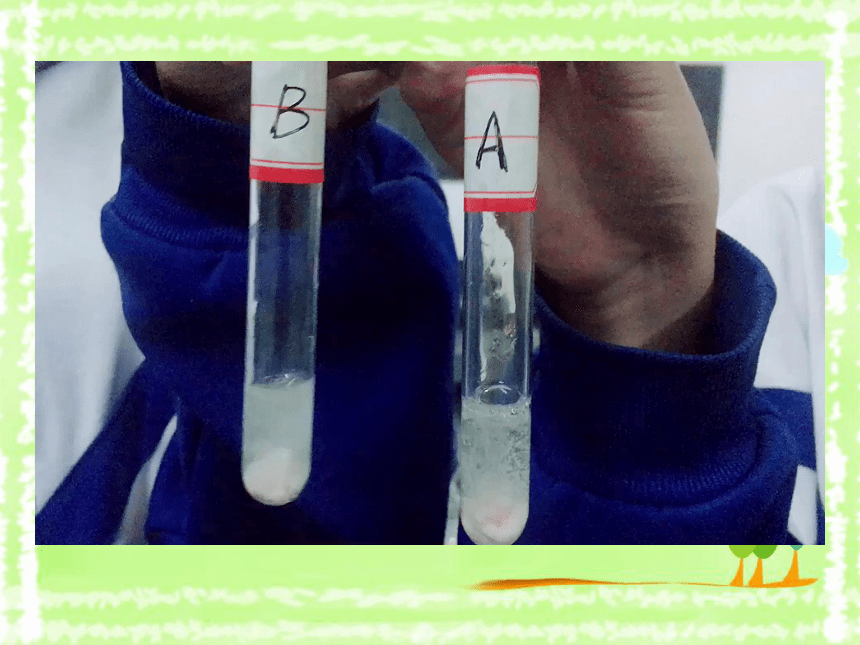
何判断各溶液的浓和稀呢?取盐酸A、盐酸B各3mL等量的碳酸钙等量的碳酸钙11.5%(V/V)
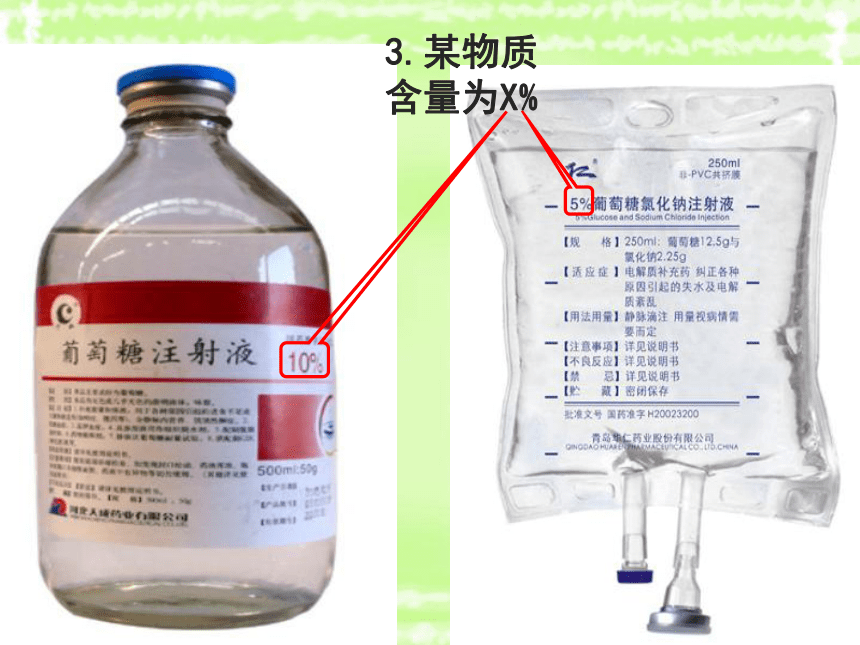
750mL3.某物质含量为X%探究目标0.1g0.5g2g溶质:溶剂: 20g 20g 20g一、溶质的质量分数1、定义:溶质质量和溶液质量之比。2、定义式:溶质质量溶液质量?100% 溶质质量分数=溶质质量=溶质质量+溶剂质量?100% 公式的换算运用 探究一【例题1】在农业生产上,常需要用
的氯化钠溶液选种。现要配制 ,需要
氯化钠和水的质量各是多少?
=150Kg × 16%
解:质量分数为16%150Kg这种溶液 ?溶剂质量=溶液质量-溶质质量
=24Kg=150Kg - 24Kg
=126Kg
答:配制150Kg质量分数为16%的氯化钠溶液,需24Kg氯化钠和126Kg水。公式的换算运用 计算的依据 :探究一溶质的质量 =溶液质量 ×溶质质量分数小结:在溶液中知道任意两个量就可以求出第三个量。 看谁又快又准?比一比解:加水:加盐:合作探究20g10%食盐溶液20g10%食盐溶液2g水2g食盐+2C%= 从上述解题过程中,你得到什么规律?求溶质的质量分数的关键是什么? 关键是准确找出溶质和溶液的质量将上述20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。答:剩余溶液的溶质质量分数不变,仍是 10 %议一议看谁脑瓜最聪明?合作探究20克氯化钠
80克水30克氯化钠
70克水10克氯化钠
90克水完全溶解10%完全溶解20%未完全溶解?实验探究讨论:已知20℃时,氯化钠的溶解度为36g。有人说:”20℃时氯化钠饱和溶液中溶质的溶质质量分数36%。”这种说法对吗?为什么? 溶质的质量分数36% 是指: 100g溶液中含有36g溶质。
溶质T0C时溶解度36g是指: 在200C 时,100g水中最多溶解该溶质36g。饱和溶液溶质质量分数的计算合作探究(注:T,S)※完全溶解10%完全溶解20% 36g
C%=————×100%
100g+36g未完全溶解?实验探究20℃:1. 80℃时,a的溶解度是( )
2.80℃时,a的饱和溶液的质量分数是
( ) (只需列计算式)85g
探究小结溶质质量溶液质量?100% 溶质质量分数=(溶质的质量 =溶液质量 ×溶质质量分数)1.溶质的质量分数2.饱和溶液溶质质量分数计算(已知:T,S)溶质质量分数=EndThank
you
何判断各溶液的浓和稀呢?取盐酸A、盐酸B各3mL等量的碳酸钙等量的碳酸钙11.5%(V/V)
750mL3.某物质含量为X%探究目标0.1g0.5g2g溶质:溶剂: 20g 20g 20g一、溶质的质量分数1、定义:溶质质量和溶液质量之比。2、定义式:溶质质量溶液质量?100% 溶质质量分数=溶质质量=溶质质量+溶剂质量?100% 公式的换算运用 探究一【例题1】在农业生产上,常需要用
的氯化钠溶液选种。现要配制 ,需要
氯化钠和水的质量各是多少?
=150Kg × 16%
解:质量分数为16%150Kg这种溶液 ?溶剂质量=溶液质量-溶质质量
=24Kg=150Kg - 24Kg
=126Kg
答:配制150Kg质量分数为16%的氯化钠溶液,需24Kg氯化钠和126Kg水。公式的换算运用 计算的依据 :探究一溶质的质量 =溶液质量 ×溶质质量分数小结:在溶液中知道任意两个量就可以求出第三个量。 看谁又快又准?比一比解:加水:加盐:合作探究20g10%食盐溶液20g10%食盐溶液2g水2g食盐+2C%= 从上述解题过程中,你得到什么规律?求溶质的质量分数的关键是什么? 关键是准确找出溶质和溶液的质量将上述20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。答:剩余溶液的溶质质量分数不变,仍是 10 %议一议看谁脑瓜最聪明?合作探究20克氯化钠
80克水30克氯化钠
70克水10克氯化钠
90克水完全溶解10%完全溶解20%未完全溶解?实验探究讨论:已知20℃时,氯化钠的溶解度为36g。有人说:”20℃时氯化钠饱和溶液中溶质的溶质质量分数36%。”这种说法对吗?为什么? 溶质的质量分数36% 是指: 100g溶液中含有36g溶质。
溶质T0C时溶解度36g是指: 在200C 时,100g水中最多溶解该溶质36g。饱和溶液溶质质量分数的计算合作探究(注:T,S)※完全溶解10%完全溶解20% 36g
C%=————×100%
100g+36g未完全溶解?实验探究20℃:1. 80℃时,a的溶解度是( )
2.80℃时,a的饱和溶液的质量分数是
( ) (只需列计算式)85g
探究小结溶质质量溶液质量?100% 溶质质量分数=(溶质的质量 =溶液质量 ×溶质质量分数)1.溶质的质量分数2.饱和溶液溶质质量分数计算(已知:T,S)溶质质量分数=EndThank
you
同课章节目录
