第二节 金属的化学性质(第一课时)(共32张PPT)
文档属性
| 名称 | 第二节 金属的化学性质(第一课时)(共32张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-30 00:00:00 | ||
图片预览











文档简介
课件32张PPT。第九单元 第二节鲁教版 化学(初中)金属的化学性质(第一课时)5典型例题4课堂小结3新课讲授2课堂导入1知识回顾1知识回顾1.金属来自地壳中天然存在的矿物。主要有两种形态:(1)单质形态:少数化学性质__________的金属,以单质形态存在,如________、________、________。
(2)化合物形态:绝大多数金属都是以__________形态存在于矿物之中,如赤铁矿、铝土矿等。很不活泼金银铂化合物一、几种金属矿物2.金属在地壳中的含量:地壳中所占的质量分数最高的金属是________,其次是________。铝铁3.金属矿物
常见的金属矿物:赤铁矿(主要成分是________)、磁铁矿(主要成分是________)、铝土矿(主要成分是Al2O3)。Fe2O3Fe3O4二、工业炼铁1.实验室模拟炼铁原理
(1)药品:_____________,_____________
(2)反应原理:________________________________
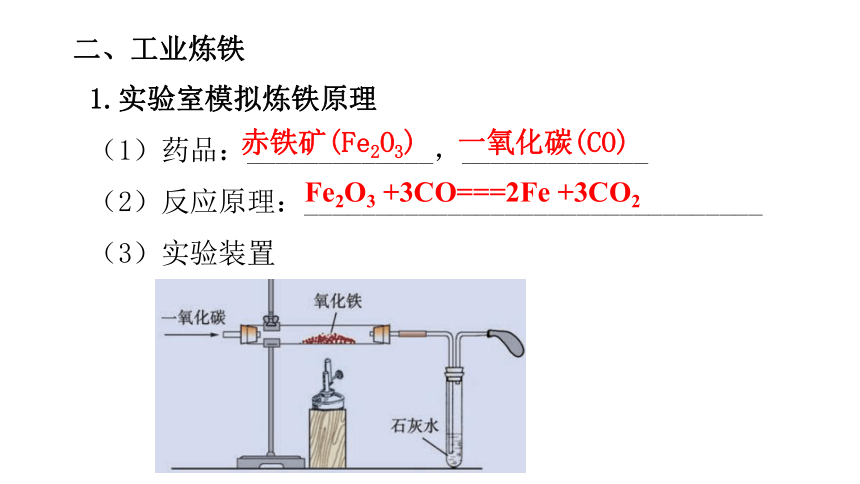
(3)实验装置
Fe2O3 +3CO===2Fe +3CO2赤铁矿(Fe2O3)一氧化碳(CO)实验现象:①红色粉末(氧化铁)逐渐变成黑色,②澄清的石灰水逐渐变浑浊,③气球膨胀。铁矿石、焦炭、石灰石、空气高炉生铁①吹氧冶炼②除磷、硫2.工业上钢铁的冶炼2课堂导入 我国有着悠久的金属冶炼历史,也为我们留下了无数的金属文物。大家或许注意到过这么一个现象:铁、铜制品易生锈,而黄金制品却一直光彩夺目。生锈的铁剑生锈的铜钱古代的金锭金蟾为什么同样都是金属,差别却如此之大?3新课讲授 金属的这些现象差别只从物理角度考虑是不能解释的,实际上,这与金属的化学性质的差异有关。那么,金属有哪些化学性质呢?01金属与氧气的反应【知识回顾】你学过哪些金属与O2的反应?①镁条在空气中燃烧实验现象:剧烈燃烧,发出耀眼的白光,放热,生成白色固体? 点燃
2Mg+O2==2MgO化学方程式:②铁丝在氧气中燃烧实验现象:剧烈燃烧,火星四射,放出大量的热,生成黑色固体? 点燃
3Fe+2O2==Fe3O4化学方程式:③铜在酒精灯上加热实验现象:由红色变为黑色 △
2Cu+O2==2CuO化学方程式:实验探究9-2铝在氧气中燃烧实验操作:用滤纸卷上少量铝粉,在酒精灯上点燃,迅速插入盛有氧气的集气瓶中观察有什么现象?4Al+3O2===2Al2O3点燃实验现象:铝粉能在氧气中剧烈燃烧,生成白色粉末 。化学方程式:【思考讨论】俗话说“真金不怕火炼”,这说明了什么事实? 在高温条件下金不能和氧气反应。
Au + O2≠
除金外,银、铂等金属也不能与氧气反应。金店在验金实验表明:大多数金属都能与氧气反应,生成相应的金属氧化物,但反应的难易和剧烈程度不同。1.常温下易与氧气反应: 以???? 、 ????为代表。
2.加热时能与氧气反应:以???? 、 ????为代表。
3.高温下也不能与氧气反应:以????????为代表。 MgAlFeCuAu【结论】金属活动性:???????????????????????????? Mg、Al>Fe、Cu>Au思考:铝比铁更易与氧气或其他物质反应,为什么在生活中很少见到铝被腐蚀?因为铝在空气中与氧气反应,其表面生成一层致密的氧化铝(Al2O3)薄膜,从而阻止铝进一步被氧化。因此,铝制品有很好的抗腐蚀性能。通过金属与氧气反应的条件的难易,可以得出金属的活动性不同,那么还有其他的方法判断金属的活动性吗?有。很多金属不仅能与氧气反应,而且还能与盐酸或稀硫酸反应。金属与盐酸或稀硫酸能否反应以及反应的剧烈程度,也可反映出金属的活泼程度。 02金属与酸的反应实验探究9-3金属与酸的反应实验操作:准备6支试管,分成两组,每组均编号1、2、3,在A组每支试管中加入等体积的稀盐酸,在B组每支试管中加入等体积的稀硫酸,然后分别在1号、2号、3号的试管中加入适量的打磨过的铁丝、铝条和铜丝,观察现象。123实验现象:A组/B组:放出气泡最迅速,
反应最剧烈。放出气泡速度很慢,反应较为缓和。溶液由无色变为浅绿色不反应2Al+3H2SO4=Al2(SO4)3+3H2↑2Al+6HCl=2AlCl3+3H2↑Fe+H2SO4=FeSO4+H2↑Fe+2HCl=FeCl2+H2↑【实验结论】Al> Fe> Cu上述实验得到的金属排序也叫做金属活动性顺序。科学家经过多方面的研究,对金属的活动性进行排列如下:CaNaMgAlZnFeSnPbHCuHgAgPtAuK金属活动性由强到弱钙钠镁铝锌铁锡铅氢铜汞银铂金钾对金属活动性顺序的理解:
(1)在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
(2)在金属活动性顺序里,排在氢前面的金属能与酸反应放出氢气,而排在氢后面的金属不能与酸反应放出氢气。Zn + H2SO4 == ZnSO4 + H2 ↑
Mg + 2HCl == MgCl2 + H2 ↑
Fe + 2HCl == FeCl2 + H2 ↑化合物 单质单质化合物观察下列化学方程式,分析这些反应有什么共同特点?像这种一种单质与一种化合物反应,生成另一种单质与另一种化合物的化学反应叫做置换反应。置换反应特点:“单换单”通式:A+BC→B+AC想一想,四类基本反应类型各有何特点?化合反应
特点:A+B=AB分解反应
特点:AB=A+BCaO + 2HCl = CaCl2 + H2O
Na2CO3 + 2HCl = 2NaCl+CO2↑+H2O
2NaOH + CuCl2 = Cu(OH)2↓+2NaCl
NaCl + AgNO3 = AgCl↓ + NaNO3}复分解反应特点:AB+CD=CB+AD B小试牛刀4课堂小结置换反应2Mg + O2 === 2MgO点燃3Fe+2O2====Fe3O4点燃2Cu + O2====2CuO2Al + 6HCl = 2AlCl3 + 3H2↑Fe + 2HCl = FeCl2 + H2↑金属的化学性质5典型例题考点一:金属氧气、酸的反应【典型例题1】(2019秋?嵊州市校级月考)下面物质中,不能用金属和酸直接反应得到的是( )
A.氯化镁 B.硫酸铝 C.氯化锌 D.硫酸铁D【迁移训练1】下列关于金属与氧气的说法,正确的是( )
A.金属铝在常温下与氧气剧烈反应
B.各种金属都能与氧气在常温下反应
C.红热的铁丝能在空气中燃烧
D.根据金属与氧气反应的难易程度,可初步判断一些金属的活动性B【典型例题2】(2019?黄冈中考)下列化学反应属于置换反应的是( )
A.Zn+H2SO4═ZnSO4+H2↑
B.Ba(OH)2+H2SO4═BaSO4↓+2H2O
C.4Fe(OH)2+O2+2H2O═4Fe(OH)3
D.2HgO 2Hg+O2↑
A考点二:置换反应【迁移训练2】铁、锌与稀盐酸反应的化学方程式分别为Fe+2HCl===FeCl2+H2↑、Zn+2HCl===ZnCl2+H2↑,关于这两个反应说法错误的是( )
A.反应物都是一种单质和一种化合物
B.生成物是另一种单质和另一种化合物
C.都是化合反应
D.都是置换反应
C考点三:金属活动性顺序C【迁移训练3】(2019?金牛区模拟改编)如图是金属活动性顺序的部分内容,则下列说法正确的是( )A.金属①是Mg
B.2Fe+6HCl=2FeCl3+3H2↑
C.金属②能置换出稀盐酸中的氢气
D.金属①的活泼性比②强D
(2)化合物形态:绝大多数金属都是以__________形态存在于矿物之中,如赤铁矿、铝土矿等。很不活泼金银铂化合物一、几种金属矿物2.金属在地壳中的含量:地壳中所占的质量分数最高的金属是________,其次是________。铝铁3.金属矿物
常见的金属矿物:赤铁矿(主要成分是________)、磁铁矿(主要成分是________)、铝土矿(主要成分是Al2O3)。Fe2O3Fe3O4二、工业炼铁1.实验室模拟炼铁原理
(1)药品:_____________,_____________
(2)反应原理:________________________________
(3)实验装置
Fe2O3 +3CO===2Fe +3CO2赤铁矿(Fe2O3)一氧化碳(CO)实验现象:①红色粉末(氧化铁)逐渐变成黑色,②澄清的石灰水逐渐变浑浊,③气球膨胀。铁矿石、焦炭、石灰石、空气高炉生铁①吹氧冶炼②除磷、硫2.工业上钢铁的冶炼2课堂导入 我国有着悠久的金属冶炼历史,也为我们留下了无数的金属文物。大家或许注意到过这么一个现象:铁、铜制品易生锈,而黄金制品却一直光彩夺目。生锈的铁剑生锈的铜钱古代的金锭金蟾为什么同样都是金属,差别却如此之大?3新课讲授 金属的这些现象差别只从物理角度考虑是不能解释的,实际上,这与金属的化学性质的差异有关。那么,金属有哪些化学性质呢?01金属与氧气的反应【知识回顾】你学过哪些金属与O2的反应?①镁条在空气中燃烧实验现象:剧烈燃烧,发出耀眼的白光,放热,生成白色固体? 点燃
2Mg+O2==2MgO化学方程式:②铁丝在氧气中燃烧实验现象:剧烈燃烧,火星四射,放出大量的热,生成黑色固体? 点燃
3Fe+2O2==Fe3O4化学方程式:③铜在酒精灯上加热实验现象:由红色变为黑色 △
2Cu+O2==2CuO化学方程式:实验探究9-2铝在氧气中燃烧实验操作:用滤纸卷上少量铝粉,在酒精灯上点燃,迅速插入盛有氧气的集气瓶中观察有什么现象?4Al+3O2===2Al2O3点燃实验现象:铝粉能在氧气中剧烈燃烧,生成白色粉末 。化学方程式:【思考讨论】俗话说“真金不怕火炼”,这说明了什么事实? 在高温条件下金不能和氧气反应。
Au + O2≠
除金外,银、铂等金属也不能与氧气反应。金店在验金实验表明:大多数金属都能与氧气反应,生成相应的金属氧化物,但反应的难易和剧烈程度不同。1.常温下易与氧气反应: 以???? 、 ????为代表。
2.加热时能与氧气反应:以???? 、 ????为代表。
3.高温下也不能与氧气反应:以????????为代表。 MgAlFeCuAu【结论】金属活动性:???????????????????????????? Mg、Al>Fe、Cu>Au思考:铝比铁更易与氧气或其他物质反应,为什么在生活中很少见到铝被腐蚀?因为铝在空气中与氧气反应,其表面生成一层致密的氧化铝(Al2O3)薄膜,从而阻止铝进一步被氧化。因此,铝制品有很好的抗腐蚀性能。通过金属与氧气反应的条件的难易,可以得出金属的活动性不同,那么还有其他的方法判断金属的活动性吗?有。很多金属不仅能与氧气反应,而且还能与盐酸或稀硫酸反应。金属与盐酸或稀硫酸能否反应以及反应的剧烈程度,也可反映出金属的活泼程度。 02金属与酸的反应实验探究9-3金属与酸的反应实验操作:准备6支试管,分成两组,每组均编号1、2、3,在A组每支试管中加入等体积的稀盐酸,在B组每支试管中加入等体积的稀硫酸,然后分别在1号、2号、3号的试管中加入适量的打磨过的铁丝、铝条和铜丝,观察现象。123实验现象:A组/B组:放出气泡最迅速,
反应最剧烈。放出气泡速度很慢,反应较为缓和。溶液由无色变为浅绿色不反应2Al+3H2SO4=Al2(SO4)3+3H2↑2Al+6HCl=2AlCl3+3H2↑Fe+H2SO4=FeSO4+H2↑Fe+2HCl=FeCl2+H2↑【实验结论】Al> Fe> Cu上述实验得到的金属排序也叫做金属活动性顺序。科学家经过多方面的研究,对金属的活动性进行排列如下:CaNaMgAlZnFeSnPbHCuHgAgPtAuK金属活动性由强到弱钙钠镁铝锌铁锡铅氢铜汞银铂金钾对金属活动性顺序的理解:
(1)在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
(2)在金属活动性顺序里,排在氢前面的金属能与酸反应放出氢气,而排在氢后面的金属不能与酸反应放出氢气。Zn + H2SO4 == ZnSO4 + H2 ↑
Mg + 2HCl == MgCl2 + H2 ↑
Fe + 2HCl == FeCl2 + H2 ↑化合物 单质单质化合物观察下列化学方程式,分析这些反应有什么共同特点?像这种一种单质与一种化合物反应,生成另一种单质与另一种化合物的化学反应叫做置换反应。置换反应特点:“单换单”通式:A+BC→B+AC想一想,四类基本反应类型各有何特点?化合反应
特点:A+B=AB分解反应
特点:AB=A+BCaO + 2HCl = CaCl2 + H2O
Na2CO3 + 2HCl = 2NaCl+CO2↑+H2O
2NaOH + CuCl2 = Cu(OH)2↓+2NaCl
NaCl + AgNO3 = AgCl↓ + NaNO3}复分解反应特点:AB+CD=CB+AD B小试牛刀4课堂小结置换反应2Mg + O2 === 2MgO点燃3Fe+2O2====Fe3O4点燃2Cu + O2====2CuO2Al + 6HCl = 2AlCl3 + 3H2↑Fe + 2HCl = FeCl2 + H2↑金属的化学性质5典型例题考点一:金属氧气、酸的反应【典型例题1】(2019秋?嵊州市校级月考)下面物质中,不能用金属和酸直接反应得到的是( )
A.氯化镁 B.硫酸铝 C.氯化锌 D.硫酸铁D【迁移训练1】下列关于金属与氧气的说法,正确的是( )
A.金属铝在常温下与氧气剧烈反应
B.各种金属都能与氧气在常温下反应
C.红热的铁丝能在空气中燃烧
D.根据金属与氧气反应的难易程度,可初步判断一些金属的活动性B【典型例题2】(2019?黄冈中考)下列化学反应属于置换反应的是( )
A.Zn+H2SO4═ZnSO4+H2↑
B.Ba(OH)2+H2SO4═BaSO4↓+2H2O
C.4Fe(OH)2+O2+2H2O═4Fe(OH)3
D.2HgO 2Hg+O2↑
A考点二:置换反应【迁移训练2】铁、锌与稀盐酸反应的化学方程式分别为Fe+2HCl===FeCl2+H2↑、Zn+2HCl===ZnCl2+H2↑,关于这两个反应说法错误的是( )
A.反应物都是一种单质和一种化合物
B.生成物是另一种单质和另一种化合物
C.都是化合反应
D.都是置换反应
C考点三:金属活动性顺序C【迁移训练3】(2019?金牛区模拟改编)如图是金属活动性顺序的部分内容,则下列说法正确的是( )A.金属①是Mg
B.2Fe+6HCl=2FeCl3+3H2↑
C.金属②能置换出稀盐酸中的氢气
D.金属①的活泼性比②强D
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
