北京版九年级化学下第十一章第三节几种常见的碱教学设计
文档属性
| 名称 | 北京版九年级化学下第十一章第三节几种常见的碱教学设计 |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-31 00:00:00 | ||
图片预览


文档简介
第11章 酸和碱
第三节 几种常见的碱
教学指导思想
本节课以物质分类观为指导,构建碱的概念。培养学生从熟悉的已知物质推知未知的物质,学会总结归纳从几种物质的性质,推知一类物质的性质;又能从一类物质的性质,推知某种未知物质的性质,形成从零散经验到通性框架的认识角度。学生学会共同的结构与相似的化学性质之间的关系。同时认识到对于物质进行分类的重要性和必要性。
教学背景分析
教材分析
北京版化学教材体现了化学学科的知识结构体系,多角度的选择和组织教材内容,帮助学生建构分类观。在第一章《空气之谜》中第一节“空气”,首次引入分类思想,将物质分为纯净物和混合物。第三章《构成物质的微粒》中,从分子、原子、离子微观粒子的角度,将物质分类。分成由分子构成的物质、由原子构成的物质、由离子构成的物质等,初步接触微粒观和分类观。第五章《化学元素与物质组成的表示》使学生初步建立分类的观点去认识物质。第一节“初步认识化学元素”中分析原子、元素与单质的关系,认识元素的分类观,每一种元素都有自己的家族,而建立起元素与物质的关系。通过关系图和实例体会物质分类的体系,认识物质是如何分类的,分类标准由物质种类拓展到元素种类。引导学生建立元素观和分类观,体会分类是化学学习和研究中常用的一种科学方法。第九章《溶液》中根据是否澄清透明,分成溶液、浊液;根据溶液的状态,分成饱和溶液和不饱和溶液。在溶液的研究中,初步体会二级分类研究问题的必要性。第十一章《酸与碱》在酸碱概念的学习中,建立结构与性质之间的关系。使学生体会到共同的结构特点与相似的化学性质之间的关系。使学生学会归纳从几种物质的性质,推知一类物质的性质,又能从一类物质的性质,推知某种物质的性质,形成从零散经验到通性框架的认识角度,同时认识到对于物质进行分类的重要性和必要性。
化学反应分类的内容,在教材中主要根据反应物、生成物的种类和组成的变化,从宏观物质的角度分为四种基本反应类型、氧化反应、还原反应。
学情分析
学生对物质的认识通常是一个由现象到本质的逐步深化过程,一开始是对物质颜色、状态、形状等外部特征的认识,接下来通过对组成、结构和性质的研究获得物质本质属性和内在联系的认识。学生在单质、化合物、氧化物等概念的建立过程,以具备能够在物质的组成元素种类上对常见的化学物质进行简单分类的能力。在酸的概念形成及性质的研究过程中,初步构建了分类标准以及一类典型代表物的研究方法。并初步认识到同类物质的共性及研究方法的相似性。
本节课促使学生在物质分类的基础上,从组成和结构上比较异同点,研究物质的性质,总结相似的结构,具有相似的性质,不同的结构,具有性质的差异性,学生从整体上认识物质组成与性质之间的关系。更深一步的掌握了物质结构决定性质、性质推断结构的科学研究的一般思想方法。为学生高中知识如元素周期律、元素周期表的学习中物质分类观的运用打下基础。
教学目标
1、通过总结、归纳氢氧化钙的化学性质,推测氢氧化钠的化学性质,总结、归纳碱的共性。
2、运用分类法,选择典型代表物,由已知物质的性质推测未知物质的性质,并进行
实验验证。
体会分类研究物质的意义和价值。
重点: 碱溶液的化学性质
难点: 分类研究物质的方法
二.教学过程
教学环节
教师活动
学生活动
设置意图
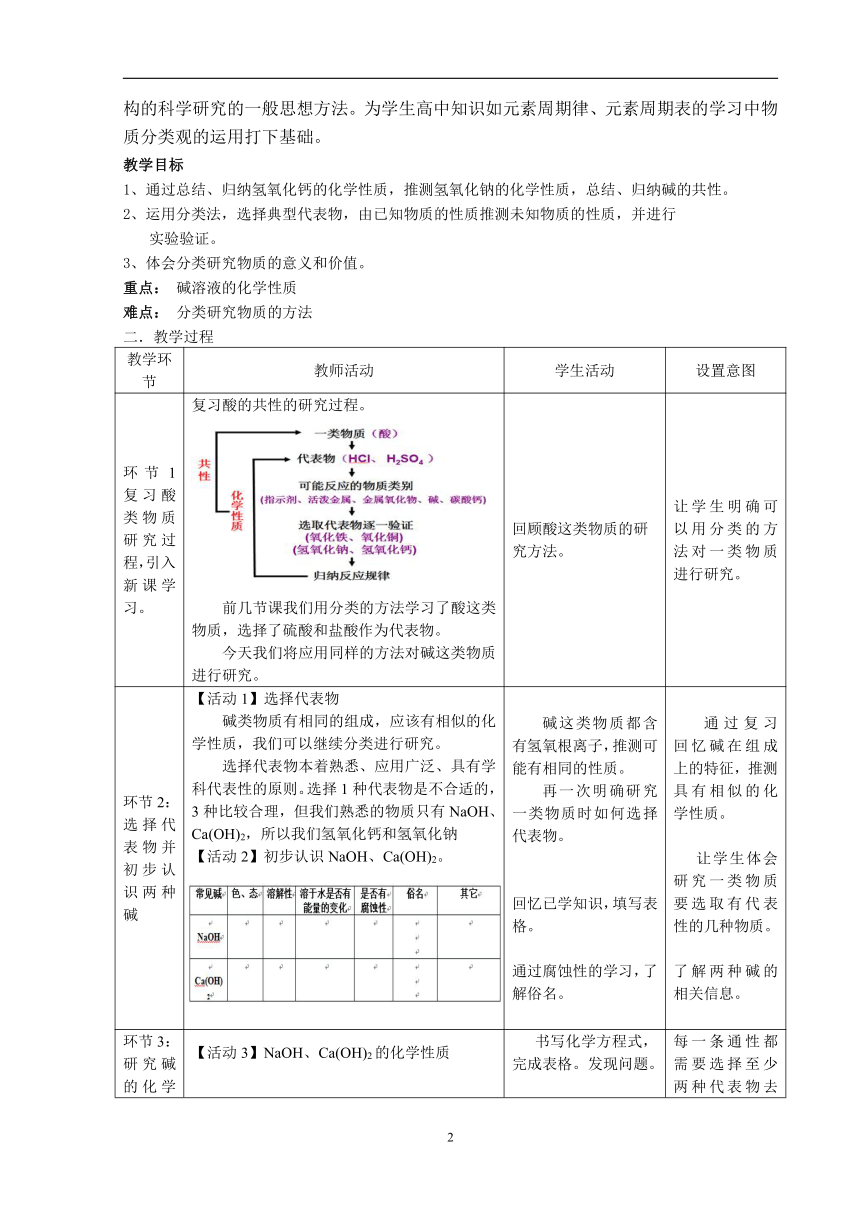
环节1复习酸类物质研究过程,引入新课学习。
复习酸的共性的研究过程。
前几节课我们用分类的方法学习了酸这类物质,选择了硫酸和盐酸作为代表物。
今天我们将应用同样的方法对碱这类物质进行研究。
回顾酸这类物质的研究方法。
让学生明确可以用分类的方法对一类物质进行研究。
环节2:
选择代表物并初步认识两种碱
【活动1】选择代表物
碱类物质有相同的组成,应该有相似的化学性质,我们可以继续分类进行研究。
选择代表物本着熟悉、应用广泛、具有学科代表性的原则。选择1种代表物是不合适的,3种比较合理,但我们熟悉的物质只有NaOH、Ca(OH)2,所以我们氢氧化钙和氢氧化钠
【活动2】初步认识NaOH、Ca(OH)2。
碱这类物质都含有氢氧根离子,推测可能有相同的性质。
再一次明确研究一类物质时如何选择代表物。
回忆已学知识,填写表格。
通过腐蚀性的学习,了解俗名。
通过复习回忆碱在组成上的特征,推测具有相似的化学性质。
让学生体会研究一类物质要选取有代表性的几种物质。
了解两种碱的相关信息。
环节3:研究碱的化学性质
【活动3】NaOH、Ca(OH)2的化学性质
明确通式的得出至少要有两种代表物。与酸的反应,是选择了盐酸和硫酸。那么碱溶液和非金属氧化物反应至少要选择两种物质。所以只有和二氧化碳的反应是不合适的。
书写化学方程式,完成表格。发现问题。
【问题1】 氢氧化钠和二氧化碳反应吗?
【问题2】能得到通式“碱溶液+非金属氧化物 →盐+水” 吗?
每一条通性都需要选择至少两种代表物去研究。
培养学生发现问题的能力。
【任务1】实验探究CO2和NaOH溶液是否反应?
实验仪器:吸管、烧杯、矿泉水瓶
实验药品:氢氧化钠溶液、氢氧化钙溶液、水、稀盐酸、二氧化碳、酚酞
【任务2】实验探究CO2和Ca(OH)2、NaOH溶液是否反应?
【小结】碱溶液的共性
【板书】
设计实验并进行实验验证。
实验结论:CO2和NaOH溶液发生了反应。
实验结论:CO2和Ca(OH)2、NaOH溶液发生了反应;碱溶液+金属氧化物→盐+水
观看幻灯片
培养学生解决问题的能力,和设计实验方案的能力。
培养学生书写方程式的能力。
总结碱溶液的共性。
应用物质分类的方法研究一类物质性质的一般思路。
环节4
学以致用
【学以致用】
氢氧化钾和氢氧化钠的化学性质相似,请写出氢氧化钾溶液分别和硫酸、二氧化碳反应的化学方程式。
体会分类研究物质的价值,举一反三。
环节5探究碱的差异性
【活动4】探究碱的差异性
实验探究Ca(OH)2、NaOH溶液与碳酸钾溶液是否反应。
结构相同,性质相似。
学生演示实验。
体会结构不同,性质有差异。
环节6拓展练习
【拓展练习】
探究二氧化碳和石灰水的反应还有许多其它的设计方案,课后小组讨论,看看大家能够设计多少种方案,咱们逐一实验验证。
课后继续深入学习。进行组间竞赛、展示、验证。
培养学生实际实验方案的能力。
三.板书设计:
学案
第三节 几种常见的碱
班级 姓名
一、初步认识Ca(OH)2和NaOH。
常见碱
色、态
溶解性
溶于水是否有能量的变化
是否有
腐蚀性
俗名
其它
NaOH
Ca(OH)2
二、两种碱的化学性质。(能写方程式的写方程式)
氢氧化钙
氢氧化钠
通式
和指示剂
反应(填变色)
和酸反应
与非金属氧化物
反应
三、碱溶液共性的探究。
【任务1】实验探究CO2和NaOH溶液 是否反应?
实验仪器:吸管、矿泉水瓶、烧杯
实验药品:氢氧化钠溶液、氢氧化钙溶液、水、稀盐酸、二氧化碳、酚酞
【任务2】实验探究SO2和Ca(OH)2、NaOH溶液是否反应?
四、【学以致用】氢氧化钾和氢氧化钠的化学性质相似,请写出氢氧化钾溶液分别和硫酸、二氧化碳反应的化学方程式。
五、碱溶液差异性的探究。
现象:
结论:化学方程式
六、【拓展练习】设计实验验证二氧化碳和氢氧化钠溶液发生了反应,仪器可另选。
第三节 几种常见的碱
教学指导思想
本节课以物质分类观为指导,构建碱的概念。培养学生从熟悉的已知物质推知未知的物质,学会总结归纳从几种物质的性质,推知一类物质的性质;又能从一类物质的性质,推知某种未知物质的性质,形成从零散经验到通性框架的认识角度。学生学会共同的结构与相似的化学性质之间的关系。同时认识到对于物质进行分类的重要性和必要性。
教学背景分析
教材分析
北京版化学教材体现了化学学科的知识结构体系,多角度的选择和组织教材内容,帮助学生建构分类观。在第一章《空气之谜》中第一节“空气”,首次引入分类思想,将物质分为纯净物和混合物。第三章《构成物质的微粒》中,从分子、原子、离子微观粒子的角度,将物质分类。分成由分子构成的物质、由原子构成的物质、由离子构成的物质等,初步接触微粒观和分类观。第五章《化学元素与物质组成的表示》使学生初步建立分类的观点去认识物质。第一节“初步认识化学元素”中分析原子、元素与单质的关系,认识元素的分类观,每一种元素都有自己的家族,而建立起元素与物质的关系。通过关系图和实例体会物质分类的体系,认识物质是如何分类的,分类标准由物质种类拓展到元素种类。引导学生建立元素观和分类观,体会分类是化学学习和研究中常用的一种科学方法。第九章《溶液》中根据是否澄清透明,分成溶液、浊液;根据溶液的状态,分成饱和溶液和不饱和溶液。在溶液的研究中,初步体会二级分类研究问题的必要性。第十一章《酸与碱》在酸碱概念的学习中,建立结构与性质之间的关系。使学生体会到共同的结构特点与相似的化学性质之间的关系。使学生学会归纳从几种物质的性质,推知一类物质的性质,又能从一类物质的性质,推知某种物质的性质,形成从零散经验到通性框架的认识角度,同时认识到对于物质进行分类的重要性和必要性。
化学反应分类的内容,在教材中主要根据反应物、生成物的种类和组成的变化,从宏观物质的角度分为四种基本反应类型、氧化反应、还原反应。
学情分析
学生对物质的认识通常是一个由现象到本质的逐步深化过程,一开始是对物质颜色、状态、形状等外部特征的认识,接下来通过对组成、结构和性质的研究获得物质本质属性和内在联系的认识。学生在单质、化合物、氧化物等概念的建立过程,以具备能够在物质的组成元素种类上对常见的化学物质进行简单分类的能力。在酸的概念形成及性质的研究过程中,初步构建了分类标准以及一类典型代表物的研究方法。并初步认识到同类物质的共性及研究方法的相似性。
本节课促使学生在物质分类的基础上,从组成和结构上比较异同点,研究物质的性质,总结相似的结构,具有相似的性质,不同的结构,具有性质的差异性,学生从整体上认识物质组成与性质之间的关系。更深一步的掌握了物质结构决定性质、性质推断结构的科学研究的一般思想方法。为学生高中知识如元素周期律、元素周期表的学习中物质分类观的运用打下基础。
教学目标
1、通过总结、归纳氢氧化钙的化学性质,推测氢氧化钠的化学性质,总结、归纳碱的共性。
2、运用分类法,选择典型代表物,由已知物质的性质推测未知物质的性质,并进行
实验验证。
体会分类研究物质的意义和价值。
重点: 碱溶液的化学性质
难点: 分类研究物质的方法
二.教学过程
教学环节
教师活动
学生活动
设置意图
环节1复习酸类物质研究过程,引入新课学习。
复习酸的共性的研究过程。
前几节课我们用分类的方法学习了酸这类物质,选择了硫酸和盐酸作为代表物。
今天我们将应用同样的方法对碱这类物质进行研究。
回顾酸这类物质的研究方法。
让学生明确可以用分类的方法对一类物质进行研究。
环节2:
选择代表物并初步认识两种碱
【活动1】选择代表物
碱类物质有相同的组成,应该有相似的化学性质,我们可以继续分类进行研究。
选择代表物本着熟悉、应用广泛、具有学科代表性的原则。选择1种代表物是不合适的,3种比较合理,但我们熟悉的物质只有NaOH、Ca(OH)2,所以我们氢氧化钙和氢氧化钠
【活动2】初步认识NaOH、Ca(OH)2。
碱这类物质都含有氢氧根离子,推测可能有相同的性质。
再一次明确研究一类物质时如何选择代表物。
回忆已学知识,填写表格。
通过腐蚀性的学习,了解俗名。
通过复习回忆碱在组成上的特征,推测具有相似的化学性质。
让学生体会研究一类物质要选取有代表性的几种物质。
了解两种碱的相关信息。
环节3:研究碱的化学性质
【活动3】NaOH、Ca(OH)2的化学性质
明确通式的得出至少要有两种代表物。与酸的反应,是选择了盐酸和硫酸。那么碱溶液和非金属氧化物反应至少要选择两种物质。所以只有和二氧化碳的反应是不合适的。
书写化学方程式,完成表格。发现问题。
【问题1】 氢氧化钠和二氧化碳反应吗?
【问题2】能得到通式“碱溶液+非金属氧化物 →盐+水” 吗?
每一条通性都需要选择至少两种代表物去研究。
培养学生发现问题的能力。
【任务1】实验探究CO2和NaOH溶液是否反应?
实验仪器:吸管、烧杯、矿泉水瓶
实验药品:氢氧化钠溶液、氢氧化钙溶液、水、稀盐酸、二氧化碳、酚酞
【任务2】实验探究CO2和Ca(OH)2、NaOH溶液是否反应?
【小结】碱溶液的共性
【板书】
设计实验并进行实验验证。
实验结论:CO2和NaOH溶液发生了反应。
实验结论:CO2和Ca(OH)2、NaOH溶液发生了反应;碱溶液+金属氧化物→盐+水
观看幻灯片
培养学生解决问题的能力,和设计实验方案的能力。
培养学生书写方程式的能力。
总结碱溶液的共性。
应用物质分类的方法研究一类物质性质的一般思路。
环节4
学以致用
【学以致用】
氢氧化钾和氢氧化钠的化学性质相似,请写出氢氧化钾溶液分别和硫酸、二氧化碳反应的化学方程式。
体会分类研究物质的价值,举一反三。
环节5探究碱的差异性
【活动4】探究碱的差异性
实验探究Ca(OH)2、NaOH溶液与碳酸钾溶液是否反应。
结构相同,性质相似。
学生演示实验。
体会结构不同,性质有差异。
环节6拓展练习
【拓展练习】
探究二氧化碳和石灰水的反应还有许多其它的设计方案,课后小组讨论,看看大家能够设计多少种方案,咱们逐一实验验证。
课后继续深入学习。进行组间竞赛、展示、验证。
培养学生实际实验方案的能力。
三.板书设计:
学案
第三节 几种常见的碱
班级 姓名
一、初步认识Ca(OH)2和NaOH。
常见碱
色、态
溶解性
溶于水是否有能量的变化
是否有
腐蚀性
俗名
其它
NaOH
Ca(OH)2
二、两种碱的化学性质。(能写方程式的写方程式)
氢氧化钙
氢氧化钠
通式
和指示剂
反应(填变色)
和酸反应
与非金属氧化物
反应
三、碱溶液共性的探究。
【任务1】实验探究CO2和NaOH溶液 是否反应?
实验仪器:吸管、矿泉水瓶、烧杯
实验药品:氢氧化钠溶液、氢氧化钙溶液、水、稀盐酸、二氧化碳、酚酞
【任务2】实验探究SO2和Ca(OH)2、NaOH溶液是否反应?
四、【学以致用】氢氧化钾和氢氧化钠的化学性质相似,请写出氢氧化钾溶液分别和硫酸、二氧化碳反应的化学方程式。
五、碱溶液差异性的探究。
现象:
结论:化学方程式
六、【拓展练习】设计实验验证二氧化碳和氢氧化钠溶液发生了反应,仪器可另选。
