科粤化学下册第7章1 溶解与乳化共17张PPT
文档属性
| 名称 | 科粤化学下册第7章1 溶解与乳化共17张PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-01 00:00:00 | ||
图片预览






文档简介
课件17张PPT。第一节 溶解与乳化
(第一课时)第七章 溶液 现在市面上销售着各式各样的饮料,这些饮料就是各种溶液,那么这些溶液是怎样形成的呢?今天我们就来学习------溶解与乳化学习目标 1.通过实验及生活经验,认识溶液的概念、特征,知道溶质和溶剂的概念,能够分辨常见溶液中的溶
质和溶剂。
2. 通过固体物质溶于水时溶液温度的变化,了解
物质溶解过程中伴随着能量的变化。
探究活动一 食盐的溶解[学生演示] 取一只小烧杯,倒入约25mL水,加入小半药匙食盐(主要成分是氯化钠),用玻璃棒搅拌。仔细观察发生的变化,直至食盐颗粒在水中消失,触摸烧杯,感受温度变化。 【讨论交流】
食盐颗粒为什么不见了?
食盐颗粒逐渐减小,最后消失形成了均一、稳定的混合物讨论分析:
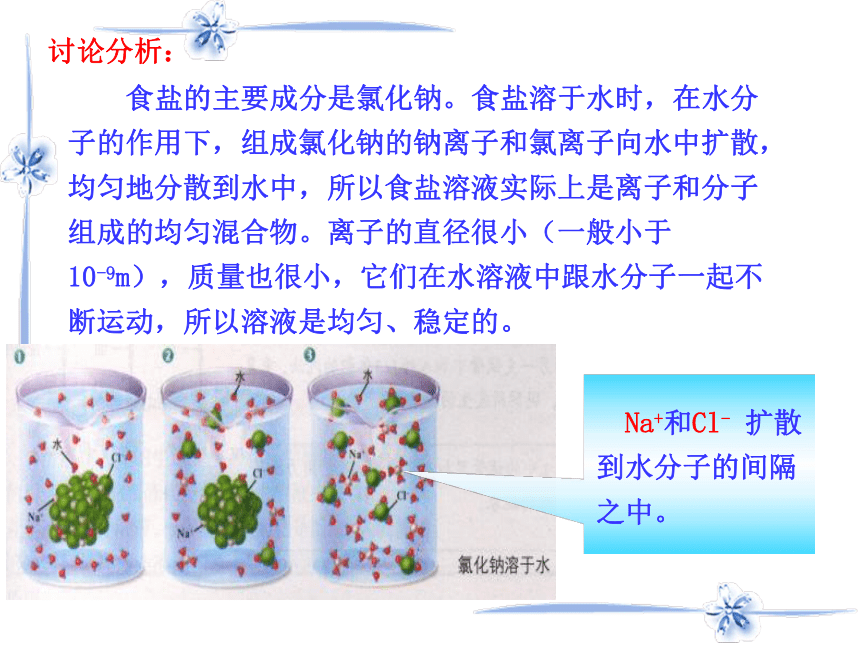
食盐的主要成分是氯化钠。食盐溶于水时,在水分子的作用下,组成氯化钠的钠离子和氯离子向水中扩散,均匀地分散到水中,所以食盐溶液实际上是离子和分子组成的均匀混合物。离子的直径很小(一般小于
10-9m),质量也很小,它们在水溶液中跟水分子一起不断运动,所以溶液是均匀、稳定的。 Na+和Cl- 扩散到水分子的间隔之中。 一、溶液定义:
【预习归纳】一种或几种物质分散到另一种物质 里,形成均一的、稳定的混合物。【问题】把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A. 泥沙 B. 氯化钠 C. 汽油 D. 蔗糖BD关于溶液的认识
(2)溶液一定是无色透明的吗? (3)均一、稳定的液体一定是溶液吗?(1)溶液的特征是什么?均一性、稳定性、 混合物。不一定。如硫酸铜溶液是蓝色的。不一定。如:水就不是溶液、
酒精也不是溶液。问题与思考(1)溶剂:能溶解其它物质的物质
(2)溶质:被溶解的物质1、溶液的组成:m溶液 = m溶剂+m溶质 2、质量关系预习展示溶液食盐溶液蔗糖溶液酒精溶液碘酒硫酸铜溶液溶质溶剂氯化钠水蔗糖 水酒精水 碘酒精硫酸铜 水【讨论展示】3、 判断下列溶液中的溶质和溶剂讨论:溶液中溶质和溶剂是如何确定的?气体液体固体液体量少 量多非水物水溶质可以是固体、气体或液体。如果其中有一种是水,一般把水叫溶剂。若两种液体互相溶解时,把量多的叫溶剂,量少的叫溶质。二、探究活动P195 7-4 物质溶解时温度的变化【学生演示】1、取两只小烧杯,分别加入20ml蒸馏水,用温度计测量水温(T1)。
2、向一只小烧杯中加入约3g氢氧化钠固体,搅拌,测量溶液的温度(T2)。
3、向另一只小烧杯中加入约3g硝酸铵固体,搅拌,测量溶液的温度(T2)。
4、向另一只小烧杯中加入约3g氯化钠固体,搅拌,测量溶液的温度(T2) 。
[结论]
氢氧化钠固体溶于水温度 ,硝酸铵固体溶于水温度 ,氯化钠固体溶于水温度 。 升高降低不变[讨论展示] 扩散
过程
(吸热) 水合
过程
(放热)吸热>放热
(溶液温度降低)
例如:NH4NO3固体溶于水吸热 = 放热
(溶液温度不变)
例如:NaCl固体溶于水吸热<放热
(溶液温度升高)
例如:NaOH 固体溶解1、如右图所示,a、b液面是相平的。请向小试管中加入一定量的物质,使右侧U形管中的a面下降、b面上升。则加入的物质是 。A.氢氧化钠固体
B.氯化钠固体
C.硝酸铵晶体 讨论交流A1、下列各组液体中,不属于溶液的是( )
A.汽水 B.冰水混合物
C.食盐水 D.75%的酒精溶液
2、可以作为溶质的( )。
A.只有固体 B. 只有液体
C. 只有气体 D.气体、液体、固体都可以
3、某边远山区,有人发高烧,小明建议可以把硝酸铵、氯化钠、氢氧化钠中的 ,加入盛水的塑料袋中,对病人进行冷敷。 交流与总结
本节课,你学到了哪些新的知识?
质和溶剂。
2. 通过固体物质溶于水时溶液温度的变化,了解
物质溶解过程中伴随着能量的变化。
探究活动一 食盐的溶解[学生演示] 取一只小烧杯,倒入约25mL水,加入小半药匙食盐(主要成分是氯化钠),用玻璃棒搅拌。仔细观察发生的变化,直至食盐颗粒在水中消失,触摸烧杯,感受温度变化。 【讨论交流】
食盐颗粒为什么不见了?
食盐颗粒逐渐减小,最后消失形成了均一、稳定的混合物讨论分析:
食盐的主要成分是氯化钠。食盐溶于水时,在水分子的作用下,组成氯化钠的钠离子和氯离子向水中扩散,均匀地分散到水中,所以食盐溶液实际上是离子和分子组成的均匀混合物。离子的直径很小(一般小于
10-9m),质量也很小,它们在水溶液中跟水分子一起不断运动,所以溶液是均匀、稳定的。 Na+和Cl- 扩散到水分子的间隔之中。 一、溶液定义:
【预习归纳】一种或几种物质分散到另一种物质 里,形成均一的、稳定的混合物。【问题】把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A. 泥沙 B. 氯化钠 C. 汽油 D. 蔗糖BD关于溶液的认识
(2)溶液一定是无色透明的吗? (3)均一、稳定的液体一定是溶液吗?(1)溶液的特征是什么?均一性、稳定性、 混合物。不一定。如硫酸铜溶液是蓝色的。不一定。如:水就不是溶液、
酒精也不是溶液。问题与思考(1)溶剂:能溶解其它物质的物质
(2)溶质:被溶解的物质1、溶液的组成:m溶液 = m溶剂+m溶质 2、质量关系预习展示溶液食盐溶液蔗糖溶液酒精溶液碘酒硫酸铜溶液溶质溶剂氯化钠水蔗糖 水酒精水 碘酒精硫酸铜 水【讨论展示】3、 判断下列溶液中的溶质和溶剂讨论:溶液中溶质和溶剂是如何确定的?气体液体固体液体量少 量多非水物水溶质可以是固体、气体或液体。如果其中有一种是水,一般把水叫溶剂。若两种液体互相溶解时,把量多的叫溶剂,量少的叫溶质。二、探究活动P195 7-4 物质溶解时温度的变化【学生演示】1、取两只小烧杯,分别加入20ml蒸馏水,用温度计测量水温(T1)。
2、向一只小烧杯中加入约3g氢氧化钠固体,搅拌,测量溶液的温度(T2)。
3、向另一只小烧杯中加入约3g硝酸铵固体,搅拌,测量溶液的温度(T2)。
4、向另一只小烧杯中加入约3g氯化钠固体,搅拌,测量溶液的温度(T2) 。
[结论]
氢氧化钠固体溶于水温度 ,硝酸铵固体溶于水温度 ,氯化钠固体溶于水温度 。 升高降低不变[讨论展示] 扩散
过程
(吸热) 水合
过程
(放热)吸热>放热
(溶液温度降低)
例如:NH4NO3固体溶于水吸热 = 放热
(溶液温度不变)
例如:NaCl固体溶于水吸热<放热
(溶液温度升高)
例如:NaOH 固体溶解1、如右图所示,a、b液面是相平的。请向小试管中加入一定量的物质,使右侧U形管中的a面下降、b面上升。则加入的物质是 。A.氢氧化钠固体
B.氯化钠固体
C.硝酸铵晶体 讨论交流A1、下列各组液体中,不属于溶液的是( )
A.汽水 B.冰水混合物
C.食盐水 D.75%的酒精溶液
2、可以作为溶质的( )。
A.只有固体 B. 只有液体
C. 只有气体 D.气体、液体、固体都可以
3、某边远山区,有人发高烧,小明建议可以把硝酸铵、氯化钠、氢氧化钠中的 ,加入盛水的塑料袋中,对病人进行冷敷。 交流与总结
本节课,你学到了哪些新的知识?
