8.4.2 盐的化学性质 复分解反应发生的条件(共30张PPT)
文档属性
| 名称 | 8.4.2 盐的化学性质 复分解反应发生的条件(共30张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 188.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-01 00:00:00 | ||
图片预览








文档简介
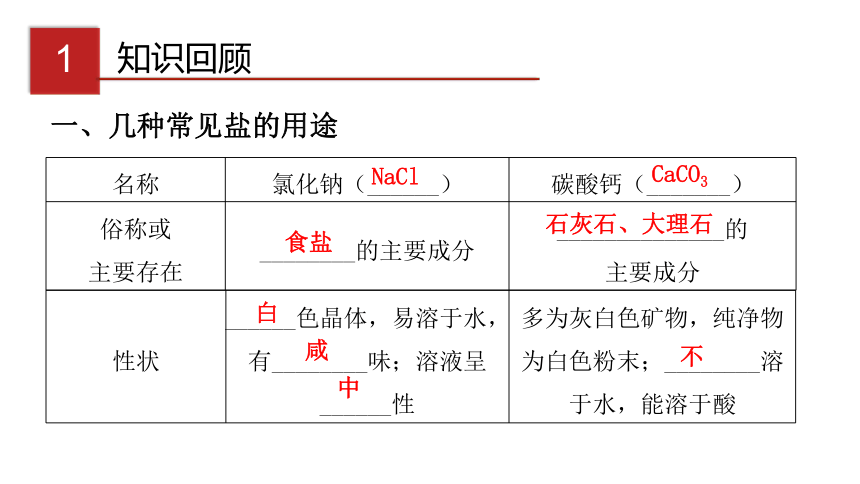
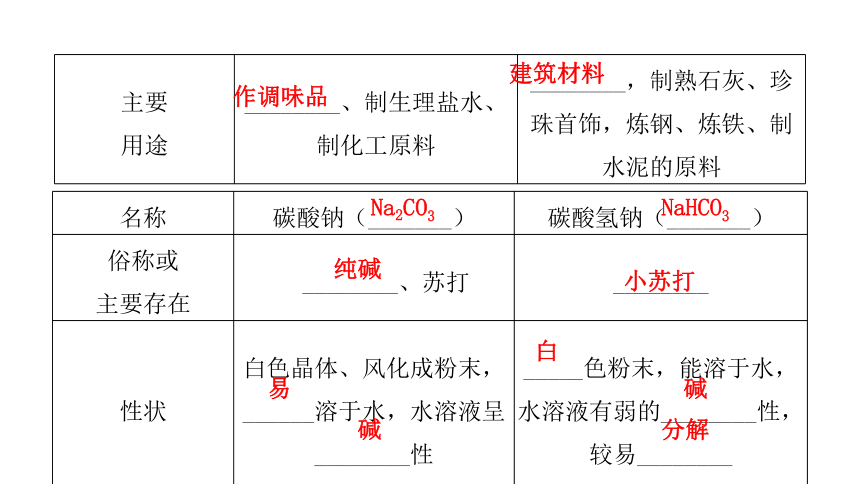
课件30张PPT。科粤版 化学(初中)第八章 第四节常见的盐(第二课时)5典型例题4课堂小结3新课讲授2课堂导入1知识回顾1知识回顾一、几种常见盐的用途CaCO3食盐石灰石、大理石 NaCl白咸中不作调味品建筑材料NaHCO3纯碱 小苏打易碱白碱分解Na2CO3洗涤剂、洗衣粉二、盐的组成和分类1.组成:由__________离子和____离子组成的________。
2.分类
(1)根据阳离子不同,可分为___盐、___盐、___盐等。
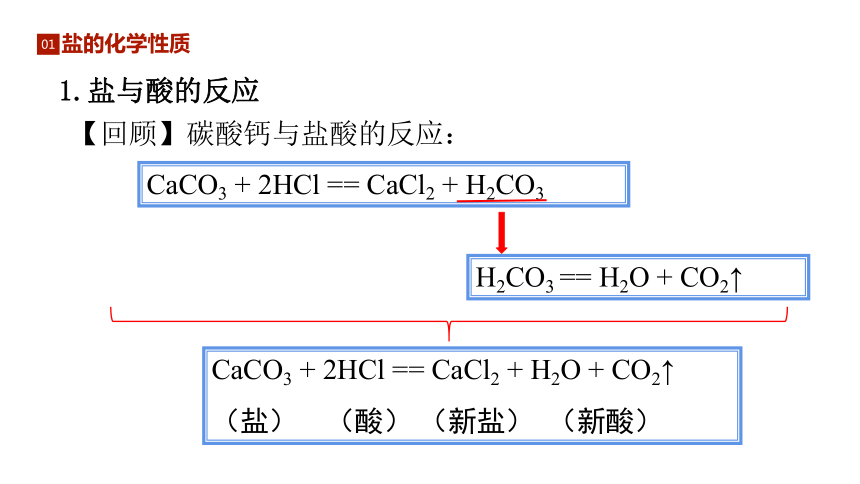
(2)根据阴离子不同,盐可分为___ 盐、___盐、____盐等。金属(或铵根)酸根化合物钠钾镁硫酸碳酸硝酸2课堂导入 通过前面的学习我们知道,盐能与活泼金属发生置换反应,如:Fe + CuSO4 == FeSO4 + Cu 除此之外,盐还能与哪些物质反应呢?我们一起来回顾一下。3新课讲授盐的化学性质01盐的化学性质【回顾】碳酸钙与盐酸的反应:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
(盐) (酸) (新盐) (新酸)CaCO3 + 2HCl == CaCl2 + H2CO3H2CO3 == H2O + CO2↑1.盐与酸的反应【回顾】硝酸银与稀盐酸的反应:据此思考,哪些盐能与稀酸发生类似的反应?碳酸盐与稀酸均可发生类似的反应,如:Na2CO3+2HCl=2NaCl+H2O+CO2↑AgNO3+HCl===AgCl↓+HNO3
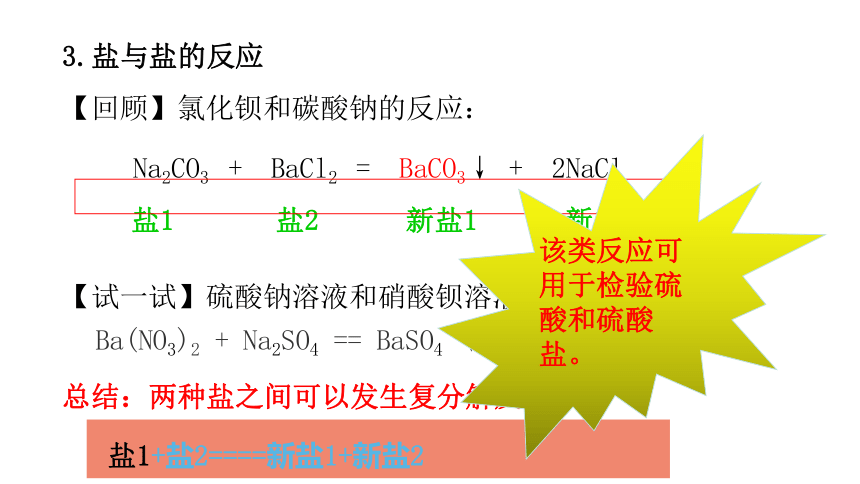
(盐)(酸)(新盐)(新酸)【总结】盐可能与酸发生复分解反应 酸+盐====新酸+新盐 2.盐与碱的反应【回顾】硫酸铜和氯化铁分别与氢氧化钙的反应:CuSO4 +2NaOH == Cu(OH)2↓+ Na2SO4 碱 盐 新碱 新盐 2FeCl3+3Ca(OH)2=2Fe(OH)3↓+3CaCl2总结:碱能与某些盐反应。 碱+盐====新碱+新盐 3.盐与盐的反应【回顾】氯化钡和碳酸钠的反应:Na2CO3 + BaCl2 = BaCO3↓ + 2NaCl盐1 盐2 新盐1 新盐2 【试一试】硫酸钠溶液和硝酸钡溶液的反应:Ba(NO3)2 + Na2SO4 == BaSO4 ↓ + 2NaNO3总结:两种盐之间可以发生复分解反应。 盐1+盐2====新盐1+新盐2 该类反应可用于检验硫酸和硫酸盐。观察活动目的:知道检验硫酸和硫酸盐的方法【实验8-15】取一支试管加入少许硝酸钡溶液,再滴入几滴稀硫酸,观察现象。【实验8-16】在上述有硫酸钡沉淀的试管中,滴加几滴稀硝酸,观察到的现象是________________实验现象:有白色沉淀生成。白色沉淀不溶解。【实验8-17】(1)取一支试管加入少许碳酸钠溶液,再滴入几滴硝酸钡溶液,观察现象。实验现象:有白色沉淀生成。Ba(NO3)2 + Na2CO3 == BaCO3 ↓ + 2NaNO3解释:(2)在上述有碳酸钡沉淀的试管中,滴加几滴稀硝酸,观察到的现象是________________白色沉淀逐渐溶解。总结:硫酸钡沉淀不溶于稀硝酸,碳酸钡沉淀溶于稀硝酸。根据这一特征,可用硝酸钡溶液鉴别硫酸和可溶性硫酸盐。盐的化学性质总结:(可溶)1.盐 + 金属 = 新盐 + 新金属 (置换反应) 2.盐 + 酸 = 新盐 + 新酸 (复分解反应)3.盐 + 碱 = 新盐 + 新碱 (复分解反应) 4.盐 + 盐 = 新盐 + 新盐 (复分解反应) 思考:任意两种盐之间一定能发生复分解反应吗?如:NaCl+kNO3==?无明显现象,因为它们不发生反应。那么复分解反应的发生需要哪些条件呢?02复分解反应发生的条件Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH观察下列反应:2NaOH + MgCl2 = Mg(OH)2↓ + 2NaClBaCl2 + Na2SO4 = BaSO4↓ + 2NaCl有沉淀生成NaOH + NH4Cl = NaCl + NH3↑+ H2O2HCl + CaCO3 = CaCl2 + CO2↑ + H2OH2SO4 + Na2CO3 = Na2SO4 + CO2↑ + H2O 有气体生成HCl + NaOH = NaCl + H2OH2SO4 + Cu(OH)2 = CuSO4 + H2OFe2O3 + 6HCl = 2FeCl3 + 3H2OAl2O3 + 3H2SO4 = 2Al2(SO4)3 + 3H2O有水生成复分解反应发生的条件:生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生,否则就不能发生。总结判断下列反应能否发生,若能发生,尝试写出化学方程式。3H2SO4 + Fe2O3 — NaCl + AgNO3 — NaOH + BaCl2 —Na2CO3 + BaCl2 ————Fe2(SO4)3+3H2ONaCl + H2O×BaSO4↓ + 2NaCl思考:复分解反应为什么能发生呢?我们从微观角度来认识一下复分解反应的实质。 2NaOH + H2SO4 = Na2SO4 + 2H2ONa+SO42-Na+Na+有水生成的复分解反应复分解反应的实质:2HCl + Na2CO3 = 2NaCl + H2O + CO2↑H2CO3有气体生成的复分解反应Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOHCaCO3↓有沉淀生成的复分解反应 Na2SO4 + 2KNO3 ——K2SO4 + 2NaNO3×K2SO4不能发生复分解反应的类型盐的溶解性规律:1、钾、钠、铵、硝酸盐都可溶。
2、盐酸盐只有氯化银不溶。
3、硫酸盐只有硫酸钡不溶。
4、碳酸盐只溶钾、钠、铵,碳酸镁微溶,剩下都不溶。1、酸都溶
2、可溶性溶碱有五位:钾、钠、铵、钙、钡。酸与碱的的溶解性规律:碳酸氢钠可能具有哪些化学性质?1、受热易分解 2、与酸反应NaHCO3+HCl== NaCl + CO2 ↑+ H2O3、溶液显碱性2NaHCO3 == Na2CO3 + CO2 ↑+ H2O△补充:4课堂小结5典型例题考点一:盐的化学性质【典型例题1】(2019?西湖区校级模拟)将某溶液分装在两支试管中,其中一支加入氢氧化钠,另一支加入硝酸钡,结果前者产生红褐色沉淀,后者产生白色沉淀,则原溶液是( )
A.CuCl2 B.Fe2(SO4)3
C.FeCl3 D.Cu (NO3)2B【迁移训练1】(2019?信阳一模)下列各组物质中,能相互反应且反应前后溶液总质量保持不变的是( )
A.氯化钾溶液和硝酸钠溶液
B.铁和硫酸铜溶液
C.稀盐酸和氢氧化钠溶液
D.硫酸和氯化钡溶液C考点二:复分解反应发生的条件【典型例题2】(2019春?石首市校级月考)下列两种物质的溶液混合后,能发生反应,且溶液的总质量不会改变的是( )
A.NaOH溶液和稀盐酸
B.Na2CO3溶液和稀盐酸
C.NaCl溶液和稀硫酸
D.Na2CO3溶液和BaCl2溶液A【迁移训练2】(2019?罗甸县校级一模)下列各组物质中,相互不能发生反应的是( )
A.氢氧化钠溶液与硝酸溶液
B.碳酸氢钠与稀盐酸
C.二氧化硫与氢氧化钙溶液
D.碳酸钡溶液与硫酸钠溶液D
2.分类
(1)根据阳离子不同,可分为___盐、___盐、___盐等。
(2)根据阴离子不同,盐可分为___ 盐、___盐、____盐等。金属(或铵根)酸根化合物钠钾镁硫酸碳酸硝酸2课堂导入 通过前面的学习我们知道,盐能与活泼金属发生置换反应,如:Fe + CuSO4 == FeSO4 + Cu 除此之外,盐还能与哪些物质反应呢?我们一起来回顾一下。3新课讲授盐的化学性质01盐的化学性质【回顾】碳酸钙与盐酸的反应:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
(盐) (酸) (新盐) (新酸)CaCO3 + 2HCl == CaCl2 + H2CO3H2CO3 == H2O + CO2↑1.盐与酸的反应【回顾】硝酸银与稀盐酸的反应:据此思考,哪些盐能与稀酸发生类似的反应?碳酸盐与稀酸均可发生类似的反应,如:Na2CO3+2HCl=2NaCl+H2O+CO2↑AgNO3+HCl===AgCl↓+HNO3
(盐)(酸)(新盐)(新酸)【总结】盐可能与酸发生复分解反应 酸+盐====新酸+新盐 2.盐与碱的反应【回顾】硫酸铜和氯化铁分别与氢氧化钙的反应:CuSO4 +2NaOH == Cu(OH)2↓+ Na2SO4 碱 盐 新碱 新盐 2FeCl3+3Ca(OH)2=2Fe(OH)3↓+3CaCl2总结:碱能与某些盐反应。 碱+盐====新碱+新盐 3.盐与盐的反应【回顾】氯化钡和碳酸钠的反应:Na2CO3 + BaCl2 = BaCO3↓ + 2NaCl盐1 盐2 新盐1 新盐2 【试一试】硫酸钠溶液和硝酸钡溶液的反应:Ba(NO3)2 + Na2SO4 == BaSO4 ↓ + 2NaNO3总结:两种盐之间可以发生复分解反应。 盐1+盐2====新盐1+新盐2 该类反应可用于检验硫酸和硫酸盐。观察活动目的:知道检验硫酸和硫酸盐的方法【实验8-15】取一支试管加入少许硝酸钡溶液,再滴入几滴稀硫酸,观察现象。【实验8-16】在上述有硫酸钡沉淀的试管中,滴加几滴稀硝酸,观察到的现象是________________实验现象:有白色沉淀生成。白色沉淀不溶解。【实验8-17】(1)取一支试管加入少许碳酸钠溶液,再滴入几滴硝酸钡溶液,观察现象。实验现象:有白色沉淀生成。Ba(NO3)2 + Na2CO3 == BaCO3 ↓ + 2NaNO3解释:(2)在上述有碳酸钡沉淀的试管中,滴加几滴稀硝酸,观察到的现象是________________白色沉淀逐渐溶解。总结:硫酸钡沉淀不溶于稀硝酸,碳酸钡沉淀溶于稀硝酸。根据这一特征,可用硝酸钡溶液鉴别硫酸和可溶性硫酸盐。盐的化学性质总结:(可溶)1.盐 + 金属 = 新盐 + 新金属 (置换反应) 2.盐 + 酸 = 新盐 + 新酸 (复分解反应)3.盐 + 碱 = 新盐 + 新碱 (复分解反应) 4.盐 + 盐 = 新盐 + 新盐 (复分解反应) 思考:任意两种盐之间一定能发生复分解反应吗?如:NaCl+kNO3==?无明显现象,因为它们不发生反应。那么复分解反应的发生需要哪些条件呢?02复分解反应发生的条件Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH观察下列反应:2NaOH + MgCl2 = Mg(OH)2↓ + 2NaClBaCl2 + Na2SO4 = BaSO4↓ + 2NaCl有沉淀生成NaOH + NH4Cl = NaCl + NH3↑+ H2O2HCl + CaCO3 = CaCl2 + CO2↑ + H2OH2SO4 + Na2CO3 = Na2SO4 + CO2↑ + H2O 有气体生成HCl + NaOH = NaCl + H2OH2SO4 + Cu(OH)2 = CuSO4 + H2OFe2O3 + 6HCl = 2FeCl3 + 3H2OAl2O3 + 3H2SO4 = 2Al2(SO4)3 + 3H2O有水生成复分解反应发生的条件:生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生,否则就不能发生。总结判断下列反应能否发生,若能发生,尝试写出化学方程式。3H2SO4 + Fe2O3 — NaCl + AgNO3 — NaOH + BaCl2 —Na2CO3 + BaCl2 ————Fe2(SO4)3+3H2ONaCl + H2O×BaSO4↓ + 2NaCl思考:复分解反应为什么能发生呢?我们从微观角度来认识一下复分解反应的实质。 2NaOH + H2SO4 = Na2SO4 + 2H2ONa+SO42-Na+Na+有水生成的复分解反应复分解反应的实质:2HCl + Na2CO3 = 2NaCl + H2O + CO2↑H2CO3有气体生成的复分解反应Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOHCaCO3↓有沉淀生成的复分解反应 Na2SO4 + 2KNO3 ——K2SO4 + 2NaNO3×K2SO4不能发生复分解反应的类型盐的溶解性规律:1、钾、钠、铵、硝酸盐都可溶。
2、盐酸盐只有氯化银不溶。
3、硫酸盐只有硫酸钡不溶。
4、碳酸盐只溶钾、钠、铵,碳酸镁微溶,剩下都不溶。1、酸都溶
2、可溶性溶碱有五位:钾、钠、铵、钙、钡。酸与碱的的溶解性规律:碳酸氢钠可能具有哪些化学性质?1、受热易分解 2、与酸反应NaHCO3+HCl== NaCl + CO2 ↑+ H2O3、溶液显碱性2NaHCO3 == Na2CO3 + CO2 ↑+ H2O△补充:4课堂小结5典型例题考点一:盐的化学性质【典型例题1】(2019?西湖区校级模拟)将某溶液分装在两支试管中,其中一支加入氢氧化钠,另一支加入硝酸钡,结果前者产生红褐色沉淀,后者产生白色沉淀,则原溶液是( )
A.CuCl2 B.Fe2(SO4)3
C.FeCl3 D.Cu (NO3)2B【迁移训练1】(2019?信阳一模)下列各组物质中,能相互反应且反应前后溶液总质量保持不变的是( )
A.氯化钾溶液和硝酸钠溶液
B.铁和硫酸铜溶液
C.稀盐酸和氢氧化钠溶液
D.硫酸和氯化钡溶液C考点二:复分解反应发生的条件【典型例题2】(2019春?石首市校级月考)下列两种物质的溶液混合后,能发生反应,且溶液的总质量不会改变的是( )
A.NaOH溶液和稀盐酸
B.Na2CO3溶液和稀盐酸
C.NaCl溶液和稀硫酸
D.Na2CO3溶液和BaCl2溶液A【迁移训练2】(2019?罗甸县校级一模)下列各组物质中,相互不能发生反应的是( )
A.氢氧化钠溶液与硝酸溶液
B.碳酸氢钠与稀盐酸
C.二氧化硫与氢氧化钙溶液
D.碳酸钡溶液与硫酸钠溶液D
