科粤版九年级化学(下)课件:7.3--溶液浓稀的表示共23张PPT
文档属性
| 名称 | 科粤版九年级化学(下)课件:7.3--溶液浓稀的表示共23张PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 440.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-01 00:00:00 | ||
图片预览





文档简介
课件23张PPT。7.3溶液浓稀的表示教学目标:
1.掌握溶液浓稀的一种定量表示方式—溶质的质量分数。
2.能进行关于溶质质量分数的简单计算。
3.理解溶解度与溶质质量分数的区别与联系。
教学重点:
溶质质量分数的概念及计算
教学难点:
溶解度与溶质质量分数的区别与联系。 你知道溶液由哪几部分组成的吗?它们之间的质量有什么关系? 溶质
溶剂让你的记忆重现:溶液质量 = 溶质质量 + 溶剂质量
溶质质量 =溶液质量 ―溶剂质量
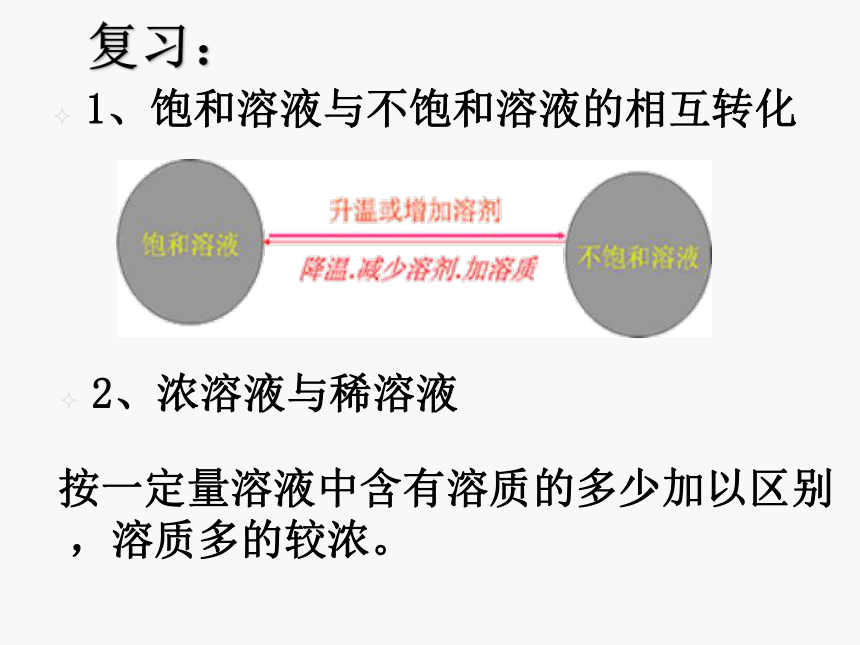
溶剂质量=溶液质量 ―溶质质量 溶液1、饱和溶液与不饱和溶液的相互转化2、浓溶液与稀溶液复习: 按一定量溶液中含有溶质的多少加以区别,溶质多的较浓。
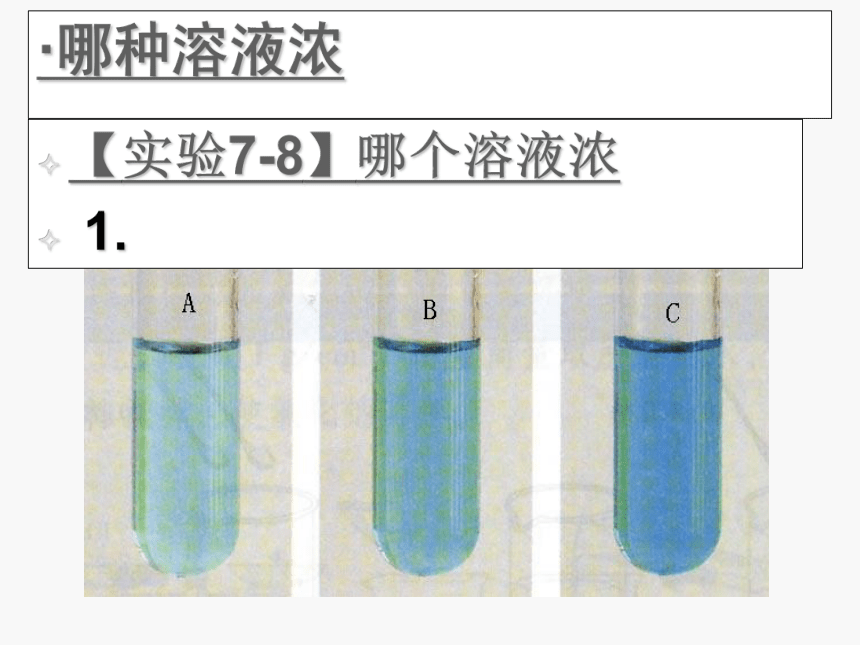
·哪种溶液浓【实验7-8】哪个溶液浓
1.【实验7-8】哪个溶液浓
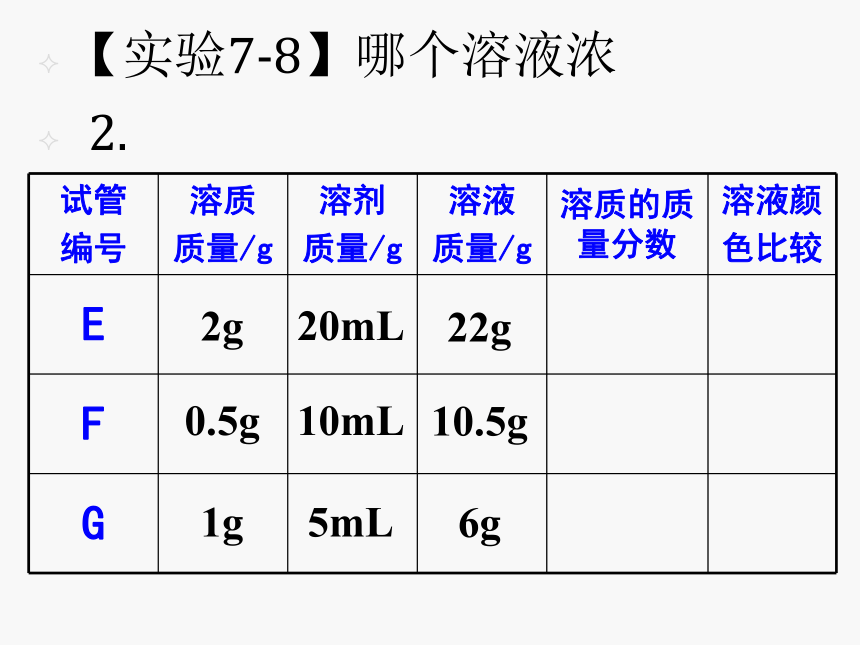
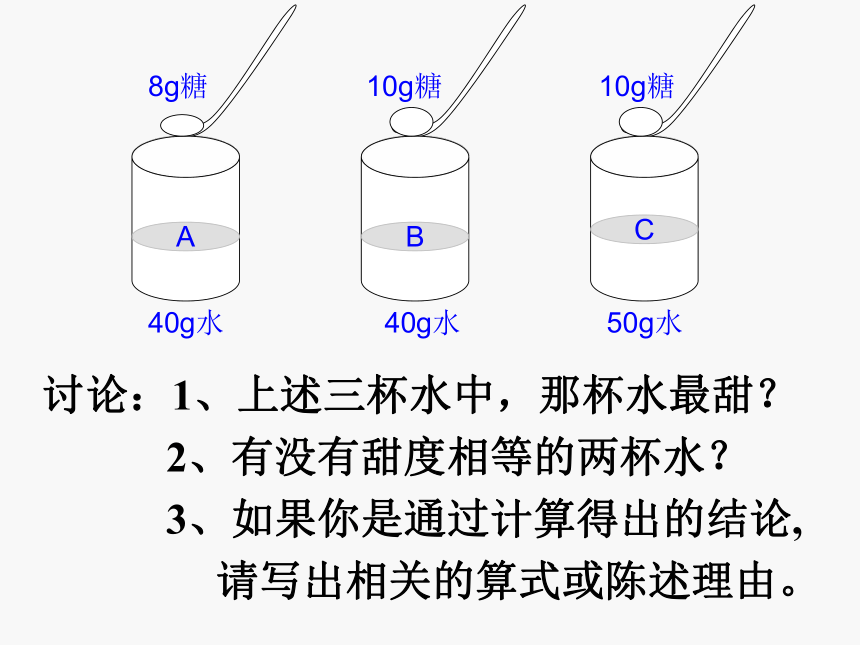
2.2g0.5g1g20mL10mL5mL22g10.5g6g讨论:1、上述三杯水中,那杯水最甜?
2、有没有甜度相等的两杯水?
3、如果你是通过计算得出的结论,
请写出相关的算式或陈述理由。一、溶质的质量分数2、计算公式1、概念溶液中溶质的质量分数是
溶质质量与溶液质量之比%100×+溶剂溶质溶质1. 现有一瓶氯化钠溶液它的质量分数为5%,则5%的含义是什么?讨 论溶质是( )份
溶剂是( )份
溶液是( )份510095算一算:上述实验配制的溶液中氯化钠的质量分数是多少?例题1:把5克食盐溶解在100克水中,所得溶液中溶质的质量分数为多少?解:溶质的质量分数==4.76%练习1:
从一瓶氯化钾溶液中取出20克溶液,蒸干后得到2.8克氯化钾固体。试确定这瓶溶液中溶质的质量分数。答:这瓶溶液中氯化钾的质量分数为14%。解:溶质氯化钾的质量分数=溶质质量分数公式变形计算M液=M质+M剂
(1)M质=M液×w%
M质=M液―M剂%100%×wM质例2:在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少? 解: M质=M液×w%
=150kg×16%
=24kg
M剂=M液-M质
=150kg-24kg
=126kg
答:配制150kg这种溶液,需要24kg氯化钠和126kg水。我来计算:
配制200g溶质的质量分数为5%的硫酸铜溶液,需要硫酸铜和水的质量各是多少?解: M质=M液×w%
=200g ×5% =10gM剂=M液-M质
=200g-10g
=190g
答:需要硫酸铜的质量为10g,水的质量190g。 医疗上的生理盐水是溶质质量分数约为0.9%的氯化钠溶液,现用1000g生理盐水给某病人输液,则有 克氯化钠
和 克水进入病人体内。 你有办法解决下列问题吗?9991走进生活:在餐桌上,当我们发现某种汤太咸时,通常做法是向汤中加 。在这个过程中一定改变的是( )
一定不变的是( )
(1)水的质量 (2)汤的质量
(3)盐的质量 (4)盐的质量分数 水(1)(2)(4)(3)知识拓展: 现有一瓶100g10%的NaOH溶液:
(1)若向其中加入100克水,它的质量分数变为多少?
(2)若向其中加入10克的氢氧化钠固体,其质量分数又变为多少?[讨论与交流] P196 溶解度与溶质质量分数的区别与联系物质溶解性的量度,受温度影响表示溶液中溶质质量的多少,不受外界条件影响100g 无要求达到饱和不一定克(g)无单位 例:20℃时KNO3的溶解度为31.6g,将20g KNO3投入50g水中,充分搅拌,制成20℃时溶液,求该溶液中溶质的质量分数?解:20℃时KNO3的溶解度为31.6g。50g水中最多溶解KNO315.8g。或答:溶液中溶质的质量分数为24%。三、有关化学方程式的溶液计算在有溶液中反应时根据的化学方程式的计算,要从以下两个方面考虑:
(1)在化学方程式中的有关反应物、生成物的质量,是指溶质的质量,而不是溶液的质量或体积。
(2)对于反应后所得溶液的质量的求法:
溶液质量 = 反应物质量总和―生成气体质量―生成沉淀质量解:设生成的氢气质量为ⅹ,所用硫酸的质量为У,
生成的硫酸锌的质量为Ζ245g2452451、32.5g锌粒可以跟200g硫酸溶液恰好完全反应。计算:(1)可制得氢气多少克?(2)这种硫酸溶液中溶质的质量分数是多少?(3)100g这种硫酸溶液自然科学稀释成20%的硫酸溶液,需要加水多少g?2、13g锌与100g稀硫酸恰好完全反应。求:(1)生成的氢气在标准状况下体积为多少升?(标准状况下氢气的密度为0.09g/L)(2)稀硫酸的溶质的质量分数是多少?(3)求反应后生成的溶液中溶质的质量分数是多少?
1.掌握溶液浓稀的一种定量表示方式—溶质的质量分数。
2.能进行关于溶质质量分数的简单计算。
3.理解溶解度与溶质质量分数的区别与联系。
教学重点:
溶质质量分数的概念及计算
教学难点:
溶解度与溶质质量分数的区别与联系。 你知道溶液由哪几部分组成的吗?它们之间的质量有什么关系? 溶质
溶剂让你的记忆重现:溶液质量 = 溶质质量 + 溶剂质量
溶质质量 =溶液质量 ―溶剂质量
溶剂质量=溶液质量 ―溶质质量 溶液1、饱和溶液与不饱和溶液的相互转化2、浓溶液与稀溶液复习: 按一定量溶液中含有溶质的多少加以区别,溶质多的较浓。
·哪种溶液浓【实验7-8】哪个溶液浓
1.【实验7-8】哪个溶液浓
2.2g0.5g1g20mL10mL5mL22g10.5g6g讨论:1、上述三杯水中,那杯水最甜?
2、有没有甜度相等的两杯水?
3、如果你是通过计算得出的结论,
请写出相关的算式或陈述理由。一、溶质的质量分数2、计算公式1、概念溶液中溶质的质量分数是
溶质质量与溶液质量之比%100×+溶剂溶质溶质1. 现有一瓶氯化钠溶液它的质量分数为5%,则5%的含义是什么?讨 论溶质是( )份
溶剂是( )份
溶液是( )份510095算一算:上述实验配制的溶液中氯化钠的质量分数是多少?例题1:把5克食盐溶解在100克水中,所得溶液中溶质的质量分数为多少?解:溶质的质量分数==4.76%练习1:
从一瓶氯化钾溶液中取出20克溶液,蒸干后得到2.8克氯化钾固体。试确定这瓶溶液中溶质的质量分数。答:这瓶溶液中氯化钾的质量分数为14%。解:溶质氯化钾的质量分数=溶质质量分数公式变形计算M液=M质+M剂
(1)M质=M液×w%
M质=M液―M剂%100%×wM质例2:在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少? 解: M质=M液×w%
=150kg×16%
=24kg
M剂=M液-M质
=150kg-24kg
=126kg
答:配制150kg这种溶液,需要24kg氯化钠和126kg水。我来计算:
配制200g溶质的质量分数为5%的硫酸铜溶液,需要硫酸铜和水的质量各是多少?解: M质=M液×w%
=200g ×5% =10gM剂=M液-M质
=200g-10g
=190g
答:需要硫酸铜的质量为10g,水的质量190g。 医疗上的生理盐水是溶质质量分数约为0.9%的氯化钠溶液,现用1000g生理盐水给某病人输液,则有 克氯化钠
和 克水进入病人体内。 你有办法解决下列问题吗?9991走进生活:在餐桌上,当我们发现某种汤太咸时,通常做法是向汤中加 。在这个过程中一定改变的是( )
一定不变的是( )
(1)水的质量 (2)汤的质量
(3)盐的质量 (4)盐的质量分数 水(1)(2)(4)(3)知识拓展: 现有一瓶100g10%的NaOH溶液:
(1)若向其中加入100克水,它的质量分数变为多少?
(2)若向其中加入10克的氢氧化钠固体,其质量分数又变为多少?[讨论与交流] P196 溶解度与溶质质量分数的区别与联系物质溶解性的量度,受温度影响表示溶液中溶质质量的多少,不受外界条件影响100g 无要求达到饱和不一定克(g)无单位 例:20℃时KNO3的溶解度为31.6g,将20g KNO3投入50g水中,充分搅拌,制成20℃时溶液,求该溶液中溶质的质量分数?解:20℃时KNO3的溶解度为31.6g。50g水中最多溶解KNO315.8g。或答:溶液中溶质的质量分数为24%。三、有关化学方程式的溶液计算在有溶液中反应时根据的化学方程式的计算,要从以下两个方面考虑:
(1)在化学方程式中的有关反应物、生成物的质量,是指溶质的质量,而不是溶液的质量或体积。
(2)对于反应后所得溶液的质量的求法:
溶液质量 = 反应物质量总和―生成气体质量―生成沉淀质量解:设生成的氢气质量为ⅹ,所用硫酸的质量为У,
生成的硫酸锌的质量为Ζ245g2452451、32.5g锌粒可以跟200g硫酸溶液恰好完全反应。计算:(1)可制得氢气多少克?(2)这种硫酸溶液中溶质的质量分数是多少?(3)100g这种硫酸溶液自然科学稀释成20%的硫酸溶液,需要加水多少g?2、13g锌与100g稀硫酸恰好完全反应。求:(1)生成的氢气在标准状况下体积为多少升?(标准状况下氢气的密度为0.09g/L)(2)稀硫酸的溶质的质量分数是多少?(3)求反应后生成的溶液中溶质的质量分数是多少?
