7.3.1 溶质的质量分数及其简单计算共33张PPT
文档属性
| 名称 | 7.3.1 溶质的质量分数及其简单计算共33张PPT |

|
|
| 格式 | zip | ||
| 文件大小 | 323.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-01 00:00:00 | ||
图片预览











文档简介
课件33张PPT。第七章 第三节科粤版 化学(初中)溶液浓稀的表示(第一课时)5典型例题4课堂小结3新课讲授2课堂导入1知识回顾1知识回顾1.固体物质的溶解度是指在一定温度下,某固体物质在100g溶剂(通常为水)里达到饱和状态时所溶解的质量。一、固体溶解度2.溶解度四要素一定温度100克溶剂(一般指水)饱和状态质量(克)3.溶解度与溶解性的关系104.溶解度曲线用纵坐标表示溶解度,横坐标表示温度,根据某物质在不同温度时的溶解度,可以画出该物质的溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。S (g)t(℃)S1MABt1二、气体溶解度1.定义:在压强为101KPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。2.气体溶解度的五要素:
(1)压强为101kPa (2)一定温度 (3)1体积水 (4)达到饱和 (5)气体的体积3.气体溶解度的影响因素:
(1)压强。压强大,溶解气体多。
(2)温度。温度高,溶解少2课堂导入生理盐水对大家来说并不陌生,它是不是溶液?你知道标签上的这个0.9%是什么意思吗?是,氯化钠溶液。3新课讲授 生理盐水标签上的这个0.9%是指的氯化钠溶液的浓度,它能准确地反应氯化钠溶液是浓还是稀。
那么溶液的浓度指的是什么?它应该如何计算呢?
01溶液的浓度观察活动知道有色溶液颜色的深浅与溶液浓稀有关【实验7-7】
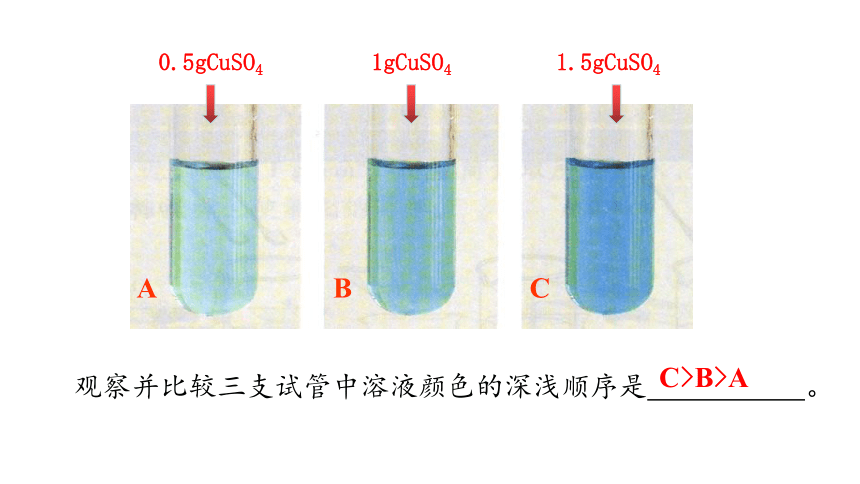
1.在三支试管A、B、C中分别加入10ml水,再分别加入0.5g、1g和1.5g硫酸铜溶液,试猜测三支试管中溶液颜色的深浅顺序是 。C>B>AABC0.5gCuSO41gCuSO41.5gCuSO4观察并比较三支试管中溶液颜色的深浅顺序是 。C>B>A2.在三支试管D、E、F中分别加入20ml、10ml、5ml水,再分别加入2g、0.5g、1g硫酸铜溶液,试猜测三支试管中溶液颜色的深浅顺序是 ;你的依据是 。观察并比较三支试管中溶液颜色的深浅顺序是 。F>D>EF>D>E 对于上述三支试管中溶液的浓稀程度除了用比较溶液颜色深浅之外,还有没有其它方法?溶质与溶剂的质量比溶质的质量分数1.定义:溶质的质量与溶液的质量之比。(通常以百分数表示) 2.计算公式9.1%4.8%16.7%比较深较浅最深1g10mL5mL10.5g6g2g0.5g20mL22g对于上述实验来说,如果用溶质质量分数来表示浓度:结论:溶质的质量分数越大,有色溶液的颜色越深。 1905%4%2412610020%4小试牛刀质量分数与溶解度的区别与联系:在一定的温度下不受外界条件的影响100g无要求一定达到饱和不一定克(g)是一个比值,单位为1有关溶解度与溶质质量分数的相互转化:例1.在20oC时,CuSO4的溶解度为25g,求20oC时CuSO4饱和溶液溶质的质量分数。溶质的质量分数==20%=解:答:20oC时溶解度为25g的CuSO4饱和溶液溶质的质量分数为20%。02有关溶质质量分数的简单计算1.配制一定量的某一组成的溶液,求所需溶质和溶剂的量例2.在农业生产中,常需要用质量分数为15%的氯化钠溶液来选种。现要配制80kg这种溶液,需要氯化钠和水的质量各是多少?解:答;需要12 Kg氯化钠,68 Kg的水小试牛刀配制500 ml质量分数为10%的氢氧化钠溶液(密度为1.1g/ml),需要氢氧化钠和水各多少克?
解:需要溶质的质量为:
500 ml×1.1g/ml×10%=55 g
需要溶质的质量为:
500 ml×1.1g/ml-55 g=495 g
答:需要溶质的质量为55g,需要溶质的质量为495g。2.有关溶液稀释的计算计算依据:稀释前后________的质量不变。溶质例3.配制铅蓄电池用的28%硫酸溶液460g,问需要98%的浓硫酸的体积是多少?已知98%浓硫酸的密度为1.84g/cm3解:设需要98%的浓硫酸的质量为X。
460g × 28%= X × 98%
X=
=131.4g
则需要98%的浓硫酸的体积为:
=71.4cm3
答:需要98%浓硫酸的体积是71.4cm3460g × 28%98%131.4g1.84g/cm3 有一种过氧乙酸消毒液,广泛用于室内外进行消毒。现要配制10kg0.4%的过氧乙酸消毒液,请计算需用含过氧乙酸40%的市售原液的质量是多少?所需稀释用水的质量为多少?小试牛刀解:设需要含过氧乙酸40%的市售原液质量为X
10kg × 0.4%= X × 40%
X= 0.1kg
则所需稀释用水的质量为:
10kg -0.1kg =9.9kg
答:需要含过氧乙酸40%的市售原液质量为0.1kg,所需稀释用水质量为9.9kg。
注意:溶液是混合物,溶液的质量不能直接代入化学方程式中计算,必须换算成溶质的质量。例题4.试求100g 9.8%硫酸可以跟多少克锌恰好完全反应?同时生成多少克氢气?3.有关化学方程式的计算 解:100g9.8%硫酸中含纯硫酸的质量为:100g?9.8%=9.8g设参加反应的锌质量为X ,生成氢气的质量为YZn + H2SO4 = ZnSO4 + H2?65 98 2X 9.8g YX=6.5g Y=0.2g答:参加反应的锌质量为6.5g,生成氢气的质量为0.2g4课堂小结溶质的质量分数及其简单计算溶液浓稀的表示颜色的深浅粗略地表示有色溶液的浓度大小= 溶质质量分数的简单计算1.根据公式的计算
2.溶液稀释问题的计算(依据:稀释前后溶质的质量不变)
3.与化学方程式结合的计算溶质的质量分数及其简单计算5典型例题考点一:溶质质量分数【典型例题1】常温下,把20 g氯化钠放在100 g水中,搅拌后氯化钠全部溶解。溶液中氯化钠的质量分数为( )
A.16.7% B.20%
C.25% D.18.5%A【迁移训练1】下列对20%的氯化钠溶液的理解正确的是( )
A.该溶液中溶质与溶剂的质量比为1∶5
B.100 g该溶液中含溶质20 g
C.该溶液100 g水中溶有溶质20 g
D.该溶液中溶剂和溶液的质量比为1∶5B考点二:溶质质量分数的有关计算【典型例题2】(2019秋?宁明县期中)将100g质量分数为25%的硝酸钾溶液,若使其质量分数增大一倍。
(1)则应该加入硝酸钾多少克?
(2)若蒸发水浓缩,则应该蒸发水多少克?(要求:设未知数作答) X=50g;
答:应该加入硝酸钾50g。
(2)设应该蒸发水的质量为y解:(1)设应该加入硝酸钾的质量为xy=50g,
答:应该蒸发水的质量为50g【迁移训练2】现有5.6 g铁与100 g某稀硫酸恰好完全反应,请通过计算填空。
(1)100 g稀硫酸中,溶质的质量为______,其溶质的质量分数为________。
(2)反应后溶液中溶质是____________,其质量为____________,溶液质量为__________,反应后溶液中溶质的质量分数为____________。9.8 g9.8%FeSO415.2 g105.4 g14.4%考点三:溶质质量分数与溶解度的综合问题【典型例题3】某温度时,KNO3饱和溶液中溶质的质量分数为20%,则该温度时KNO3的溶解度为( )
A.20 g B.25 g
C.30 g D.40 gB【迁移训练3】如图10-1是甲、乙两物质的溶解度曲线。下列说法中不正确的是( )
A.t1 ℃时,乙的溶解度大于甲的溶解度
B.t2 ℃时,甲、乙饱和溶液中溶质的质量分数相等
C.降低温度能使接近饱和的甲溶液变为饱和溶液
D.t3 ℃时,75 g甲的饱和溶液中加入50 g水,可以得到质量分数为25%的溶液D
(1)压强为101kPa (2)一定温度 (3)1体积水 (4)达到饱和 (5)气体的体积3.气体溶解度的影响因素:
(1)压强。压强大,溶解气体多。
(2)温度。温度高,溶解少2课堂导入生理盐水对大家来说并不陌生,它是不是溶液?你知道标签上的这个0.9%是什么意思吗?是,氯化钠溶液。3新课讲授 生理盐水标签上的这个0.9%是指的氯化钠溶液的浓度,它能准确地反应氯化钠溶液是浓还是稀。
那么溶液的浓度指的是什么?它应该如何计算呢?
01溶液的浓度观察活动知道有色溶液颜色的深浅与溶液浓稀有关【实验7-7】
1.在三支试管A、B、C中分别加入10ml水,再分别加入0.5g、1g和1.5g硫酸铜溶液,试猜测三支试管中溶液颜色的深浅顺序是 。C>B>AABC0.5gCuSO41gCuSO41.5gCuSO4观察并比较三支试管中溶液颜色的深浅顺序是 。C>B>A2.在三支试管D、E、F中分别加入20ml、10ml、5ml水,再分别加入2g、0.5g、1g硫酸铜溶液,试猜测三支试管中溶液颜色的深浅顺序是 ;你的依据是 。观察并比较三支试管中溶液颜色的深浅顺序是 。F>D>EF>D>E 对于上述三支试管中溶液的浓稀程度除了用比较溶液颜色深浅之外,还有没有其它方法?溶质与溶剂的质量比溶质的质量分数1.定义:溶质的质量与溶液的质量之比。(通常以百分数表示) 2.计算公式9.1%4.8%16.7%比较深较浅最深1g10mL5mL10.5g6g2g0.5g20mL22g对于上述实验来说,如果用溶质质量分数来表示浓度:结论:溶质的质量分数越大,有色溶液的颜色越深。 1905%4%2412610020%4小试牛刀质量分数与溶解度的区别与联系:在一定的温度下不受外界条件的影响100g无要求一定达到饱和不一定克(g)是一个比值,单位为1有关溶解度与溶质质量分数的相互转化:例1.在20oC时,CuSO4的溶解度为25g,求20oC时CuSO4饱和溶液溶质的质量分数。溶质的质量分数==20%=解:答:20oC时溶解度为25g的CuSO4饱和溶液溶质的质量分数为20%。02有关溶质质量分数的简单计算1.配制一定量的某一组成的溶液,求所需溶质和溶剂的量例2.在农业生产中,常需要用质量分数为15%的氯化钠溶液来选种。现要配制80kg这种溶液,需要氯化钠和水的质量各是多少?解:答;需要12 Kg氯化钠,68 Kg的水小试牛刀配制500 ml质量分数为10%的氢氧化钠溶液(密度为1.1g/ml),需要氢氧化钠和水各多少克?
解:需要溶质的质量为:
500 ml×1.1g/ml×10%=55 g
需要溶质的质量为:
500 ml×1.1g/ml-55 g=495 g
答:需要溶质的质量为55g,需要溶质的质量为495g。2.有关溶液稀释的计算计算依据:稀释前后________的质量不变。溶质例3.配制铅蓄电池用的28%硫酸溶液460g,问需要98%的浓硫酸的体积是多少?已知98%浓硫酸的密度为1.84g/cm3解:设需要98%的浓硫酸的质量为X。
460g × 28%= X × 98%
X=
=131.4g
则需要98%的浓硫酸的体积为:
=71.4cm3
答:需要98%浓硫酸的体积是71.4cm3460g × 28%98%131.4g1.84g/cm3 有一种过氧乙酸消毒液,广泛用于室内外进行消毒。现要配制10kg0.4%的过氧乙酸消毒液,请计算需用含过氧乙酸40%的市售原液的质量是多少?所需稀释用水的质量为多少?小试牛刀解:设需要含过氧乙酸40%的市售原液质量为X
10kg × 0.4%= X × 40%
X= 0.1kg
则所需稀释用水的质量为:
10kg -0.1kg =9.9kg
答:需要含过氧乙酸40%的市售原液质量为0.1kg,所需稀释用水质量为9.9kg。
注意:溶液是混合物,溶液的质量不能直接代入化学方程式中计算,必须换算成溶质的质量。例题4.试求100g 9.8%硫酸可以跟多少克锌恰好完全反应?同时生成多少克氢气?3.有关化学方程式的计算 解:100g9.8%硫酸中含纯硫酸的质量为:100g?9.8%=9.8g设参加反应的锌质量为X ,生成氢气的质量为YZn + H2SO4 = ZnSO4 + H2?65 98 2X 9.8g YX=6.5g Y=0.2g答:参加反应的锌质量为6.5g,生成氢气的质量为0.2g4课堂小结溶质的质量分数及其简单计算溶液浓稀的表示颜色的深浅粗略地表示有色溶液的浓度大小= 溶质质量分数的简单计算1.根据公式的计算
2.溶液稀释问题的计算(依据:稀释前后溶质的质量不变)
3.与化学方程式结合的计算溶质的质量分数及其简单计算5典型例题考点一:溶质质量分数【典型例题1】常温下,把20 g氯化钠放在100 g水中,搅拌后氯化钠全部溶解。溶液中氯化钠的质量分数为( )
A.16.7% B.20%
C.25% D.18.5%A【迁移训练1】下列对20%的氯化钠溶液的理解正确的是( )
A.该溶液中溶质与溶剂的质量比为1∶5
B.100 g该溶液中含溶质20 g
C.该溶液100 g水中溶有溶质20 g
D.该溶液中溶剂和溶液的质量比为1∶5B考点二:溶质质量分数的有关计算【典型例题2】(2019秋?宁明县期中)将100g质量分数为25%的硝酸钾溶液,若使其质量分数增大一倍。
(1)则应该加入硝酸钾多少克?
(2)若蒸发水浓缩,则应该蒸发水多少克?(要求:设未知数作答) X=50g;
答:应该加入硝酸钾50g。
(2)设应该蒸发水的质量为y解:(1)设应该加入硝酸钾的质量为xy=50g,
答:应该蒸发水的质量为50g【迁移训练2】现有5.6 g铁与100 g某稀硫酸恰好完全反应,请通过计算填空。
(1)100 g稀硫酸中,溶质的质量为______,其溶质的质量分数为________。
(2)反应后溶液中溶质是____________,其质量为____________,溶液质量为__________,反应后溶液中溶质的质量分数为____________。9.8 g9.8%FeSO415.2 g105.4 g14.4%考点三:溶质质量分数与溶解度的综合问题【典型例题3】某温度时,KNO3饱和溶液中溶质的质量分数为20%,则该温度时KNO3的溶解度为( )
A.20 g B.25 g
C.30 g D.40 gB【迁移训练3】如图10-1是甲、乙两物质的溶解度曲线。下列说法中不正确的是( )
A.t1 ℃时,乙的溶解度大于甲的溶解度
B.t2 ℃时,甲、乙饱和溶液中溶质的质量分数相等
C.降低温度能使接近饱和的甲溶液变为饱和溶液
D.t3 ℃时,75 g甲的饱和溶液中加入50 g水,可以得到质量分数为25%的溶液D
