人教版高中化学选修5教学讲义,复习补习资料(含知识讲解,巩固练习):11【提高】醇
文档属性
| 名称 | 人教版高中化学选修5教学讲义,复习补习资料(含知识讲解,巩固练习):11【提高】醇 |

|
|
| 格式 | zip | ||
| 文件大小 | 565.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-31 00:00:00 | ||
图片预览



文档简介
醇
【学习目标】
1、了解醇类的结构特点、一般特性和用途;
2、掌握乙醇的化学性质。
【典型例题】
类型一:醇的结构和性质
例1 乙醇分子结构中各种化学键如右图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )。
A.和金属钠反应时①键断裂
B.和浓硫酸共热到170℃时键②和⑤断裂
C.和浓硫酸共热到140℃时仅有键②断裂
D.在铜催化下与O2反应时键①和③断裂
【思路点拨】本题全面考查乙醇的化学性质,从断键情况考查乙醇在发生化学反应时的机理注意区分乙醇与浓硫酸共热时取代成醚及消去成烯的断键特点。
【答案】C
【解析】选项A乙醇与钠反应生成乙醇钠和氢气,是乙醇羟基中的O—H键①断裂;选项B乙醇与浓硫酸共热到170℃时发生消去反应生成乙烯和水,是键②和⑤断裂;选项C是乙醇发生分子间脱水反应生成乙醚,一分子断裂键①,另一分子断裂键②;选项D是乙醇催化氧化为乙醛,断裂的键是①和③。
【总结升华】醇类断裂C—O键,脱掉—OH时,可发生取代或消去反应;若同时断裂C—O键和H—O键时,可发生消去或氧化反应,要注意分析体会。
举一反三:
【变式1】(2019 新建县模拟)酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧衍生物 ⑤乙醇有刺激性气体
A.②④⑤ B.②③ C.①③ D.①④
【答案】C
【解析】①乙醇沸点低,易挥发,若饮酒,呼出的气体中含有酒精,与测定原理有关;②乙醇密度比水小,可与水以任意比混溶,与测定原理无关;③乙醇分子中含有羟基,具有还原性,K2Cr2O7具有强氧化性,可以把乙醇迅速氧化为乙酸而变成蓝绿色的Cr3+,与测定原理有关;④乙醇可看成是乙烷中的氢原子被羟基取代后的产物,是烃的含氧化合物,与测定原理无关;⑤乙醇有刺激性气体,与测定原理无关,故对乙醇的描述与此测定原理有关的是①③,故选C。
例2关于乙醇的说法中正确的是( )
A.乙醇结构中有-OH,所以乙醇溶解于水,可以电离出OH-而显碱性
B.乙醇燃烧生成二氧化碳和水,说明乙醇具有氧化性
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
【思路点拨】本题注重对乙醇基础知识的考查,难度不大,仔细分析各个选项即可得出正确答案。
【答案】D
【解析】A项乙醇结构中有-OH,能与水形成氢键,所以乙醇溶解于水,但不能电离出OH-,故A错误;B项乙醇燃烧生成二氧化碳和水,乙醇作燃料,是还原剂,具有还原性,故B错误;C项乙醇与钠反应可以产生氢气,但乙醇不能电离出氢离子,不显酸性,故C错误;D项水是弱电解质,乙醇是非电解质,乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼,故D正确。
【总结升华】醇的性质微点拨:(1)含有相同碳原子数的醇中,所含羟基数目越多,沸点越高。
(2)醇类和卤代烃都能发生消去反应,但条件不同。醇消去反应的条件是浓硫酸、加热;卤代烃消去反应的条件是氢氧化钠醇溶液、加热。
(3)某一元醇发生消去反应生成的烯烃不一定只有一种,要看连羟基的碳原子的邻位碳原子上不同化学环境下氢原子的种数。
举一反三:
【变式1】二甘醇可用作溶剂、纺织助剂等。一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式是HO—CH2CH2—O—CH2CH2—OH。下列有关二甘醇的叙述正确的是( )。
A.不能发生消去反应 B.能发生取代反应
C.能溶于水,不溶于乙醇 D.符合分子通式CnH2nO3
【答案】B
【变式2】下列物质能发生消去反应生成相应的烯烃,但不能氧化生成相应醛的是( )
A.CH3OH B.CH3CH2CH2OH C./ D./
【答案】D
【解析】与羟基相连的碳原子上有两个或三个氢原子(即含有-CH2OH)时才能被氧化为醛、与羟基相连的碳原子的邻位碳原子上至少有一个氢原子时才能发生消去反应。
类型二:醇的命名
例3 对某一醇类作系统命名,其中正确的是( )。
A.1,1-二甲基-3-丙醇 B.2-甲基-4-戊醇
C.3-甲基-2-丁醇 D.3,3-二甲基-1-丁醇
【思路点拨】本题考查醇的命名。注意主链的选择、官能团的位置及标识。
【答案】C、D
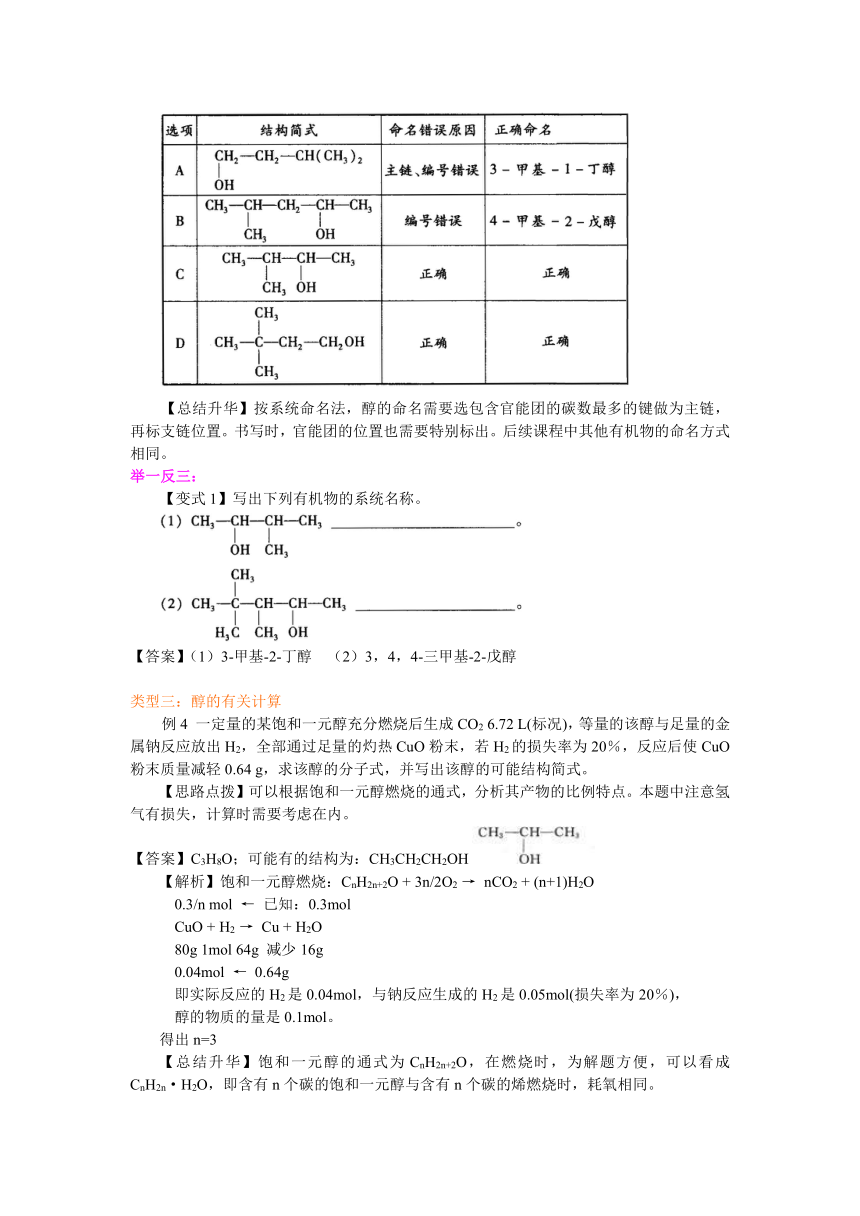
【解析】先根据题给各选项的名称写出醇的结构简式,再由醇的系统命名法分析其正误。
/
【总结升华】按系统命名法,醇的命名需要选包含官能团的碳数最多的键做为主链,再标支链位置。书写时,官能团的位置也需要特别标出。后续课程中其他有机物的命名方式相同。
举一反三:
【变式1】写出下列有机物的系统名称。
/
【答案】(1)3-甲基-2-丁醇 (2)3,4,4-三甲基-2-戊醇
类型三:醇的有关计算
例4 一定量的某饱和一元醇充分燃烧后生成CO2?6.72 L(标况),等量的该醇与足量的金属钠反应放出H2,全部通过足量的灼热CuO粉末,若H2的损失率为20%,反应后使CuO粉末质量减轻0.64 g,求该醇的分子式,并写出该醇的可能结构简式。
【思路点拨】可以根据饱和一元醇燃烧的通式,分析其产物的比例特点。本题中注意氢气有损失,计算时需要考虑在内。
【答案】C3H8O;可能有的结构为:CH3CH2CH2OH?/
【解析】饱和一元醇燃烧:CnH2n+2O + 3n/2O2?→ nCO2?+ (n+1)H2O
0.3/n mol ← 已知:0.3mol
CuO + H2?→ Cu + H2O
80g 1mol 64g 减少16g
0.04mol ← 0.64g
即实际反应的H2是0.04mol,与钠反应生成的H2是0.05mol(损失率为20%),
醇的物质的量是0.1mol。
得出n=3
【总结升华】饱和一元醇的通式为CnH2n+2O,在燃烧时,为解题方便,可以看成CnH2n·H2O,即含有n个碳的饱和一元醇与含有n个碳的烯燃烧时,耗氧相同。
举一反三:
【变式1】等物质的量的乙醇、乙二醇、丙三醇分别与足量的钠反应,生成氢气的物质的量之比为________;乙醇、乙二醇、丙三醇分别同足量的钠反应生成等质量的氢气,则三种醇消耗的物质的量之比为________。
【答案】1∶2∶3 6∶3∶2
【巩固练习】
一、选择题
1.下列反应中断裂的是乙醇分子C—O键的是( ) A、乙醇与金属钠反应产生氢气 B、乙醇在浓硫酸存在下加热产生乙烯? C、乙醇与氢卤酸发生取代反应生成卤代烃 D、乙醇在酸性重铬酸钾的氧化下生成乙醛、乙酸
2.现在组成为CH4O和C3H8O的混合物,在一定条件下进行脱水反应,可能生成的有机物的种数为( ) A、5 B、6 C、7 D、8
3.一定量乙醇在氧气不足的情况下燃烧,得CO、CO2和水的总质量为27.6 g。若其中水的质量为10.8 g,则CO的质量是( )。
A.4.4 g B.2.2 g C.1.4 g D.在2.2 g和4.4 g之间
4.(2019 广东揭阳期中)下列说法不正确的是( )
A.CH3—CH=CH2和CH2=CH2的最简式相同
B.乙二醇和丙三醇为同系物
C.CH≡CH和C6H6的含碳量相同
D.2—甲基—2—丙醇不能被催化氧化成相应的醛
5.下列化学方程式书写错误的是() A.乙醇催化氧化制取乙醛: 2CH3CH2OH+O2/2CH3CHO+2H2O B.苯与浓硫酸、浓硝酸的混合液共热制硝基苯: / C.乙酸和乙醇发生反应生成乙酸乙酯: CH3CH2OH+CH3COOH?/CH3COOC2H5+H2O D.乙烯使溴的四氯化碳溶液褪色: CH2=CH2+Br2—→CH2Br—CH2Br
6.化合物A(C4H8Br2)可由下列反应制得,C4H10O/C4H8/?C4H8Br2,则结构式不可能的是 ( ) A、CH3CH2CHBrCH2BrB、CH3CH(CH2Br)2? C、CH3CHBrCHBrCH3 D、(CH3)2CBrCH2Br?
7.分子式为C7H16O的饱和一元醇发生消去反应时,可以得到两种单烯烃,则该醇的结构简式可能是下列中的( )。
/
8.(2019 海南海口调研)有机物M的分子式为C4H10O,M能与金属钠反应产生氢气,则M与乙酸发生酯化反应生成的酯共有(不考虑立体异构)( )
A.3种 B.4种 C.5种 D.6种
9.(2019 北京西城期末)下列图示的实验操作,不能实现相应实验目的的是( )
/
10.(2019 江苏江阴期中)下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
/
二、填空题
1.小明把两枚邮票剪下来,浸在水中以便去掉邮票背面的粘合剂。通常邮票的粘合剂成分是/(聚乙烯醇),试根据其分子结构,解释它在水中被溶解的原因__________________________________________。
2.某实验小组用如下图所示装置进行乙醇液化氧化实验:
/
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:________。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是________反应。
(2)甲和乙两个水浴作用不相同。甲的作用是________;乙的作用是________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是________。集气瓶中收集到的气体的主要成分是________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________。要除去该物质,可先在混合液中加入________(填字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过________(填实验操作名称)即可除去。
3.(2019 陕西质量检测)三颈瓶在化学实验中的应用非常广泛,下面是三颈瓶在部分无机实验或有机实验中的一些应用。
Ⅰ.在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热。下列有关说法错误的是________。
A.反应后溶液中含有NO3-
B.反应后溶液中c(H+)增大
C.实验过程中有化合反应发生
D.实验过程中NH3·H2O的电离程度不可能发生变化
Ⅱ.有学生用五氧化二磷作乙醇脱水制乙烯的催化剂,进行相关实验。按下表所示的量和反应条件在三颈瓶中先加入一定量P2O5,再注入95%的乙醇,并加热,观察现象。
/
实验
P2O5/g
95%乙醇/mL
加热方式
实验1
2
4
酒精灯
实验2
2
4
水浴70℃
实验结果如下:
实验
实验现象
三颈瓶
收集瓶
试管
实验1
酒精加入时,立刻产生白雾,当用酒精灯加热时,有气泡产生,并逐渐沸腾,生成黏稠状液体
有无色液体
溶液褪色
实验2
酒精加入时,立刻产生白雾,当用水浴加热时,不产生气泡,一段时间后,生成黏稠状液体
有无色液体
溶液不褪色
根据上述材料,完成下列填空。
(1)写出实验室用乙醇制乙烯的化学方程式:________。
(2)如图装置中冷凝管的作用是________,进水口为________(填“a”或“b”),浓硫酸的作用是________。
(3)实验l使溴的四氯化碳溶液褪色的物质是________。
(4)实验2中,水浴加热所需仪器有________(加热仪器、夹持仪器、石棉网除外)。
(5)三颈瓶、收集瓶中的液体经检验为磷酸三乙酯,写出三颈瓶中生成磷酸的化学方程式:________。
(6)根据实验1、2可以推断:
①以P2O5作为催化剂获得乙烯的反应条件是________。
②P2O5与95%乙醇在水浴70℃加热条件下可以发生的有机反应的类型是________反应。
【参考答案与解析】
一、选择题
1.BC 【解析】乙醇与金属钠反应产生氢气断裂O—H;乙醇在酸性重铬酸钾的氧化断裂O—H、C—H。?
2.C 【解析】CH4O代表甲醇,C3H8O代表正丙醇或异丙醇,两两之间发生分子间脱水,可生成6种醚;正丙醇或异丙醇可发生分子内脱水生成相同的烯烃——丙烯。
3.C 【解析】由H2O的物质的量可求出C2H5OH的物质的量为0.2 mol,则n (CO)+n (CO2)=0.4 mol。而m (CO)+m (CO2)=27.6 g-10.8 g,联立可解得n (CO)=0.05 mol,m (CO)=1.4 g。
4.B? 【解析】CH3—CH=CH2和CH2=CH2的最简式都是CH2,故A正确;乙二醇和丙三醇含有的羟基数目不相同,不互为同系物,故B错误;CH≡CH和C6H6的最简式均为CH,二者的含碳量相同,故C正确;2—甲基—2—丙醇中羟基连接的碳原子上没有氢原子,不能被催化氧化,故D正确。
5. B 【解析】B项中硝基苯的结构简式写错。。 6.B 【解析】化合物C4H8Br2由C4H8与溴的四氯化碳溶液通过加成反应生成,所以Br原子应该在相邻的两个C原子上。
7.C
【解析】因该醇发生消去反应时,生成两种单烯烃,这表明连有—OH的碳原子相邻的β碳原子上应连有氢原子且氢原子的化学环境不同。分析题给4个选项,只有选项C符合此条件。
8.B
【解析】能与金属钠反应生成氢气说明含有羟基,所以该物质是丁醇,丁醇能与乙酸发生酯化反应,而丁醇的同分异构体有CH3CH2CH2CH2OH、CH3CH2CH(CH3)OH、(CH3)3COH、(CH3)2CHCH2OH,共4种。
9.C
【解析】A项,甲苯能使高锰酸钾溶液褪色,而己烷不能;B项,溶液中加入NaOH,可以降低Fe3+的浓度;D项中可以通过澄清石灰水是否变浑浊来判断试管中的固体是否分解;C项,乙醇与浓硫酸在加热条件下可以发生氧化还原反应,乙烯气体中含有二氧化硫,二氧化硫具有还原性,也可以使酸性高锰酸钾溶液褪色。
10.B
【解析】乙醇制乙烯的反应温度在170℃左右,温度计水银球应该插入液面以下,A项错误;乙醇、冰醋酸和浓硫酸混合加热制取乙酸乙酯时,导气管不能伸入饱和碳酸钠溶液中以防倒吸,B项正确;石油分馏时冷凝管中冷却水应该下口进上口出,且温度计水银球应位于蒸馏烧瓶支管口处,C项错误;制硝基苯时水浴的温度为50℃到60℃,D项错误。
二、填空题
1.聚乙烯醇分子链上含有多个羟基,水溶性大(如果回答相似相溶,也正确) 【解析】含有羟基的有机分子与水分子之间可以形成氢键,因此含有这些官能团的低碳原子数的有机分子,均具有良好的水溶性。聚乙烯醇分子C原子数多,但羟基数目也多。
2.(1)2Cu+O/2CuO、CH3CH2OH+CuOCH3CHO+H2O+Cu 放热
(2)加热 冷却 (3)乙醛、乙醇、水氮气 (4)乙酸 c 蒸馏
【解析】解答本题应先理解实验目的,再掌握各装置的作用,最后运用所学知识进行分析解答。该实验的目的是:乙醇的催化氧化。实验原理:2Cu+O2/2CuO,CH3CH2OH+CuOCH3CHO+H2O+Cu。实验流程:甲中的水为热水,将无水乙醇加热成乙醇蒸气,与空气一起进入玻璃管中,在铜网的作用下进行反应后,从玻璃管中出来的物质有:未反应的乙醇蒸气及少量O2水蒸气、乙醛蒸气和大量的N2,它们一起进入试管a中,乙中的水为冷水,其作用是将乙醇蒸气、水蒸气、乙醛蒸气进行冷却变为液体,不能冷却的少量O2和大量的N2进入到集气瓶中。(4)由题意知,该物质呈酸性,说明该物质为乙酸,若要除去乙醇、水、乙醛中的乙酸,可先在混合液中加入NaHCO3溶液,发生CH3COOH+NaHCO3—→CH3COONa+H2O+CO2↑反应,使CH3COOH转化为CH3COONa,再通过蒸馏即可除去。
3.Ⅰ.D
Ⅱ.(1)CH3CH2OHCH2=CH2↑+H2O
(2)冷凝、导气 b 除水
(3)乙烯(或CH2=CH2)
(4)大烧杯、温度计
(5)P2O5+3H2O2H3PO4
(6)①较高温度下(或直接加热) ②酯化
【解析】I.氨的催化氧化反应为4NH3+5O2/4NO+6H2O,NO与O2化合生成NO2:2NO+O2==2NO2,NO2与水反应:3NO2+H2O==2HNO3+NO。因此反应后溶液中有NO3-,溶液中c (H+)增大,A、B项正确;实验过程中NO和O2的反应为化合反应,C项正确;溶液中c (H+)增大,因此NH3·H2O的电离平衡NH3·H2O NH4++OH-正向移动,电离程度增大,D项错误。Ⅱ.(1)实验室制取乙烯是利用乙醇、浓硫酸混合加热至170℃,乙醇发生分子内脱水反应。(2)冷凝管的作用是冷凝、导气。冷却水从下口进、上口出,故进水口为b。浓硫酸的作用是除去水分。(3)实验1中溴的四氯化碳溶液褪色,是因为乙烯与溴发生了加成反应。(4)实验2中水浴加热所需仪器为大烧杯、温度计。(5)三颈瓶中P2O5与水化合生成H3PO4。(6)①以P2O5作为催化剂获得乙烯的反应条件是较高温度下或直接加热。②P2O5是磷酸的酸酐,P2O5与水反应生成磷酸,磷酸与乙醇在水浴70℃时可以发生酯化反应。
【学习目标】
1、了解醇类的结构特点、一般特性和用途;
2、掌握乙醇的化学性质。
【典型例题】
类型一:醇的结构和性质
例1 乙醇分子结构中各种化学键如右图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )。
A.和金属钠反应时①键断裂
B.和浓硫酸共热到170℃时键②和⑤断裂
C.和浓硫酸共热到140℃时仅有键②断裂
D.在铜催化下与O2反应时键①和③断裂
【思路点拨】本题全面考查乙醇的化学性质,从断键情况考查乙醇在发生化学反应时的机理注意区分乙醇与浓硫酸共热时取代成醚及消去成烯的断键特点。
【答案】C
【解析】选项A乙醇与钠反应生成乙醇钠和氢气,是乙醇羟基中的O—H键①断裂;选项B乙醇与浓硫酸共热到170℃时发生消去反应生成乙烯和水,是键②和⑤断裂;选项C是乙醇发生分子间脱水反应生成乙醚,一分子断裂键①,另一分子断裂键②;选项D是乙醇催化氧化为乙醛,断裂的键是①和③。
【总结升华】醇类断裂C—O键,脱掉—OH时,可发生取代或消去反应;若同时断裂C—O键和H—O键时,可发生消去或氧化反应,要注意分析体会。
举一反三:
【变式1】(2019 新建县模拟)酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧衍生物 ⑤乙醇有刺激性气体
A.②④⑤ B.②③ C.①③ D.①④
【答案】C
【解析】①乙醇沸点低,易挥发,若饮酒,呼出的气体中含有酒精,与测定原理有关;②乙醇密度比水小,可与水以任意比混溶,与测定原理无关;③乙醇分子中含有羟基,具有还原性,K2Cr2O7具有强氧化性,可以把乙醇迅速氧化为乙酸而变成蓝绿色的Cr3+,与测定原理有关;④乙醇可看成是乙烷中的氢原子被羟基取代后的产物,是烃的含氧化合物,与测定原理无关;⑤乙醇有刺激性气体,与测定原理无关,故对乙醇的描述与此测定原理有关的是①③,故选C。
例2关于乙醇的说法中正确的是( )
A.乙醇结构中有-OH,所以乙醇溶解于水,可以电离出OH-而显碱性
B.乙醇燃烧生成二氧化碳和水,说明乙醇具有氧化性
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
【思路点拨】本题注重对乙醇基础知识的考查,难度不大,仔细分析各个选项即可得出正确答案。
【答案】D
【解析】A项乙醇结构中有-OH,能与水形成氢键,所以乙醇溶解于水,但不能电离出OH-,故A错误;B项乙醇燃烧生成二氧化碳和水,乙醇作燃料,是还原剂,具有还原性,故B错误;C项乙醇与钠反应可以产生氢气,但乙醇不能电离出氢离子,不显酸性,故C错误;D项水是弱电解质,乙醇是非电解质,乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼,故D正确。
【总结升华】醇的性质微点拨:(1)含有相同碳原子数的醇中,所含羟基数目越多,沸点越高。
(2)醇类和卤代烃都能发生消去反应,但条件不同。醇消去反应的条件是浓硫酸、加热;卤代烃消去反应的条件是氢氧化钠醇溶液、加热。
(3)某一元醇发生消去反应生成的烯烃不一定只有一种,要看连羟基的碳原子的邻位碳原子上不同化学环境下氢原子的种数。
举一反三:
【变式1】二甘醇可用作溶剂、纺织助剂等。一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式是HO—CH2CH2—O—CH2CH2—OH。下列有关二甘醇的叙述正确的是( )。
A.不能发生消去反应 B.能发生取代反应
C.能溶于水,不溶于乙醇 D.符合分子通式CnH2nO3
【答案】B
【变式2】下列物质能发生消去反应生成相应的烯烃,但不能氧化生成相应醛的是( )
A.CH3OH B.CH3CH2CH2OH C./ D./
【答案】D
【解析】与羟基相连的碳原子上有两个或三个氢原子(即含有-CH2OH)时才能被氧化为醛、与羟基相连的碳原子的邻位碳原子上至少有一个氢原子时才能发生消去反应。
类型二:醇的命名
例3 对某一醇类作系统命名,其中正确的是( )。
A.1,1-二甲基-3-丙醇 B.2-甲基-4-戊醇
C.3-甲基-2-丁醇 D.3,3-二甲基-1-丁醇
【思路点拨】本题考查醇的命名。注意主链的选择、官能团的位置及标识。
【答案】C、D
【解析】先根据题给各选项的名称写出醇的结构简式,再由醇的系统命名法分析其正误。
/
【总结升华】按系统命名法,醇的命名需要选包含官能团的碳数最多的键做为主链,再标支链位置。书写时,官能团的位置也需要特别标出。后续课程中其他有机物的命名方式相同。
举一反三:
【变式1】写出下列有机物的系统名称。
/
【答案】(1)3-甲基-2-丁醇 (2)3,4,4-三甲基-2-戊醇
类型三:醇的有关计算
例4 一定量的某饱和一元醇充分燃烧后生成CO2?6.72 L(标况),等量的该醇与足量的金属钠反应放出H2,全部通过足量的灼热CuO粉末,若H2的损失率为20%,反应后使CuO粉末质量减轻0.64 g,求该醇的分子式,并写出该醇的可能结构简式。
【思路点拨】可以根据饱和一元醇燃烧的通式,分析其产物的比例特点。本题中注意氢气有损失,计算时需要考虑在内。
【答案】C3H8O;可能有的结构为:CH3CH2CH2OH?/
【解析】饱和一元醇燃烧:CnH2n+2O + 3n/2O2?→ nCO2?+ (n+1)H2O
0.3/n mol ← 已知:0.3mol
CuO + H2?→ Cu + H2O
80g 1mol 64g 减少16g
0.04mol ← 0.64g
即实际反应的H2是0.04mol,与钠反应生成的H2是0.05mol(损失率为20%),
醇的物质的量是0.1mol。
得出n=3
【总结升华】饱和一元醇的通式为CnH2n+2O,在燃烧时,为解题方便,可以看成CnH2n·H2O,即含有n个碳的饱和一元醇与含有n个碳的烯燃烧时,耗氧相同。
举一反三:
【变式1】等物质的量的乙醇、乙二醇、丙三醇分别与足量的钠反应,生成氢气的物质的量之比为________;乙醇、乙二醇、丙三醇分别同足量的钠反应生成等质量的氢气,则三种醇消耗的物质的量之比为________。
【答案】1∶2∶3 6∶3∶2
【巩固练习】
一、选择题
1.下列反应中断裂的是乙醇分子C—O键的是( ) A、乙醇与金属钠反应产生氢气 B、乙醇在浓硫酸存在下加热产生乙烯? C、乙醇与氢卤酸发生取代反应生成卤代烃 D、乙醇在酸性重铬酸钾的氧化下生成乙醛、乙酸
2.现在组成为CH4O和C3H8O的混合物,在一定条件下进行脱水反应,可能生成的有机物的种数为( ) A、5 B、6 C、7 D、8
3.一定量乙醇在氧气不足的情况下燃烧,得CO、CO2和水的总质量为27.6 g。若其中水的质量为10.8 g,则CO的质量是( )。
A.4.4 g B.2.2 g C.1.4 g D.在2.2 g和4.4 g之间
4.(2019 广东揭阳期中)下列说法不正确的是( )
A.CH3—CH=CH2和CH2=CH2的最简式相同
B.乙二醇和丙三醇为同系物
C.CH≡CH和C6H6的含碳量相同
D.2—甲基—2—丙醇不能被催化氧化成相应的醛
5.下列化学方程式书写错误的是() A.乙醇催化氧化制取乙醛: 2CH3CH2OH+O2/2CH3CHO+2H2O B.苯与浓硫酸、浓硝酸的混合液共热制硝基苯: / C.乙酸和乙醇发生反应生成乙酸乙酯: CH3CH2OH+CH3COOH?/CH3COOC2H5+H2O D.乙烯使溴的四氯化碳溶液褪色: CH2=CH2+Br2—→CH2Br—CH2Br
6.化合物A(C4H8Br2)可由下列反应制得,C4H10O/C4H8/?C4H8Br2,则结构式不可能的是 ( ) A、CH3CH2CHBrCH2BrB、CH3CH(CH2Br)2? C、CH3CHBrCHBrCH3 D、(CH3)2CBrCH2Br?
7.分子式为C7H16O的饱和一元醇发生消去反应时,可以得到两种单烯烃,则该醇的结构简式可能是下列中的( )。
/
8.(2019 海南海口调研)有机物M的分子式为C4H10O,M能与金属钠反应产生氢气,则M与乙酸发生酯化反应生成的酯共有(不考虑立体异构)( )
A.3种 B.4种 C.5种 D.6种
9.(2019 北京西城期末)下列图示的实验操作,不能实现相应实验目的的是( )
/
10.(2019 江苏江阴期中)下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
/
二、填空题
1.小明把两枚邮票剪下来,浸在水中以便去掉邮票背面的粘合剂。通常邮票的粘合剂成分是/(聚乙烯醇),试根据其分子结构,解释它在水中被溶解的原因__________________________________________。
2.某实验小组用如下图所示装置进行乙醇液化氧化实验:
/
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:________。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是________反应。
(2)甲和乙两个水浴作用不相同。甲的作用是________;乙的作用是________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是________。集气瓶中收集到的气体的主要成分是________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________。要除去该物质,可先在混合液中加入________(填字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过________(填实验操作名称)即可除去。
3.(2019 陕西质量检测)三颈瓶在化学实验中的应用非常广泛,下面是三颈瓶在部分无机实验或有机实验中的一些应用。
Ⅰ.在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热。下列有关说法错误的是________。
A.反应后溶液中含有NO3-
B.反应后溶液中c(H+)增大
C.实验过程中有化合反应发生
D.实验过程中NH3·H2O的电离程度不可能发生变化
Ⅱ.有学生用五氧化二磷作乙醇脱水制乙烯的催化剂,进行相关实验。按下表所示的量和反应条件在三颈瓶中先加入一定量P2O5,再注入95%的乙醇,并加热,观察现象。
/
实验
P2O5/g
95%乙醇/mL
加热方式
实验1
2
4
酒精灯
实验2
2
4
水浴70℃
实验结果如下:
实验
实验现象
三颈瓶
收集瓶
试管
实验1
酒精加入时,立刻产生白雾,当用酒精灯加热时,有气泡产生,并逐渐沸腾,生成黏稠状液体
有无色液体
溶液褪色
实验2
酒精加入时,立刻产生白雾,当用水浴加热时,不产生气泡,一段时间后,生成黏稠状液体
有无色液体
溶液不褪色
根据上述材料,完成下列填空。
(1)写出实验室用乙醇制乙烯的化学方程式:________。
(2)如图装置中冷凝管的作用是________,进水口为________(填“a”或“b”),浓硫酸的作用是________。
(3)实验l使溴的四氯化碳溶液褪色的物质是________。
(4)实验2中,水浴加热所需仪器有________(加热仪器、夹持仪器、石棉网除外)。
(5)三颈瓶、收集瓶中的液体经检验为磷酸三乙酯,写出三颈瓶中生成磷酸的化学方程式:________。
(6)根据实验1、2可以推断:
①以P2O5作为催化剂获得乙烯的反应条件是________。
②P2O5与95%乙醇在水浴70℃加热条件下可以发生的有机反应的类型是________反应。
【参考答案与解析】
一、选择题
1.BC 【解析】乙醇与金属钠反应产生氢气断裂O—H;乙醇在酸性重铬酸钾的氧化断裂O—H、C—H。?
2.C 【解析】CH4O代表甲醇,C3H8O代表正丙醇或异丙醇,两两之间发生分子间脱水,可生成6种醚;正丙醇或异丙醇可发生分子内脱水生成相同的烯烃——丙烯。
3.C 【解析】由H2O的物质的量可求出C2H5OH的物质的量为0.2 mol,则n (CO)+n (CO2)=0.4 mol。而m (CO)+m (CO2)=27.6 g-10.8 g,联立可解得n (CO)=0.05 mol,m (CO)=1.4 g。
4.B? 【解析】CH3—CH=CH2和CH2=CH2的最简式都是CH2,故A正确;乙二醇和丙三醇含有的羟基数目不相同,不互为同系物,故B错误;CH≡CH和C6H6的最简式均为CH,二者的含碳量相同,故C正确;2—甲基—2—丙醇中羟基连接的碳原子上没有氢原子,不能被催化氧化,故D正确。
5. B 【解析】B项中硝基苯的结构简式写错。。 6.B 【解析】化合物C4H8Br2由C4H8与溴的四氯化碳溶液通过加成反应生成,所以Br原子应该在相邻的两个C原子上。
7.C
【解析】因该醇发生消去反应时,生成两种单烯烃,这表明连有—OH的碳原子相邻的β碳原子上应连有氢原子且氢原子的化学环境不同。分析题给4个选项,只有选项C符合此条件。
8.B
【解析】能与金属钠反应生成氢气说明含有羟基,所以该物质是丁醇,丁醇能与乙酸发生酯化反应,而丁醇的同分异构体有CH3CH2CH2CH2OH、CH3CH2CH(CH3)OH、(CH3)3COH、(CH3)2CHCH2OH,共4种。
9.C
【解析】A项,甲苯能使高锰酸钾溶液褪色,而己烷不能;B项,溶液中加入NaOH,可以降低Fe3+的浓度;D项中可以通过澄清石灰水是否变浑浊来判断试管中的固体是否分解;C项,乙醇与浓硫酸在加热条件下可以发生氧化还原反应,乙烯气体中含有二氧化硫,二氧化硫具有还原性,也可以使酸性高锰酸钾溶液褪色。
10.B
【解析】乙醇制乙烯的反应温度在170℃左右,温度计水银球应该插入液面以下,A项错误;乙醇、冰醋酸和浓硫酸混合加热制取乙酸乙酯时,导气管不能伸入饱和碳酸钠溶液中以防倒吸,B项正确;石油分馏时冷凝管中冷却水应该下口进上口出,且温度计水银球应位于蒸馏烧瓶支管口处,C项错误;制硝基苯时水浴的温度为50℃到60℃,D项错误。
二、填空题
1.聚乙烯醇分子链上含有多个羟基,水溶性大(如果回答相似相溶,也正确) 【解析】含有羟基的有机分子与水分子之间可以形成氢键,因此含有这些官能团的低碳原子数的有机分子,均具有良好的水溶性。聚乙烯醇分子C原子数多,但羟基数目也多。
2.(1)2Cu+O/2CuO、CH3CH2OH+CuOCH3CHO+H2O+Cu 放热
(2)加热 冷却 (3)乙醛、乙醇、水氮气 (4)乙酸 c 蒸馏
【解析】解答本题应先理解实验目的,再掌握各装置的作用,最后运用所学知识进行分析解答。该实验的目的是:乙醇的催化氧化。实验原理:2Cu+O2/2CuO,CH3CH2OH+CuOCH3CHO+H2O+Cu。实验流程:甲中的水为热水,将无水乙醇加热成乙醇蒸气,与空气一起进入玻璃管中,在铜网的作用下进行反应后,从玻璃管中出来的物质有:未反应的乙醇蒸气及少量O2水蒸气、乙醛蒸气和大量的N2,它们一起进入试管a中,乙中的水为冷水,其作用是将乙醇蒸气、水蒸气、乙醛蒸气进行冷却变为液体,不能冷却的少量O2和大量的N2进入到集气瓶中。(4)由题意知,该物质呈酸性,说明该物质为乙酸,若要除去乙醇、水、乙醛中的乙酸,可先在混合液中加入NaHCO3溶液,发生CH3COOH+NaHCO3—→CH3COONa+H2O+CO2↑反应,使CH3COOH转化为CH3COONa,再通过蒸馏即可除去。
3.Ⅰ.D
Ⅱ.(1)CH3CH2OHCH2=CH2↑+H2O
(2)冷凝、导气 b 除水
(3)乙烯(或CH2=CH2)
(4)大烧杯、温度计
(5)P2O5+3H2O2H3PO4
(6)①较高温度下(或直接加热) ②酯化
【解析】I.氨的催化氧化反应为4NH3+5O2/4NO+6H2O,NO与O2化合生成NO2:2NO+O2==2NO2,NO2与水反应:3NO2+H2O==2HNO3+NO。因此反应后溶液中有NO3-,溶液中c (H+)增大,A、B项正确;实验过程中NO和O2的反应为化合反应,C项正确;溶液中c (H+)增大,因此NH3·H2O的电离平衡NH3·H2O NH4++OH-正向移动,电离程度增大,D项错误。Ⅱ.(1)实验室制取乙烯是利用乙醇、浓硫酸混合加热至170℃,乙醇发生分子内脱水反应。(2)冷凝管的作用是冷凝、导气。冷却水从下口进、上口出,故进水口为b。浓硫酸的作用是除去水分。(3)实验1中溴的四氯化碳溶液褪色,是因为乙烯与溴发生了加成反应。(4)实验2中水浴加热所需仪器为大烧杯、温度计。(5)三颈瓶中P2O5与水化合生成H3PO4。(6)①以P2O5作为催化剂获得乙烯的反应条件是较高温度下或直接加热。②P2O5是磷酸的酸酐,P2O5与水反应生成磷酸,磷酸与乙醇在水浴70℃时可以发生酯化反应。
