人教版九年级下册第九单元溶液单元测试题(含答案)
文档属性
| 名称 | 人教版九年级下册第九单元溶液单元测试题(含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 209.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-01-31 10:41:39 | ||
图片预览




文档简介
溶液
1.有关溶液说法正确的是( )
A.溶液都是均一、稳定的混合物
B.所有饱和溶液都比不饱和溶液要浓
C.形成溶液的溶质都是固体
D.溶液的体积等于溶质的体积与溶剂的体积之和
2.对下列事实或做法解释正确的是( )
A.门把手表面镀铬可防锈﹣﹣改变了金属的内部结构
B.洗涤剂洗油污﹣洗涤剂能溶解油污
C.钢的性能优于生铁﹣钢的含碳量比生铁高
D.氧气能被液化贮存于钢瓶中﹣分子间有间隔且间隔能改变
3.我国北方有许多盐湖,湖中溶有大量的碳酸钠和氯化钠,那里的农民冬天捞“碱”(碳酸钠),夏天晒盐(氯化钠)。请你判断图中能反映碳酸钠的溶解度的变化曲线的是( )
A.a B.b C.c D.d
4.现有一杯30℃的硝酸钾饱和溶液(如图甲所示),将其升温至70℃,得到如图乙所示的溶液(不考虑水分蒸发),此变化过程中,下列说法正确的是( )
A.硝酸钾的溶解度不变
B.溶液的溶质质量变大
C.溶液的质量不变
D.溶液的溶质质量分数变小
5.下列说法中,错误的是( )
A.生活中煮沸可以降低水的硬度
B.降低含碳量可以使生铁炼成钢
C.降低可燃物的温度至着火点以下可以灭火
D.降低温度可以使不饱和溶液变饱和
6.下列有关溶液的说法中,正确的是( )
A.溶液由溶质和溶剂组成,溶质必须是固体,溶剂必须是液体
B.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
C.通过震荡、搅拌等方法可以增大固体物质在水中的溶解度
D.要从溶液中获得晶体,可以采用蒸发溶剂或冷却热饱和溶液的方法
7.氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是( )
A.硝酸钾的溶解度比氯化铵的大
B.a℃时,氯化铵与硝酸钾溶液中溶质的质量分数相等
C.将20℃的硝酸钾不饱和溶液升温可以变为饱和溶液
D.40℃时,50g水中加入50g硝酸钾,充分搅拌,得到质量分数为39.02%的硝酸钾溶液
8.如图是利用海水提取粗盐的过程:根据海水晒盐的原理,下列说法中正确的是( )
A.海水进入贮水池,海水的成分发生了变化
B.在蒸发池中,海水中氯化钠的质量逐渐增加
C.在蒸发池中,海水中水的质量逐渐减少
D.析出晶体后的母液是氯化钠的不饱和溶液
9.下列说法错误的是( )
A.同一溶质的溶液,饱和溶液的浓度比不饱和溶液的浓度大
B.用洗洁精洗去餐具上的油污,属于乳化在日常生活中的应用
C.生石灰与水接触发热,是化学能转化为热能
D.验证Zn、Fe、Cu的金属活动性强弱,用FeSO4溶液、Zn、Cu试剂组合可以达到目的
10.如表为硝酸钾和氯化钠在不同温度下的溶解度,下列说法中正确的是( )
温度/℃ 0 10 20 30 40 50
溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5
NaCl 35.7 35.8 36.0 36.3 36.6 37.0
温度/℃ 60 70 80 90 100 ﹣﹣
溶解度/g KNO3 110 138 169 202 246 ﹣﹣
A.KNO3的溶解度大于NaCl的溶解度
B.将100℃等质量的饱和的KNO3溶液和饱和的NaCl溶液分别降温至50℃,析出的NaCl的质量大于KNO3的质量
C.0℃的饱和的KNO3溶液的溶质质量分数是13.3%
D.要将50℃的KNO3饱和溶液升高至60℃仍为饱和溶液,可以向溶液中加KNO3固体
11.若烧碱溶液不小心沾到皮肤上,可先用大量水冲洗,然后涂上 3%的硼酸溶液。现要配制 300g质量分数为 3%的硼酸溶液,相关叙述正确的是( )
A.称量硼酸固体的质量时,若托盘天平的指针稍偏向左盘,可尝试向右移动游码
B.量取水的体积时,将蒸馏水直接注入量筒,直至 291mL 刻度线处
C.溶解过程中,需要用到的玻璃仪器是烧杯和玻璃棒
D.装瓶过程中,若少量硼酸溶液洒出,则剩余硼酸溶液的溶质质量分数会变小
12.20℃时,通过增加溶质的方法,将硝酸钾的不饱和溶液变为饱和溶液,下列说法正确的是( )
A.溶质的质量一定不变
B.溶剂的质量一定减少
C.溶液的质量一定不变
D.溶液的溶质质量分数一定增大
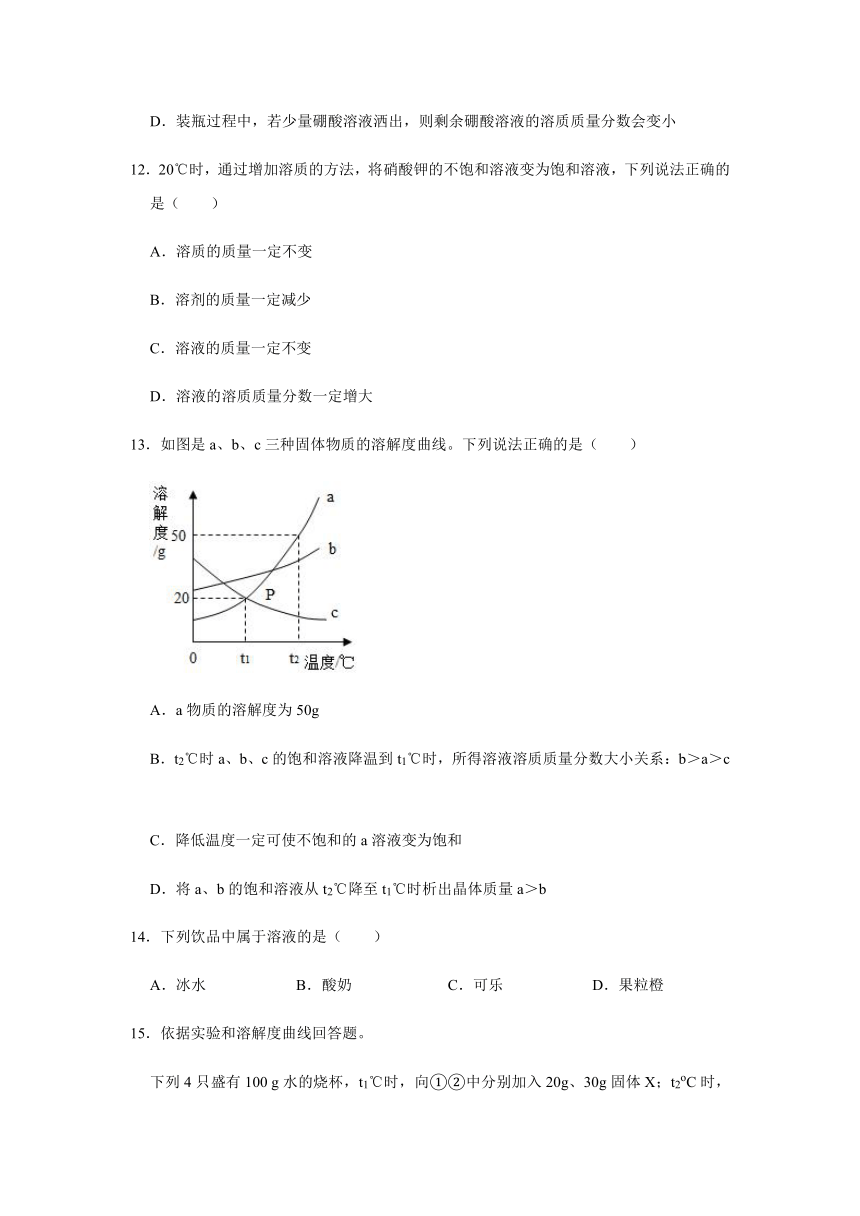
13.如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是( )
A.a物质的溶解度为50g
B.t2℃时a、b、c的饱和溶液降温到t1℃时,所得溶液溶质质量分数大小关系:b>a>c
C.降低温度一定可使不饱和的a溶液变为饱和
D.将a、b的饱和溶液从t2℃降至t1℃时析出晶体质量a>b
14.下列饮品中属于溶液的是( )
A.冰水 B.酸奶 C.可乐 D.果粒橙
15.依据实验和溶解度曲线回答题。
下列4只盛有100 g水的烧杯,t1℃时,向①②中分别加入20g、30g固体X;t2oC时,向③④中分别加入50g、60g固体Y,充分溶解
①中溶液的质量为( )
A.20g B.80g C.120 g D.125 g
16.下列有关溶液的说法正确的是( )
A.将饱和澄清石灰水升温,可以观察到浑浊现象
B.配制溶液时,搅拌可以增大溶质的溶解度
C.将10%的KNO3溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.将高锰酸钾粉末与汽油混合,可以得到高锰酸钾的汽油溶液
17.下列清洁方法错误的是( )
A.用汽油清洗手上的油漆
B.用洗涤剂清洗餐具上的油污
C.用酒精清洗残留碘的试管
D.用洗衣粉洗涤久置石灰水的试剂瓶
18.汽车、电动车一般使用铅酸蓄电池,某铅酸蓄电池用的是28%的稀硫酸,现要用1.0kg98%的浓硫酸配制该稀硫酸,则需加水( )
A.0.5kg B.1.5kg C.2.5kg D.3.5kg
19.如图中曲线为KNO3饱和溶液的质量分数(W)随温度(T)变化的曲线。M、N、P三点分别表示三份KNO3溶液的质量分数和温度。当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,下列判断不正确的是( )
A.M、N点代表的是饱和溶液,P点代表的是不饱和溶液
B.其它条件不变,加水稀释N点溶液可使其至M点
C.其它条件不变,将P点或N点溶液降温40℃后溶液均可至M点
D.维持溶液原温度蒸发溶剂时,M、N点均不动,P点垂直上移可至N点
20.能增大氧气在水中溶解度的方法是( )
A.增大压强 B.增加氧气的体积
C.增加水的质量 D.升高温度
21.如表为甲、乙两种固体物质的溶解度表格
温度/℃ 0 10 20 40 60 80 100
甲的溶解度(g) 13 20 40 67 110 169 246
乙的溶解度(g) 0.18 0.17 0.16 0.14 0.12 0.10 0.07
(1)溶解度随温度升高而增大的物质是 (填“甲”或“乙”)
(2)某同学按如图所示进行实验,得到相应温度下的A、B、C溶液,不考虑水分蒸发,在A、B、C三种溶液中属于饱和溶液的是 (填字母),向溶液C中再加入25克甲,充分搅拌,恢复到20℃时,所得溶液中溶质的质量分数为 (结果精确到0.1%)
22.实验室配制100 g溶质质量分数为10%的氯化钠溶液,下列出现的操作失误中,会引起所配溶液的溶质质量分数偏小的是
A.量水时,仰视读数 B.称取氯化钠时,砝码和食盐放反
C.装瓶时,溶液溅出 D.
23.如表为硝酸钾和氯化钠的部分溶解度数据,某同学进行了如图的溶解实验
物质/溶解度/g/温度 10℃ 20℃ 30℃ 40℃ 50℃ 60℃ 70℃ 80℃
NaCl 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4
KNO3 20.9 31.6 45.8 63.9 85.5 110 138 169
①溶解度随温度升高变化显著的物质是 。
②20℃时硝酸钾的溶解度为 g/100g 水。
③上述溶液中属于饱和溶液的是 ,把上述的饱和溶液转化成不饱和溶液的方法有 、 。
④实验中升温和搅拌的目的分别是 、 。
⑤BCEF 溶液中溶质质量分数由大到小的关系是 (用“<”、“>”、“=”表示)。
⑥硝酸钾中含有少量氯化钠时,提纯硝酸钾的方法是 。
24.甲、乙、丙三种固体物质的溶解度如图所示,请回答下列问题。
(1)0℃时,三种物质溶解度最大的是 ;
(2)将t2℃的甲、乙、丙三种物质的饱和溶液降温到t0℃时,所得溶液中溶质的质量分数由大到小的顺序为 ;
(3)t1℃时,乙的饱和溶液中含有少量的甲物质,提纯乙物质的方法是 ;
(4)如图2,将放有固体X的试管放入烧杯中,然后向试管中加入液体Y,一段时间后丙溶液中有固体析出,则对应的x和Y物质是 (填序号)。
A.氯化钠和水 B.镁条和稀盐酸 C.硝酸铵和水 D.氢氧化钠和水
25.厨房中用洗洁精除去餐具上的油污时,会出现 (填“溶解”或“乳化”)现象。
26.某兴趣小组展开对硝酸钾固体及其溶液的实验探究,现配制50克5%的硝酸钾溶液。
①如图所示操作正确的顺序是 (填序号)。
A.④⑤①②③
B.①②③④⑤
C.⑤②①④③
D.③④①②⑤
②本实验需称取硝酸钾固体 g。
27.某同学配制50 g 6%的氯化钠溶液,整个操作过程如图所示,回答下列问题:
(1)配制溶液的正确操作顺序为 (填序号,下同),其中操作错误的是 。
(2)图②中盛放氯化钠固体的仪器名称是 ,需称取氯化钠 g。
(3)量取水时选用的量筒的量程最合适的是 (填序号),读数时视线要与量筒内 保持水平。
A.10 mL B.25 mL C.50 mL D.100 mL
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是 (填序号)。
A.氯化钠固体不纯
B.用生锈砝码称量
C.装瓶时有少量溶液洒出
D.溶解时烧杯内壁有水珠
28.硝酸钾和氯化钾的溶解度曲线如图所示
(1)t1℃时,硝酸钾的溶解度为 g。
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为 。
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是 。
(4)将t3℃时硝酸钾和氯化钾的饱和溶液各100g,降温至t2℃,过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是 。
A.都是饱和溶液 B.溶液质量a<b C.溶质质量a=b
D.溶剂质量a<b E.溶质的质量分数a>b
29.某同学用市售浓盐酸(溶质质量分数为37%,密度为1.18g?mL﹣1)配制800g溶质质量分数为10%的稀盐酸。通过计算可知需要浓盐酸 mL,水(密度为1g?mL﹣1) mL.(上述两空答案都精确到0.1mL)
30.实验室用溶质质量分数为20%的氯化钠溶液配制200g溶质质量分数为0.9%的生理盐水,则需要20%的氯化钠溶液 g,需要水 g。
参考答案
1.A; 2.D; 3.A; 4.B; 5.D; 6.D; 7.D; 8.C; 9.A; 10.D; 11.C; 12.D; 13.B; 14.C; 15.C; 16.A; 17.D; 18.C; 19.B; 20.A;
21.甲;B;28.6%; 22.AB;溶解时,烧杯中预先有少水; 23.KNO3;31.6;BE;升温;加溶剂;增大NaCl的溶解度;加速溶解;C>B>E>F;降温结晶; 24.丙;乙>甲>丙;蒸发溶剂;BD; 25.乳化; 26.A;2.5; 27.②①⑤③④;①;广口瓶;3;C;液体凹液面的最低处;AD; 28.25;20%;蒸发溶剂;ABD;
29.183.2;583.8; 30.9;191;
同课章节目录
