江苏省新沂市高塘中学初中化学沪教版(全国)九年级上册课件:3.1-4核外电子的分层排布(共16张PPT)
文档属性
| 名称 | 江苏省新沂市高塘中学初中化学沪教版(全国)九年级上册课件:3.1-4核外电子的分层排布(共16张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 561.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-01 00:00:00 | ||
图片预览





文档简介
(共16张PPT)
核外电子的分层排布
新沂市高塘中学
氢原子的原子核有一个质子,核外有一个电子,它在核外一定距离的空间内作高速运动。
那么在含有多个电子的原子里,所有的电子是否在同一区域内运动?
在含有多个电子的原子里,电子是分层运动的。
离核最近的叫第一层
离核稍远的叫第二层
由里往外依此类推
叫三、四、五、六、七层
核外电子的分层排步
1、电子层
符号
K L M N O P Q
n
1 2 3 4 5 6 7
能量高低
离核远近
低
高
近
远
2、各电子层最多容纳的电子数( 2n2个)
2个 8个 18个 32个 ……
电子排步的一般规律
①电子按能量高低先排入能量最低的电子层,然后再排入能量较高的电子层
②作为最外层,最多不超过8个电子(K层2个)
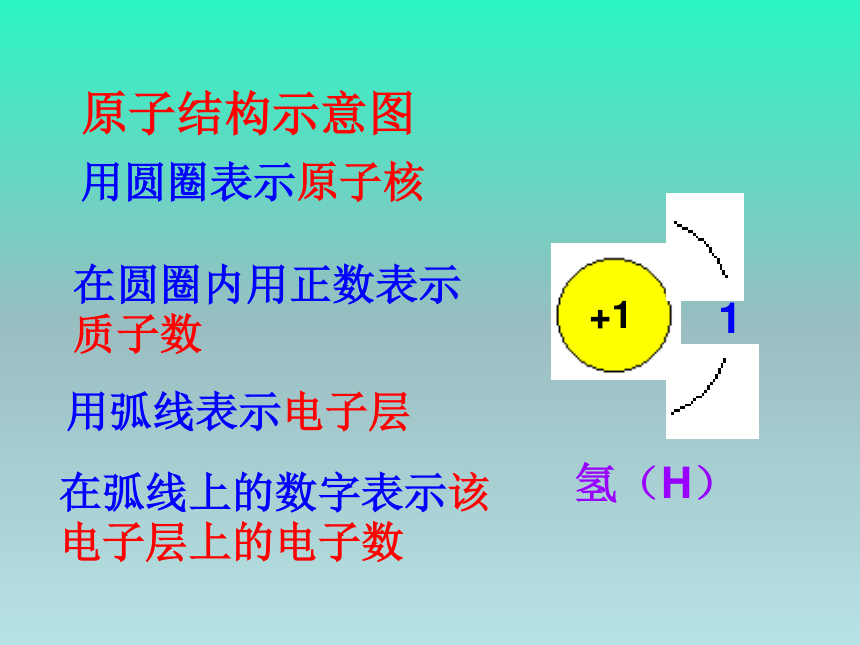
原子结构示意图
用圆圈表示原子核
在圆圈内用正数表示质子数
用弧线表示电子层
在弧线上的数字表示该电子层上的电子数
+1
1
氢(H)
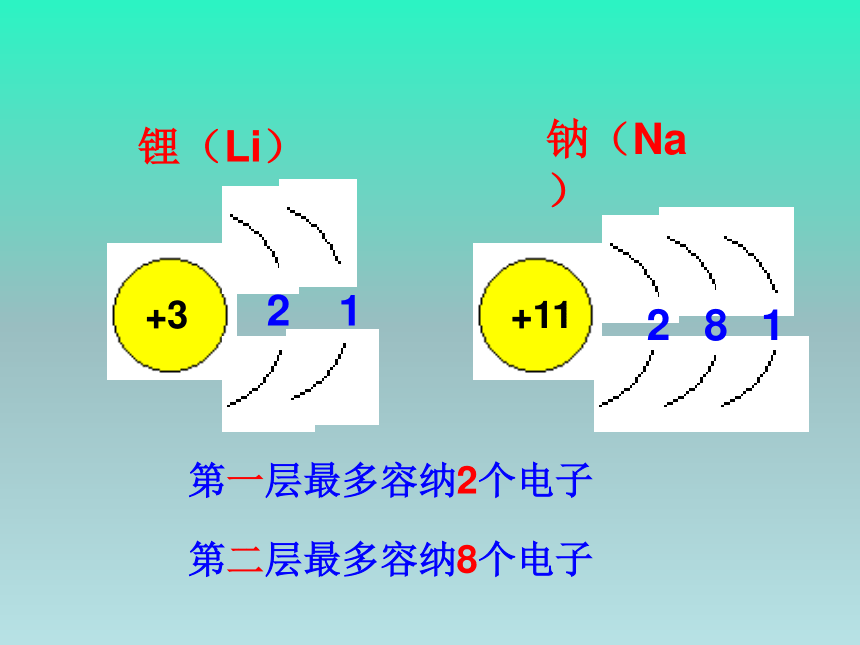
锂(Li)
+3
2
1
钠(Na)
+11
2
8
1
第一层最多容纳2个电子
第二层最多容纳8个电子
+19
2
8
8
1
+20
2
8
8
2
学生画图
钾(K)
钙(Ca)
注意:
①核电核数=质子数=核外电子数
②电子层上的电子数必须符合核外电子的排步规律
学生观察附录五(146页)
记住核电荷数为1-18元素及结构示意图。
观察
(1)横行共性:
纵向共性:
(2)分析金属元素,非金属元素,稀有气体元素原子最外层电子数特点
电子层数相同,最外层电子数依此增多
最外层电子数相同,电子层数依此增多
①稀有气体元素的原子最外层电子数一般是多少?
稀有气体,如氖、氩等,它们的最外层电子都是8个(氦为2个)。由于它们均不易与其他物质发生化学反应,呈现“化学惰性”,
所以人们认为最外层具有8个电子(只有一个电子层的具有2个电子)的结构,属于相对稳定结构。
它们的化学性质是否稳定?
②金属元素的原子最外层电子数有什么特点?他们的化学性质是否稳定?
金属元素,如钠、镁、铝等,最外层电子数一般少于4个,化学性质不稳定,
但在化学反应中易失去电子,趋向达到相对稳定结构。
③非金属元素的原子最外层电子数有什么特点?他们的化学性质是否稳定?
非金属元素,如氧、氯、硫、磷等,最外层电子一般多于4个,化学性质也不稳定,
一般在化学反应中易得到电子,趋向达到相对稳定结构。
稀有气体元素
最外层8个电子(氦最外层2个)
化学性质稳定
金属元素
最外层电子数一般少于4个
化学性质不稳定
不易失去或得到电子
容易失去电子达到稳定结构
非金属元素
最外层电子数一般多于4个
化学性质不稳定
容易得到电子达到稳定结构
结论:
(1)质子数决定元素种类
(2)最外层电子数决定元素的化学性质
核外电子的分层排布
新沂市高塘中学
氢原子的原子核有一个质子,核外有一个电子,它在核外一定距离的空间内作高速运动。
那么在含有多个电子的原子里,所有的电子是否在同一区域内运动?
在含有多个电子的原子里,电子是分层运动的。
离核最近的叫第一层
离核稍远的叫第二层
由里往外依此类推
叫三、四、五、六、七层
核外电子的分层排步
1、电子层
符号
K L M N O P Q
n
1 2 3 4 5 6 7
能量高低
离核远近
低
高
近
远
2、各电子层最多容纳的电子数( 2n2个)
2个 8个 18个 32个 ……
电子排步的一般规律
①电子按能量高低先排入能量最低的电子层,然后再排入能量较高的电子层
②作为最外层,最多不超过8个电子(K层2个)
原子结构示意图
用圆圈表示原子核
在圆圈内用正数表示质子数
用弧线表示电子层
在弧线上的数字表示该电子层上的电子数
+1
1
氢(H)
锂(Li)
+3
2
1
钠(Na)
+11
2
8
1
第一层最多容纳2个电子
第二层最多容纳8个电子
+19
2
8
8
1
+20
2
8
8
2
学生画图
钾(K)
钙(Ca)
注意:
①核电核数=质子数=核外电子数
②电子层上的电子数必须符合核外电子的排步规律
学生观察附录五(146页)
记住核电荷数为1-18元素及结构示意图。
观察
(1)横行共性:
纵向共性:
(2)分析金属元素,非金属元素,稀有气体元素原子最外层电子数特点
电子层数相同,最外层电子数依此增多
最外层电子数相同,电子层数依此增多
①稀有气体元素的原子最外层电子数一般是多少?
稀有气体,如氖、氩等,它们的最外层电子都是8个(氦为2个)。由于它们均不易与其他物质发生化学反应,呈现“化学惰性”,
所以人们认为最外层具有8个电子(只有一个电子层的具有2个电子)的结构,属于相对稳定结构。
它们的化学性质是否稳定?
②金属元素的原子最外层电子数有什么特点?他们的化学性质是否稳定?
金属元素,如钠、镁、铝等,最外层电子数一般少于4个,化学性质不稳定,
但在化学反应中易失去电子,趋向达到相对稳定结构。
③非金属元素的原子最外层电子数有什么特点?他们的化学性质是否稳定?
非金属元素,如氧、氯、硫、磷等,最外层电子一般多于4个,化学性质也不稳定,
一般在化学反应中易得到电子,趋向达到相对稳定结构。
稀有气体元素
最外层8个电子(氦最外层2个)
化学性质稳定
金属元素
最外层电子数一般少于4个
化学性质不稳定
不易失去或得到电子
容易失去电子达到稳定结构
非金属元素
最外层电子数一般多于4个
化学性质不稳定
容易得到电子达到稳定结构
结论:
(1)质子数决定元素种类
(2)最外层电子数决定元素的化学性质
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
