人教版初中化学九年级下册第九单元《溶液》测试题(含答案)
文档属性
| 名称 | 人教版初中化学九年级下册第九单元《溶液》测试题(含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 377.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-03 08:22:56 | ||
图片预览


文档简介
第九单元《溶液》测试题
一、单选题(每小题只有一个正确答案)
1.下列说法正确的是
A.红磷在空气中燃烧产生大量的白雾
B.洗洁精和汽油去除油污的原理相同
C.金刚石、石墨化学性质不同,因为它们原子排列方式不同
D.消防员利用风力灭火机喷出高速空气流将森林大火吹灭,其灭火原理是降低温度至可燃物的着火点以下
2.夏日里随时想喝到冰凉的饮料,我们可以自制化学“冰箱”,既把一种化学试剂放入一定量的水中,就可以形成低温小环境,这种试剂可以是下列物质中的( )
A.食盐 B.蔗糖 C.熟石灰 D.硝酸铵
3.小明同学要用6%的氯化钠溶液配制100g 3%的氯化钠溶液,下列说法错误的是( )
A.小明同学需要量取水的体积为50mL
B.实验的步骤为计算、称量、量取、溶解、装瓶贴签
C.实验中所需玻璃仪器为玻璃棒、胶头滴管、烧杯、量筒、细口瓶
D.在其他操作均正确的情况下,若在量取6%的氯化钠溶液过程中,仰视刻度量取该溶液了,则所配制溶液的溶质质量分数大于3%
4.如图是NaCl、MgSO4、KCl固体的溶解度曲线,下列说法正确的是( )
A.60℃时三种物质的饱和溶液中,溶质质量分数最大的是KCl溶液
B.将80℃不饱和的MgSO4溶液降温至40℃,一定能得到其饱和溶液
C.40℃时MgSO4的溶解度比NaCl小
D.将80℃含有少量NaCl的KCl饱和溶液降温至20℃,可得到KCl晶体
5.现有a、b、c三种物质的溶解度曲线如上图所示.下列说法正确的是( )
A.a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B.t2℃时,30ga物质加入到50g水中不断搅拌,所得溶液的质量为80 g
C.将t1℃时c的饱和溶液升温到t2℃,析出晶体
D.t2℃时,将a、b、c三种物质的饱和溶液降温到t1℃,析出晶体最多的是a
6.下列推理结论正确的是
A.原子在化学变化中不能再分,则分子在化学变化中也不能再分
B.洗涤剂除去衣服上油污是乳化作用,则汽油除去油污也是乳化作用
C.化学反应伴随能量变化,所以金属腐蚀过程中一定有能量变化
D.置换反应中有元素化合价变化,则有元素化合价变化的反应一定是置换反应
7.用NaCl固体配制100g溶质质量分数为10%的NaCl溶液.下列有关说法错误的是(????)
A.需要依次经过计算、称量、溶解、装瓶保存等步骤
B.选用100ml量筒量取所需的水
C.取水时仰视读数,可能导致配制的溶液溶质质量分数偏大
D.若改用20%的氯化钠溶液稀释得到上述溶液,则需加入20%的氯化钠溶液50g
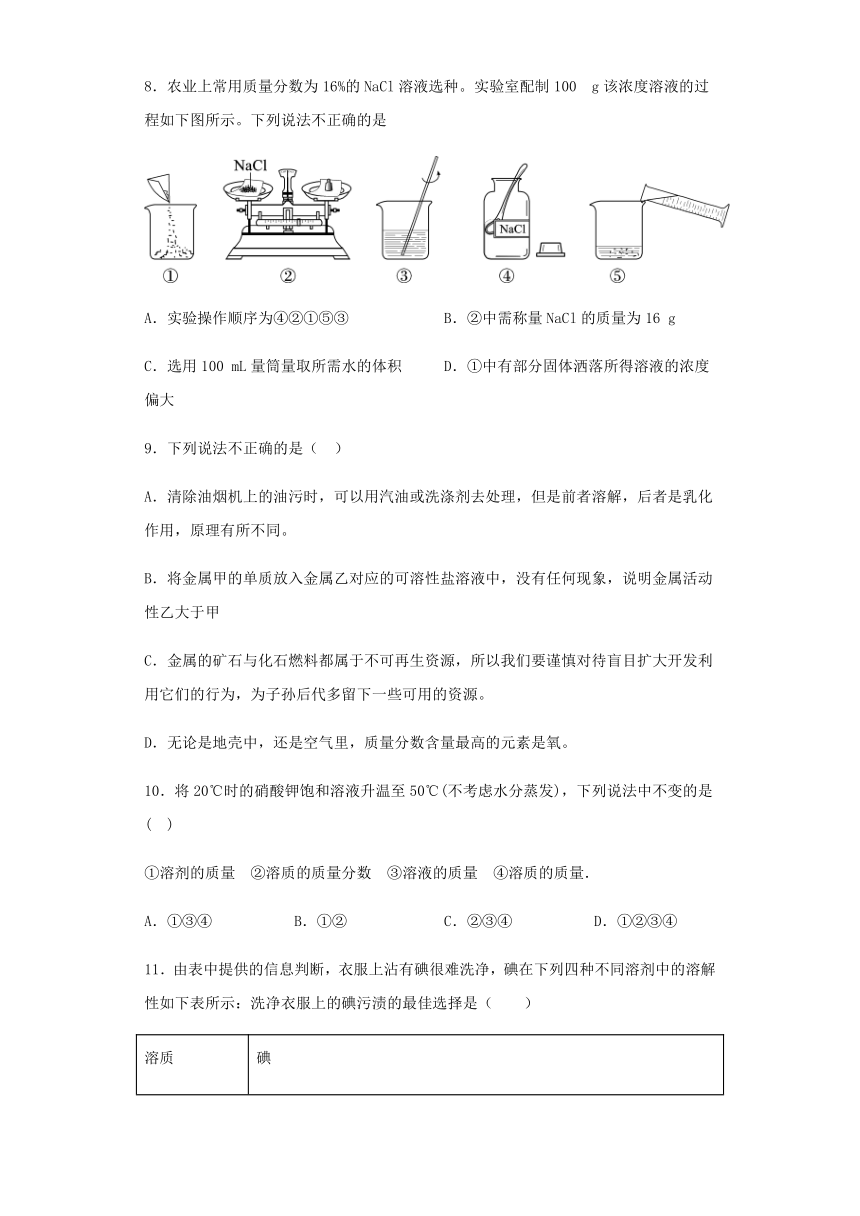
8.农业上常用质量分数为16%的NaCl溶液选种。实验室配制100 g该浓度溶液的过程如下图所示。下列说法不正确的是
A.实验操作顺序为④②①⑤③ B.②中需称量NaCl的质量为16 g
C.选用100 mL量筒量取所需水的体积 D.①中有部分固体洒落所得溶液的浓度偏大
9.下列说法不正确的是( )
A.清除油烟机上的油污时,可以用汽油或洗涤剂去处理,但是前者溶解,后者是乳化作用,原理有所不同。
B.将金属甲的单质放入金属乙对应的可溶性盐溶液中,没有任何现象,说明金属活动性乙大于甲
C.金属的矿石与化石燃料都属于不可再生资源,所以我们要谨慎对待盲目扩大开发利用它们的行为,为子孙后代多留下一些可用的资源。
D.无论是地壳中,还是空气里,质量分数含量最高的元素是氧。
10.将20℃时的硝酸钾饱和溶液升温至50℃(不考虑水分蒸发),下列说法中不变的是( )
①溶剂的质量 ②溶质的质量分数 ③溶液的质量 ④溶质的质量.
A.①③④ B.①② C.②③④ D.①②③④
11.由表中提供的信息判断,衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如下表所示:洗净衣服上的碘污渍的最佳选择是( )
溶质 碘
溶剂 水 酒精 汽油 苯(有毒)
溶解性 微溶 可溶 易溶 易溶
A.水 B.酒精 C.汽油 D.苯
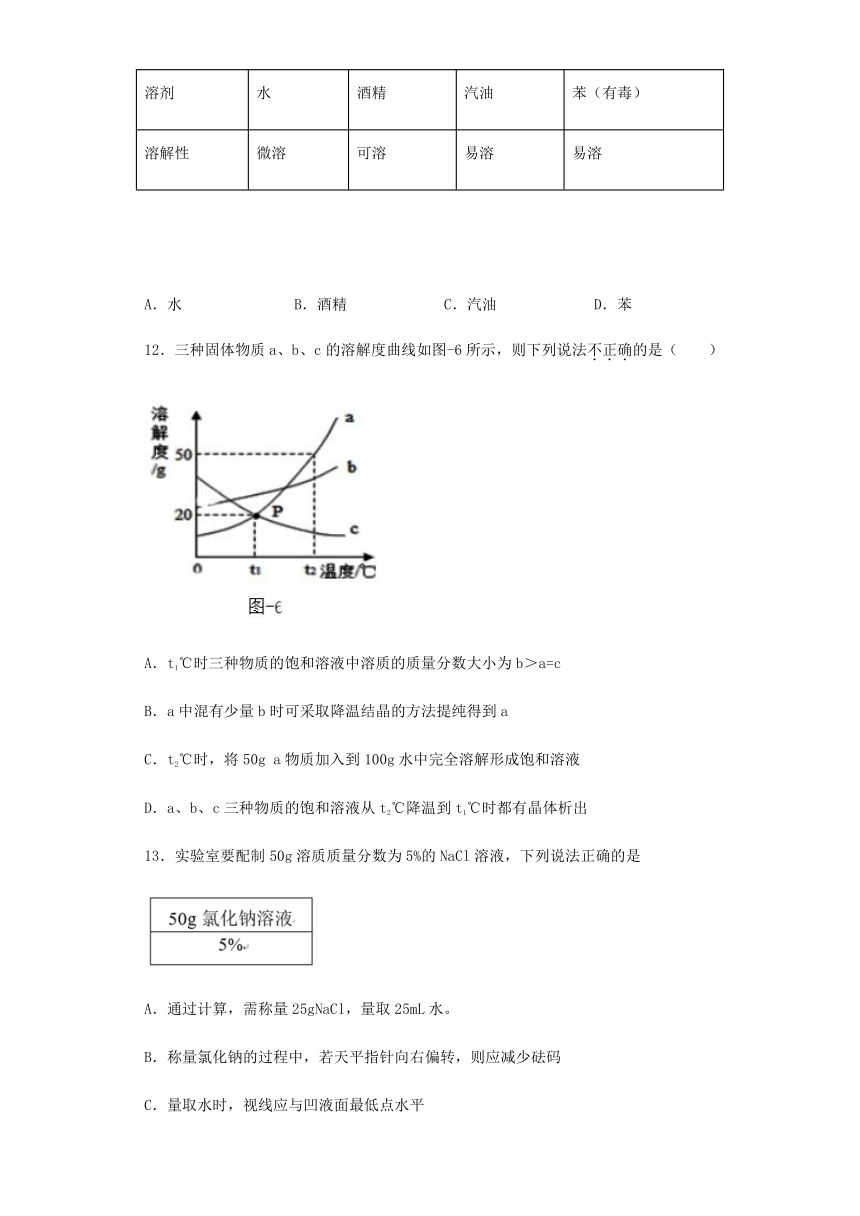
12.三种固体物质a、b、c的溶解度曲线如图-6所示,则下列说法不正确的是( )
A.t1℃时三种物质的饱和溶液中溶质的质量分数大小为b>a=c
B.a中混有少量b时可采取降温结晶的方法提纯得到a
C.t2℃时,将50g a物质加入到100g水中完全溶解形成饱和溶液
D.a、b、c三种物质的饱和溶液从t2℃降温到t1℃时都有晶体析出
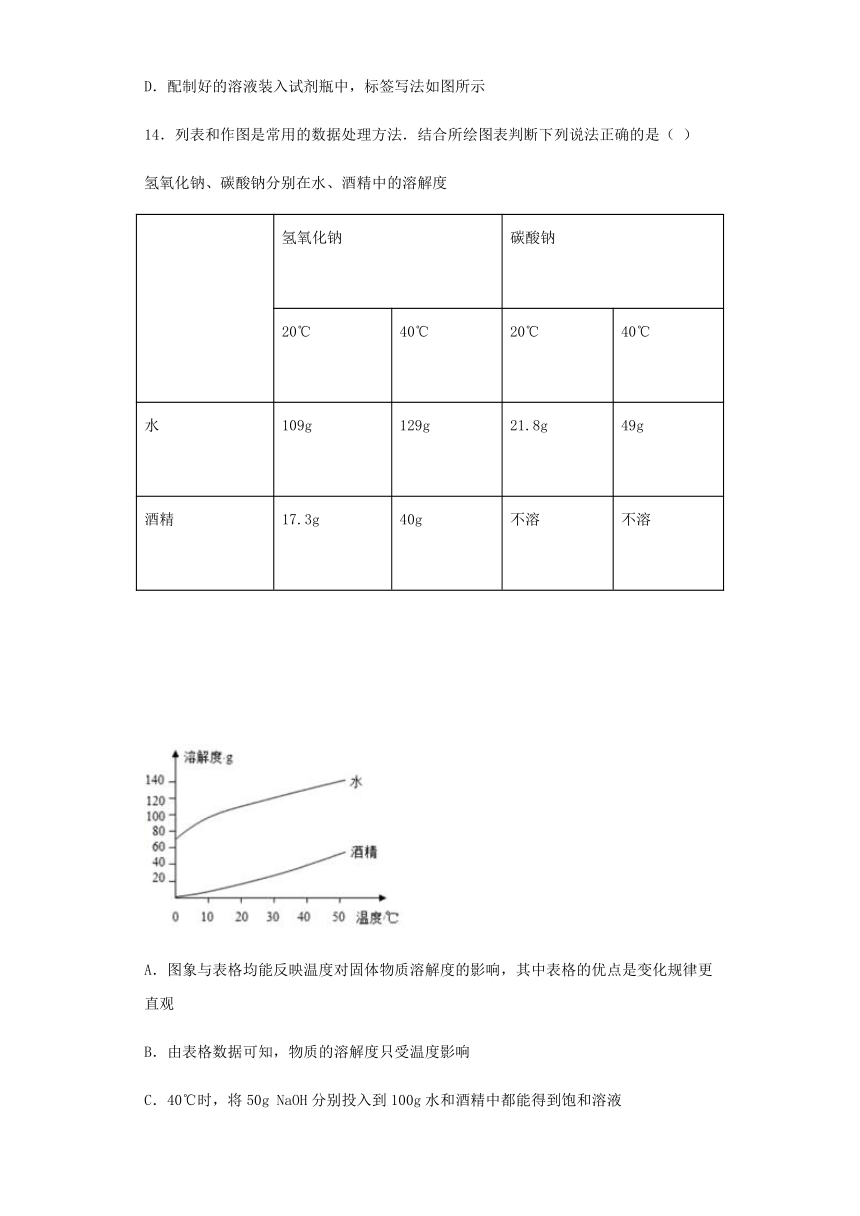
13.实验室要配制50g溶质质量分数为5%的NaCl溶液,下列说法正确的是
A.通过计算,需称量25gNaCl,量取25mL水。
B.称量氯化钠的过程中,若天平指针向右偏转,则应减少砝码
C.量取水时,视线应与凹液面最低点水平
D.配制好的溶液装入试剂瓶中,标签写法如图所示
14.列表和作图是常用的数据处理方法.结合所绘图表判断下列说法正确的是( )
氢氧化钠、碳酸钠分别在水、酒精中的溶解度
氢氧化钠
碳酸钠
20℃
40℃
20℃
40℃
水
109g
129g
21.8g
49g
酒精
17.3g
40g
不溶
不溶
A.图象与表格均能反映温度对固体物质溶解度的影响,其中表格的优点是变化规律更直观
B.由表格数据可知,物质的溶解度只受温度影响
C.40℃时,将50g NaOH分别投入到100g水和酒精中都能得到饱和溶液
D.40℃时,将CO2通入饱和的NaOH酒精溶液中有沉淀生成
15.甲、乙两种物质的溶解度曲线如右图所示。下列说法正确的是( )
A.a1℃时甲的饱和溶液,升温至a2℃时仍是饱和溶液
B.乙的溶解度随温度的升高而增大
C.相同温度时,甲的溶解度一定大于乙的溶解度
D.分别将甲、乙的饱和溶液从a2℃将至a1℃时,所得溶液中溶质的质量分数相等
二、填空题
16.相互转化:对于大部分固体物质来说:
____、____、____;____、____、____。
17.按要求回答
(1)硬水与软水相比,是因为硬水中含有较多的可溶性 化合物,把等量的肥皂水分别加到等量的硬水、软水中,泡沫多的为 。在净水器中装有活性炭,这是利用了活性炭的 性。
(2)要除去硫酸亚铁溶液中混有的硫酸铜杂质,可加入的试剂为 ,主要操作方法为 。
(3)硝酸钾在60℃时的溶解度为110g,这说明在60℃时,110g硝酸钾溶解在 g水中,恰好可以形成 溶液。
18.如图所示,在一个温度不变的密闭容器内,放入一杯饱和硫酸铜溶液,用细线吊住一块有缺口的硫酸铜晶体并浸在溶液中.过几天后观察到:晶体上的缺口(填“有”或“没有”)存在,晶体的质量________(填“减小”、“增大”或“不变”).
19.化学是研究物质的组成、结构、性质及其变化规律的基础自然科学,请回答下列问题:
(1)①从组成角度看:水是由 组成的。
②从微粒角度看:水是由 构成的。
③从资源角度看:水是生命之源,下图是用来净化河水的简易装置,下列说法错误的是 。
A.利用上图装置能把硬水变为软水
B.通过过滤可以除去水中所有的杂质
C.利用上图装置能对水杀菌消毒
④从变化角度看:水通电分解能生成最理想的能源 气,电解一定量的水,当其中一个电极产生5 mL气体时,另一电极产生的气体体积可能是 mL。
(2)水是很好的溶剂。下图是KNO3和KCl在不同温度时的溶解度,回答下列问题:
①t1℃时,两物质中溶解度较大的是 。
②t2℃时,两物质的等质量饱和溶液降温至t1℃,析出固体质量较多的是 的溶液。
③t2℃时,将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的 (填“饱和”或“不饱和”)溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数 (填“变大”或“不变”或“变小”)。
④欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是 。
20.请根据如图A、B、C三种物质的溶解度曲线,回答下列问题:
(1)温度越高,溶解度越小的物质是(填写代号)___;
(2)现有A、B、C三种物质的浓溶液,适用海水晒盐原理进行结晶提纯的是(填写代号)___;
(3)当溶液的浓度都用溶质的质量分数(m)表示时,下列说法中不正确的是(选填序号)___
①t1℃时,A、C两种物质的溶解度相等,两种溶液的浓度也相等
②t2℃时,A、B、C三种溶液的浓度可能相等
③将t2℃的A、B、C三种饱和溶液的温度分别降至t1℃时,A溶液中析出的晶体最多
④将t2℃的A、B、C三种饱和溶液的温度分别降至t1℃时,所得溶液浓度的大小顺序为m(B)>m(A)=m(C)
⑤将t1℃的A、B、C三种溶液分别升温,其浓度都不可能发生变化
⑥将t1℃的A、B、C三种溶液分别降温,其浓度都可能发生变化.
三、推断题
21.同学们到实验室去进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请你填空。
(1)若将所得滤渣放入稀盐酸中,有气泡产生,则
①滤液里一定含有_____(填写化学式,下同),可能含有_____;
②滤渣中一定含有_____,可能含有_____。
(2)若反应后所得滤液呈无色,则滤渣中一定含有_____(填写化学式)。
(3)反应后所得滤液的溶质质量分数_____(选填“大于”、“等于”或“小于”)原硝酸银溶液的溶质质量分数。
22.A、B、C、D是初中化学常见的物质,它们之间的转化关系如图所示:
(1)若该反应为高温下进行的置换反应,且A、C为黑色固体,A具有磁性,D在常温常压下为无色无味的液体,反应的化学方程式为_______________________________.
(2)若该反应为A燃烧不充分的反应,且A由两种元素组成,质量比为3:1,B可供给动物呼吸,常温下C为气体,反应的化学方程式为_____________________________.
(3)若在20℃时,将B溶于乙醇中配成饱和溶液,通入适量A发生反应,且A是参与光合作用的气体,B为碱,C为纯碱,则在乙醇中该反应的化学方程式为_________________________.
20℃时,B、C在水中和乙醇中的溶解度
物质 水中的溶解度 乙醇中的溶解度
B 109g 17.3g
C 21.8g <0.01g
四、实验题
23.水的作用不可忽视.如图中五个实验分别用到水.
请回答下列问题:
(1)实验A中水作________(填“溶剂”或“溶质”),玻璃棒的作用________;
(2)实验B中反应的化学方程式为________,集气瓶中水的作用是________;
(3)实验C中反应的化学方程式是________,烧杯中的水进入集气瓶中的原理是________;
(4)实验D中水的作用是提供热量和________;
(5)用化学方程式表示实验E中水的作用________.
24.(8分)粗盐中除NaCl外还含有MgSO4以及泥沙等杂质。初步提纯粗盐的实验流程如下:
(1)“滤渣”是粗盐中含有的 。
(2)实验过程中四次用到玻璃棒,分别是:
第一次:溶解时搅拌;
第二次: ;
第三次: ;
第四次:将精盐从蒸发皿转移出来。
(3)本实验从滤液得到精盐,采用的是蒸发溶剂的方法而不用降低溶液温度的方法,参考溶解度曲线图分析的原因:
(4)看图可知,200C时NaCl的溶解度为 g,本实验溶解3.6g的粗盐,蒸馏水的最佳使用量约为 ml.增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是 。
五、计算题
25.汽车蓄电池中稀硫酸的溶质质量分数为28%,密度为1.2克/厘米3。若要在实验室用溶质质量分数为98%的浓硫酸配制这种稀硫酸630 克。求:
(1)630 克稀硫酸的体积是多少毫升___________?
(2)需要浓硫酸多少克_______________________?
26.石灰石是我国主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验。
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是__________g。
(2)该石灰石样品的纯度是否符合要求?________(假设石灰石样品中的杂质不与盐酸反应也不溶水)
参考答案
1.D 2.D 3.B 4.D 5.C 6.C 7.C 8.D 9.D 10.D 11.C 12.D 13.C 14.D 15.D 16.增加溶剂 减少溶质 升高温度 增加溶质 减少溶剂 降低温度
17.(1)钙、镁 软水 吸附
(2)铁(或Fe) 过滤 (3)100 饱和
18.不变
19.(1)①氢、氧两种元素 ②水分子 ③ABC ④氢 10或2.5
(2)①氯化钾 ②硝酸钾 ③饱和 不变 ④温度大于或等于t1℃
20.C B ①③④⑤⑥
21.Zn(NO3)2 Fe(NO3)2 Ag、Fe Zn Ag、Fe 小于
22.Fe3O4+2C3Fe+2CO2↑2CH4+3O22CO+4H2O2NaOH+CO2=Na2CO3↓+H2O
23.溶剂搅拌,加速溶解3Fe+2O2Fe3O4防止高温熔融物炸裂集气瓶底部4P+5O22P2O5红磷燃烧消耗集气瓶中的氧气,装置内气压减小,大气压把水压入集气瓶中约占集气瓶内气体体积的五分之一隔绝空气CO2+H2O=H2CO3
24.⑴泥沙 ; ⑵过滤时引流; 蒸发时搅拌; ⑶氯化钠的溶解度受温度影响不大 ;
⑷36; 10 ; 不利于后续蒸发溶剂,蒸发溶剂时间会大大延长,消耗燃料。
25.525毫升 180克
26.4.4 因83.3%<85%,所以该石灰石样品的纯度不符合要求
同课章节目录
