ATP和酶
图片预览



文档简介
第四章光合作用和呼吸作用
第一节ATP和酶
(第一课时)
备课人:康娟盈
课标要求
1.知识目标:简述ATP的化学组成和特点并写出ATP的分子简式;解释ATP在能量代谢中的作用。
2.能力目标:通过ATP与ADP相互转换示意图,初步形成图文转化能力和用规范的生物学语言来表述问题的能力。
3情感目标:通过小组学习过程中的合作与交往培养学生的协作意识与交往的态度.
教学重点
ATP的分子特点和ATP与ADP的相互转化在新陈代谢中的作用及特点
教学难点
ATP在能量的储存、转移和利用中的作用
教学方法
实验探究、分析法
课时安排
一课时
教学过程
引入
“银烛秋光冷画屏,轻罗小衫扑流萤。天阶夜色凉如水,坐看牵牛织女星。”这是唐代诗人杜牧的诗句,它能让我们想象夜空中与星光媲美的点点流萤。可你是否曾经思考过下面的有关生物学问题:
萤火虫体内有特殊的发光物质吗?萤火虫发光的过程有能量的转化吗?萤火虫体内的化学反应为什么在常温常压下可以迅速而又规律的进行
新课讲授
忆旧引新
生物体进行各项生命活动的主要能源物质-------糖类
生物体进行各项生命活动的主要储能物质-------脂肪
生物体进行各项生命活动的最终(根本)能源-----光能
生物体进行各项生命活动的直接能源物质-----ATP(为什么?)
实验探究:
用小刀将数十只荧光虫的发光器割下,干燥后砚成粉末,取两等分分别装入两只试管中,各加入等量的水,使之混合,可见到试管中发出淡黄色荧光,约过15分钟荧光消失,这时,再将ATP溶液加入其中一只试管,将葡萄糖溶液加入另一只试管中,发现加ATP溶液的试管中发出荧光,而加葡萄糖溶液的试管中不发光。
提问:
1. 为什么加水后发荧光?
2. 为什么约15分钟荧光消失?
3. 为什么加ATP溶液的试管发荧光,而加葡萄糖溶液的试管不发荧光?
4. 通过本实验可得出什么结论?
组织学生讨论得出结论:
1. 加水发荧光是因为有ATP存在
2. 约15分钟消失是因为ATP已经消耗完了
3. 因为ATP是生命活动的直接能源物质,而葡萄糖不是
4. ATP是生命活动所需能量的直接来源
ATP为什么是能量的直接来源,而葡萄糖等其他物质不是呢?
这就和ATP的分子结构有关系
ATP的分子结构
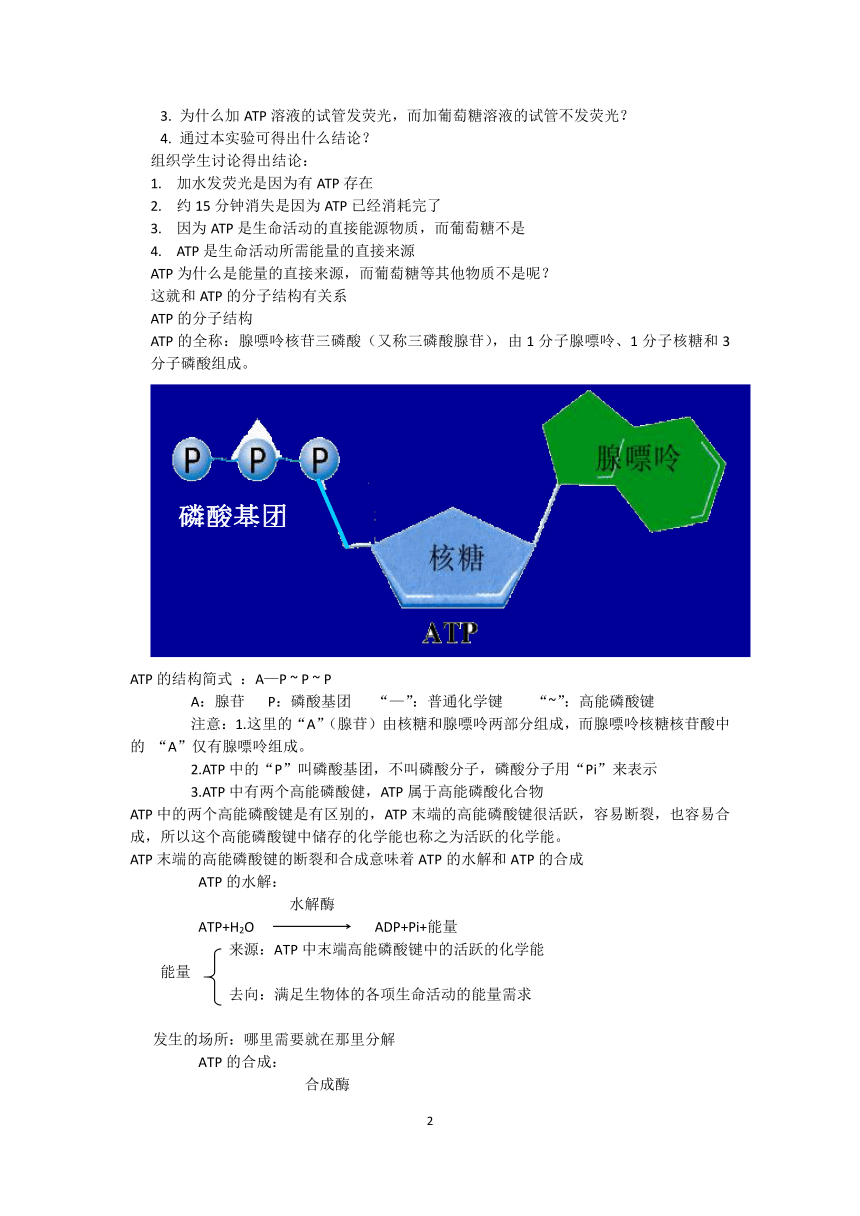
ATP的全称:腺嘌呤核苷三磷酸(又称三磷酸腺苷),由1分子腺嘌呤、1分子核糖和3分子磷酸组成。
ATP的结构简式 :A—P ~ P ~ P
A:腺苷 P:磷酸基团 “—”:普通化学键 “~”:高能磷酸键
注意:1.这里的“A”(腺苷)由核糖和腺嘌呤两部分组成,而腺嘌呤核糖核苷酸中的 “A”仅有腺嘌呤组成。
2.ATP中的“P”叫磷酸基团,不叫磷酸分子,磷酸分子用“Pi”来表示
3.ATP中有两个高能磷酸健,ATP属于高能磷酸化合物
ATP中的两个高能磷酸键是有区别的,ATP末端的高能磷酸键很活跃,容易断裂,也容易合成,所以这个高能磷酸键中储存的化学能也称之为活跃的化学能。
ATP末端的高能磷酸键的断裂和合成意味着ATP的水解和ATP的合成
ATP的水解:
水解酶
ATP+H2O ADP+Pi+能量
来源:ATP中末端高能磷酸键中的活跃的化学能
能量
去向:满足生物体的各项生命活动的能量需求
发生的场所:哪里需要就在那里分解
ATP的合成:
合成酶
ADP+Pi+能量 ATP+H2O
来源:有机物中稳定的化学能、光能
能量
去向:ATP中末端高能磷酸键中的活跃的化学能
产生ATP的生理反应:呼吸作用和光合作用
产生ATP的场所:细胞质基质、线粒体、叶绿体
注意:ATP的水解和ATP的合成反应不是可逆反应,原因由三:
1.这两个反应的能量来源与去向不一样
2.这两个反应场所不一样
3.这两个反应的条件不一样
但是这两个反应可以说物质是可逆的,
通过上面的讲述及前面所学的知识就可以看出ATP是能量的直接来源的原因:
1. ATP的结构中有一个很活跃的高能磷酸键,导致它在供能时很方便,而糖类等其他的有机物中的化学能很稳定,就不具备这个特点。
2. ATP的分解可直接进行,但糖类等有机物的分解离不开线粒体,这也使得ATP成为各项生命活动的直接能量来源的最佳选择。
ATP虽然是生物体各项生命活动所需能量的直接来源,但ATP在细胞内的含量是很少的,也就是ATP在一个很低的水平上保持了一个动态平衡,之所以这样,也是因为ATP中的远离“A”的高能磷酸健很活跃,它很容易合成也很容易断裂。
课堂小结:
本节课主要是讲了ATP的结构,通过ATP的结构使学生认识到为什么ATP是生物体的各项生命活动所需能量的直接来源。
课堂评价练习:
1. 萤火虫发光所需的能量来自()
A. 葡萄糖B.蛋白质C.脂肪D.ATP
2. ATP转化为ADP可表示如下,式中的X代表()
能量 X
酶
ATP ADP
A.H20 B.[H] C.P D.Pi
3. ATP的结构简式是 ,其中A代表 ,T代表
,P代表 , 代表高能磷酸键。
4.写出ATP与ADP相互转变的反应式 。
5.动物细胞中,ADP转化为ATP的能量主要来自 作用,对于植物来说,ADP转化为ATP的能量还可以来自 作用。在生物体内,ATP水解成
ADP时,释放的能量直接用于 。
(第二课时)
课标要求
1.知识目标:说出酶的本质;举例说明酶的特性,举例说明酶促反应的过程;说明影响酶活性的因素。
2.能力目标:尝试完成实验一,说出酶的催化效率很高;操作完成实验二,说明酶的催化作用具有特异性;观察教科书第49页图4—4,说明酶促反应的过称;使用推荐器材,进行课题研究,交流影响酶作用的因素。
3.情感目标:参与实践活动和课题研究;与同学探讨酶的特性、酶促反应的过程和影响没活动的因素;通过实验、课题研究等,确立事实求是的学习态度。
教学重点
1.说出酶的本质。
1. 边做边学:酶的特性。
2. 酶促反应的过程。
3. 课题研究:影响酶作用速率的因素
教学难点
1. 实验一:说明为什么选用新鲜的酵母菌液和蒸馏水进行实验
2. 完成实验二并进行讨论。
3. 完成课题研究,说明酶的活性受PH、温度、酶的浓度、底物浓度影响。
教学手段
实验探究
教学方法
实验法、讨论法、分析法、探究式学习
课时安排
一课时
教学过称
引入
萤火虫体内的化学反应为什么能在常温常压下迅速而又规律的进行?
而平常学生在实验室所作的化学反应能进行他们又都做了什么?
通过学生的讨论引入本节课的内容。
新课讲授
酶的概念:
酶通常指由活细胞产生的、具有催化活性的一类特殊的蛋白质,又称为生物催化剂
化学成分:绝大多数为蛋白质,少数酶为RNA
产生的场所:活细胞,凡是活细胞都能产生酶,在细胞内的核糖体上面或细胞核中产生。
作用:催化作用,而且只有催化作用。
发挥作用的场所:可以在细胞内,也可以在细胞外。
认识酶:
1. 酶的特性
实验一:酶具有催化性
实验目的 通过比较H2O2在不同条件下分解的速率,了解过氧化氢酶的作用和意义
实验原理 过氧化氢在一定催化剂的作用下分解成氧气和水
方法步骤 试管编号 1 2
H2O2溶液 3mL 3mL
单一变量 2滴新鲜的酵母菌溶液 2滴蒸馏水
实验观察(气泡的多少 很多气泡使卫生香燃烧猛烈 无气泡
组织学生讨论下列问题:
1. 为什么要设置2号试管?起什么作用?
2. 本实验中什么是变量?对照组?实验组?两只试管除了变量不同外,其他的呢?
3. 加入新鲜的酵母菌溶液后预计会有何种现象?气泡的成分是什么?如何证明?
4. 1号试管产生气泡的量比2号试管多的多,且卫生香燃烧很猛烈。为什么会出现这一现象?说明酶具有什么作用?并具备什么特性?
5. 如果不用新鲜的酵母菌溶液能否得到上述现象
学生在老师的引导下经过讨论就会得出:
1. 设置2号试管的作用在于对照,排出无关变量对实验过程造成的影响
2. 变量为有无酶的存在,对照组为2号试管,实验组为1号试管,
3. 预计会产生气泡,成分为O2,通过O2具有助燃作用来证明
4. 说明酶具有催化作用,而且具有高效性。
5. 不能。
实验二:酶具有特异性
实验目的 通过比较淀粉酶对淀粉和蔗糖的分解,了解酶的特性
实验原理 淀粉和蔗糖都是非还原性糖,用斐林试剂鉴定不会产生砖红色沉淀,可它们在酶的催化作用下都可分解产生还原性糖,用斐林试剂鉴定就会产生砖红色沉淀,但酶具有特异性,淀粉酶只能催化淀粉的分解
方法步骤 试管编号 1 2
3%的可溶性淀粉溶液 2mL
3%的蔗糖溶液 2mL
2%的新鲜淀粉酶溶液 2mL(振荡) 2mL(振荡)
60℃的水温保温 5min 5min
加入斐林试剂 2mL(振荡) 2mL(振荡)
水浴煮沸 1min 1min
现象记录 有砖红色沉淀 无砖红色沉淀
组织学生讨论一下问题:
1. 这个实验中采用了那种酶?反应的底物是什么?
2. 通过那些现象能够说明酶的催化作用?
3. 保温和加热的目的是什么?
4. 这个实验能说明酶具有什么特性?
5. 这个实验能否确定淀粉酶只能催化淀粉的水解?
6. 能否将检测用的试剂改成碘液?
学生在老师的引导下通过讨论可以得出
1. 这个实验采用了淀粉酶,反应的底物是淀粉和蔗糖
2. 加入斐林试剂后,溶液中生成了砖红色沉淀。因为还原性糖与斐林试剂反应,说明淀粉被分解,产生了还原兴糖
3. 保温是提供酶反应所需要的最适宜的温度,加热是为了加快还原糖与斐林试剂反应的速度
4. 淀粉酶只能催化淀粉的分解,说明酶的作用具有特异性
5. 能确定,因为用斐林试剂测定淀粉的水解产物,发现产生了还原性糖。而蔗糖溶液则没有产生还原性糖
6. 不能改,若将斐林试剂改为碘液,只能说明有无淀粉,不能说明是否产生还原性糖,所以不能改
教师和学生共同总结:像上述这样,由酶催化的化学反应叫酶促反应。
而酶所具备的特性就是高效性和特异性。
为什么酶具有高效性?
指导学生阅读课本中的知识海洋
在这里只是让学生了解一下,知道酶具有高效性的原因:
它可以降低化学反应的活化能,从而让化学反应可以在常温、常压、适宜的PH等温和条件下就可以迅速而有规律的进行。
为什么酶具有特异性?教师要求学生在观察图示后,说明酶和底物的关系
1. 关键:酶的活性中心
2. 关系:酶的活性中心与底物分子的关系就像锁和钥匙的关系,所以酶具有特异性
3. 从课本上的图示还可以发现酶参与反应过程,催化化学反应的进行,与其他的催化剂一样,反应前后酶本身的形态结构并没有发生什么变化,它只是加快了反应的速率。
而且通过上述的两个实验还可以发现
酶在发挥它的作用的时候需要一定的条件,比如说第一个实验必须用新鲜的酵母菌液,第二个实验必须要保温。这是因为酶有活性。而很多因素都会影响到酶的活性。
由此引出酶的活性的概念
酶的活性:酶对化学反应的催化效率称为酶的活性,用反应速率来表示。
课题研究:
那些因素会影响酶的活性即酶促反应的速率呢?
1. 教师提出探究要求:
仔细阅读教材,明确研究目的,了解实验器材,分析研究指导,观察图示说明,选择实验课题,做出合理假设,积极参与实验。
2. 学生参与探究活动:
小组讨论,提出问题,做出假设,设计实验,进行实验,观察实验,收集证据,交流合作,得出结果。
3. 明确培养干酵母形成新鲜酵母菌液的方法,酵母菌细胞中的酶参与有关生物化学反应。
4. 实验分组参考:
每个小组可选择一个变量,设置一个实验组,如:
探究:温度对酶作用速率的影响
实验假说:温度影响酶作用的速率。
实验器材:冰箱 烧杯 试管 量筒 温度计 酒精灯 淀粉溶液 稀释的唾液 碘液
等
实验步骤:
试管编号 1 2 3 4 5 6 7 8
可溶性淀粉溶液 2mL 2mL 2mL 2mL 2mL 2mL 2mL 2mL
温度控制5分钟 0℃ 17℃ 27℃ 37℃ 47℃ 57℃ 67℃ 100℃
另一组试管编号 1 2 3 4 5 6 7 8
稀释的唾液 2mL 2mL 2mL 2mL 2mL 2mL 2mL 2mL
温度控制5分钟 0℃ 17℃ 27℃ 37℃ 47℃ 57℃ 67℃ 100℃
将稀释的唾液分别加入到对应温度的试管中,再水浴保持相应温度5分钟
取出试管,加入碘液2~3滴,观察颜色变化,用“+”表示颜色变化的深浅
实验数据与分析
试管号实验数据 1 2 3 4 5 6 7 8
加入碘液后颜色变化 +++ ++ + — + +++ +++ +++
数据分析(酶作用速度) — + ++ +++ ++ — — —
关于实验数据的分析说明:试验中,加入碘液后颜色变化越明显,直接表明淀粉被水解的越少,间接证明酶在该温度下的催化活性越低,酶作用速率越低;反之,则相反。
教师提出下列问题,学生进行实验或讨论:
1. 假如试验中将碘液换成斐林试剂,后水浴加热会出现怎样的结果?
学生探究的结果:在试管4中出现的砖红色沉淀最明显,而1、7、8试管几乎无沉淀。
2.假如进行重复实验,在加碘液之前,将实验中的试管1、7、8再置于37℃的条件下水浴5分钟,有何现象?
学生探究结果:试管1中加入碘液后无颜色变化,(不显蓝色);而7、8试管加入碘液显蓝色。
3. 上述实验说明了什么
学生讨论的结果:说明了在0℃时,酶的活性会受到抑制,但在一定范围内温度升高其活性会增加,说明这种低温导致的酶的活性的降低是可以被恢复的:而在57℃、67℃、100℃时,酶的活性会受到抑制,并且随着温度的降低,其活性不再变化,说明高温导致的这种活性的降低时不可以被恢复的。
4. 能否根据数学的函数思想,绘出唾液淀粉酶作用速率与温度之间关系的函数示意图?你能否对该函数图进行解释?
学生自主完成(见下图)
学生解释:说明酶的催化活性需要适宜的温度范围,并
且特定的酶具有一个特定的最适宜温度;在最适温度范
围内随着温度的升高,酶作用的速率增加;超过最适温
度范围后,随着温度的升高,酶作用速率降低,最终失
去活性;低温对酶活性的抑制是可以恢复的,而高温导
致酶的活性丧失是不可以恢复的。为什么呢?
老师进行解释:
高温导致了酶的空间结构的破坏,而这种破坏是不可以恢复的,因而酶的活性中心失去其催化活性;低温仅抑制了酶的活性中心的催化能力,并没有破坏酶的空间结构,所以这种酶活性的降低是可以被恢复的。
5.有些细菌生活在火山喷发口,也有一些生物生活在温泉中,你如何解释这种现象呢?
小组讨论、代表发言:生活在这些环境中的生物,其体内的酶与人体内的酶的种类是不同的,所以所需要的最适温度与人的不同。
6.人体内有许多种酶,这些酶所需的最适温度都相同吗?
老师解释:人体内不同的酶所需要的最适温度是有所不同的,但大多是37℃左右。
参照本探究实验及课本上的PH对酶活性的影响的实验,再深入探究酶的浓度、底物浓度对酶促反应的影响。
课堂小结:
酶促反应的速率受到多种因素的共同影响,单单考虑一种因素而忽略另一种因素都是不可取的,研究其中一种因素的作用,要注意控制变量。
引导学生阅读“放眼社会”的“酶与疾病”,让学生了解酶和疾病的关系,如先天性酶缺陷病、酶的活性变化而导致疾病的产生、酶的诊断和治疗疾病中的应用,更重要的是理解酶是生物体内进行新陈代谢的重要物质。教师还可以鼓励学生收集社会生活中,尤其是医疗卫生事业中有关酶的应用的例子。
学生活动:阅读“酶与疾病”,利用网络、图书馆、报刊等途径,通过资料收集与整理、实地走访与考察等多种方式,写出一片有关“酶与疾病”的调查报告。
课堂评价练习:
1.下列有关酶的叙述正确的是 ( )
A.活细胞产生的,在细胞内起作用 B.酶和激素的作用相同
C.酶的产生受遗传物质控制 D.在催化过程中不断被消耗
2.催化淀粉酶水解的酶是 ( )
A.肽酶 B.蛋白酶 C.脂肪酶 D.淀粉酶
3.将乳清蛋白、淀粉、胃蛋白酶、唾液淀粉酶和适量水混合装入一容器内,调整pH至2.0,保存在37℃的水浴锅内。过一段时间后,容器内剩余的物质是 ( )
A.淀粉、胃蛋白酶、多肽、水
B.唾液淀粉酶、麦芽糖、胃蛋白酶、多肽、水
C.唾液淀粉酶、胃蛋白酶、多肽、水
D.唾液淀粉酶、淀粉、胃蛋白酶、水
4.胰蛋白酶作用于一定量的某种物质(底物),温度保持37℃,pH保持在最适值,生成物量与反应时间关系如下图,请回答下列问题:
(1)该酶作用的底物是______________。
(2)在140分钟后,曲线变成水平,这是因为_______________。
(3)若增加胰蛋白酶浓度,其他条件不变,请在原图上画出生成物量变化的示意曲线。
(4)若胰蛋白酶浓度和其他条件不变,反应液pH值由2逐渐升高到10,则酶催化应的速度将___________,原因是___________。
(5)下图中能正确表示胰蛋白酶对底物的分解速度和温度关系的是( )
反
应
速
率
最适温度
温度
磷酸基团
8
第一节ATP和酶
(第一课时)
备课人:康娟盈
课标要求
1.知识目标:简述ATP的化学组成和特点并写出ATP的分子简式;解释ATP在能量代谢中的作用。
2.能力目标:通过ATP与ADP相互转换示意图,初步形成图文转化能力和用规范的生物学语言来表述问题的能力。
3情感目标:通过小组学习过程中的合作与交往培养学生的协作意识与交往的态度.
教学重点
ATP的分子特点和ATP与ADP的相互转化在新陈代谢中的作用及特点
教学难点
ATP在能量的储存、转移和利用中的作用
教学方法
实验探究、分析法
课时安排
一课时
教学过程
引入
“银烛秋光冷画屏,轻罗小衫扑流萤。天阶夜色凉如水,坐看牵牛织女星。”这是唐代诗人杜牧的诗句,它能让我们想象夜空中与星光媲美的点点流萤。可你是否曾经思考过下面的有关生物学问题:
萤火虫体内有特殊的发光物质吗?萤火虫发光的过程有能量的转化吗?萤火虫体内的化学反应为什么在常温常压下可以迅速而又规律的进行
新课讲授
忆旧引新
生物体进行各项生命活动的主要能源物质-------糖类
生物体进行各项生命活动的主要储能物质-------脂肪
生物体进行各项生命活动的最终(根本)能源-----光能
生物体进行各项生命活动的直接能源物质-----ATP(为什么?)
实验探究:
用小刀将数十只荧光虫的发光器割下,干燥后砚成粉末,取两等分分别装入两只试管中,各加入等量的水,使之混合,可见到试管中发出淡黄色荧光,约过15分钟荧光消失,这时,再将ATP溶液加入其中一只试管,将葡萄糖溶液加入另一只试管中,发现加ATP溶液的试管中发出荧光,而加葡萄糖溶液的试管中不发光。
提问:
1. 为什么加水后发荧光?
2. 为什么约15分钟荧光消失?
3. 为什么加ATP溶液的试管发荧光,而加葡萄糖溶液的试管不发荧光?
4. 通过本实验可得出什么结论?
组织学生讨论得出结论:
1. 加水发荧光是因为有ATP存在
2. 约15分钟消失是因为ATP已经消耗完了
3. 因为ATP是生命活动的直接能源物质,而葡萄糖不是
4. ATP是生命活动所需能量的直接来源
ATP为什么是能量的直接来源,而葡萄糖等其他物质不是呢?
这就和ATP的分子结构有关系
ATP的分子结构
ATP的全称:腺嘌呤核苷三磷酸(又称三磷酸腺苷),由1分子腺嘌呤、1分子核糖和3分子磷酸组成。
ATP的结构简式 :A—P ~ P ~ P
A:腺苷 P:磷酸基团 “—”:普通化学键 “~”:高能磷酸键
注意:1.这里的“A”(腺苷)由核糖和腺嘌呤两部分组成,而腺嘌呤核糖核苷酸中的 “A”仅有腺嘌呤组成。
2.ATP中的“P”叫磷酸基团,不叫磷酸分子,磷酸分子用“Pi”来表示
3.ATP中有两个高能磷酸健,ATP属于高能磷酸化合物
ATP中的两个高能磷酸键是有区别的,ATP末端的高能磷酸键很活跃,容易断裂,也容易合成,所以这个高能磷酸键中储存的化学能也称之为活跃的化学能。
ATP末端的高能磷酸键的断裂和合成意味着ATP的水解和ATP的合成
ATP的水解:
水解酶
ATP+H2O ADP+Pi+能量
来源:ATP中末端高能磷酸键中的活跃的化学能
能量
去向:满足生物体的各项生命活动的能量需求
发生的场所:哪里需要就在那里分解
ATP的合成:
合成酶
ADP+Pi+能量 ATP+H2O
来源:有机物中稳定的化学能、光能
能量
去向:ATP中末端高能磷酸键中的活跃的化学能
产生ATP的生理反应:呼吸作用和光合作用
产生ATP的场所:细胞质基质、线粒体、叶绿体
注意:ATP的水解和ATP的合成反应不是可逆反应,原因由三:
1.这两个反应的能量来源与去向不一样
2.这两个反应场所不一样
3.这两个反应的条件不一样
但是这两个反应可以说物质是可逆的,
通过上面的讲述及前面所学的知识就可以看出ATP是能量的直接来源的原因:
1. ATP的结构中有一个很活跃的高能磷酸键,导致它在供能时很方便,而糖类等其他的有机物中的化学能很稳定,就不具备这个特点。
2. ATP的分解可直接进行,但糖类等有机物的分解离不开线粒体,这也使得ATP成为各项生命活动的直接能量来源的最佳选择。
ATP虽然是生物体各项生命活动所需能量的直接来源,但ATP在细胞内的含量是很少的,也就是ATP在一个很低的水平上保持了一个动态平衡,之所以这样,也是因为ATP中的远离“A”的高能磷酸健很活跃,它很容易合成也很容易断裂。
课堂小结:
本节课主要是讲了ATP的结构,通过ATP的结构使学生认识到为什么ATP是生物体的各项生命活动所需能量的直接来源。
课堂评价练习:
1. 萤火虫发光所需的能量来自()
A. 葡萄糖B.蛋白质C.脂肪D.ATP
2. ATP转化为ADP可表示如下,式中的X代表()
能量 X
酶
ATP ADP
A.H20 B.[H] C.P D.Pi
3. ATP的结构简式是 ,其中A代表 ,T代表
,P代表 , 代表高能磷酸键。
4.写出ATP与ADP相互转变的反应式 。
5.动物细胞中,ADP转化为ATP的能量主要来自 作用,对于植物来说,ADP转化为ATP的能量还可以来自 作用。在生物体内,ATP水解成
ADP时,释放的能量直接用于 。
(第二课时)
课标要求
1.知识目标:说出酶的本质;举例说明酶的特性,举例说明酶促反应的过程;说明影响酶活性的因素。
2.能力目标:尝试完成实验一,说出酶的催化效率很高;操作完成实验二,说明酶的催化作用具有特异性;观察教科书第49页图4—4,说明酶促反应的过称;使用推荐器材,进行课题研究,交流影响酶作用的因素。
3.情感目标:参与实践活动和课题研究;与同学探讨酶的特性、酶促反应的过程和影响没活动的因素;通过实验、课题研究等,确立事实求是的学习态度。
教学重点
1.说出酶的本质。
1. 边做边学:酶的特性。
2. 酶促反应的过程。
3. 课题研究:影响酶作用速率的因素
教学难点
1. 实验一:说明为什么选用新鲜的酵母菌液和蒸馏水进行实验
2. 完成实验二并进行讨论。
3. 完成课题研究,说明酶的活性受PH、温度、酶的浓度、底物浓度影响。
教学手段
实验探究
教学方法
实验法、讨论法、分析法、探究式学习
课时安排
一课时
教学过称
引入
萤火虫体内的化学反应为什么能在常温常压下迅速而又规律的进行?
而平常学生在实验室所作的化学反应能进行他们又都做了什么?
通过学生的讨论引入本节课的内容。
新课讲授
酶的概念:
酶通常指由活细胞产生的、具有催化活性的一类特殊的蛋白质,又称为生物催化剂
化学成分:绝大多数为蛋白质,少数酶为RNA
产生的场所:活细胞,凡是活细胞都能产生酶,在细胞内的核糖体上面或细胞核中产生。
作用:催化作用,而且只有催化作用。
发挥作用的场所:可以在细胞内,也可以在细胞外。
认识酶:
1. 酶的特性
实验一:酶具有催化性
实验目的 通过比较H2O2在不同条件下分解的速率,了解过氧化氢酶的作用和意义
实验原理 过氧化氢在一定催化剂的作用下分解成氧气和水
方法步骤 试管编号 1 2
H2O2溶液 3mL 3mL
单一变量 2滴新鲜的酵母菌溶液 2滴蒸馏水
实验观察(气泡的多少 很多气泡使卫生香燃烧猛烈 无气泡
组织学生讨论下列问题:
1. 为什么要设置2号试管?起什么作用?
2. 本实验中什么是变量?对照组?实验组?两只试管除了变量不同外,其他的呢?
3. 加入新鲜的酵母菌溶液后预计会有何种现象?气泡的成分是什么?如何证明?
4. 1号试管产生气泡的量比2号试管多的多,且卫生香燃烧很猛烈。为什么会出现这一现象?说明酶具有什么作用?并具备什么特性?
5. 如果不用新鲜的酵母菌溶液能否得到上述现象
学生在老师的引导下经过讨论就会得出:
1. 设置2号试管的作用在于对照,排出无关变量对实验过程造成的影响
2. 变量为有无酶的存在,对照组为2号试管,实验组为1号试管,
3. 预计会产生气泡,成分为O2,通过O2具有助燃作用来证明
4. 说明酶具有催化作用,而且具有高效性。
5. 不能。
实验二:酶具有特异性
实验目的 通过比较淀粉酶对淀粉和蔗糖的分解,了解酶的特性
实验原理 淀粉和蔗糖都是非还原性糖,用斐林试剂鉴定不会产生砖红色沉淀,可它们在酶的催化作用下都可分解产生还原性糖,用斐林试剂鉴定就会产生砖红色沉淀,但酶具有特异性,淀粉酶只能催化淀粉的分解
方法步骤 试管编号 1 2
3%的可溶性淀粉溶液 2mL
3%的蔗糖溶液 2mL
2%的新鲜淀粉酶溶液 2mL(振荡) 2mL(振荡)
60℃的水温保温 5min 5min
加入斐林试剂 2mL(振荡) 2mL(振荡)
水浴煮沸 1min 1min
现象记录 有砖红色沉淀 无砖红色沉淀
组织学生讨论一下问题:
1. 这个实验中采用了那种酶?反应的底物是什么?
2. 通过那些现象能够说明酶的催化作用?
3. 保温和加热的目的是什么?
4. 这个实验能说明酶具有什么特性?
5. 这个实验能否确定淀粉酶只能催化淀粉的水解?
6. 能否将检测用的试剂改成碘液?
学生在老师的引导下通过讨论可以得出
1. 这个实验采用了淀粉酶,反应的底物是淀粉和蔗糖
2. 加入斐林试剂后,溶液中生成了砖红色沉淀。因为还原性糖与斐林试剂反应,说明淀粉被分解,产生了还原兴糖
3. 保温是提供酶反应所需要的最适宜的温度,加热是为了加快还原糖与斐林试剂反应的速度
4. 淀粉酶只能催化淀粉的分解,说明酶的作用具有特异性
5. 能确定,因为用斐林试剂测定淀粉的水解产物,发现产生了还原性糖。而蔗糖溶液则没有产生还原性糖
6. 不能改,若将斐林试剂改为碘液,只能说明有无淀粉,不能说明是否产生还原性糖,所以不能改
教师和学生共同总结:像上述这样,由酶催化的化学反应叫酶促反应。
而酶所具备的特性就是高效性和特异性。
为什么酶具有高效性?
指导学生阅读课本中的知识海洋
在这里只是让学生了解一下,知道酶具有高效性的原因:
它可以降低化学反应的活化能,从而让化学反应可以在常温、常压、适宜的PH等温和条件下就可以迅速而有规律的进行。
为什么酶具有特异性?教师要求学生在观察图示后,说明酶和底物的关系
1. 关键:酶的活性中心
2. 关系:酶的活性中心与底物分子的关系就像锁和钥匙的关系,所以酶具有特异性
3. 从课本上的图示还可以发现酶参与反应过程,催化化学反应的进行,与其他的催化剂一样,反应前后酶本身的形态结构并没有发生什么变化,它只是加快了反应的速率。
而且通过上述的两个实验还可以发现
酶在发挥它的作用的时候需要一定的条件,比如说第一个实验必须用新鲜的酵母菌液,第二个实验必须要保温。这是因为酶有活性。而很多因素都会影响到酶的活性。
由此引出酶的活性的概念
酶的活性:酶对化学反应的催化效率称为酶的活性,用反应速率来表示。
课题研究:
那些因素会影响酶的活性即酶促反应的速率呢?
1. 教师提出探究要求:
仔细阅读教材,明确研究目的,了解实验器材,分析研究指导,观察图示说明,选择实验课题,做出合理假设,积极参与实验。
2. 学生参与探究活动:
小组讨论,提出问题,做出假设,设计实验,进行实验,观察实验,收集证据,交流合作,得出结果。
3. 明确培养干酵母形成新鲜酵母菌液的方法,酵母菌细胞中的酶参与有关生物化学反应。
4. 实验分组参考:
每个小组可选择一个变量,设置一个实验组,如:
探究:温度对酶作用速率的影响
实验假说:温度影响酶作用的速率。
实验器材:冰箱 烧杯 试管 量筒 温度计 酒精灯 淀粉溶液 稀释的唾液 碘液
等
实验步骤:
试管编号 1 2 3 4 5 6 7 8
可溶性淀粉溶液 2mL 2mL 2mL 2mL 2mL 2mL 2mL 2mL
温度控制5分钟 0℃ 17℃ 27℃ 37℃ 47℃ 57℃ 67℃ 100℃
另一组试管编号 1 2 3 4 5 6 7 8
稀释的唾液 2mL 2mL 2mL 2mL 2mL 2mL 2mL 2mL
温度控制5分钟 0℃ 17℃ 27℃ 37℃ 47℃ 57℃ 67℃ 100℃
将稀释的唾液分别加入到对应温度的试管中,再水浴保持相应温度5分钟
取出试管,加入碘液2~3滴,观察颜色变化,用“+”表示颜色变化的深浅
实验数据与分析
试管号实验数据 1 2 3 4 5 6 7 8
加入碘液后颜色变化 +++ ++ + — + +++ +++ +++
数据分析(酶作用速度) — + ++ +++ ++ — — —
关于实验数据的分析说明:试验中,加入碘液后颜色变化越明显,直接表明淀粉被水解的越少,间接证明酶在该温度下的催化活性越低,酶作用速率越低;反之,则相反。
教师提出下列问题,学生进行实验或讨论:
1. 假如试验中将碘液换成斐林试剂,后水浴加热会出现怎样的结果?
学生探究的结果:在试管4中出现的砖红色沉淀最明显,而1、7、8试管几乎无沉淀。
2.假如进行重复实验,在加碘液之前,将实验中的试管1、7、8再置于37℃的条件下水浴5分钟,有何现象?
学生探究结果:试管1中加入碘液后无颜色变化,(不显蓝色);而7、8试管加入碘液显蓝色。
3. 上述实验说明了什么
学生讨论的结果:说明了在0℃时,酶的活性会受到抑制,但在一定范围内温度升高其活性会增加,说明这种低温导致的酶的活性的降低是可以被恢复的:而在57℃、67℃、100℃时,酶的活性会受到抑制,并且随着温度的降低,其活性不再变化,说明高温导致的这种活性的降低时不可以被恢复的。
4. 能否根据数学的函数思想,绘出唾液淀粉酶作用速率与温度之间关系的函数示意图?你能否对该函数图进行解释?
学生自主完成(见下图)
学生解释:说明酶的催化活性需要适宜的温度范围,并
且特定的酶具有一个特定的最适宜温度;在最适温度范
围内随着温度的升高,酶作用的速率增加;超过最适温
度范围后,随着温度的升高,酶作用速率降低,最终失
去活性;低温对酶活性的抑制是可以恢复的,而高温导
致酶的活性丧失是不可以恢复的。为什么呢?
老师进行解释:
高温导致了酶的空间结构的破坏,而这种破坏是不可以恢复的,因而酶的活性中心失去其催化活性;低温仅抑制了酶的活性中心的催化能力,并没有破坏酶的空间结构,所以这种酶活性的降低是可以被恢复的。
5.有些细菌生活在火山喷发口,也有一些生物生活在温泉中,你如何解释这种现象呢?
小组讨论、代表发言:生活在这些环境中的生物,其体内的酶与人体内的酶的种类是不同的,所以所需要的最适温度与人的不同。
6.人体内有许多种酶,这些酶所需的最适温度都相同吗?
老师解释:人体内不同的酶所需要的最适温度是有所不同的,但大多是37℃左右。
参照本探究实验及课本上的PH对酶活性的影响的实验,再深入探究酶的浓度、底物浓度对酶促反应的影响。
课堂小结:
酶促反应的速率受到多种因素的共同影响,单单考虑一种因素而忽略另一种因素都是不可取的,研究其中一种因素的作用,要注意控制变量。
引导学生阅读“放眼社会”的“酶与疾病”,让学生了解酶和疾病的关系,如先天性酶缺陷病、酶的活性变化而导致疾病的产生、酶的诊断和治疗疾病中的应用,更重要的是理解酶是生物体内进行新陈代谢的重要物质。教师还可以鼓励学生收集社会生活中,尤其是医疗卫生事业中有关酶的应用的例子。
学生活动:阅读“酶与疾病”,利用网络、图书馆、报刊等途径,通过资料收集与整理、实地走访与考察等多种方式,写出一片有关“酶与疾病”的调查报告。
课堂评价练习:
1.下列有关酶的叙述正确的是 ( )
A.活细胞产生的,在细胞内起作用 B.酶和激素的作用相同
C.酶的产生受遗传物质控制 D.在催化过程中不断被消耗
2.催化淀粉酶水解的酶是 ( )
A.肽酶 B.蛋白酶 C.脂肪酶 D.淀粉酶
3.将乳清蛋白、淀粉、胃蛋白酶、唾液淀粉酶和适量水混合装入一容器内,调整pH至2.0,保存在37℃的水浴锅内。过一段时间后,容器内剩余的物质是 ( )
A.淀粉、胃蛋白酶、多肽、水
B.唾液淀粉酶、麦芽糖、胃蛋白酶、多肽、水
C.唾液淀粉酶、胃蛋白酶、多肽、水
D.唾液淀粉酶、淀粉、胃蛋白酶、水
4.胰蛋白酶作用于一定量的某种物质(底物),温度保持37℃,pH保持在最适值,生成物量与反应时间关系如下图,请回答下列问题:
(1)该酶作用的底物是______________。
(2)在140分钟后,曲线变成水平,这是因为_______________。
(3)若增加胰蛋白酶浓度,其他条件不变,请在原图上画出生成物量变化的示意曲线。
(4)若胰蛋白酶浓度和其他条件不变,反应液pH值由2逐渐升高到10,则酶催化应的速度将___________,原因是___________。
(5)下图中能正确表示胰蛋白酶对底物的分解速度和温度关系的是( )
反
应
速
率
最适温度
温度
磷酸基团
8
