人教版九年级下册 第九单元 溶液 课题2溶解度
文档属性
| 名称 | 人教版九年级下册 第九单元 溶液 课题2溶解度 |

|
|
| 格式 | zip | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-06 00:00:00 | ||
图片预览









文档简介
(共33张PPT)
课题2 溶 解 度
不行
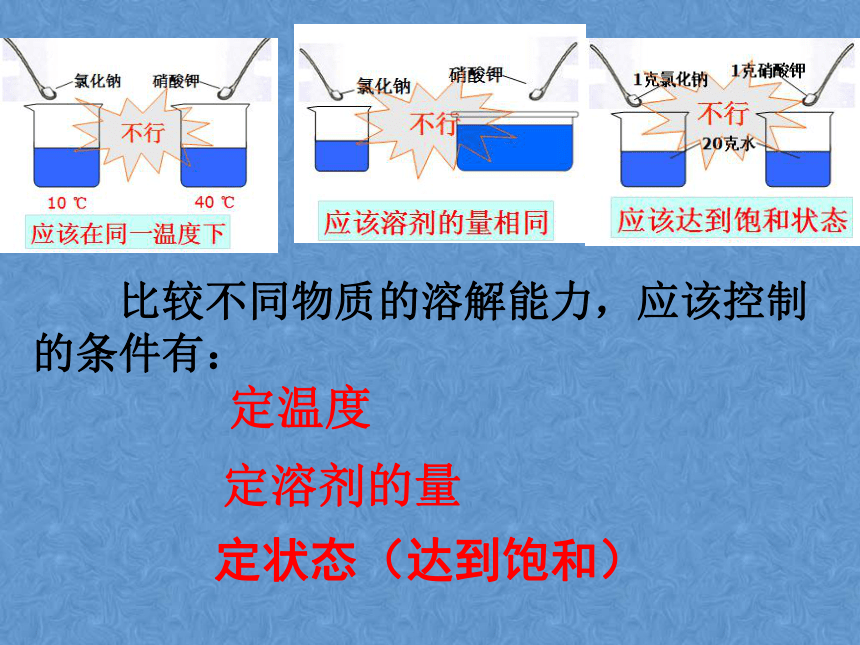
应该在同一温度下
这样行吗?
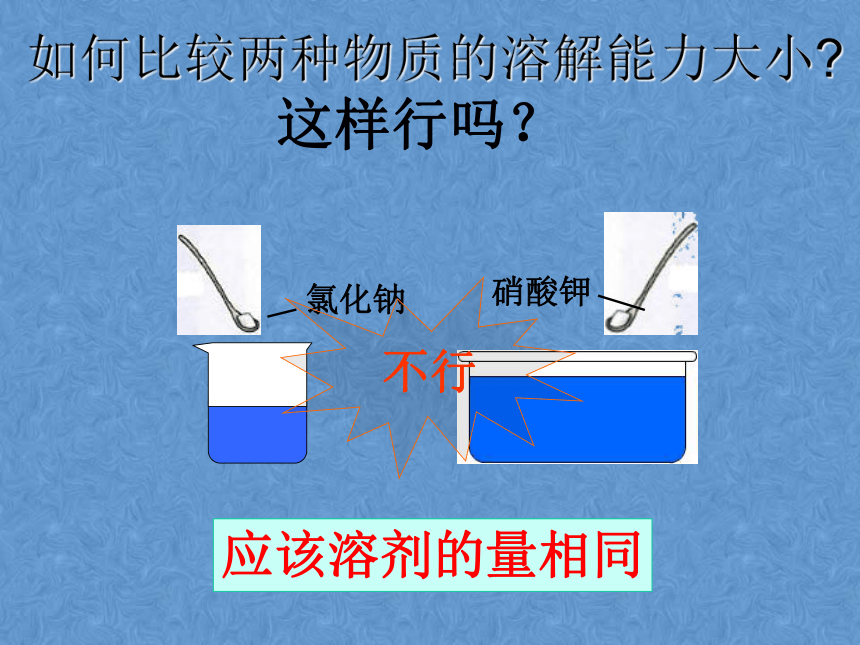
如何比较两种物质的溶解能力大小?
应该溶剂的量相同
不行
这样行吗?
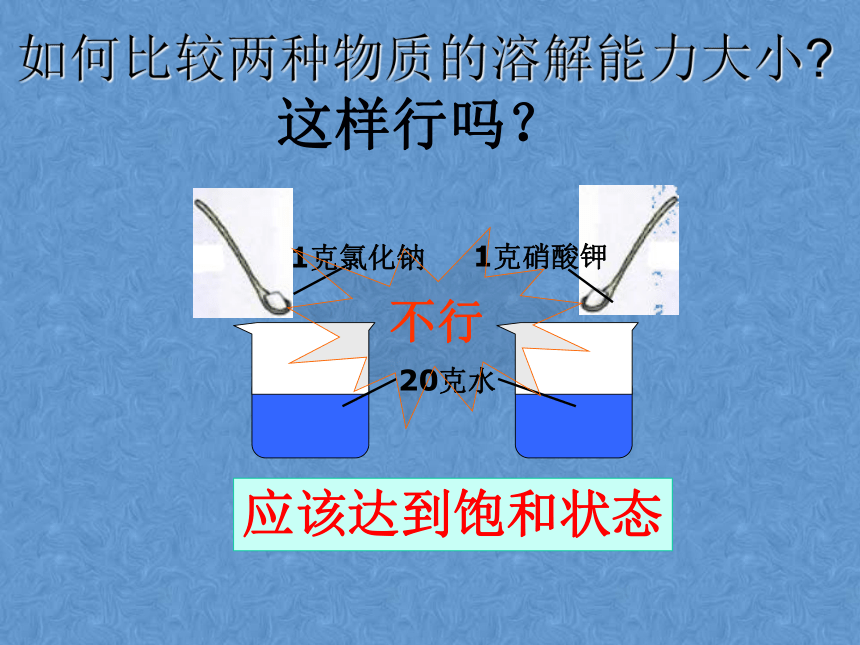
如何比较两种物质的溶解能力大小?
应该达到饱和状态
这样行吗?
如何比较两种物质的溶解能力大小?
不行
定状态(达到饱和)
比较不同物质的溶解能力,应该控制的条件有:
定温度
定溶剂的量
二、固体的溶解度(s)
1、定义:
在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
一定温度
100克溶剂(一般指水)
饱和状态
质量(克)
2.固体的溶解度的四要素:
表示该物质在此温度下,在100g溶剂里达到饱和状态时所溶解的质量
3、溶解度的含义:
例:蔗糖在20℃时的溶解度是203.9g。
在20℃时,100g水中最多可溶解203.9g蔗糖。
在20℃时,100g水中溶解203.9g蔗糖,达到饱和。
练习:
1、20 ℃,硝酸钾的溶解度是31克。
2、20 ℃,氯化钠的溶解度是36克。
3、80 ℃,硝酸钾的溶解度是161克。
4、 在20℃时,100g水中最多可溶解203.9g蔗糖。
从溶解度可以获得的信息
食盐在20℃时的溶解度S=36克
在 ___℃时,食盐(氯化钠)在_____ 克水里达到 ____ 时溶解了____克。
此时的溶液一定是______溶液。
该溶液的质量为_________。溶液中食盐(NaCl)的质量为________ ,水为___ 。
归纳:若某物质在某温度时的溶解度为S克,则此时
M质 = S克,M剂 = 100克,
M液= M质+M剂 = 100+S 克
20
100
饱和
36
饱和
136克
36克
100克
练习
1、20 ℃,氯化钠的溶解度为36克,则在此温度下,在50克水中最多能溶解多少克氯化钠?
公式:
2、20 ℃,68克饱和氯化钠溶液蒸干得氯化钠18克,求20 ℃氯化钠的溶解度?
3、20 ℃,氯化钠的溶解度为36克,求20 ℃,100克饱和溶液中溶质的质量?
4、20℃时,硝酸钾的溶解度是70克。在此温度下,将40克的硝酸钾放入50克的水中,充分搅拌,振荡,所得溶液多少克,是否是饱和溶液。
℃
判断下列说法是否正确
1、在20?C时,100克水中溶解了23克食盐,则食盐在20?C时的溶解度为23克。
2、在20?C时,100克溶液中含有溶质23克,则该物质的溶解度为23克。
3、在100克水中最多能溶解NaCl36.5克,则氯化钠的溶解度为36.5克。
4、在20?C时,在100克水中最多能溶解NaCl36.5克,则氯化钠的溶解度为36.5克。
温度不同不能比较溶解度的大小!
100克水中最多溶解20克A物质和100克水最多溶解30克B物质哪一个溶解度大?
注 意
◆
不能比较,因为温度不同.
3、影响固体溶解度大小的因素
内因:溶质和溶剂的种类
外因:温度
注意:对于固体物质来说改变溶剂的量不会改变溶解度
二、溶解度与溶解性的关系
易溶
可溶
微溶
难(不)溶
练习: 1、不溶物就是绝对不溶于水的物质。此话是否正确? 2、20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。 3、20℃时氯化钠的溶解度是36g,则氯化钠属于( )
A.易溶 物质 B.可溶物质 C.微溶物质 D.难溶物质
难
>10g
1g~10g
0.01~1g
<0.01g
A
易溶
可溶
微溶
难(不)溶
20℃
溶解性
溶解度/g (20℃)
.
.
.
.
50
10
20
30
40
0
60
70
808
90
100
50
10
20
30
40
80
60
70
8 0
90
100
110
180
170
160
150
140
130
120
190
200
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钾
氯化钠
硼酸
.
硝酸钾
.
.
.
.
硝酸钾在不同温度时的溶解度:
13.3
31.6
20.9
45.8
63.9
85.5
110
138
168
202
246
4、溶解度的表示方法:
(1)列表法:
(2)溶解度曲线(点、线、面、交点)
.A
温度/℃ 0 10 20 30 40 50 60 70 80 90 100
溶解度/g
溶解度(克)
温度(t)
160
150
140
130
120
110
100
90
80
70
60
50
40
30
20
10
200
190
180
170
10
100
90
80
70
60
50
40
30
20
0
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钠
硼酸
1:同种物质在不同温度下的溶解度大小。
2:不同物质在同一温度下的溶解度相对大小。
说出
50℃各物质溶解度相对大小
3:物质的溶解性
50
由一根曲线可以看出什么
说出溶解性
4、固体物质的溶解
度随温度的变化情况
0.05
0.10
0.15
0.20
90
70
40
0
10
20
50
60
80
100
30
0.05
0.10
0.15
0.20
90
70
40
0
10
20
50
60
80
100
30
温度/℃
熟石灰的溶解度曲线:
讨论:
固体物质溶解度受温度变化影响情况:
大多数固体物质溶解度随温度升高而增大, 例如 硝酸钾、氯化铵等。
少数固体物质溶解度受温度影响不大, 例如食盐。
极少数固体物质溶解度随温度升高反而减小,例如熟石灰。
甲
乙
丙
B
温度(℃)
溶解度
(g)
T1 T2
(1)T2时,溶解度最大的是________;
(2)B点代表的含义是
_______________________
_______________;
(3)T1时的甲溶液升温到T2,甲溶液变成
_______________.
甲
T1℃时,甲、丙两种物质
的溶解度相等
不饱和溶液
巩固练习:
50
10
20
30
40
0
60
70
808
90
100
50
10
20
30
40
80
60
70
8 0
90
100
110
180
170
160
150
140
130
120
190
200
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钾
氯化钠
硼酸
100
硼酸
硝酸 铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
温度/℃
固体的溶解度曲线:
1、横坐标60,纵坐标110 的交点表示什么意义?
练习:
A.
.
2.比较硝酸钠与硝酸钾的溶解度大小
在680C时,NaNO3与KNO3的溶解度相等
温度大于680C时, KNO3的溶解度大于NaNO3
温度小于680C时,NaNO3的溶解度大于KNO3
100
硼酸
硝酸铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
温度/℃
固体的溶解度曲线:
小于
B.
2、在40℃时,硝酸钾的溶解度____ (填大于、小于)硝酸钠的溶解度。
3、在80℃时氯化钠、氯化钾、氯化铵、硼酸的溶解度由大到小的顺序是_______________________________。
氯化铵、氯化钾、氯化钠、硼酸
1.两曲线交点B表示:_____________
___________________________________
__________________________
在68℃时,硝酸钾与硝酸钠的溶解度相等,均为133g
68
133
.
.
.
.
.
硝酸钾
.
.
.
.
ll在80℃时,将110g硝酸钾加入到100g水中,充分溶解后,形成的溶液为该温度下硝酸钾的____溶液。欲使其刚好形成饱和溶液,可采用的方法有:
加入一定量的硝酸钾
蒸发掉一定量的水份
降温到60℃
若再降温到10℃,会怎样?
会析出89g硝酸钾晶体
21
169
不饱和
59g
89g
在90℃时,将36g氯化钠加入到100g水中,充分溶解后,形成的溶液为该温度下氯化钠的______溶液。欲使其刚好形成饱和溶液,可采用的方法有:
加入3g氯化钠
蒸发掉一定量的水份
降温至20℃
若再降温,会怎样?
会析出极少量的晶体
硝酸钾
氯化钠
不饱和
若仅将题中“36g”换成“30g”,会怎样?
39
36
溶解度(克)
温度(t)
160
150
140
130
120
110
100
90
80
70
60
50
40
30
20
10
200
190
180
170
10
100
90
80
70
60
50
40
30
20
0
硝酸钾
氯化钠
固体溶解度曲线
从溶解度曲线分析结晶情况
1、降温结晶
(又叫冷却热饱和溶液法)
2、蒸发溶剂法
适用于溶解度随温度变化较小的物质如:NaCl
适用于溶解度随温度变化较大的物质如:KNO3
.
.
.
.
.
硝酸钾
.
.
.
.
21
169
1、将80?C一定量的硝酸钾的饱和溶液降温至20?C后,下列量怎样变( )
A、溶质 B、溶剂 C、溶液
D溶解度 E、溶质的质量分数
2、将20?C一定量硝酸钾的饱和溶液降升温至80?C后,下列量怎样变( )
A、溶质 B、溶剂 C、溶液
D溶解度 E、溶质的质量分数
混合物
适量水
加热
KNO3热饱和溶液
降温
结晶
过滤
滤纸上:KNO3固体
滤液中:
大部分NaCl 少量KNO3
硝酸钾固体中含有少量氯化钠,如何提纯硝酸钾?
降温结晶法提纯硝酸钾
(又叫冷却热饱和溶液法)
2.右图是A.B.C三种固体物质的溶解度曲线,回答下列问题:
(1)从B溶液中得到晶体宜采用的方法是
(2)除去A中混有的少量B的方法是
(3)除去B中混有的少量A的方法是
( 4)分离B与C混合物采用的方法是
蒸发结晶
溶解,蒸发结晶,过滤,
配制热饱和溶液,降温结晶,过滤
温度
溶解度
A
B
C
0.01克
8克
溶解,蒸发结晶,过滤,
1、定义:
通常讲的气体溶解度是指该气体在压强为101KPa, 一定温度时溶解在1体积水里达到饱和状态时的气体体积。
三、气体的溶解度
1、定义:
通常讲的气体溶解度是指该气体在( )为101KPa, 一定( )时溶解在1体积水里达到()状态时的气体( )。
三、气体的溶解度
想一想
当打开汽水瓶盖时,汽水会自动喷出来
喝进体内会有打嗝现象
你能解释这种现象吗?
打开瓶盖时,压强减小,CO2的溶解度减小,气体逸出.
当喝进体内后温度升高,CO2的溶解度减小,气体逸出.
[讨论] 天气闷热时,鱼儿为什么总爱在水面上
进行呼吸?
气体溶解度一般随压强增大而增大,压强减小而减小。
气体溶解度一般随温度升高而减小,温度降低而增大。
2、影响气体溶解度的因素:
[讨论] 天气闷热时,鱼儿为什么总爱在水面上
进行呼吸?
气体溶解度一般随( )增大而( ),( )减小而( )。
气体溶解度一般随( )升高而( ),( )降低而( )。
2、影响气体溶解度的因素:
溶解度
同种溶质在不同的溶 剂中的溶解能力不同
不同的溶质在同种溶 剂中的溶解能力不同
溶解性
物质的溶解度
易溶 、可溶 、 微溶 、 难(不)溶
固体的溶解度
气体的溶解度
影响因素(温度)
影响因素 (温度、压强)
表示方法
表示方法
课题2 溶 解 度
不行
应该在同一温度下
这样行吗?
如何比较两种物质的溶解能力大小?
应该溶剂的量相同
不行
这样行吗?
如何比较两种物质的溶解能力大小?
应该达到饱和状态
这样行吗?
如何比较两种物质的溶解能力大小?
不行
定状态(达到饱和)
比较不同物质的溶解能力,应该控制的条件有:
定温度
定溶剂的量
二、固体的溶解度(s)
1、定义:
在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
一定温度
100克溶剂(一般指水)
饱和状态
质量(克)
2.固体的溶解度的四要素:
表示该物质在此温度下,在100g溶剂里达到饱和状态时所溶解的质量
3、溶解度的含义:
例:蔗糖在20℃时的溶解度是203.9g。
在20℃时,100g水中最多可溶解203.9g蔗糖。
在20℃时,100g水中溶解203.9g蔗糖,达到饱和。
练习:
1、20 ℃,硝酸钾的溶解度是31克。
2、20 ℃,氯化钠的溶解度是36克。
3、80 ℃,硝酸钾的溶解度是161克。
4、 在20℃时,100g水中最多可溶解203.9g蔗糖。
从溶解度可以获得的信息
食盐在20℃时的溶解度S=36克
在 ___℃时,食盐(氯化钠)在_____ 克水里达到 ____ 时溶解了____克。
此时的溶液一定是______溶液。
该溶液的质量为_________。溶液中食盐(NaCl)的质量为________ ,水为___ 。
归纳:若某物质在某温度时的溶解度为S克,则此时
M质 = S克,M剂 = 100克,
M液= M质+M剂 = 100+S 克
20
100
饱和
36
饱和
136克
36克
100克
练习
1、20 ℃,氯化钠的溶解度为36克,则在此温度下,在50克水中最多能溶解多少克氯化钠?
公式:
2、20 ℃,68克饱和氯化钠溶液蒸干得氯化钠18克,求20 ℃氯化钠的溶解度?
3、20 ℃,氯化钠的溶解度为36克,求20 ℃,100克饱和溶液中溶质的质量?
4、20℃时,硝酸钾的溶解度是70克。在此温度下,将40克的硝酸钾放入50克的水中,充分搅拌,振荡,所得溶液多少克,是否是饱和溶液。
℃
判断下列说法是否正确
1、在20?C时,100克水中溶解了23克食盐,则食盐在20?C时的溶解度为23克。
2、在20?C时,100克溶液中含有溶质23克,则该物质的溶解度为23克。
3、在100克水中最多能溶解NaCl36.5克,则氯化钠的溶解度为36.5克。
4、在20?C时,在100克水中最多能溶解NaCl36.5克,则氯化钠的溶解度为36.5克。
温度不同不能比较溶解度的大小!
100克水中最多溶解20克A物质和100克水最多溶解30克B物质哪一个溶解度大?
注 意
◆
不能比较,因为温度不同.
3、影响固体溶解度大小的因素
内因:溶质和溶剂的种类
外因:温度
注意:对于固体物质来说改变溶剂的量不会改变溶解度
二、溶解度与溶解性的关系
易溶
可溶
微溶
难(不)溶
练习: 1、不溶物就是绝对不溶于水的物质。此话是否正确? 2、20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。 3、20℃时氯化钠的溶解度是36g,则氯化钠属于( )
A.易溶 物质 B.可溶物质 C.微溶物质 D.难溶物质
难
>10g
1g~10g
0.01~1g
<0.01g
A
易溶
可溶
微溶
难(不)溶
20℃
溶解性
溶解度/g (20℃)
.
.
.
.
50
10
20
30
40
0
60
70
808
90
100
50
10
20
30
40
80
60
70
8 0
90
100
110
180
170
160
150
140
130
120
190
200
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钾
氯化钠
硼酸
.
硝酸钾
.
.
.
.
硝酸钾在不同温度时的溶解度:
13.3
31.6
20.9
45.8
63.9
85.5
110
138
168
202
246
4、溶解度的表示方法:
(1)列表法:
(2)溶解度曲线(点、线、面、交点)
.A
温度/℃ 0 10 20 30 40 50 60 70 80 90 100
溶解度/g
溶解度(克)
温度(t)
160
150
140
130
120
110
100
90
80
70
60
50
40
30
20
10
200
190
180
170
10
100
90
80
70
60
50
40
30
20
0
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钠
硼酸
1:同种物质在不同温度下的溶解度大小。
2:不同物质在同一温度下的溶解度相对大小。
说出
50℃各物质溶解度相对大小
3:物质的溶解性
50
由一根曲线可以看出什么
说出溶解性
4、固体物质的溶解
度随温度的变化情况
0.05
0.10
0.15
0.20
90
70
40
0
10
20
50
60
80
100
30
0.05
0.10
0.15
0.20
90
70
40
0
10
20
50
60
80
100
30
温度/℃
熟石灰的溶解度曲线:
讨论:
固体物质溶解度受温度变化影响情况:
大多数固体物质溶解度随温度升高而增大, 例如 硝酸钾、氯化铵等。
少数固体物质溶解度受温度影响不大, 例如食盐。
极少数固体物质溶解度随温度升高反而减小,例如熟石灰。
甲
乙
丙
B
温度(℃)
溶解度
(g)
T1 T2
(1)T2时,溶解度最大的是________;
(2)B点代表的含义是
_______________________
_______________;
(3)T1时的甲溶液升温到T2,甲溶液变成
_______________.
甲
T1℃时,甲、丙两种物质
的溶解度相等
不饱和溶液
巩固练习:
50
10
20
30
40
0
60
70
808
90
100
50
10
20
30
40
80
60
70
8 0
90
100
110
180
170
160
150
140
130
120
190
200
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钾
氯化钠
硼酸
100
硼酸
硝酸 铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
温度/℃
固体的溶解度曲线:
1、横坐标60,纵坐标110 的交点表示什么意义?
练习:
A.
.
2.比较硝酸钠与硝酸钾的溶解度大小
在680C时,NaNO3与KNO3的溶解度相等
温度大于680C时, KNO3的溶解度大于NaNO3
温度小于680C时,NaNO3的溶解度大于KNO3
100
硼酸
硝酸铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
温度/℃
固体的溶解度曲线:
小于
B.
2、在40℃时,硝酸钾的溶解度____ (填大于、小于)硝酸钠的溶解度。
3、在80℃时氯化钠、氯化钾、氯化铵、硼酸的溶解度由大到小的顺序是_______________________________。
氯化铵、氯化钾、氯化钠、硼酸
1.两曲线交点B表示:_____________
___________________________________
__________________________
在68℃时,硝酸钾与硝酸钠的溶解度相等,均为133g
68
133
.
.
.
.
.
硝酸钾
.
.
.
.
ll在80℃时,将110g硝酸钾加入到100g水中,充分溶解后,形成的溶液为该温度下硝酸钾的____溶液。欲使其刚好形成饱和溶液,可采用的方法有:
加入一定量的硝酸钾
蒸发掉一定量的水份
降温到60℃
若再降温到10℃,会怎样?
会析出89g硝酸钾晶体
21
169
不饱和
59g
89g
在90℃时,将36g氯化钠加入到100g水中,充分溶解后,形成的溶液为该温度下氯化钠的______溶液。欲使其刚好形成饱和溶液,可采用的方法有:
加入3g氯化钠
蒸发掉一定量的水份
降温至20℃
若再降温,会怎样?
会析出极少量的晶体
硝酸钾
氯化钠
不饱和
若仅将题中“36g”换成“30g”,会怎样?
39
36
溶解度(克)
温度(t)
160
150
140
130
120
110
100
90
80
70
60
50
40
30
20
10
200
190
180
170
10
100
90
80
70
60
50
40
30
20
0
硝酸钾
氯化钠
固体溶解度曲线
从溶解度曲线分析结晶情况
1、降温结晶
(又叫冷却热饱和溶液法)
2、蒸发溶剂法
适用于溶解度随温度变化较小的物质如:NaCl
适用于溶解度随温度变化较大的物质如:KNO3
.
.
.
.
.
硝酸钾
.
.
.
.
21
169
1、将80?C一定量的硝酸钾的饱和溶液降温至20?C后,下列量怎样变( )
A、溶质 B、溶剂 C、溶液
D溶解度 E、溶质的质量分数
2、将20?C一定量硝酸钾的饱和溶液降升温至80?C后,下列量怎样变( )
A、溶质 B、溶剂 C、溶液
D溶解度 E、溶质的质量分数
混合物
适量水
加热
KNO3热饱和溶液
降温
结晶
过滤
滤纸上:KNO3固体
滤液中:
大部分NaCl 少量KNO3
硝酸钾固体中含有少量氯化钠,如何提纯硝酸钾?
降温结晶法提纯硝酸钾
(又叫冷却热饱和溶液法)
2.右图是A.B.C三种固体物质的溶解度曲线,回答下列问题:
(1)从B溶液中得到晶体宜采用的方法是
(2)除去A中混有的少量B的方法是
(3)除去B中混有的少量A的方法是
( 4)分离B与C混合物采用的方法是
蒸发结晶
溶解,蒸发结晶,过滤,
配制热饱和溶液,降温结晶,过滤
温度
溶解度
A
B
C
0.01克
8克
溶解,蒸发结晶,过滤,
1、定义:
通常讲的气体溶解度是指该气体在压强为101KPa, 一定温度时溶解在1体积水里达到饱和状态时的气体体积。
三、气体的溶解度
1、定义:
通常讲的气体溶解度是指该气体在( )为101KPa, 一定( )时溶解在1体积水里达到()状态时的气体( )。
三、气体的溶解度
想一想
当打开汽水瓶盖时,汽水会自动喷出来
喝进体内会有打嗝现象
你能解释这种现象吗?
打开瓶盖时,压强减小,CO2的溶解度减小,气体逸出.
当喝进体内后温度升高,CO2的溶解度减小,气体逸出.
[讨论] 天气闷热时,鱼儿为什么总爱在水面上
进行呼吸?
气体溶解度一般随压强增大而增大,压强减小而减小。
气体溶解度一般随温度升高而减小,温度降低而增大。
2、影响气体溶解度的因素:
[讨论] 天气闷热时,鱼儿为什么总爱在水面上
进行呼吸?
气体溶解度一般随( )增大而( ),( )减小而( )。
气体溶解度一般随( )升高而( ),( )降低而( )。
2、影响气体溶解度的因素:
溶解度
同种溶质在不同的溶 剂中的溶解能力不同
不同的溶质在同种溶 剂中的溶解能力不同
溶解性
物质的溶解度
易溶 、可溶 、 微溶 、 难(不)溶
固体的溶解度
气体的溶解度
影响因素(温度)
影响因素 (温度、压强)
表示方法
表示方法
同课章节目录
