人教版 选修4 高二化学 3.4难溶电解质的溶解平衡 上课课件(共45张ppt)
文档属性
| 名称 | 人教版 选修4 高二化学 3.4难溶电解质的溶解平衡 上课课件(共45张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-07 00:00:00 | ||
图片预览








文档简介
(共45张PPT)
新课导入
离子反应发生条件:
①生成难溶的物质。
如生成BaSO4、AgCl、CaCO3等。
②生成难电离的物质。
如生成CH3COOH、H2O、NH3?H2O、HClO等。
HClO
③生成挥发性物质。
如生成CO2、SO2、H2S等。
SO2
只要具备上述三个条件中的一个,离子互换反应即可发生。
这是由于溶液中离子间相互作用生成难溶物质、难电离物质、易挥发物质时,都可使溶液中某几种、自由移动离子浓度减小的缘故。
溶解平衡:一定条件下,强电解质溶解成离子的速率等于离子重新结合成沉淀的速率,溶液中各离子的浓度保持不变的状态。
原因:
第4节 难溶电解质的溶解平衡
一、Ag+和Cl-的反应真能进行到底吗?
二、沉淀反应的应用
知识目标
教学目标
能力目标
2.掌握沉淀的生成、溶解、转化的规律。
2.了解难溶电解质的溶解平衡及溶解平衡的应用。
1.运用平衡移动原理分析、解决沉淀的溶解和沉淀的转化问题。
1.理解难溶电解质的溶解度。
情感态度与价值观
2.体会“实验方法、逻辑推理、科学抽象法”在自然科学研究中的应用。
1.领会“本质决定现象,现象是本质的具体体现”的科学思想。
重点
教学重难点
难点
难溶电解质的溶解平衡。
难溶电解质的溶解和转化。
一、Ag+和Cl-的反应真能进行到底吗?
1.谈谈你对酸、碱和盐的溶解度表中“溶”与”不溶“的理解。
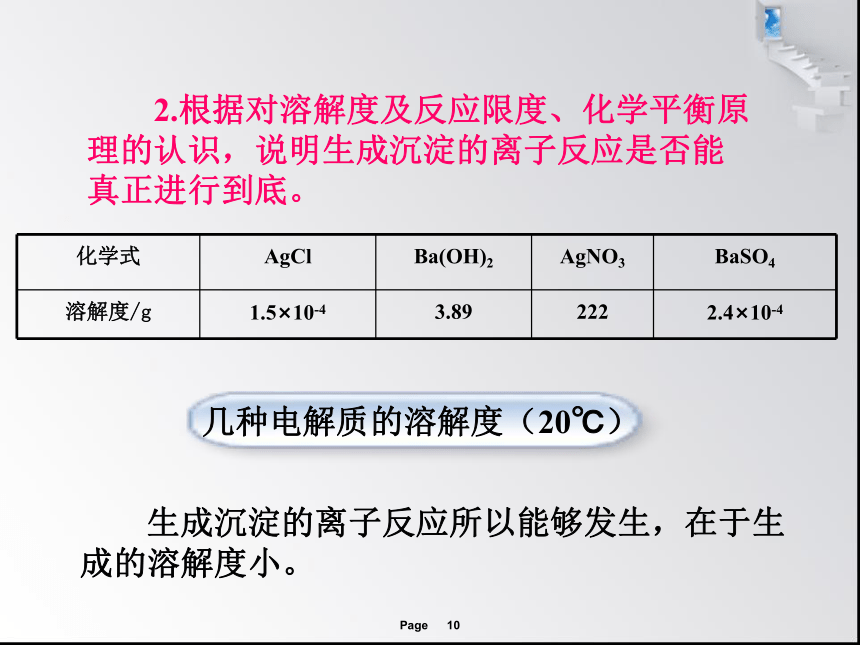
2.根据对溶解度及反应限度、化学平衡原理的认识,说明生成沉淀的离子反应是否能真正进行到底。
化学式 AgCl Ba(OH)2 AgNO3 BaSO4
溶解度/g 1.5×10-4 3.89 222 2.4×10-4
几种电解质的溶解度(20℃)
生成沉淀的离子反应所以能够发生,在于生成的溶解度小。
尽管AgCl溶解度很小,但并不是绝对不溶,生成的AgCl沉淀会有少量溶解。
生成AgCl沉淀后的溶液中三种有关反应的粒子在反应体系中共存:
Ag+
Cl-
Ag+
Cl-
Ag+
Cl-
Ag+
Cl-
Ag+
Cl-
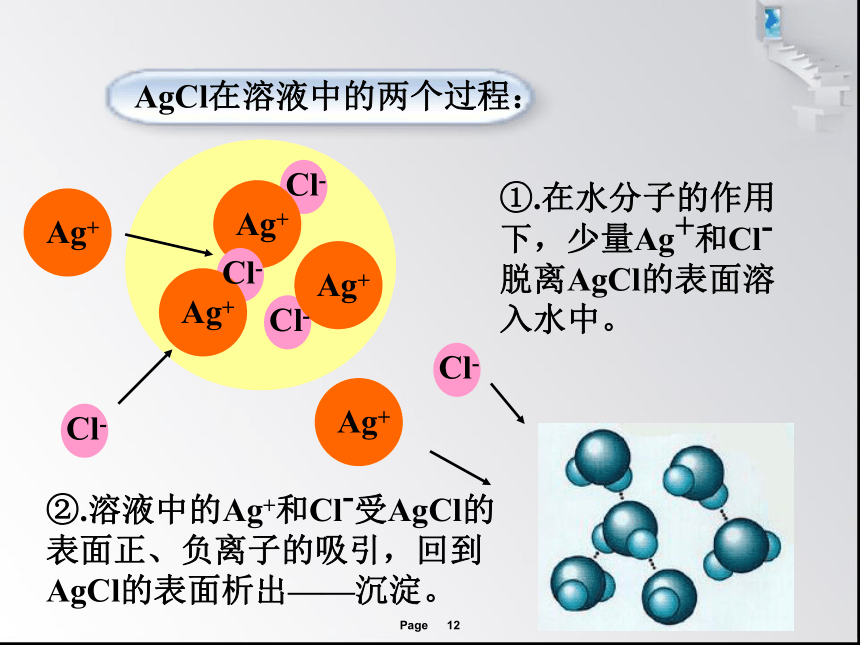
AgCl在溶液中的两个过程:
①.在水分子的作用下,少量Ag+和Cl-脱离AgCl的表面溶入水中。
②.溶液中的Ag+和Cl-受AgCl的表面正、负离子的吸引,回到AgCl的表面析出——沉淀。
在一定温度下,当沉淀溶解和生成的速率相等时,得到AgCl的饱和溶液,即建立下列动态平衡:
通常,我们习惯认为AgCl是“不溶”性物质,AgNO3溶液与NaCl溶液的反应是“不可逆反应”,现在看来,这些都不是绝对的 。
溶解
沉淀
不同电解质在水中的溶解度差别很大,例如AgCl和AgNO3,但难溶电解质与易溶电解质之间并无严格的界限,习惯上将溶解度小于0.01g的电解质称为难溶电解质。
难溶电解质的溶解度尽管很小,但不会等于0,如Ag2S。因此,难溶电解质在水中都存在类似于上述AgCl沉淀在水中的溶解平衡。
溶解度与溶解性的关系:20℃
10
易溶
可溶
1
微溶
0.01
难溶
S /g
沉淀反应在生产、科研、环保等领域的许多应用,正是利用了难溶电解质的溶解平衡。
二、沉淀反应的应用
生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂质或提纯物质的重要方法之一。
难溶电解质的溶解平衡也是动态平衡,同样可以通过改变条件使平衡移动——溶液中的离子转化为沉淀,或沉淀转化为溶液中的离子。
1.沉淀的生成
在涉及无机制备、提纯工艺的生产、科研、废水处理等领域中,常利用生成沉淀来达到分离或除去某些离子的目的。
应用 1
工业原料氯化铵中含有杂质氯化铁,使其溶解于水中,再加入氨水调节pH至7-8,可使Fe3+生成Fe(OH)3沉淀而除去。
Fe(OH)3
应用 2
以Na2S 、H2S等作沉淀剂,使某些金属离子如Cu2+、Hg2+等,生成极难溶的硫化物CuS、HgS等沉淀,也是分离、除去杂质常用的方法。
CuS
HgS
化学沉淀法废水处理工艺流程图
进水
预处理设备
混合
反应沉淀
补充处理
出水
药剂制备
投药
部分回流
沉淀物
处理设备
沉淀物排除
如果要除去某溶液中的SO42-,你选择加入钙盐还是钡盐?为什么?
在无需考虑其他因素的情况下,从溶解度大小考虑,应选择钡盐。
2.沉淀的溶解
在实际工作中,常常会遇到需要使难溶物质溶解的问题。
根据平衡移动原理,对于在水中难容的电解质,如果能设法不断地移去溶解平衡体系中相应离子,使平衡向沉淀溶解的方向移动,就可以使沉淀溶解。
难溶于水中的CaCO3沉淀可以溶于盐酸中:
+H+
+H+
气体CO2的生成和逸出,使CaCO3溶解平衡体系中的CO32-浓度不断减小,平衡向沉淀溶解的方向移动。主要盐酸的量足够,CaCO3就可溶解完全。
应用 1
应用 2
类似的可用强酸溶解的难溶电解质还有FeS、Al(OH)3、Cu(OH)2等。
实验 1
Mg(OH)2
盐酸
蒸馏水
氯化铵
实验结果:
滴加试剂 蒸馏水 盐酸 氯化铵
现象
固体无明显溶解现象
迅速溶解
可溶
3.沉淀的转化
向盛有10滴0.1mol/L AgNO3溶液的试管中滴加0.1mol/L NaCl溶液,至不再有白色沉淀生成。向其中滴加0.1mol/L KI溶液,观察、记录;再向其中滴加0.1mol/L的Na2S溶液,观察并记录现象。
实验 2
步骤 NaCl和AgNO3溶液混合 滴加KI溶液 滴加Na2S
溶液
现象
有白色沉淀析出
白色沉淀转化为黄色
黄的沉淀转化为黑色
KI
Na2S
AgCl
AgI
Ag2S
实验 3
在盛有1mL 0.1mol/LMgCl2溶液的试管中滴加1-2滴2mol/L NaOH溶液,有白色沉淀生成,再滴加2滴0.1mol/L FeCl3溶液,静置。观察并记录现象。
步骤 滴加NaOH溶液 滴加FeCl3溶液 静置
现象
有白色沉淀析出
白色沉淀转化为红褐色
红褐色沉淀析出,溶液褪至无色
FeCl3
静置
Mg(OH)2↓
Fe(OH)3↓
应用 1
锅炉水垢即会降低燃料的利用率,造成能源浪费,也会影响锅炉的使用寿命,形成安全隐患,因此要定期去除锅炉水垢。
水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松,易溶于酸的CaCO3。而后用酸除去。
从CaSO4到CaCO3的沉淀转化中,并存着两个沉淀溶解平衡:
CaCO3(s)
沉淀转化的实质是:沉淀溶解平衡的移动。
一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现。
自然界一些溶解度下的矿物转化为溶解度更小的矿物的现象。
读一读
钟乳石(stalactite),又称钟乳石,是指碳酸盐岩地区洞穴内在漫长地质历史中和特定地质条件下形成的石钟乳、石笋、石柱等不同形态碳酸钙沉淀物的总称,它的形成往往需要上万年或几十万年时间。由于形成时间漫长,钟乳石对远古地质考察有着重要的研究价值。
课堂小结
1.AgCl沉淀特点:
①Ag+和Cl-之间存在着强烈的相互作用;
②AgCl在水中的溶解度确实很小;
③在一定条件下,AgCl在水中的溶解可以处于平衡状态。
2.AgCl在溶液中的两个过程:
①在水分子的作用下,少量Ag+和Cl-脱离AgCl的表面溶入水中。
3.沉淀反应的应用
①沉淀的生成
②沉淀的溶解
③沉淀的转化
②溶液中的Ag+和Cl-受AgCl的表面正、负离子的吸引,回到AgCl的表面析出——沉淀。
课堂练习
1.一定条件下,强电解质溶解成离子的速率等于离子重新结合成沉淀的速率,溶液中各离子的浓度保持不变的状态: 。
溶解平衡
2.习惯上将溶解度小于0.01g的电解质称为
。
难溶电解质
3.为除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入的一种试剂是( )
A.NaOH B.Na2CO3
C.氨水 D.MgO
D
4.下列各组离子,在水溶液中能以较高浓度大量共存的是( )
①I- ClO- NO3- H+
②K+ NH4+ HCO3- OH-
③ SO42- SO3-2 Cl- OH-
④Fe3+ Cu2+ SO42- Cl -
⑤H+ K+ AlO2- HSO3-
⑥Ca2+ Na+ SO42- CO32-
A①⑥ B③④ C②⑤ D①④
B
5.常温下某无色透明溶液中所含的离子仅有NH4+和Cl-等四种离子,请回答下列问题:
①该溶液所含的离子中除上述两种外还应有_______________(填离子符号)两种离子。
②如溶液中c(NH4+)=c(Cl-),则溶液中的溶质为_______________________(填化学式)。该溶液的pH_____7(填<、>或=)。
H+、OH-
NH4Cl 、 NH3·H2O
=
6.某课外小组对一些金属单质和化合物的性质进行研究。
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
实验步骤 实验现象
将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中 产生气泡,析出疏松的红色固体,溶液逐渐变为无色
反应结束后分离出溶液备用 ?
红色固体用蒸馏水洗涤后,置于潮湿空气中 一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3]
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是________________________________________________________________________________________。
置换反应:___________________________________________________________________________;
化合反应:__________________________________。
①按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式)。
2Cu+O2+H2O+CO2=Cu2(OH)2CO3
2Al+6H+=2Al3++3H2↑
或2Al+3Cu2+=2Al3++3Cu
3MnO2+4Al=(高温)3Mn+2Al2O3
MnO2+H2O2+2H+=Mn2++O2↑+2H2O
7.KMnO4溶液常用做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此精确配制KMnO4标准溶液的操作是:
(1)称取稍多于所需量的KMnO4固体溶于水,将溶液加热并保持微沸l h;
(2)用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;
(3)过滤得到的KMnO4溶液贮存于棕色试剂瓶放在暗处:
(4)利用氧化还原滴定方法,在70 ℃-80 ℃条件下用基准试剂(纯度高、稳定性好的物质)溶液测定其浓度。
回答下列问题:
(1)如何保证在70 ℃~80 ℃条件下进行滴定操作:_______________________
(2)下列物质中,可以用于测定KMnO4溶液浓度的基准试剂是________(填写序号)
A.H2C2O4·2H2O
B.FeSO4·7H2O? ?
C.浓盐酸 ???
D.Na2SO3
可在水浴中加热?
A?
新课导入
离子反应发生条件:
①生成难溶的物质。
如生成BaSO4、AgCl、CaCO3等。
②生成难电离的物质。
如生成CH3COOH、H2O、NH3?H2O、HClO等。
HClO
③生成挥发性物质。
如生成CO2、SO2、H2S等。
SO2
只要具备上述三个条件中的一个,离子互换反应即可发生。
这是由于溶液中离子间相互作用生成难溶物质、难电离物质、易挥发物质时,都可使溶液中某几种、自由移动离子浓度减小的缘故。
溶解平衡:一定条件下,强电解质溶解成离子的速率等于离子重新结合成沉淀的速率,溶液中各离子的浓度保持不变的状态。
原因:
第4节 难溶电解质的溶解平衡
一、Ag+和Cl-的反应真能进行到底吗?
二、沉淀反应的应用
知识目标
教学目标
能力目标
2.掌握沉淀的生成、溶解、转化的规律。
2.了解难溶电解质的溶解平衡及溶解平衡的应用。
1.运用平衡移动原理分析、解决沉淀的溶解和沉淀的转化问题。
1.理解难溶电解质的溶解度。
情感态度与价值观
2.体会“实验方法、逻辑推理、科学抽象法”在自然科学研究中的应用。
1.领会“本质决定现象,现象是本质的具体体现”的科学思想。
重点
教学重难点
难点
难溶电解质的溶解平衡。
难溶电解质的溶解和转化。
一、Ag+和Cl-的反应真能进行到底吗?
1.谈谈你对酸、碱和盐的溶解度表中“溶”与”不溶“的理解。
2.根据对溶解度及反应限度、化学平衡原理的认识,说明生成沉淀的离子反应是否能真正进行到底。
化学式 AgCl Ba(OH)2 AgNO3 BaSO4
溶解度/g 1.5×10-4 3.89 222 2.4×10-4
几种电解质的溶解度(20℃)
生成沉淀的离子反应所以能够发生,在于生成的溶解度小。
尽管AgCl溶解度很小,但并不是绝对不溶,生成的AgCl沉淀会有少量溶解。
生成AgCl沉淀后的溶液中三种有关反应的粒子在反应体系中共存:
Ag+
Cl-
Ag+
Cl-
Ag+
Cl-
Ag+
Cl-
Ag+
Cl-
AgCl在溶液中的两个过程:
①.在水分子的作用下,少量Ag+和Cl-脱离AgCl的表面溶入水中。
②.溶液中的Ag+和Cl-受AgCl的表面正、负离子的吸引,回到AgCl的表面析出——沉淀。
在一定温度下,当沉淀溶解和生成的速率相等时,得到AgCl的饱和溶液,即建立下列动态平衡:
通常,我们习惯认为AgCl是“不溶”性物质,AgNO3溶液与NaCl溶液的反应是“不可逆反应”,现在看来,这些都不是绝对的 。
溶解
沉淀
不同电解质在水中的溶解度差别很大,例如AgCl和AgNO3,但难溶电解质与易溶电解质之间并无严格的界限,习惯上将溶解度小于0.01g的电解质称为难溶电解质。
难溶电解质的溶解度尽管很小,但不会等于0,如Ag2S。因此,难溶电解质在水中都存在类似于上述AgCl沉淀在水中的溶解平衡。
溶解度与溶解性的关系:20℃
10
易溶
可溶
1
微溶
0.01
难溶
S /g
沉淀反应在生产、科研、环保等领域的许多应用,正是利用了难溶电解质的溶解平衡。
二、沉淀反应的应用
生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂质或提纯物质的重要方法之一。
难溶电解质的溶解平衡也是动态平衡,同样可以通过改变条件使平衡移动——溶液中的离子转化为沉淀,或沉淀转化为溶液中的离子。
1.沉淀的生成
在涉及无机制备、提纯工艺的生产、科研、废水处理等领域中,常利用生成沉淀来达到分离或除去某些离子的目的。
应用 1
工业原料氯化铵中含有杂质氯化铁,使其溶解于水中,再加入氨水调节pH至7-8,可使Fe3+生成Fe(OH)3沉淀而除去。
Fe(OH)3
应用 2
以Na2S 、H2S等作沉淀剂,使某些金属离子如Cu2+、Hg2+等,生成极难溶的硫化物CuS、HgS等沉淀,也是分离、除去杂质常用的方法。
CuS
HgS
化学沉淀法废水处理工艺流程图
进水
预处理设备
混合
反应沉淀
补充处理
出水
药剂制备
投药
部分回流
沉淀物
处理设备
沉淀物排除
如果要除去某溶液中的SO42-,你选择加入钙盐还是钡盐?为什么?
在无需考虑其他因素的情况下,从溶解度大小考虑,应选择钡盐。
2.沉淀的溶解
在实际工作中,常常会遇到需要使难溶物质溶解的问题。
根据平衡移动原理,对于在水中难容的电解质,如果能设法不断地移去溶解平衡体系中相应离子,使平衡向沉淀溶解的方向移动,就可以使沉淀溶解。
难溶于水中的CaCO3沉淀可以溶于盐酸中:
+H+
+H+
气体CO2的生成和逸出,使CaCO3溶解平衡体系中的CO32-浓度不断减小,平衡向沉淀溶解的方向移动。主要盐酸的量足够,CaCO3就可溶解完全。
应用 1
应用 2
类似的可用强酸溶解的难溶电解质还有FeS、Al(OH)3、Cu(OH)2等。
实验 1
Mg(OH)2
盐酸
蒸馏水
氯化铵
实验结果:
滴加试剂 蒸馏水 盐酸 氯化铵
现象
固体无明显溶解现象
迅速溶解
可溶
3.沉淀的转化
向盛有10滴0.1mol/L AgNO3溶液的试管中滴加0.1mol/L NaCl溶液,至不再有白色沉淀生成。向其中滴加0.1mol/L KI溶液,观察、记录;再向其中滴加0.1mol/L的Na2S溶液,观察并记录现象。
实验 2
步骤 NaCl和AgNO3溶液混合 滴加KI溶液 滴加Na2S
溶液
现象
有白色沉淀析出
白色沉淀转化为黄色
黄的沉淀转化为黑色
KI
Na2S
AgCl
AgI
Ag2S
实验 3
在盛有1mL 0.1mol/LMgCl2溶液的试管中滴加1-2滴2mol/L NaOH溶液,有白色沉淀生成,再滴加2滴0.1mol/L FeCl3溶液,静置。观察并记录现象。
步骤 滴加NaOH溶液 滴加FeCl3溶液 静置
现象
有白色沉淀析出
白色沉淀转化为红褐色
红褐色沉淀析出,溶液褪至无色
FeCl3
静置
Mg(OH)2↓
Fe(OH)3↓
应用 1
锅炉水垢即会降低燃料的利用率,造成能源浪费,也会影响锅炉的使用寿命,形成安全隐患,因此要定期去除锅炉水垢。
水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松,易溶于酸的CaCO3。而后用酸除去。
从CaSO4到CaCO3的沉淀转化中,并存着两个沉淀溶解平衡:
CaCO3(s)
沉淀转化的实质是:沉淀溶解平衡的移动。
一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现。
自然界一些溶解度下的矿物转化为溶解度更小的矿物的现象。
读一读
钟乳石(stalactite),又称钟乳石,是指碳酸盐岩地区洞穴内在漫长地质历史中和特定地质条件下形成的石钟乳、石笋、石柱等不同形态碳酸钙沉淀物的总称,它的形成往往需要上万年或几十万年时间。由于形成时间漫长,钟乳石对远古地质考察有着重要的研究价值。
课堂小结
1.AgCl沉淀特点:
①Ag+和Cl-之间存在着强烈的相互作用;
②AgCl在水中的溶解度确实很小;
③在一定条件下,AgCl在水中的溶解可以处于平衡状态。
2.AgCl在溶液中的两个过程:
①在水分子的作用下,少量Ag+和Cl-脱离AgCl的表面溶入水中。
3.沉淀反应的应用
①沉淀的生成
②沉淀的溶解
③沉淀的转化
②溶液中的Ag+和Cl-受AgCl的表面正、负离子的吸引,回到AgCl的表面析出——沉淀。
课堂练习
1.一定条件下,强电解质溶解成离子的速率等于离子重新结合成沉淀的速率,溶液中各离子的浓度保持不变的状态: 。
溶解平衡
2.习惯上将溶解度小于0.01g的电解质称为
。
难溶电解质
3.为除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入的一种试剂是( )
A.NaOH B.Na2CO3
C.氨水 D.MgO
D
4.下列各组离子,在水溶液中能以较高浓度大量共存的是( )
①I- ClO- NO3- H+
②K+ NH4+ HCO3- OH-
③ SO42- SO3-2 Cl- OH-
④Fe3+ Cu2+ SO42- Cl -
⑤H+ K+ AlO2- HSO3-
⑥Ca2+ Na+ SO42- CO32-
A①⑥ B③④ C②⑤ D①④
B
5.常温下某无色透明溶液中所含的离子仅有NH4+和Cl-等四种离子,请回答下列问题:
①该溶液所含的离子中除上述两种外还应有_______________(填离子符号)两种离子。
②如溶液中c(NH4+)=c(Cl-),则溶液中的溶质为_______________________(填化学式)。该溶液的pH_____7(填<、>或=)。
H+、OH-
NH4Cl 、 NH3·H2O
=
6.某课外小组对一些金属单质和化合物的性质进行研究。
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
实验步骤 实验现象
将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中 产生气泡,析出疏松的红色固体,溶液逐渐变为无色
反应结束后分离出溶液备用 ?
红色固体用蒸馏水洗涤后,置于潮湿空气中 一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3]
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是________________________________________________________________________________________。
置换反应:___________________________________________________________________________;
化合反应:__________________________________。
①按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式)。
2Cu+O2+H2O+CO2=Cu2(OH)2CO3
2Al+6H+=2Al3++3H2↑
或2Al+3Cu2+=2Al3++3Cu
3MnO2+4Al=(高温)3Mn+2Al2O3
MnO2+H2O2+2H+=Mn2++O2↑+2H2O
7.KMnO4溶液常用做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此精确配制KMnO4标准溶液的操作是:
(1)称取稍多于所需量的KMnO4固体溶于水,将溶液加热并保持微沸l h;
(2)用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;
(3)过滤得到的KMnO4溶液贮存于棕色试剂瓶放在暗处:
(4)利用氧化还原滴定方法,在70 ℃-80 ℃条件下用基准试剂(纯度高、稳定性好的物质)溶液测定其浓度。
回答下列问题:
(1)如何保证在70 ℃~80 ℃条件下进行滴定操作:_______________________
(2)下列物质中,可以用于测定KMnO4溶液浓度的基准试剂是________(填写序号)
A.H2C2O4·2H2O
B.FeSO4·7H2O? ?
C.浓盐酸 ???
D.Na2SO3
可在水浴中加热?
A?
