人教版 选修4 高二化学 4.2化学电源 上课课件(共40张ppt)
文档属性
| 名称 | 人教版 选修4 高二化学 4.2化学电源 上课课件(共40张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-02-07 00:00:00 | ||
图片预览











文档简介
(共40张PPT)
新课导入
各种电池
使用锂电源的手机和笔记本电脑
纽扣电池作为电源的纽扣电池
使用氢氧燃料电池动力的法国产标致TAXI
一、化学电池与其他能源相比较有那
些优点?
二、一次电池、二次电池、燃料电池
第2节 化学电源
教学目标
知识目标
能力目标
1.知道常见电池的组成及应用。
2.了解燃料电池的组成和工作原理。
3.了解新型化学电源与人们生活实践的重要关系。
运用观察、实验、查阅资料等方法,结合生产、生活实践学习常见电池的组成及应用,关注新型化学电源。
亲自动手实验,体验科学探究的艰辛与喜悦;关注科技前沿知识,激发兴趣,热爱科学;关注与化学有关的社会问题,体会理论研究转化为技术产品的复杂过程。
情感态度与价值观
一次电池、二次电池和燃料电池的反应原理、性能及其应用。
化学电池的反应原理。
重点
教学重难点
难点
在生活中,你用过那些电池?它们属于哪一类电池?你知道他们的工作原理及应用吗?
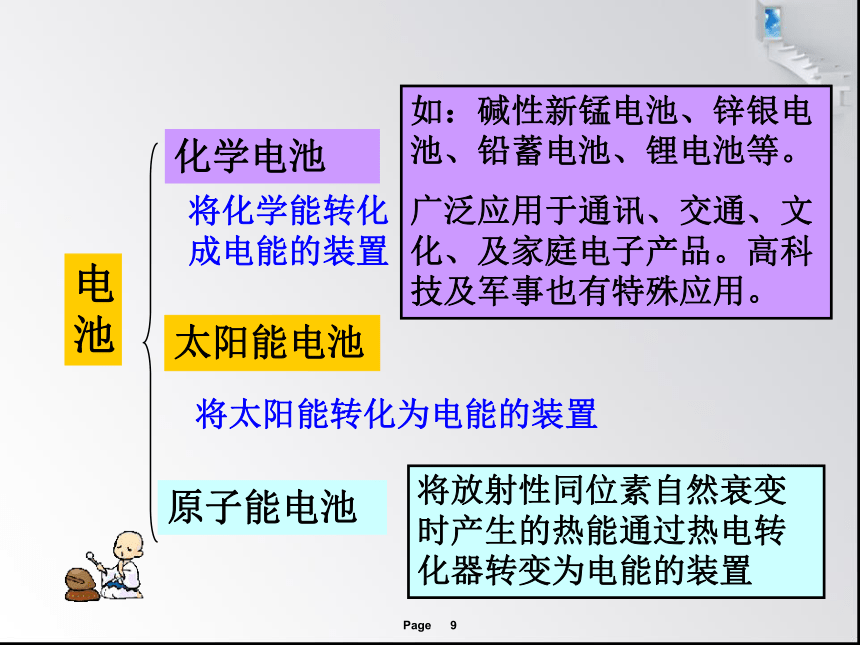
电池
化学电池
太阳能电池
原子能电池
将化学能转化成电能的装置
将太阳能转化为电能的装置
如:碱性新锰电池、锌银电池、铅蓄电池、锂电池等。
广泛应用于通讯、交通、文化、及家庭电子产品。高科技及军事也有特殊应用。
将放射性同位素自然衰变时产生的热能通过热电转化器转变为电能的装置
锌锰干电池
铅蓄电池
1792年,物理学教授伏特根据一位名叫伽伐尼的解剖学家发表的一篇论文说动物肌肉里贮存着电,用金属接触它们,电就会跑出来。伏特经过一次又一次的实验,终于在1800年找到了“动物肌肉里贮存着电”的秘密所在。为纪念伏特,电压的单位以他的名字来命名。
伏特
读一读
伏特
一、化学电池与其他能源相比较有
那些优点?
化学电池 定义 举例
一次电池
二次电池
三次电池
1.电池分类
电池中的活性物质消耗到一定程度就不能使用。
普通锌锰电池
碱性锌锰电池
锌银纽扣电池
又称充电电池或蓄电池,放电后可以再充电使活性物质获得再生
铅蓄电池
锌银蓄电池
锂离子电池
又称连续电池,是一种连续性的将燃料和氧化剂的化学能转化为电能的化学电源
氢氧燃料电池
2.化学电池的优点:
(1)能量转化效率较高,供能稳定可靠。
(2)可以制成各种形状和大小、不同容量和电压的电池及电池组。
(3)使用方便,易于维护,并可在各种环境下工作。
形态各异的化学电池
3.判断电池优劣的标准:
⑴.比能量,指这种电池单位质量或单位体积所能输出电能的多少。【单位是:(W·h)/kg, (W·h)/L】
⑵.比功率,输出功率大小。【单位是:W /kg ,W /L】
⑶.可存储时间的长短。
除特殊情况外,质量轻、体积小而输出电能多、功率大可存储时间长的电池,更适合受使用者的需要。
一次电池:活性物质(发生氧化还原反应的物质)消耗到一定程度就不能使用的电池。一次电池中电解质溶液成胶状不流动,因此也叫干电池。
纽扣电池
普通干电池
二、一次电池
正极
碳棒
锌皮
纸隔板
氯化锌和氯化铵的糊状物
二氧化锰石墨
负极
普通锌锰干电池
碱性锌锰电池
电池符号:
(-)Zn|KOH(7~9mol·dm-3) | MnO2| C(+)
电极反应:
电池反应:
二、二次电池
二次电池:又称充电电池或蓄电池,放电后可以再充电使活性物质获得再生。
铅蓄电池
水、硫酸
氧化铅板
铅板
铅蓄电池原理
负极:
正极:
电池反应:
负极——Pb
正极——PbO 2
Pb
PbO 2
硫酸
铅蓄电池:
铅蓄电池充放电示意图
充电
放电
充电时的两极反应:
阴极(A极)
阳极(B极)
总反应式:
放电时的两极反应:
负极(A极)
正极(B极)
电池反应:
充电
放电
铅蓄电池的充放电程度,可用测定硫酸密
度的方法来判断。
铅蓄电池的缺点:笨重、抗震动性差、易溢出酸液等。
三、燃料电池
燃料电池:又称连续电池,是一种连续性的将燃料和氧化剂的化学能转化为电能的化学电源。
燃料电池
(-)C | H2 (p) | KOH(aq) | O 2 (p) | C(+)
(-) 2H2 (g) +4OH (aq) = 4H2 O(l)+4e-
(+)O2 (g)+ 2H 2O(l) +4e- =4OH- (aq)
2H2(g) + O2(g) = 2H2O(l)
电极反应:
电池反应:
电池符号:
燃料电池特点:
②电极材料一般不参加化学反应,只起传导
电子的作用。
①燃料做负极,助燃剂氧气为正极。
燃料电池与前几种电池比较:
?环保清洁型能源
?能量转化率高
?寿命长
?能够连续大功率供电
化学能源与新能源
化学能源有污染,这个问题怎样解决?
发电
风力发电
地热发电
生活垃圾发电
核电
潮汛发电
……
组成 负极 正极 电解质
电极材料 能导电的物质 酸、碱盐溶液或熔融液
电击上发生反应的物质 还原性较强的物质 氧化性较强的物质
电子流向 流出电子 流入电子
反应类型 氧化反应 还原反应
1.化学电池的组成
课堂小结
电池名称 电压 主要优缺点
普通电池(锌锰电池) 1.5V 优点:使用方便便宜。
缺点:寿命短存,放不能充电。
碱性锌锰
1.5V
优点:电容量大寿命长。
缺点:不能充电,价格高。
锌银纽扣电池 1.5V 优点:体积质量小,寿命长。
缺点:不能充电,价格高。
铅蓄电池 2V 优点:电压稳定,电容量大,可充电,便宜。
缺点:笨重,防震性差。
2.部分主流产品供电的基本原理、性能
1.氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等。请写出将图中氢气换成甲烷时所构成的甲烷燃料电池中a极的电极反应式:
此时电池内总的反应式 :
KOH溶液
CH4
O2
H2O
a b
课堂练习
2.航天技术上使用的氢氧燃料电池具有高能、轻便、无污染的优点。氢氧燃料电池有酸式和碱式两种,它们放电时的总反应都可以表示为2H 2 +O2 =2H2 O,酸式电池中电解质是酸,其负极反应可表示为: ,则其正极反应式为: 。碱式电池的电解质是碱,其正极反应式为:________________________则其负极反应可表示为: _____________________________-。
3.已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。关于标有“+”的接线柱,下列说法中正确的是( )
A.充电时作阳极,放电时作负极
B.充电时作阳极,放电时作正极
C.充电时作阴极,放电时作负极
D.充电时作阴极,放电时作正极
B
4.据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:
,则下列说法错误的是( )
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:
D.充电时每生成1 mol CH3OH转移6 mol电子
A
5.熔融盐燃料电池具有高的发电效率,因而受到重视.可用 和 的熔融盐混合物用电解质,CO为阳极燃气,空气与 的混合气为阴极助燃气,制得在6500℃下工作的燃料电池,完成有关的电池反应式:
负极反应式: __________________________。
正极反应式: _________________________。
总电池反式: _________________________________-。
负极:
正极:
总:
6.心脏起博器中用了这样一个原电池(示意图):
已知人体血液的pH值在7.35~7.45之间。将心脏起博器,植入如图红色区域静脉血管内,请写出电极反应式并分析其工作原理。
放出电脉冲进行工作。
Zn-负极,Pt-正极;人体体液作电解质,溶解氧做氧化剂。
负极反应:2Zn-4e+4OH-=2Zn(OH)2
正极反应:O2+4e+2H2O=4OH-
电池反应:2Zn+O2+2H2O=2Zn(OH)2
7.某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为:
放电时:LiMn2O4发生还原反应
放电时:正极反应为:Li++LiMn2O4+e-=Li2Mn2O4
习题答案
4. 铅蓄电池放电时的电极反应如下:
负极:Pb(s)+SO42-(aq)-2e- = PbSO4(s)
正极:PbO2 (s)+4H+(aq)+SO42-(aq)+2e- =PbSO4 (s)+2H2O(l)
铅蓄电池充电时的电极反应如下:
PbSO4 (s)+2e- = Pb(s)+SO42-(aq)
PbSO4 (s)+2H2O(l)-2e- =PbO2(s)+4H+(aq)+SO4(aq)??????????????????????????????????????????
1. A;???? 2. C;?? 3. C。
总反应方程式:???????
阳极:
阴极:
PbO2 (s)+Pb(s)+2H2SO4(aq)
=PbSO4(s)+2H2O(l)??????????????????????????
新课导入
各种电池
使用锂电源的手机和笔记本电脑
纽扣电池作为电源的纽扣电池
使用氢氧燃料电池动力的法国产标致TAXI
一、化学电池与其他能源相比较有那
些优点?
二、一次电池、二次电池、燃料电池
第2节 化学电源
教学目标
知识目标
能力目标
1.知道常见电池的组成及应用。
2.了解燃料电池的组成和工作原理。
3.了解新型化学电源与人们生活实践的重要关系。
运用观察、实验、查阅资料等方法,结合生产、生活实践学习常见电池的组成及应用,关注新型化学电源。
亲自动手实验,体验科学探究的艰辛与喜悦;关注科技前沿知识,激发兴趣,热爱科学;关注与化学有关的社会问题,体会理论研究转化为技术产品的复杂过程。
情感态度与价值观
一次电池、二次电池和燃料电池的反应原理、性能及其应用。
化学电池的反应原理。
重点
教学重难点
难点
在生活中,你用过那些电池?它们属于哪一类电池?你知道他们的工作原理及应用吗?
电池
化学电池
太阳能电池
原子能电池
将化学能转化成电能的装置
将太阳能转化为电能的装置
如:碱性新锰电池、锌银电池、铅蓄电池、锂电池等。
广泛应用于通讯、交通、文化、及家庭电子产品。高科技及军事也有特殊应用。
将放射性同位素自然衰变时产生的热能通过热电转化器转变为电能的装置
锌锰干电池
铅蓄电池
1792年,物理学教授伏特根据一位名叫伽伐尼的解剖学家发表的一篇论文说动物肌肉里贮存着电,用金属接触它们,电就会跑出来。伏特经过一次又一次的实验,终于在1800年找到了“动物肌肉里贮存着电”的秘密所在。为纪念伏特,电压的单位以他的名字来命名。
伏特
读一读
伏特
一、化学电池与其他能源相比较有
那些优点?
化学电池 定义 举例
一次电池
二次电池
三次电池
1.电池分类
电池中的活性物质消耗到一定程度就不能使用。
普通锌锰电池
碱性锌锰电池
锌银纽扣电池
又称充电电池或蓄电池,放电后可以再充电使活性物质获得再生
铅蓄电池
锌银蓄电池
锂离子电池
又称连续电池,是一种连续性的将燃料和氧化剂的化学能转化为电能的化学电源
氢氧燃料电池
2.化学电池的优点:
(1)能量转化效率较高,供能稳定可靠。
(2)可以制成各种形状和大小、不同容量和电压的电池及电池组。
(3)使用方便,易于维护,并可在各种环境下工作。
形态各异的化学电池
3.判断电池优劣的标准:
⑴.比能量,指这种电池单位质量或单位体积所能输出电能的多少。【单位是:(W·h)/kg, (W·h)/L】
⑵.比功率,输出功率大小。【单位是:W /kg ,W /L】
⑶.可存储时间的长短。
除特殊情况外,质量轻、体积小而输出电能多、功率大可存储时间长的电池,更适合受使用者的需要。
一次电池:活性物质(发生氧化还原反应的物质)消耗到一定程度就不能使用的电池。一次电池中电解质溶液成胶状不流动,因此也叫干电池。
纽扣电池
普通干电池
二、一次电池
正极
碳棒
锌皮
纸隔板
氯化锌和氯化铵的糊状物
二氧化锰石墨
负极
普通锌锰干电池
碱性锌锰电池
电池符号:
(-)Zn|KOH(7~9mol·dm-3) | MnO2| C(+)
电极反应:
电池反应:
二、二次电池
二次电池:又称充电电池或蓄电池,放电后可以再充电使活性物质获得再生。
铅蓄电池
水、硫酸
氧化铅板
铅板
铅蓄电池原理
负极:
正极:
电池反应:
负极——Pb
正极——PbO 2
Pb
PbO 2
硫酸
铅蓄电池:
铅蓄电池充放电示意图
充电
放电
充电时的两极反应:
阴极(A极)
阳极(B极)
总反应式:
放电时的两极反应:
负极(A极)
正极(B极)
电池反应:
充电
放电
铅蓄电池的充放电程度,可用测定硫酸密
度的方法来判断。
铅蓄电池的缺点:笨重、抗震动性差、易溢出酸液等。
三、燃料电池
燃料电池:又称连续电池,是一种连续性的将燃料和氧化剂的化学能转化为电能的化学电源。
燃料电池
(-)C | H2 (p) | KOH(aq) | O 2 (p) | C(+)
(-) 2H2 (g) +4OH (aq) = 4H2 O(l)+4e-
(+)O2 (g)+ 2H 2O(l) +4e- =4OH- (aq)
2H2(g) + O2(g) = 2H2O(l)
电极反应:
电池反应:
电池符号:
燃料电池特点:
②电极材料一般不参加化学反应,只起传导
电子的作用。
①燃料做负极,助燃剂氧气为正极。
燃料电池与前几种电池比较:
?环保清洁型能源
?能量转化率高
?寿命长
?能够连续大功率供电
化学能源与新能源
化学能源有污染,这个问题怎样解决?
发电
风力发电
地热发电
生活垃圾发电
核电
潮汛发电
……
组成 负极 正极 电解质
电极材料 能导电的物质 酸、碱盐溶液或熔融液
电击上发生反应的物质 还原性较强的物质 氧化性较强的物质
电子流向 流出电子 流入电子
反应类型 氧化反应 还原反应
1.化学电池的组成
课堂小结
电池名称 电压 主要优缺点
普通电池(锌锰电池) 1.5V 优点:使用方便便宜。
缺点:寿命短存,放不能充电。
碱性锌锰
1.5V
优点:电容量大寿命长。
缺点:不能充电,价格高。
锌银纽扣电池 1.5V 优点:体积质量小,寿命长。
缺点:不能充电,价格高。
铅蓄电池 2V 优点:电压稳定,电容量大,可充电,便宜。
缺点:笨重,防震性差。
2.部分主流产品供电的基本原理、性能
1.氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等。请写出将图中氢气换成甲烷时所构成的甲烷燃料电池中a极的电极反应式:
此时电池内总的反应式 :
KOH溶液
CH4
O2
H2O
a b
课堂练习
2.航天技术上使用的氢氧燃料电池具有高能、轻便、无污染的优点。氢氧燃料电池有酸式和碱式两种,它们放电时的总反应都可以表示为2H 2 +O2 =2H2 O,酸式电池中电解质是酸,其负极反应可表示为: ,则其正极反应式为: 。碱式电池的电解质是碱,其正极反应式为:________________________则其负极反应可表示为: _____________________________-。
3.已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。关于标有“+”的接线柱,下列说法中正确的是( )
A.充电时作阳极,放电时作负极
B.充电时作阳极,放电时作正极
C.充电时作阴极,放电时作负极
D.充电时作阴极,放电时作正极
B
4.据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:
,则下列说法错误的是( )
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:
D.充电时每生成1 mol CH3OH转移6 mol电子
A
5.熔融盐燃料电池具有高的发电效率,因而受到重视.可用 和 的熔融盐混合物用电解质,CO为阳极燃气,空气与 的混合气为阴极助燃气,制得在6500℃下工作的燃料电池,完成有关的电池反应式:
负极反应式: __________________________。
正极反应式: _________________________。
总电池反式: _________________________________-。
负极:
正极:
总:
6.心脏起博器中用了这样一个原电池(示意图):
已知人体血液的pH值在7.35~7.45之间。将心脏起博器,植入如图红色区域静脉血管内,请写出电极反应式并分析其工作原理。
放出电脉冲进行工作。
Zn-负极,Pt-正极;人体体液作电解质,溶解氧做氧化剂。
负极反应:2Zn-4e+4OH-=2Zn(OH)2
正极反应:O2+4e+2H2O=4OH-
电池反应:2Zn+O2+2H2O=2Zn(OH)2
7.某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为:
放电时:LiMn2O4发生还原反应
放电时:正极反应为:Li++LiMn2O4+e-=Li2Mn2O4
习题答案
4. 铅蓄电池放电时的电极反应如下:
负极:Pb(s)+SO42-(aq)-2e- = PbSO4(s)
正极:PbO2 (s)+4H+(aq)+SO42-(aq)+2e- =PbSO4 (s)+2H2O(l)
铅蓄电池充电时的电极反应如下:
PbSO4 (s)+2e- = Pb(s)+SO42-(aq)
PbSO4 (s)+2H2O(l)-2e- =PbO2(s)+4H+(aq)+SO4(aq)??????????????????????????????????????????
1. A;???? 2. C;?? 3. C。
总反应方程式:???????
阳极:
阴极:
PbO2 (s)+Pb(s)+2H2SO4(aq)
=PbSO4(s)+2H2O(l)??????????????????????????
